肾活检时高尿酸血症与IgA肾病临床及牛津病理相关性研究
2020-06-12鲁珍珍邓跃毅刘旺意
鲁珍珍,邓跃毅,刘旺意
原发性IgA肾病是一组免疫病理综合征,表现为以IgA为主的免疫复合物颗粒状沉积在肾小球系膜区或(和)毛细血管袢。作为世界范围内最常见的肾小球疾病,其分布根据社会人口学特征、区域环境及肾活检策略的不同而不尽相同[1],其临床表现多样,疾病转归及预后难以预测。尿酸是人体嘌呤代谢的最终产物,主要由肝脏产生,经肾脏(65%~75%)和胃肠道(25%~35%)排泄。研究[2]发现高尿酸血症(hyperuricemia, HUA)是慢性肾脏病进展的独立危险因素。IgA肾病伴HUA患者肾小球硬化、肾小管间质和血管损伤评分更高。然而HUA与IgA肾病牛津病理的关系尚未完全阐明。该研究旨在探索肾活检时HUA与IgA肾病临床及牛津病理的关系,为IgA肾病确诊之初判断病情,防治疾病提供理论依据。
1 材料与方法
1.1 病例资料回顾性分析2012年1月~2019年1月在上海中医药大学附属龙华医院肾病科接受治疗并随访的原发性IgA肾病患者共289例。其中男性147例,女性142例,年龄14~76(37.0±11.8)岁。所有纳入患者均具有完整的肾穿报告及临床资料,肾穿报告均符合2009年《国际肾脏》正式公布的IgA肾病牛津分型标准。排除标准:① 过敏性紫癜、系统性红斑狼疮、乙肝病毒相关性肾炎等继发性IgA肾病;② 合并严重的心、脑、肝、肾等器官病变及功能障碍的患者;③ 合并严重感染和危及生命的并发症的患者。
1.2 一般资料① 基本资料:姓名、性别、年龄、首发症状、病程、高血压史。② 实验室资料:肾活检时的血肌酐、尿素氮、白蛋白、血尿酸、血红蛋白(hemoglobin, Hb)、总胆固醇(total cholesterol, TC)、三酰甘油(total glycerin, TG)、低密度脂蛋白(low density lipoprotein,LDL)、高密度脂蛋白(high density lipoprotein,HDL)、24小时尿蛋白(24 h urine protein, 24hpro)、肾小球滤过滤(estimated glomerular filtration rate,eGFR);HUA为空腹血尿酸水平男性>420 μmol/L,女性>357 μmol/L。③病理资料:按照2009年的牛津病理分型标准对IgA肾病进行分型。系膜增生(M):<4个系膜细胞/系膜区为M0,≥4个系膜细胞/系膜区为M1;肾小球毛细血管内增生性病变(E):E0(无)、E1(有);肾小球节段硬化或黏连(S):S0(无)、S1(有);肾小管萎缩或间质纤维化(T):0%~25% 为T0,>25%~50% 为 T1,>50%为 T2。

2 结果
2.1 不同尿酸水平基线临床特征共纳入289例IgA肾病患者,男性147例,伴HUA 71例,女性142例,伴HUA 49例,男女患有HUA的比例为1.45 ∶1。尿酸正常组的高血压发病率为25.4%,高尿酸组为52.5%,高血压发病率、肌酐、尿素氮比较差异有统计学意义(P<0.000 1),24 hpro比较差异有统计学意义(P=0.013),TC、TG、HDL、LDL比较差异有统计学意义(P<0.05),但Hb和白蛋白差异无统计学意义。见表1。
2.2 尿酸与牛津病理分型的相关性Spearman等级相关分析显示,HUA与牛津分型中系膜增生(r=0.254,P<0.000 1)、肾小球节段硬化或黏连(r=0.145,P=0.013)以及肾小管萎缩或间质纤维化(r=0.315,P<0.000 1)正相关,而与肾小球毛细血管内增生性病变(r=-0.029,P=0.626)的相关性差异无统计学意义。
2.3 牛津分型M、S和T与临床指标的比较将与尿酸相关的病理因素M、S、T进行分组,M0、M1组尿酸、肌酐以及24 hpro比较,差异有统计学意义(P<0.05)。T2组的尿酸水平高于T0和T1组,白蛋白水平低于T0和T1组,差异有统计学意义(P<0.05);3组间肌酐比较,差异有统计学意义(P<0.05);S0、S1两组间比较,差异均无统计学意义(P>0.05)。见表2。
2.4 尿酸对牛津病理M和S的影响多因素Logistic回归对性别、年龄、血压、肌酐、尿素氮、白蛋白、TC、TG、HDL、LDL、eGFR、24 hpro、Hb进行调整后发现,HUA是系膜增生(OR=3.336,95%CI:1.848~6.020)和小球节段硬化(OR=2.238,95%CI:1.084~4.621)的独立危险因素。结合不同临床指标建立3个不同的模型,采用ROC曲线联合诊断显示当加入尿酸这个因素后,ROC曲线下面积均大于没有增加尿酸的因素,见表3、图1、2、3。且对于诊断M的曲线下面积大于诊断S的曲线下面积,认为尿酸可以提高对系膜增生和小球节段硬化的诊断,对提高系膜增生的敏感性大于小球节段硬化。与其他两个模型相比,Model 3中联合的指标最多,曲线下面积最大。

表1 不同尿酸分组基线临床特征

表2 牛津分型M、S和T与临床指标的比较
与T0组比较:aP<0.05;与T1组比较:bP<0.05

表3 不同模型中有无尿酸对于预测M和S的曲线下面积
Model 1:性别,年龄,血压,肌酐;Model 2:性别,年龄,血压,肌酐,eGFR,24 hpro;Model 3:性别,年龄,血压,肌酐,eGFR,24 hpro,TC,TG,HDL,LDL,Hb, 白蛋白
3 讨论
近年来HUA的发病率随着人们生活水平的提高而不断上升,中国成人HUA发病率由8.4%上升到13.3%[3]。现多认为该病与代谢综合征相关,会增加痛风、糖尿病以及心血管、脑血管疾病的发生风险[4]。一项研究[5]对 1 965 例IgA肾病平均随访7年,对各混杂因素调整后发现HUA与IgA肾病进展呈正相关。有研究[6]显示尿酸可预测女性IgA肾病进展,与肾脏存活呈J型关系[7]。另有研究[8]显示HUA是G3a期进展的独立危险因素。
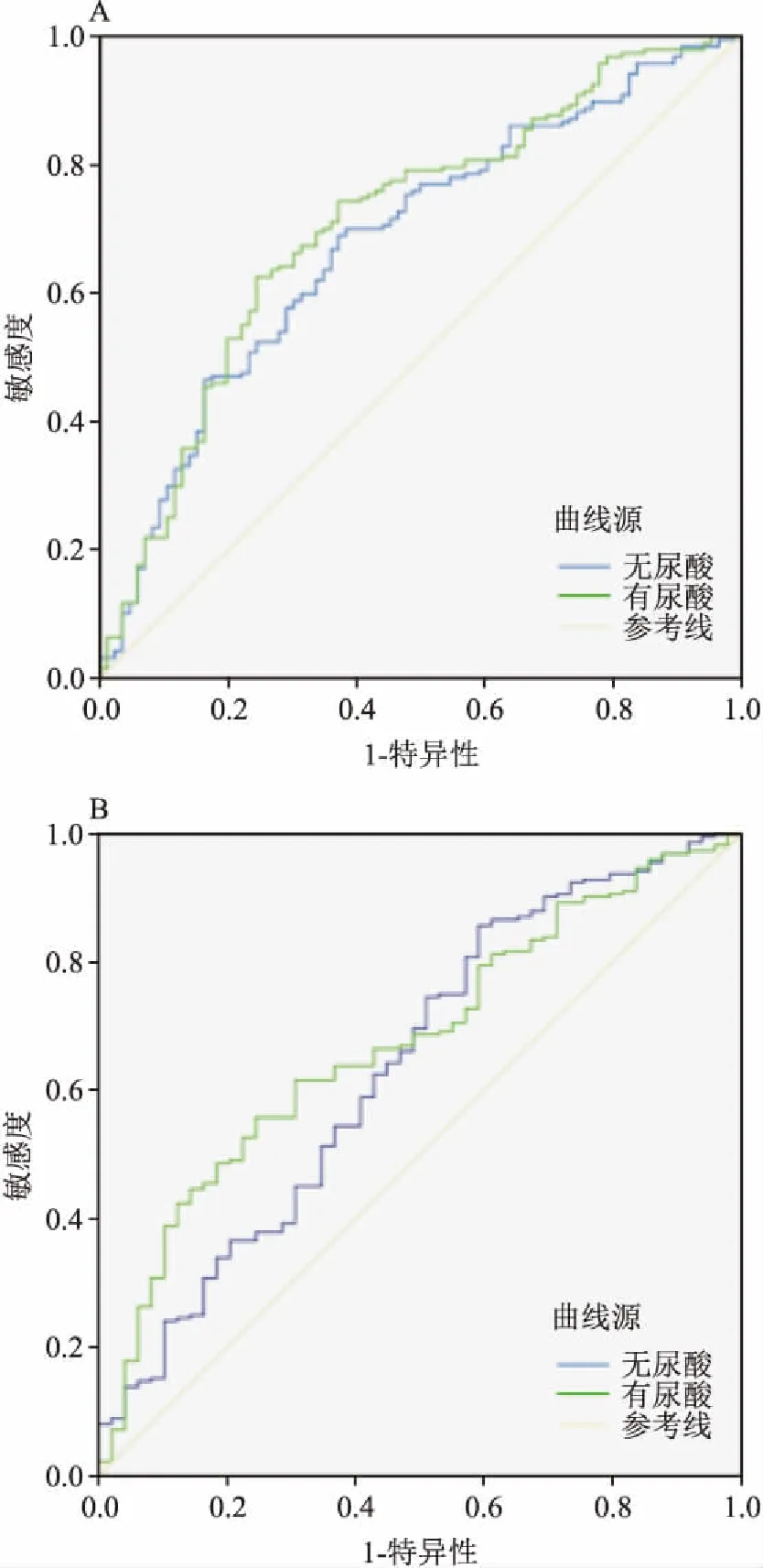
图3 Model 3有无尿酸对于诊断系膜增生和小球节段硬化的曲线下面积
本研究显示肾活检时HUA的发生率为41.5%。高尿酸组的高血压发病率更高,肾功能损伤更为严重,脂质代谢更为异常,不论是HUA伴其他代谢综合征,还是高血压或脂质代谢紊乱加重HUA程度,可能都会加重IgA肾病的进展,对血压、血脂、血尿酸的及时干预治疗或可在一定程度上延缓IgA肾病进展。HUA不仅与IgA肾病临床指标相关,也与组织病理损伤密切相关。既往对HUA与IgA肾病的牛津病理关系研究多集中在肾小管萎缩和间质纤维化以及小球硬化方面[9-10],而HUA与IgA肾病系膜细胞增生相关研究较少。本研究提示肾活检时HUA与IgA肾病牛津分型中的M、S和T相关。多因素Logistic回归调整其他因素后发现肾穿时尿酸水平是M和S的独立危险因素。通过建立3种模型进行联合诊断显示,增加尿酸因素后3种模型的ROC曲线下面积均大于未增加尿酸的模型,提示肾穿时尿酸水平提高了对M和S诊断的敏感性,尤其在Model 3中曲线下面积最大,表明尿酸联合的指标越多,对诊断IgA肾病M和S的效能越大。分析其原因可能与HUA在无尿酸盐结晶形成的溶解状态下诱导肾小球系膜细胞增生有关。系膜细胞属于肾固有细胞,其与毛细血管袢之间不存在基底膜,因此,任何来自血流异常信号等多种病理因素可直接对肾小球系膜产生影响[11]。相关体外实验研究[12]也表明,尿酸可促进体外培养的系膜细胞在一定范围内的增生和表型转化且呈剂量依赖性增强。随着慢性肾脏病的发展,肾小球滤过率下降,长期HUA导致尿酸盐在肾脏沉积,使肾脏病变从早期肾小球系膜增生,炎症细胞浸润向晚期小球节段硬化发展,进一步加重肾脏损伤。本研究分析肾活检时尿酸水平与IgA肾病病理关系,多属于早期阶段,故可能对系膜增生更为敏感,所以尿酸对诊断M的曲线下面积大于诊断S的曲线下面积。综上,临床上对于高度怀疑IgA肾病的患者,或不愿意做肾活检的患者,可以结合尿酸、血压、肌酐、eGFR、24 hpro等指标,对预测肾脏系膜增生和小球硬化具有一定的帮助,当然,临床指标越齐全,对预测M和S诊断的敏感性越高。同时,HUA可以作为治疗M和S的潜在靶点,对HUA及相关代谢综合征的及早干预或可在一定程度上延缓IgA肾病的进展。
本研究结果表明HUA与IgA肾病临床指标及组织病理相关,同时HUA作为IgA肾病系膜增生和小球硬化的独立危险因素,可以提高对系膜增生和小球硬化的诊断,故在发现尿酸水平升高之初对其进行积极控制,对于减轻系膜增生、小球硬化的损伤,延缓肾脏病情发展具有重要意义。
