再生纸与原纸中矿物油成分的LC-GC-MS检测及鉴别
2020-06-01朱丽娴林勤保钟怀宁
朱丽娴,林勤保*,陈 胜,钟怀宁,李 忠,廖 佳
(1.暨南大学 包装工程研究所,广东 珠海 519070;2.广州海关检验检疫技术中心,广东省动植物与食品进出口技术措施研究重点实验室,食品接触材料国家重点实验室,广东 广州 510623;3.拱北海关技术中心化学分析实验室,广东 珠海 519015)
废纸回收过程中无法完全清除纸张中所有的污染物(重金属、印刷油墨等),因此是否将再生纸用作食品包装材料一直存在争议。美国食品和药品管理局规定满足一定安全条件的再生纤维可用作食品接触材料[1];在欧洲,食品接触用纸和纸板材料(包括再生纤维制成的纸)必须符合欧盟各成员国的相应法规[2-3]。这些国家和地区建立了限制食品接触用纸(包括再生纸)中多种有害物质含量的法规[1-4],此外,我国也建立了相关标准以评估食品接触用纸的安全性[5]。但再生纸中可能还存在其它未知有害物质,这些物质目前尚无规定或无法检测。此外,由于纸张的物理化学结构,潜在的迁移物会吸附在纤维素纤维上,甚至可能通过顶空或直接接触的方式释放到食品中[6]。
科学研究表明,再生纸食品接触材料(盒子、纸袋)含有的一系列污染物可能迁移到食品中,例如重金属(镉、汞和铅)、增塑剂和矿物油[7-9],其中,再生纸中矿物油的研究颇受关注。学者Biedermann等[10]的研究表明,再生纸食品接触材料是食品受矿物油污染的潜在来源之一;然而其另一项研究使当局陷入了两难境地:废纸回收是为了材料的可持续利用,但根据毒理学评估,再生纸中有害物质的迁移通常是不可接受的[11]。
此外,不少学者研究了再生纸和原纸的鉴别方法。Asensio等[12]分析了再生纸和原纸中的挥发性化合物残留,并对两者进行分类。Xin等[13]通过傅里叶变换近红外光谱(FTIR)结合主成分分析(PCA)和偏最小二乘判别分析(PLS-DA),对仅由原生纤维制成的薄纸和含再生、原生两种纤维制成的薄纸进行分类,该方法无损且省时,但并未研究造成原生纤维和再生纤维之间差异的化学成分。Song等[14]利用气相色谱-质谱法结合主成分分析成功鉴别了原生和再生聚苯乙烯发泡餐盒,且筛选出差异性物质。
本研究基于PCA、正交偏最小二乘判别分析法(OPLS-DA),使用在线液相色谱-气相色谱-质谱(LC-GC-MS)检测再生纸和原纸的矿物油(MOH)成分,分析再生纸和原纸中饱和烃矿物油(MOSH)和芳香烃矿物油(MOAH)馏分之间的差异,并鉴别出可作为再生纸化学标记物的成分。
1 实验部分
1.1 材料与试剂
50种纸样品(24种再生纸、26种原纸)来源于不同的纸张供应商和生产商(广东、上海等),纸样相关信息(克重、厚度、再生浆比例、类型)列于表1。
MOSH馏分内标:十二烷(CAS号112-40-3)、十四烷(CAS号629-59-4)、十六烷(CAS号544-76-3)、二十烷(CAS号112-95-8)、二十四烷(CAS号646-31-1) 、三十五烷(CAS号630-07-9)、四十烷(CAS号4181-95-7)、5-α-胆甾烷(CAS号481-21-0);MOAH馏分内标:正己基苯(CAS号1077-16-3)、1,3,5-三叔丁基苯(CAS号1460-02-2)、联苯(CAS号92-52-4)、正壬基苯(CAS号1081-77-2)、苝(CAS号198-55-0);上述试剂均购自美国Sigma-Aldrich公司。二氯甲烷和正己烷(色谱纯,德国Merck公司),乙醇(HPLC级,荷兰Biosolve公司)。

(续表1)
R1-R24 are recycled samples,V1-V26 are virgin samples
1.2 仪器与设备
振动筛(SM-30 CONTROL,德国EdmündBuhler GmbH);离心机(4-15,德国Sigma公司);LC-GC-Q-Orbitrap-MS系统(德国Thermo Scientific公司),包括TriPlus RSH自动进样器、Phoenix 9000 液相色谱、UVIS 20UV微型紫外检测器、带预备柱进样器的TRACE 1310 气相色谱、转移开关阀门、电子电离(EI)源和Orbitrap MS。
1.3 实验方法
1.3.1 纸样中矿物油的提取参考前人研究方法[15],称取1.000 g纸样于40 mL的带盖玻璃小瓶中,加入20 mL萃取溶液(乙醇-正己烷,体积比1∶1)和50 μL内标液(质量浓度:5-α-胆甾烷和苝为500 mg/L,其它MOSH内标为300 mg/L,其它MOAH内标为100 mg/L,溶剂为正己烷);将混合物在振动筛上以190 r/min振动2 h后,加入20 mL超纯水,并以2 000 r/min离心2 min,取出有机相(上层液体)于进样小瓶中,待上机。每5个纸样进样前,对试剂空白进行分析,以识别设备或使用材料中的系统或非系统污染。
1.3.2 LC-GC-Q-Orbitrap-MS分析在线LC分析:流动相A为正己烷,B为二氯甲烷;色谱柱为LiChrospher 60 SI柱(250 mm× 2.0 mm,5 μm,德国Merck公司)。除另有说明外,流动相流速为300 μL/min。梯度洗脱:初始为0%B,0.5 min内升为30%B,保持至3.5 min;在1 min内升为40%B,保持至6.3 min;在6.4 min时将流动相换成100%B(流速增至500 μL/min),保持至15 min;15.1 min起,流动相改为0%B,保持至35 min(15.1~25 min流速为500 μL/min)[16],此设置用于重新平衡,并与GC-Q-Orbitrap-MS分析配合使用。进样量为50 μL。
转移系统:通过保留间隙技术进行LC-GC转移[17],LC分离中,MOSH馏分在保留时间2.0~3.5 min洗脱,而MOAH馏分在保留时间4.0~5.5 min洗脱[17],本实验中MOSH和MOAH馏分的转移时间(LC至GC-MS)分别为2.0~3.5 min和4.0~6.5 min。每个样品需进样2次,以分别获得MOSH和MOAH馏分的原始数据(包括总离子流色谱图)。LC系统用于分离MOSH和MOAH馏分,当MOSH馏分中不存在芳香烃,MOAH馏分中不存在脂肪烃,说明分离成功。
GC分析:ZB5-MS气相色谱柱(15 m×0.25 mm,0.25 μm,美国Phenomenex公司),柱箱温度为60 ℃(保持10 min),以20 ℃/min升至350 ℃,保持8 min。载气为氦气,流速为1.2 mL/min。
MS分析:使用Tune 2.7和Xcalibur 4.1软件(德国Thermo Scientific)控制该仪器。EI源(70 eV),离子源温度为250 ℃,全扫描模式,质量范围为m/z50~650。溶剂延迟至9 min。在每批进样序列之前,以全氟三丁胺作为校正气体进行调谐、质量校正和泄漏评估。
1.3.3 谱图收集与数据预处理利用Xcalibur 4.1和TraceFinder 4.0软件(德国Thermo Scientific)对色谱图进行处理。通过谱图解卷积和NIST谱库(NIST 2014/EPA/NIH)进行化合物筛选鉴定。将LC-GC-Q-Orbitrap-MS原始数据文件(各样品的MOSH和MOAH馏分文件)导入TraceFinder,并进行峰检测、解卷积和保留时间对准。解卷积参数参照文献[18-19],使用“所有离子”选项和名为“保留时间对齐”的参数(值为10 s)执行色谱峰解卷积,质量提取窗口精确至5 ppm,信噪比(S/N)阈值为10,最小强度信号为2×106,离子重叠窗口为98%。
在TraceFinder中进行未知物筛选后,导出样品的保留时间、峰面积、未知物表格。由于太多的值可能对数据分析产生影响,因此缺少值估计至关重要。使用“替换为一个小值(原始数据中最小正值的一半)”选项来估计缺失值。采用对数变换使得数据更具可比性[20]。使用Pareto方法对数据集进行缩放,即每个变量的响应均以其中心值减去平均值,然后除以其标准偏差的平方根,对经上述处理后的数据进行多元统计分析。
1.3.4 多元统计分析SIMCA 14.1(Umetrics,瑞典)用于多变量统计分析。PCA是一种常见的探索性数据分析方法,对原始数据中的变量进行线性拟合,生成互不相关的新变量,即主成分,这些主成分可以反映原始变量的绝大部分信息。主成分得分图中样品的分布情况可以显示样品间的相似性,而载荷图显示每个原始变量对主成分的贡献[6]。
PLS-DA是一种结合偏最小二乘回归模型和判别分析的方法,可同时分解自变量矩阵X和分类变量Y,并找出自变量X和变量Y间的线性关系。OPLS-DA是将正交信号矫正方法与偏最小二乘法相互结合的判别方法,可过滤自变量矩阵(X)与变量矩阵(Y)无关的信息(即随机噪声),因此OPLS-DA建立的分类模型可以更好地找出不同样品组间的差异[21]。
变量权重值(VIP)用于衡量变量差异对各组样本分类判别的影响强度和解释能力,根据VIP值可筛查再生纸和原纸的差异性物质。本研究的OPLS-DA模型中,选择VIP值大于1的变量,并对选取变量对应的峰面积进行t检验,仅选择VIP> 1且P<0.05的变量作为潜在标记化合物。
2 结果与讨论
2.1 纸样的MOSH与MOAH馏分中多种化合物的分析
采用LC-GC-Q-Orbitrap-MS技术分析纸样中MOSH和MOAH组分中的化合物,使用解卷积、NIST库进行化合物定性。其中,原纸和再生纸中MOAH部分的总离子流图见图1,MOAH馏分检测的物质列于表2,包括单体(即萘、2-甲基萘)和异构体(即二甲基萘同分异构体、三甲基萘同分异构体等)。二异丙基萘同分异构体是无碳复写纸的一种染料溶剂,主要存在于回收纸浆中[12]。噻吩化合物可能来源于麻袋中的少量精炼油,在大米样品中也可检测到噻吩化合物,研究表明二甲基二苯并噻吩和甲基二苯并噻吩可作为矿物油污染的标志物[16,22-23]。另外,化合物2,2′-5,5′-四甲基-1,1′-联苯和二甲基萘同分异构体作为污染物[24]在本文亦被检出。芳香族化合物(即二甲基萘)可能来自印刷油墨的染料或溶剂残留物,或者来自回收纤维的污染物(MOH残留物,降解产物和燃烧过程,煤焦油的成分)。
MOSH馏分中检测出具有不同分子量的饱和烃(N-烷烃)。一些正构烷烃可能来源于石蜡,通常作为涂层材料[25]。值得关注的是,再生纸中均含有高浓度的高分子量饱和烷烃(C25~C33)。可能是由于矿物油污染,或是再生样品中含有聚烯烃组分残留物[24]。


图1 原纸(A)和再生纸(B)中MOAH部分的总离子流图Fig.1 Representative total ion chromatograms of MOAH fraction in virgin(A) and recycled(B) papers

表2 纸样中MOAH馏分检出的化合物Table 2 Compounds detected in MOAH fraction of paper samples
there is no exact VIP value for alkylated benzenes and dialkylated benzenes
2.2 再生纸与原纸的多元统计分析鉴别
应用多元统计方法研究再生纸和原纸之间的差异性,图2A和2B显示了再生纸和原纸样品中MOSH和MOAH馏分的PCA得分图。
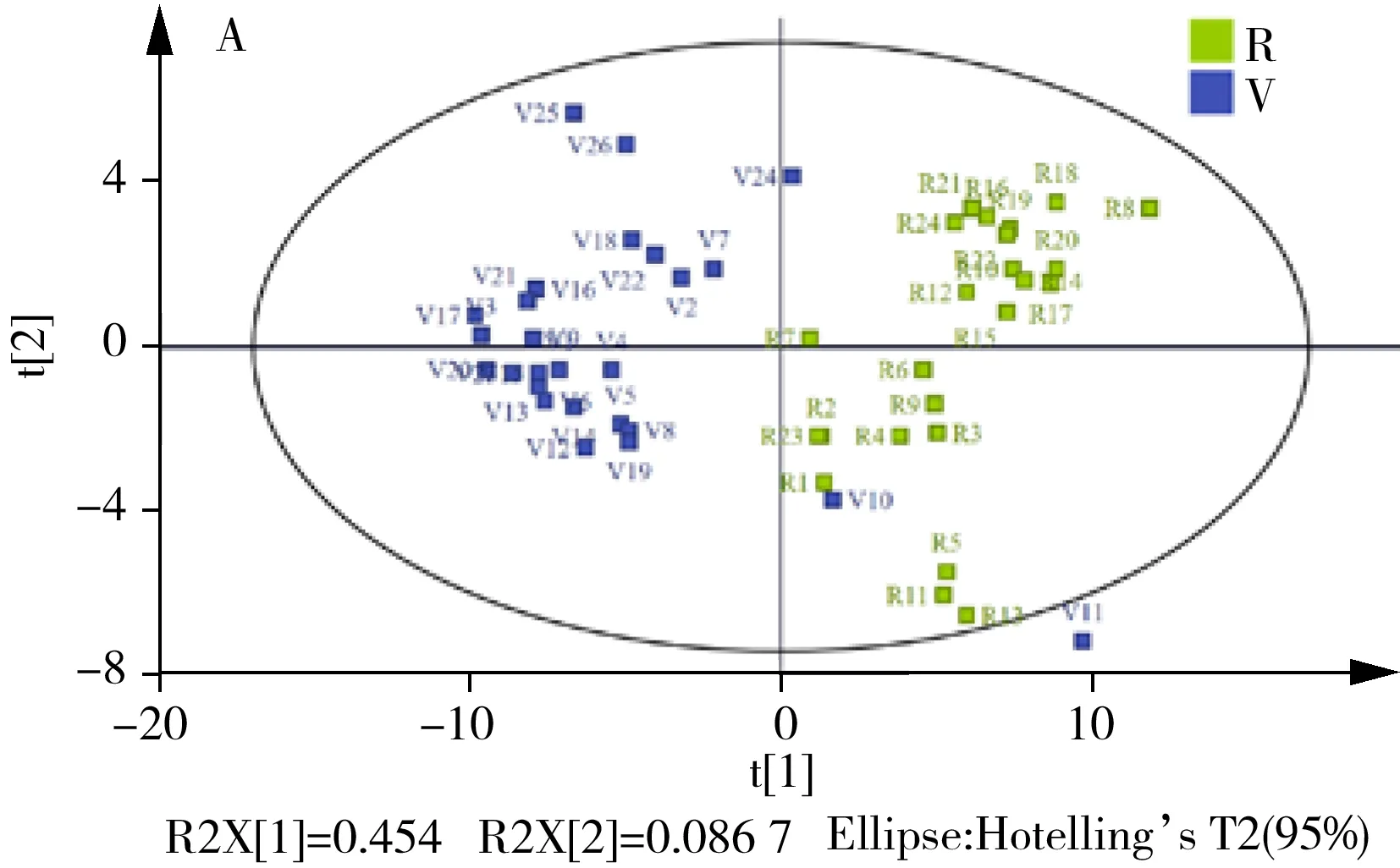

图2 再生纸和原纸样品中MOSH馏分(A)与MOAH馏分(B)的PCA得分图Fig.2 PCA score plots of MOSH fraction(A) and MOAH fraction(B) in recycled and virgin paper samplesR:recycled paper;V:virgin paper
结果显示,再生纸和原纸的聚类未明显分开,导致某些原纸样品与再生纸聚类。图2A中,原纸样品V10、V11与再生纸聚集,可能是由于饱和烃(C25~C33)的污染或在造纸过程中添加或产生这些化合物,因为样品V10和V11中的饱和烃(C25~C33)含量高于其它原纸(P<0.05)。图2A和2B中,大部分再生纸样品形成一个集簇,而再生纸样品R11和R13有向原纸聚集的趋势(图2B),这是由于R11和R13两个样品中的再生浆比例小于其它再生纸样品(表1)。因此,再生纸与原纸的分类受样品中再生浆比例和再生浆来源的影响,不同来源、不同比例的再生浆可能会导致重要成分种类、含量的不同,从而影响PCA得分图中纸样的聚集情况。使用PCA模型未能很好地区分再生纸和原纸,可能是因为再生浆不同或次要变量成分的干扰。因此,对模型进行了优化,选择再生纸和原纸样品(V10、V11异常值除外)MOSH馏分的色谱数据建立OPLS-DA模型,以及所有再生纸和原纸样品MOAH馏分的色谱数据建立OPLS-DA模型。
PCA是一种无监督模型,在进行主成分分析过程中考虑了所有变量,而监督模型OPLS-DA可以提取变量信息,最大程度地提高群体之间的差异,并有助于识别潜在的差异性物质。使用OPLS-DA模型可以区分再生纸和原纸(图3A和图3B)。两种模型的R2Y(cum)和Q2(cum)值分别为0.990和0.924(图3A),0.968和0.838(图3B),表明OPLS-DA模型具有良好的适用性和可预测性。通过置换检验(Permutation test,n=200)对模型进行验证。置换检验用于评估模型是否存在伪造的风险:验证思想是将Y观测值的顺序随机排列而X矩阵保持不变,以比较原始模型与实际模型的拟合优度,将随机化产生的R2、Q2值与原始积累的R2、Q2值比较。200次置换实验结果为:R2=(0.0,0.805),Q2=(0.0,-0.663)(图3A);R2=(0.0,0.77),Q2=(0.0,-0.527)(图3B)。表明OPLS-DA模型具有较好的可靠性,不存在过拟合现象。
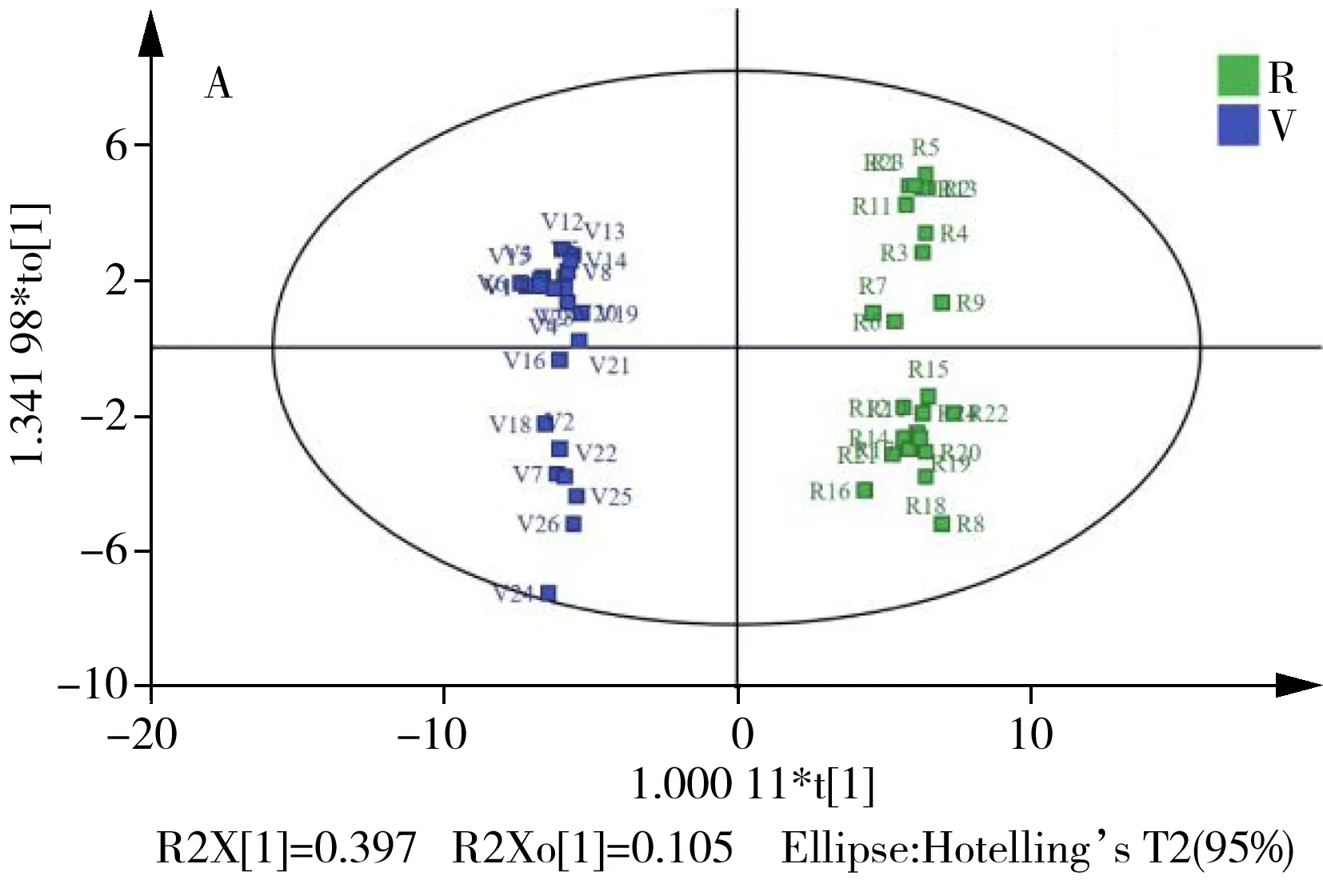

图3 再生纸和原纸样品中MOSH馏分(A)与MOAH馏分(B)的OPLS-DA得分图Fig.3 OPLS-DA score plots of MOSH fraction(A) and MOAH fraction(B) in recycled and virgin paper samplesR:recycled paper;V:virgin paper
2.3 原纸与再生纸的差异性物质
基于差异性化合物的选择标准,VIP>1且P<0.05,可确定的差异性化合物为:MOAH馏分的二异丙基萘同分异构体、四甲基联苯同分异构体、二甲基联苯同分异构体、异丙基联苯同分异构体,以及MOSH馏分的正构烷烃(C25~C33);表2中保留时间18.63 min和18.71 min对应的两个峰未能定性。再生纸中这些物质的含量高,而在原纸中浓度低或未检出,因此这些化合物具有区分原纸和再生纸的潜力。
2.4 基于再生纸和原纸差异性物质的多变量分析
为评估所选差异性标记物的判别能力,分别基于所选化合物的PCA和OPLS-DA模型对再生纸和原纸的MOSH和MOAH馏分进行鉴别分析。图4A为基于差异性物质的再生纸和原纸MOSH馏分的PCA得分图,再生纸和原纸实现了良好分离,前两个主成分共解释了95.8%的变量。图4B为再生纸和原纸MOAH馏分的PCA得分图,前两个主成分解释了90.1%的变量,再生纸和原纸之间的分离效果优于图2B。但图4B中再生纸样品R1、R5、R7、R9、R11和R13倾向于与原纸聚集,主要归因于这几种再生纸的回收纸浆来源和比例,检测结果表明这几种样品中差异性物质(二异丙基萘同分异构体、四甲基联苯同分异构体、二甲基联苯同分异构体、异丙基联苯同分异构体)的含量低于其它再生纸样品。相比之下,再生纸和原纸中MOSH馏分的差异性物质具有更好的区分效果。
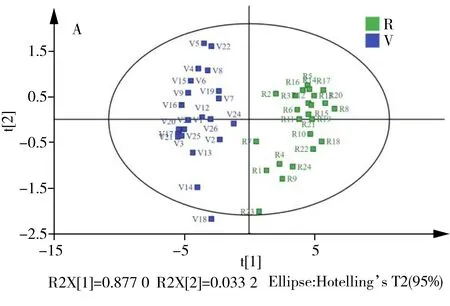

图4 基于差异性物质的再生纸(R)和原纸样品(V)的PCA得分图Fig.4 PCA score plots of recycled(R) and virgin(V) paper samples based on differential substancesA:MOSH;B:MOAH

图5 基于MOH中差异性物质的再生纸和原纸样品的PCA得分图Fig.5 PCA score plots of recycled and virgin paper samples based on MOH differential substancesR:recycled paper;V:virgin paper
使用所选差异性化合物建立OPLS-DA模型,两种模型的R2Y(cum)和Q2(cum)分别为0.916和0.913(MOSH馏分),0.937和0.913(MOAH馏分)。为验证模型,进行了置换实验(n=200),得R2=(0.0,-0.076 9),Q2=(0.0,-0.145)(MOSH馏分);R2=(0.0,0.064),Q2=(0.0,-0.297)(MOAH馏分),表明OPLS-DA模型具有良好的适应性和可预测性。
综合考虑MOSH和MOAH馏分中的差异性物质,建立PCA模型,如图5(不包括V10和V11)。结果显示,再生纸和原纸具有更明显的区分效果;再生纸样品R1、R5、R7、R9、R11和R13与原纸样品不再聚集,这6个样品聚为一小类。表明这些样品的再生纸浆在MOAH馏分中的差异性化合物(如二异丙基萘同分异构体)含量较低,但MOSH馏分中有足够的正构烷烃(C25~C33)可将它们与原生纸区分开。
3 结 论
本研究利用LC-GC-MS分析了再生纸和原纸中的矿物油成分,结合化学计量学对再生纸和原纸进行鉴定。由于回收过程中废纸的污染并不能完全清除,再生纸中含有较多的饱和烃矿物油与芳香烃矿物油。筛选出再生纸和原纸的差异性物质有:MOAH馏分中的二异丙基萘同分异构体、四甲基联苯同分异构体、二甲基联苯同分异构体、异丙基联苯同分异构体,以及MOSH馏分中正构烷烃(C25~C33)。基于再生纸和原纸中MOH的差异性物质建立的PCA模型能够很好地区分再生纸和原纸。
致谢:感谢瑞士苏黎世SQTS提供设备仪器的使用便利,以及Thomas Gude博士对本论文的帮助。感谢暨南大学研究生短期出国交流计划的资助。
