现有病毒疫苗用于防治新冠肺炎的可行性分析
2020-05-13孙晨何秋霞高燕张磊李宁刘可春
孙晨,何秋霞,高燕,张磊,李宁,刘可春*
(1.齐鲁工业大学(山东省科学院) 山东省科学院生物研究所,a. 山东省人类疾病斑马鱼模型与药物筛选工程技术研究中心;b. 山东省生物检测技术工程实验室,山东 济南 250103; 2.澳大利亚联邦药物管理局 生物部,澳大利亚 西蒙斯顿 2609)
2019年12月,中国湖北省武汉市的部分医院陆续发现不明原因肺炎病例,后被证实是由一种新型冠状病毒(2019-nCoV)感染所引起的急性呼吸道类传染疾病(新冠肺炎)。新冠肺炎现已纳入《中华人民共和国传染病防治法》规定的乙类传染病,并按照甲类传染病管理,其具有传染性强、潜伏期长、传播途径复杂等特点,感染患者的临床表现多样。大多数患者在发病时伴有轻微的发烧、咳嗽、肌痛、气促或疲劳等症状。在危重症患者中,感染可导致肺炎、严重急性呼吸综合征、肾衰竭,甚至死亡[1]。临床数据表明, 2019-nCoV感染的危重患者多为老年人、高血压患者、糖尿病患者等有基础疾病的人群[2]。截至2020年2月,2019-nCoV已在中国感染七万余人,并导致两千余人死亡[3]。
疫苗免疫是防控病毒感染的最有效策略,但是由于目前还没有专门针对2019-nCoV的疫苗,因此临床上对新冠肺炎仍以对症支持治疗为主,主要治疗方法包括抗病毒药物治疗,如洛匹那韦与利托那韦联合用药、利巴韦林等;中医药治疗,如双黄连、连花清瘟和甘草酸等;以及新冠状病毒特免血浆品治疗等[4-5]。
虽然世界各地的研究小组现正加紧步伐开发研制2019-nCoV的针对性疫苗,但是疫苗研发是一个比较耗时的过程,且2019-nCoV是一种新的病毒,目前对其认识还不是非常清楚,因此在疫苗的研发过程中还存在一些不确定的因素,2019-nCoV的特效疫苗应用到临床的具体时限仍未可知。考虑到当前疫情的严重性,本文对同为RNA病毒的流感病毒、其他冠状病毒相关疫苗的研究进行了综述,分析了现有病毒疫苗用于防治新冠肺炎的可行性,旨在找到一种可用于该疾病短期防控的替代物。
1 流感病毒
1.1 一般特征
流感病毒是一种可引起类似感冒症状的呼吸道病毒,主要引起高热、乏力、全身酸痛及呼吸道症状[6]。 流感病毒的感染传播非常迅速,流行性感冒即是由该病毒引起的一类严重威胁人类健康的急性呼吸道传染病,全球范围内每年约有29万~65万人死于季节性流感病毒感染[7]。流感病毒主要通过飞沫传播,老年人、儿童、孕妇、免疫缺陷人群以及有慢性基础疾病的人群均是易感染流感病毒的高危人群[8]。
流感病毒属于正黏病毒科,重要的遗传信息储备在单链RNA中,可编码血凝素 (hemagglutinin,HA) 糖蛋白、神经氨酸酶(neuraminidase,NA)、核蛋白(nucleoprotein,NP)、基质蛋白(matrix protein)和非结构蛋白(non-structural protein)等[9]。其中HA糖蛋白由流感病毒基因片段4编码而来,以同源三聚体的形式跨膜存在于流感病毒的包膜中。成熟的HA糖蛋白外观像蘑菇,包括头部与茎部。头部具有很高的变异性,由HA1结构域组成。该结构域含有受体结合位点与抗原决定簇,主要负责识别并结合宿主细胞表面的唾液酸受体,并可刺激宿主机体产生免疫反应[10]。茎部由HA2和小部分HA1结构域组成,主要介导流感病毒与宿主细胞膜的融合,是流感病毒相对保守的区域[11-12]。根据流感病毒的核蛋白与基质蛋白,可将其分成4型,分别是A、B、C和D型,其中A、B和C型可感染人类。A型流感病毒因其HA位点的结构常易发生突变,因此流行规模通常较大,根据其HA和NA的蛋白结构与基因特性可分为多种亚型,在鸟类和哺乳动物中,目前已确定了18个HA和11个NA亚型[6]。B型流感病毒只有一个亚型,根据抗原性和HA1区的核苷酸序列基因特性,在1990年将其分成两大谱系,简称Victoria系和Yamagata系。B型流感病毒流行规模较小[6,13]。C型流感病毒一般呈散发流行,且病情较轻。目前,引起流感季节性流行的病毒主要是A型中的H1N1、H3N2亚型和B型中的Victoria和Yamagata系。全球已上市的季节性流感疫苗,也主要针对上述4种流感病毒[14]。
1.2 流感疫苗
世界卫生组织每年对流感进行全球性监测,定期更改用于疫苗生产的推荐病毒疫苗株[15]。由于流感病毒是通过HA糖蛋白识别并进入宿主细胞的,因此目前已上市的流感疫苗主要以HA糖蛋白作为主要靶点。当流感疫苗作用机体后,可诱导机体产生靶向HA糖蛋白的中和抗体,该抗体可与HA糖蛋白相互作用,进而阻断病毒颗粒附着和进入宿主细胞[16-17]。根据感染性与毒性的有无,可将全球已上市的流感疫苗分为灭活流感疫苗(inactivated influenza vaccine,IIV)和减毒流感疫苗(live attenuated influenza vaccine, LAIV)。按照疫苗所含成分,流感疫苗又可分为三价与四价。三价疫苗自1978年开始投入使用,目前的三价流感疫苗组份中含有H1N1亚型、H3N2亚型和B型流感病毒株的Victoria系。2012年12月,葛兰素史克公司研发出四价流感疫苗,该疫苗在原来三价的基础上又增加了1个B型流感病毒株(Yamagata系)。根据生产工艺,流感疫苗又可分为基于鸡胚、基于细胞培养和重组流感疫苗[18]。
我国现已批准上市的流感疫苗包括三价灭活流感疫苗和四价灭活流感疫苗。其中三价灭活流感疫苗包括裂解疫苗和亚单位疫苗,适用于6月龄及以上的人群接种;四价灭活流感疫苗为裂解疫苗,适用于36月龄及以上的人群接种。根据我国国家药监局网站和疫苗批签发信息,2019—2020年,有7家厂家供应流感疫苗 (表1)。除此之外,一种鼻喷三价流感减毒疫苗正在上市审批过程中,其适用于3~17岁人群[14]。

表1 2019—2020年国内批签发的流感疫苗
2 冠状病毒
冠状病毒(corvonavirus, CoV)是一种单链正义RNA病毒,基因总长约为28~32 kb,属于冠状病毒科。是目前发现最大的RNA类病毒,基因组大致可分成6至7个区,每个区域均包含1至多条开放阅读框(opten-reading frame,ORF)。CoV主要有4种结构蛋白,分别是棘突(spike,S)糖蛋白、小衣壳(envelope, E)糖蛋白、膜(membrane, M)糖蛋白和核衣壳(nucleocapsid,N)核蛋白,少数冠状病毒还具有血凝素酯酶(hemagglutinin esterase,HE)糖蛋白。S糖蛋白主要负责CoV早期的宿主细胞黏附、红细胞凝集和膜融合等,是CoV的主要抗原位点;E糖蛋白与CoV颗粒的形成和组装有关;M糖蛋白主要负责CoV颗粒的组装;N核蛋白位于病毒颗粒的核心部分,主要负责病毒基因组RNA的复制等[19-20]。图1为CoV的基因组结构示意图。

图1 冠状病毒基因组结构示意图Fig. 1 The structure diagram of CoV genome
CoV主要感染鸟类和哺乳类动物,可导致多种严重疾病。近年来,越来越多的研究显示CoV也可感染人类,并在不同程度上引起肠道或呼吸道类疾病。CoV感染的潜伏期一般为2~5 d。典型的CoV感染呈流涕、不适等感冒症状。人冠状病毒229E(huamn coronavirus 229E,HCoV-229E)、人冠状病毒OC43(huamn coronavirus OC43,HCoV-OC43)、人冠状病毒NL63(huamn coronavirus NL63,HCoV-NL63)和人冠状病毒HKU1(huamn coronavirus HKU1,HCoV-HKU1)是4种可以感染人类,但一般不具高致病性的冠状病毒[21-24]。
HCoV-229E和HCoV-OC43在20世纪60年代首次被发现,感染人类后均能引发普通感冒症状,并很少造成下呼吸道感染。HCoV-229E感染引发的感冒症状通常较轻微,主要表现为鼻部症状。HCoV-OC43感染后常伴有咳嗽、咽炎和鼻腔炎等[22]。HCoV-NL63是2004年从一名患有结膜炎和支气管炎的7月龄婴儿身上分离得到的,该病毒感染人类后,患者常表现出咳嗽、发热和呼吸道感染等症状[23]。HCoV-HKU1是2005年从一名71岁的肺炎患者体内分离得到的。该病毒感染人类后可造成轻度上呼吸道感染,症状包括发烧、咳嗽和鼻涕等。研究发现,老年人或带有基础疾病的患者感染HCoV-HKU1后,可能会出现严重肺炎甚至死亡。除此之外,HCoV-HKU1还可能导致儿童惊厥或胃肠道疾病[24]。截至目前为止,尚无针对上述4种CoV的有效疫苗。严重急性呼吸系统综合征冠状病毒(severe acute respiratory syndrome corvonavirus,SARS-CoV)和中东呼吸综合征冠状病毒(middle east respiratory syndrome coronavirus,MERS-CoV)是两种可以感染人类且具有高致病性的冠状病毒。
2.1 SARS冠状病毒
2.1.1 一般特征
SARS冠状病毒(SARS-CoV)呈球形,直径为80~120 nm,基因组全长约29.4 kb,编码11种蛋白质,血管紧张素转化酶2 (ACE2)为其受体。2002年该病毒首先爆发于我国广东地区,并迅速蔓延至加拿大、美国和越南等30多个国家,导致了SARS的爆发,感染9000余人,死亡近800人[25]。SARS是一种起病急、传播快、死亡率高的传染病,被传染的病人多数都与患者有过直接或间接接触,或生活在疫区内。SARS临床上表现为缺氧、紫绀、38 ℃以上高热、呼吸加速或呼吸窘迫综合征、气促等,X片表现为肺部不同程度改变[26]。到目前为止,仍没有临床认可的抗病毒药物、疫苗或单克隆抗体来治疗SARS。
2.1.2 SARS-CoV疫苗研究现状
S糖蛋白是SARS-CoV的主要表面抗原成分,具有抗原决定簇,可以诱导抗体的产生,因此SARS-CoV疫苗主要围绕S糖蛋白进行研制[27]。目前在研的SARS-CoV疫苗主要包括灭活病毒疫苗、减毒病毒疫苗、病毒载体疫苗、亚单位疫苗和DNA疫苗等。表2为SARS-CoV疫苗的研究现状。
(1)灭活病毒疫苗
灭活病毒疫苗主要诱导机体产生中和抗体,这种疫苗在制备时,首先需要对SARS-CoV进行大量培养,然后采用紫外线、福尔马林或β-丙内酯对其进行灭活[28]。灭活病毒疫苗的研制周期较短,且相对稳定,甚至不需要冷藏,在疾病爆发或紧急状态下便于运输。但是由于需要对病毒进行大规模培养,因此这种疫苗对生产的安全性条件要求较高[29]。灭活病毒疫苗是最早进入临床试验的SARS-CoV疫苗[30]。
(2)减毒病毒疫苗
减毒病毒疫苗可诱导机体同时发生体液免疫和细胞免疫,在制备时,首先需要通过化学诱导或定点突变等方法,使SARS-CoV的基因组发生突变,造成毒性减弱但仍保留其S糖蛋白的免疫原性。由于该疫苗使用的是活体病毒,因此可在机体内长时间起作用,进而诱导较强的免疫反应。但是这种疫苗的保存和运输条件要求较高。除此之外,由于减毒病毒疫苗保留了一定的毒性,因此对一些个体,例如免疫缺陷者而言,有可能会诱发严重疾病[31]。
(3)病毒载体疫苗
病毒载体疫苗是指以另一病毒(简称宿主病毒)作为载体,将SARS-CoV的S糖蛋白基因与N核蛋白基因重组到宿主病毒基因组中,使其可以表达S糖蛋白和N核蛋白,进而制成疫苗。此类疫苗可有效诱导机体产生高效价的中和抗体。但是由于此类疫苗是以病毒为载体,因此机体易对宿主病毒产生免疫反应[31]。
(4)亚单位疫苗
亚单位疫苗指通过提取SARS-CoV的S糖蛋白片段(包含14~762位的氨基酸)与N核蛋白制成的疫苗。此类疫苗可以避免产生许多无关抗原诱发的抗体,进而减少疫苗的副反应和疫苗引起的相关疾病。但是其免疫原性较低,通常需要佐剂合用才能产生良好的免疫效果[32]。
(5)DNA疫苗
DNA疫苗是指将SARS-CoV的S糖蛋白与N核蛋白基因克隆至质粒载体,并直接诱导机体产生特异性免疫的一种疫苗。该类疫苗制备简单、安全性好,可同时诱导体液免疫和细胞免疫,并可在体内持续表达。但是有研究发现,含有N核蛋白基因的DNA疫苗有可能会引起迟发型的超敏反应,从而危害机体健康[33]。

表2 SARS-CoV疫苗研究现状
2.2 MERS-CoV
2.2.1 一般特征
MERS-CoV最早于2012年9月在沙特被发现,早期因与SARS临床症状相似得名“类SARS病毒”,是第6种已知可以感染人类的冠状病毒,该病毒会引发严重的中东呼吸综合征(MERS)。MERS-CoV轻度感染的患者多表现为低烧、干咳、流鼻涕、肌痛和喉痛等;严重者则逐渐发展成急性呼吸窘迫综合征、多系统疾病,直至器官衰竭[44]。截至目前为止,全球累计确诊的MERS-CoV感染病例为2494例,其中858例死亡,病死率约为34%。这些病例来自27个国家和地区,并多集中在沙特阿拉伯、阿联酋等中东地区,该地区以外国家的确诊病例发病前多有中东地区工作或旅游史[45]。
2.2.2 MERS-CoV疫苗研究现状
MERS-CoV疫苗的研究状况与SARS-CoV类似,也主要围绕其S糖蛋白进行研制。目前有两个MERS-CoV疫苗已在美国获得临床实验批准,分别是表达全长S糖蛋白的腺病毒疫苗(ChAdOx1)和DNA疫苗(GLS-5300)[46-47]。 除了结构蛋白,MERS-CoV 还表达5种辅助蛋白。这些辅助蛋白虽然不参与MERS-CoV的基因组转录和复制,但是却可帮助MERS-CoV逃避宿主的免疫反应。因此这些辅助蛋白也可以作为抗原,用于产生抑制MERS-CoV活力的抗体[48]。
2.3 新型冠状病毒
2.3.1 一般特征
2019-nCoV是迄今为止发现的第7个可以感染人类的冠状病毒,其基因组约29 891 bp,包括一个完整的ORF和两端非翻译区(untranslated regions, UTR),编码9860个氨基酸,G+C含量约38%[49]。目前的研究发现,2019-nCoV基因组有两个核心位置具有高度变异性,分别是ORF1ab基因中的沉默变异和氨基酸ORF8中的多态性[50-51]。2019-nCoV 的S糖蛋白是一个三聚体结构,每一个单体上都有细胞受体的结合位点。当病毒与宿主细胞结合之后,这个三聚体会发生变构,使病毒质膜与宿主细胞膜发生融合,便于病毒侵入宿主细胞,从而进行扩增繁殖[52]。
2.3.2 2019-nCoV疫苗的研究现状
此次新冠肺炎疫情从武汉爆发不久,2019-nCoV的全基因组即被准确测序,并于2020年1月11日在网络共享。在此基础上,来自世界各地的研究团队例如Vir生物技术公司、Morderna生物科技公司与美国国立卫生研究院团队、葛兰素史克公司、俄罗斯卫生部、昆士兰大学、Novavax医药公司等均宣布开始新冠病毒的疫苗研发工作。与此同时,中国也有多个科研团队投入疫苗研发当中,包括中国疾病预防控制中心、香港大学袁国勇教授团队、清华大学张琳琦教授团队、浙江三叶草生物制药公司团队、上海东方医院与斯微生物、北京艾棣维欣与Invio团队、武汉博沃与GeoVax等公司合作团队等。上述研发团队采取的技术路线不同,其中张林琦教授团队、武汉博沃与GeoVax团队是通过腺病毒技术研发;北京艾棣维欣与Inovio团队是通过DNA技术平台研发;斯微生物与上海东方医院合作团队、Moderna与美国国立卫生研究院合作团队是通过mRNA技术平台研发;浙江三叶草生物制药公司团队是通过其独有的蛋白三聚体化专利和基因重组方法进行研发[53-56](见表3)。
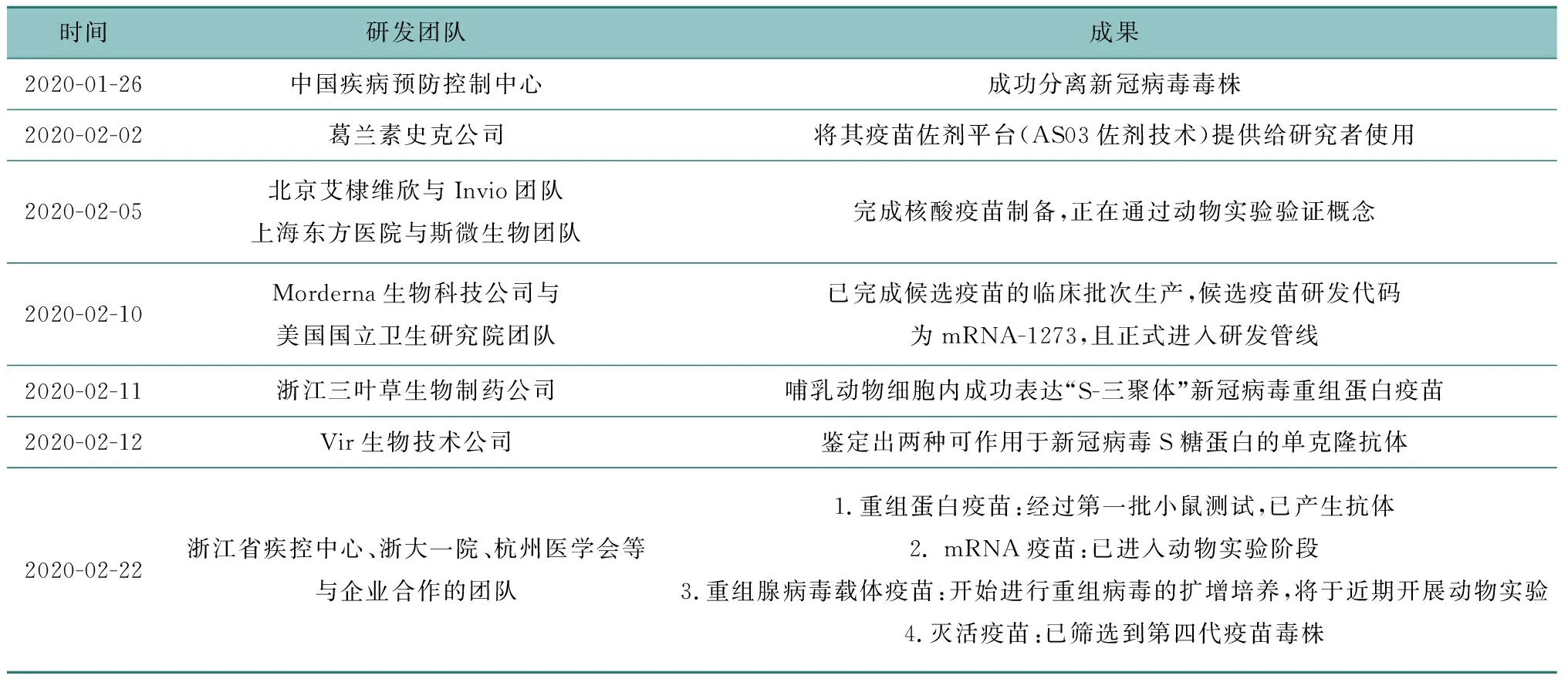
表3 2019-nCoV的疫苗研究进展
3 2019-nCoV与其他病毒的相似性
虽然2019-nCoV是一种新发现的冠状病毒,但是与本文所述其他病毒间仍存在一定的联系,具体如表4所示[6, 49, 56]。

表4 2019-nCoV 与流感病毒、HCoV-229E、HCoV-OC43、HCoV-NL63、HCoV-HKU1、SARS-CoV、MERS-CoV的主要相似性
基于上述多种相似性,我们在氨基酸水平上对2019-nCoV的S糖蛋白与A和B型流感病毒的HA糖蛋白进行了序列比对,如表5和图2所示。比对结果显示,2019-nCoV的S糖蛋白与流感病毒的HA糖蛋白之间具有一定的一致性。由于HA糖蛋白上具有抗原决定簇,可以刺激宿主机体产生免疫反应,进而生成相应抗体[10]。因此基于氨基酸序列比对结果中存在的一致性,我们推测,2019-nCoV的S糖蛋白上可能也具有与HA糖蛋白相似的抗原决定簇。当季节性商用流感病毒疫苗作用机体后,体内产生的抗体在一定程度上也能识别2019-nCoV的S糖蛋白,并与其相互作用,阻断S糖蛋白宿主细胞受体ACE2的结合。
由于在氨基酸水平上2019-nCoV 的S糖蛋白和N核蛋白与SARS-CoV也具有高度的相似性,而SARS-CoV疫苗又主要是在上述两种蛋白的基础上制备而来[56],因此我们推测,机体经SARS-CoV疫苗刺激后产生的抗体可能也会识别并作用2019-nCoV 的S糖蛋白与N核蛋白,进而干扰病毒颗粒对宿主细胞的入侵。

表5 2019-nCoV的S糖蛋白与流感病毒的HA糖蛋白的一致性

*表示序列一致;. 表示序列相似图2 2019-nCoV的S糖蛋白与流感病毒的HA糖蛋白氨基酸水平序列比对结果Fig 2 The amino acid sequences comparison results between spike of 2019-nCoV and HA of Influenza virus
4 结论
为了分析现有病毒疫苗用于防治新冠肺炎的可行性,本文对流感病毒和7种冠状病毒(HCoV-229E, HCoV-OC43, HCoV-NL63, HCoV-HKU1, SARS-CoV MERS-CoV和2019-nCoV)进行了综述,并通过氨基酸水平的序列比对发现,2019-nCoV的S糖蛋白与H1N1、H3N2、B型Victoria系和B型Yamagata系流感病毒的HA糖蛋白之间具有一定的相似性,2019-nCoV的 S糖蛋白和N核蛋白与SARS-CoV也具有高度的相似性。基于此,我们建议:
(1)在目前病毒爆发的态势下,流感疫苗和实验性SARS-CoV疫苗在2019-nCoV防控方面可能具有一定的应用潜能。虽然就特异性而言,这些疫苗不是最理想的,但是由于商业流感疫苗的安全性已得到证实,且一些SARS-CoV疫苗已经进入中国临床试验阶段,因此可以考虑在短期内将其作为2019-nCoV特效疫苗的替代物使用。
(2)可以考虑给2019-nCoV的高危易感人群,例如儿童、孕妇、老人以及长期奋战在一线的医务工作者们注射现有的季节性商用流感疫苗,从而提高他们自身的抗病毒能力。
