可降解生物镁合金材料的研究现状
2020-05-06彭泽惠喻正文刘建国
彭泽惠,喻正文,刘建国,
(1.遵义医科大学 口腔医学院,贵州 遵义 563099;2.遵义医科大学 贵州省普通高等学校口腔疾病研究特色重点实验室暨遵义市口腔疾病研究重点实验室,贵州 遵义 563099)
每年因外伤、肿瘤造成的骨折和骨缺损患者高达数千万,其治疗需要各类医用生物材料,目前常用于临床的医用生物材料有:316L不锈钢、钛及钛合金、钴铬合金、镍钛合金等金属医用生物材料,但在临床应用过程中发现,传统金属医用生物材料存在众多不足:①医用生物材料的弹性模量较高(钛及钛合金:103 ~ 110 GPa,316L不锈钢:190 GPa,钴铬合金:200 GPa),在修复损伤骨组织时易诱发“应力遮挡”效应,导致局部骨质疏松或骨折[1];②金属生物材料因生物腐蚀释放的金属离子或颗粒,易诱发损伤骨组织周围炎症反应,延长损伤骨组织愈合时间;③金属生物材料制备骨钉、骨板、骨针、支架材料等临时性植入材料时,愈后需二次手术取出,不仅造成患者身心和经济负担,还极易引发二次损伤,严重时可导致二次骨折。为此,研发新型的高性能可降解金属医用生物材料,已逐渐成为材料研究领域的热点和难点。
镁合金同传统金属医用生物材料相比,具有以下优点:①镁合金生物材料具有与人体天然骨组织接近的弹性模量(40 ~ 45 GPa),能显著缓解金属植入材料引起的应力遮挡效应;②镁及镁合金生物材料具有与人体皮质骨接近的密度(1.75 g/cm3);③Mg是人体必需的元素(Mg在人体中的正常含量为25g,其中大部分存在于骨组织中),能显著激活生物体内多种酶、抑制神经异常兴奋、维持核酸结构的稳定性、参与蛋白质合成、调节体温等。此外,最新研究还表明Mg元素影响Na、K、Ca等离子细胞内外分子通路,有利于促进Ca离子的沉积,形成新生骨组织。
尽管如此,镁合金生物材料仍然存在着许多不足。金属Mg因其较低的标准电极电位(-2.36 VSCE),在植入生物体内后易发生腐蚀,导致镁及镁合金生物材料具有较差的耐腐蚀降解性能,尤其是生物体液中大量存在的Cl离子,加速了生物镁合金植入材料的腐蚀降解,致使植入材料丧失力学稳定性,不利于新生骨组织再生空间的建立和保持,是阻碍生物镁合金材料在医学领域进一步推广应用的主要原因。因此,设计并研发具有良好生物腐蚀降解性能的植入材料,一直是镁合金生物材料研究领域的热点和难点。本文对近些年来镁合金生物材料在腐蚀性能、生物学性能领域的研究进展进行了归纳总结。
1 镁合金生物材料的研究现状
20世纪初,金属Mg作为骨科植入材料,在临床上得到较为广泛的应用。但是,由于体液的作用,金属Mg植入体内后发生严重腐蚀,导致术后纯Mg骨钉破裂,并在患处产生大量气泡,致使医用镁及镁合金生物材料曾一度退出生物医学领域。尽管如此,随着人们对镁及镁合金腐蚀降解机制认识的深入,以及对植入材料强韧化机制研究的不断深入,发现对纯镁生物材料进行合金化处理、表面改性处理、复合化处理后,可显著改善镁及镁合金生物材料的生物腐蚀降解性能、力学性能、生物学性能等。
1.1 镁合金生物材料合金化元素选择 生物镁合金的设计,不仅要求材料具有优异的力学性能、物理性能和化学稳定性,还要求植入材料具备良好的生物学性能。为此,在设计新型生物镁合金植入材料时,选择合适的合金化元素,不仅有利于改善植入材料的生物腐蚀降解性能,提高其生物体内力学稳定性,还有利于增强植入材料诱导细胞成骨、成纤维以及血管内皮化等生物学功能。根据合金元素的性质,目前可供选择的合金化元素主要有Al、Si、Ca、Mn、RE等。
1.1.1 Mg-Al系生物镁合金 Al元素是镁合金中重要的合金元素之一,有研究表明,添加1%~5%Al元素后,材料的微观组织显著细化[2],同时随着Al元素含量的增加,材料中析出了大量的第二相Mg17Al12,白力静等研究了Mg17Al12相含量和分布形态,对AZ91镁合金耐腐蚀性的影响,发现β相为13% (质量分数) 且为连续分布时,合金的耐腐蚀性最好[3],且第二相Mg17Al12被验证为具有优异的细胞相容性[4]。尽管如此,由于Al元素被证明是引起老年痴呆症主要的原因[5]。因此,在设计和制备镁合金生物材料时,必须考虑Al元素对细胞的影响。AZ91D镁合金显示出良好的细胞相容性[6]。Liu等对Mg-Al-Zn合金生物相容性的研究发现,Mg-Al-Zn对L929、MC3T3-E1、BMSCs细胞均无细胞毒性[4]。其中细胞黏附实验结果(见图1),Mg-Al-Zn上粘附细胞数明显高于纯Mg表面。Mg-Al-Zn表面细胞数量随培养时间的延长而明显增多。而对于纯Mg,表面产生了越来越多的点状腐蚀产物,影响细胞在纯Mg表面的生长。
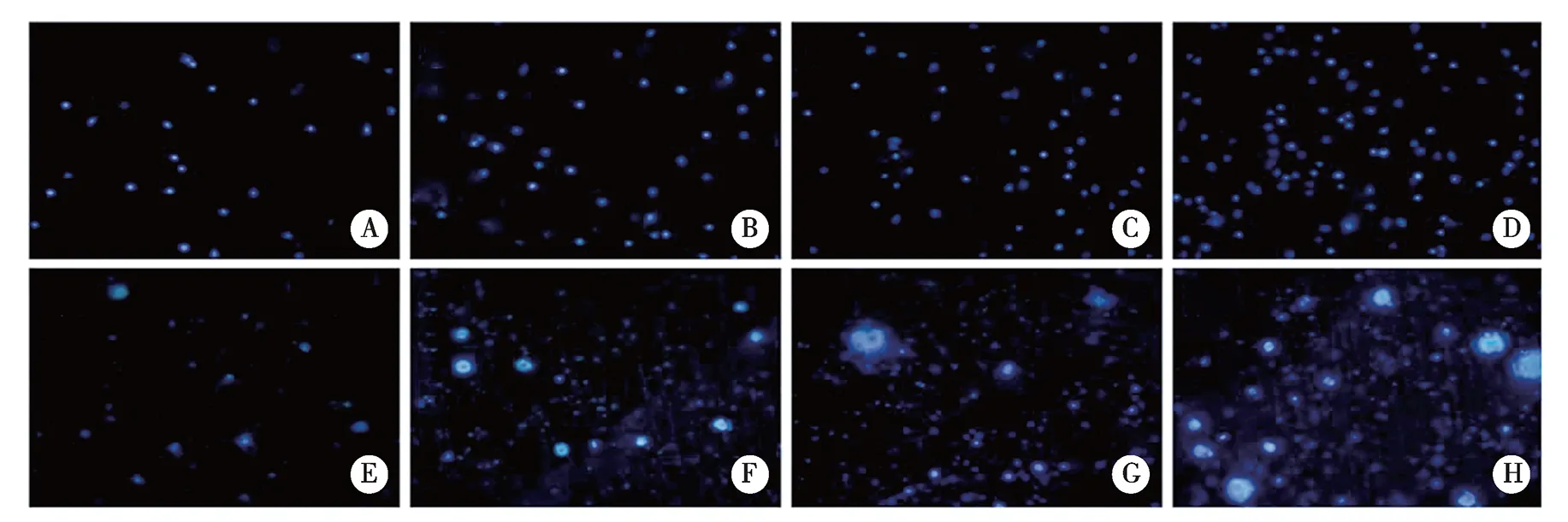
A:Mg-Al-Zn,30 min;B:Mg-Al-Zn,60 min;C:Mg-Al-Zn,90 min;D:Mg-Al-Zn,120 min;E:纯Mg,30 min;F:纯Mg,60 min;G:纯Mg,90 min;H:纯Mg,120 min[4]。图1 MC3T3-E1粘附在Mg-Al-Zn和纯Mg上的荧光图像
1.1.2 Mg-Ca系生物镁合金 Ca作为骨骼的主要成分,是人体内一种重要的矿物质元素,对化学传导起着至关重要的作用[7-8]。近年来实验研究表明,Mg-Ca合金的显微组织随Ca含量的增加得到细化,并且合金的抗压强度和屈服强度随Ca含量的增加而增大[9]。但较多实验表明,随着Ca含量增加,Mg-Ca合金的腐蚀速率逐渐增大[10-11]。Zheng 等建议医用镁合金中Ca 元素含量应制控在0.6%~1.0%[12]。Mg-Ca合金具有良好的细胞生物相容性和成骨性能[13]。Li等[14]设计了二元Mg-Ca合金,并进行了细胞毒性实验,结果表明Mg-Ca合金没有表现出细胞毒性,呈现较好的细胞相容性(见图2),符合临床医用的基本要求。而且最近研究表明,Mg-0.8Ca对HEK293细胞无细胞毒性[15]。Erdamann等比较了可降解镁钙合金(Mg-0.8Ca)螺钉与常用不锈钢(S316L)螺钉的生物力学性能,评价Mg-0.8Ca在体内的降解行为[16]。将Mg-0.8Ca螺钉和S316L螺钉分别植入成年家兔胫骨,随访2、4、6、8周。研究结果显示Mg-0.8Ca在植入后2~3周具有良好的耐受性和生物力学性能。Li等将镁钙合金棒植入兔股骨中,3个月后金属棒完全降解,病检发现植入部位有新生骨生成[13]。

A:2 d;B:4 d;C:7 d的光学形态[14]。图2 不同浓度Mg-1Ca合金对L-929细胞的影响
1.1.3 Mg-Zn系生物镁合金 Zn是一种无毒元素,作为某些酶的辅助因子在人体代谢中发挥重要作用,对免疫系统至关重要[17-18]。Zn具有良好的生物相容性,人体血清中Zn含量约为806~1131 μg/L,成年人每天需要摄入15mgZn满足新陈代谢的需求,过量的Zn可以通过肠胃和肾脏代谢排出体外。Zn缺乏则会降低成骨细胞活性与碱性磷酸酶活性[19]。Zn是一种重要合金元素,在镁中溶解度最高可达6.2 wt%,Zn含量达到4 wt%时,铸态镁合金的极限抗拉程度和延伸率显著增高,但随着Zn含量越高,则合金的性能和耐蚀性均降低[20-22]。将Mg-Zn合金与MC3T3-E1、L-929细胞共培养时,研究结果均证明Mg-Zn合金无细胞毒性[21,23-25],并在兔股骨植入模型中,观察到Mg-Zn合金植入物周围新骨形成的现象(图3所示)。非晶态Mg-5Zn合金在动物体内具有优良的强度,高耐蚀性、低析氢率和良好生物相容性[20]。这些研究结果表明,Mg-Zn合金具有优异的耐腐蚀性能、力学性能、生物相容性,可作为可降解植入物的应用。
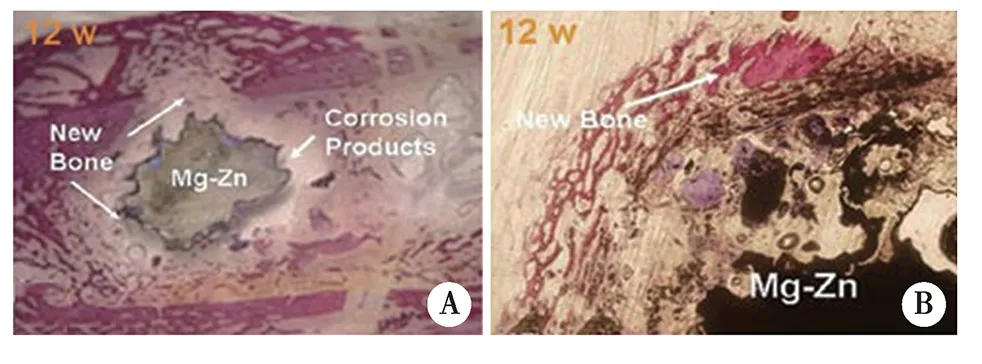
A:×40 ;B:×100 [23] 。图3 van Gieson 染色的Mg-Zn合金植入界面的组织切片
1.1.4 Mg-Mn系生物镁合金 Mn是脂类、氨基酸和碳水化合物代谢循环中起重要作用的基本元素,它还影响免疫系统的功能、骨骼生长和血液凝固[26]。在镁合金中,锰主要用于增强延展性。更重要的是,在含铝的镁合金中,形成铝锰金属间相。这些相可以吸收铁,抑制铁对腐蚀行为的有害影响,用于控制镁合金的腐蚀。对于改善Mg-Mn合金的腐蚀性能,Kim等[27]从制作工艺上对其进行了研究,证明HRDSR工艺能显著提高合金的硬度,改善合金的腐蚀性能。多项研究表明,Mn在细胞培养过程中无毒影响[28]。在镁锰锌合金作为大鼠股骨植骨材料的体内试验研究表明,镁锰锌合金具有良好的生物相容性,炎症和肾功能失调未发生并且相对于9周前,在植入后第18周发现更多的新骨形成(见图4)[29]。

A:种植后9周;B:种植后18周(M、金属;D、退化层;N、新骨)[29] 。图4 Mg-Mn-Zn植入物与骨结合断面的光学图像
1.1.5 Mg-RE系生物镁合金 镁合金中的稀土元素主要用于增强和改善耐蚀性[30]。稀土元素总共包含17种,即钪(Sc)、钇(Y)、镧(La)、铈(Ce)、镨(Pr)、钕(Nd)、铕(Eu)、钆(Gd)、铽(Tb)、镝(Dy)、钬(Ho)、铒(Er)、铥(Tm)、镱(Yb)、 镥(Lu)和钷(Pm)。通过中间合金或所谓的硬化剂将它们引入镁合金中,这些中间合金主要包含1或2种稀土元素以及几乎所有其它少量的稀土元素。在镁合金的ASTM命名法中,稀土元素统一用E表示,但钇特别用W表示。
Drynda等人用16种稀土元素(不包括放射性元素Pm)的三价氯化物培养人血管平滑肌细胞(VSMC),发现低浓度的稀土金属对VSMC的增殖没有重大不利影响[31]。 Feyerabend等建议,对于在镁中具有高固溶度的稀土元素,Gd和Dy比Y更合适,而Eu,Nd和Pr是对镁的低溶解度合适的元素[32]。 La和Ce具有很高的细胞毒性,因此应谨慎使用。
当前发明的用于生物医学的基于Mg-RE的合金包括JDBM、WE43、LAE442等[33-36]。其中,WE43合金因其优异的机械性能和耐腐蚀性而被广泛研究。张等制备了一种新型的Mg-Nd-Zn-Zr合金(称为JDBM),其力学性能和耐腐蚀性优于WE43[37]。Castellani等将Mg-Y-Nd-HRE和Ti-6Al-7Nb分别植入大鼠两侧股骨,研究表明,可生物降解镁合金棒的骨-植入界面强度显著高于钛对照组[38]。Micro-CT显示骨组织对镁合金的反应增强,表现为骨与种植体接触显著增加。此外,在任何试验动物中均未观察到严重的炎症反应。实验结果清楚地表明,所测试的镁合金比目前使用的钛合金具有更高的植入稳定性和骨整合性。LAE442支架动物体内研究表明,LAE442支架缓慢、均匀的降解显示出优异的腐蚀降解性能,并观察到良好成骨现象[39]。
1.2 表面改性镁合金生物材料 为了有效地提高镁合金在生理环境中的耐腐蚀性,并保持其机械完整性和改善界面生物相容性,已开发了各种表面改性方法。与合金化技术不同,表面改性可将镁合金与周围的生物环境直接隔离开,并防止体液渗透到基体中。 根据镁合金表面是否产生新的相,表面改性的方法可以分为三类:化学改性、物理改性以及这两种方法的结合[40]。
1.2.1 化学改性 化学改性去除了由于Mg基体的高反应性而易于形成的天然氧化层,该氧化层的钝化性质不能有效地防止腐蚀。化学改性通常包括酸蚀刻、碱热处理、氟化物处理、阳极氧化和微弧氧化(MAO)[40]。
1.2.2 物理改性 与化学改性方法不同,在表面和基体之间没有形成化学键。物理改性是提供一个物理屏障,以提高镁基板的耐腐蚀性。物理改性可以通过引入磷灰石涂层、聚合物涂层、激光表面处理或冷喷涂涂层来实现[40-41]。
1.2.3 化学结合物理改性 考虑到单一化学和物理处理的局限性,涉及化学结合物理处理的复合改性引起越来越多关注。据报道,双改性层可有效提高基材的抗生物降解性,并在较大范围内控制降解速率[40]。郭等在其上制造了MAO /聚L-乳酸(PLLA)复合涂层WE42合金表面通过物理互锁将PLLA密封到MAO涂层上。发现该MAO/PLLA改性的WE42合金具有良好的耐腐蚀性和细胞相容性。
1.3 镁基复合生物材料 镁基复合材料由于其低密度、良好的机械和物理性能而成为航空航天和国防领域应用的潜在材料。与常规工程材料相比,向金属基质中添加增强元素会显着影响比强度、刚度、阻尼性能、磨损性能、蠕变和疲劳性能的改善。在可生物降解的复合物中,所有组分必须是生物相容的、可生物降解的并且对生理状况无毒。目前研究表明,磷酸钙基陶瓷被用作镁复合材料的增强材料,治愈骨折组织,并在毒性和免疫反应方面表现出出色的性能。现有聚磷酸钙颗粒(CPP),羟基磷灰石(HAP)和磷酸三钙(β-TCP)[42-45]等磷酸钙基陶瓷作为镁增强复合材料。
2 展望
具有生物相容性的镁及其合金在人体体液中易于腐蚀而不产生任何有毒物质的能力,使其成为最适合生物降解的临时植入物的候选材料之一。然而,非常高的腐蚀速率限制了它们作为植入物的使用,在愈合完成之前,它们很有可能降解,从而影响愈合。为了提高镁合金的耐腐蚀性,可以通过合金化、表面改性和复合化处理等方法。镁合金材料的研究需在减缓降解速率和如何使得镁合金的降解速度与骨形成的速度相匹配,从而提供一个稳定的成骨空间仍需要进一步探究。进一步完善腐蚀性能的生物医用镁合金在骨科及外创手术领域具有巨大应用潜力。
