褐煤负载有机钠盐水蒸气气化实验与动力学分析*
2020-04-24韩志杰王雪颖崔孝洋李昊洋肖显斌郑宗明
韩志杰 王雪颖 崔孝洋 李昊洋 肖显斌 郑宗明
(生物质成套设备国家工程实验室,华北电力大学,102206 北京)
0 引 言
煤炭是我国消费占比最大的化石能源,在为社会发展做出巨大贡献的同时,煤炭的直接燃烧也对环境产生了巨大的污染,由于褐煤的有机组成成分和比表面积特性,直接燃烧并不能发挥其最大潜能,因此,为了减少煤炭利用过程中对环境的污染,煤的气化是未来煤炭清洁利用的重要研究方向。近些年来,煤的催化气化受到了国内外学者的广泛关注。大量研究证实[1-4],碱金属是煤气化技术中良好的催化剂,国内外研究团队在碱金属催化方面取得不少成果。BAI et al[5]研究了煤焦在四种气化剂(空气、CO、H2、H2O)条件下碱金属的催化性能,发现水蒸气条件下碱金属催化性能由强到弱依次为K,Ca,Na;在O2和CO2条件下,碱金属催化性能由强到弱依次为Na,K,Ca。在进行SJH高铝煤的水蒸气气化实验当中,WANG et al[6]分别用Na2CO3和K2CO3作为催化剂在800 ℃条件下进行气化实验,结果表明,Na2CO3比K2CO3具有更高的催化活性。
碱金属作催化剂的催化气化方法多年来仍处于实验室及中试研发阶段[7-9],其催化剂的成本与回收以及二次污染等因素明显影响着实际工业化进程。工业废碱液(纸浆黑液、黏胶纤维废液、双马来酰亚胺工业废液等)中含有大量的碱金属离子,这些工业废碱液比金属盐更廉价,经济性更高,但目前以碱金属无机物为催化剂的研究成果报道较多,而以废液中有机催化剂进行煤催化气化的报道较少。张济宇等[10]研究了十二烷基苯磺酸钠(LAS)和柠檬酸三钠(NMS-NA)两种有机钠盐对无烟煤的水蒸气气化动力学,并与Na2CO3作催化剂进行了比较,发现在相同负载浓度条件下,LAS有机催化剂与Na2CO3具有接近的气化反应动力学,LAS中的Na元素质量分数为0.79%,远低于Na2CO3中的Na元素质量分数5.21%,说明LAS有机钠催化剂是良好的煤进行水蒸气气化的催化剂。
双马来酰亚胺工业废液中含有大量的醋酸钠,具有很高的回收利用价值[11]。为进一步研究利用废液中的有机催化剂,本实验模拟双马来酰亚胺工业废液的特性,将乙酸钠和碳酸钠分别负载到褐煤上进行固定床气化实验,对影响气化结果的反应温度和催化剂负载浓度进行研究,比较乙酸钠和碳酸钠作用的不同,并对实验结果进行动力学分析,比较两种不同的动力学模型对本实验结果描述的差异,分析两种催化条件下的动力学特点,为利用双马来酰亚胺工业废液开发新型催化剂提供参考。
1 实验部分
1.1 原料及样品制备
实验用煤为内蒙古宝日希勒褐煤,依据国标GB/T 31391-2015[12]和国标GB/T 212-2008[13]进行的工业分析和元素分析如表1所示。

表1 褐煤样品工业分析
实验试剂有无水碳酸钠(Na2CO3)、乙酸钠(CH2COONa)和去离子水,载气为氮气。
实验用浸渍法[14-15]将钠盐负载到褐煤上,具体步骤如下:
1)首先将褐煤用磨煤机进行粉碎,筛出其中粒径为0.045 mm~0.078 mm之间的煤粉,干燥后收集备用;
2)称取12 g的褐煤样品分为三组,一组为只有褐煤的对照组,另外两组分别与碳酸钠或乙酸钠在烧杯当中进行混合,加入足量的去离子水,用磁力搅拌器在40 ℃条件下搅拌0.5 h之后冷却至室温。碱金属化合物的负载浓度分别是5%,10%,15%;
3)将步骤2)中磁力搅拌器处理后的混合溶液在室温条件下静置24 h,使其中的碱金属盐充分负载到褐煤上;
4)将静置后的褐煤溶液放入电热恒温鼓风干燥箱,在105 ℃条件下将溶液中的水分缓慢蒸干,干燥时间为24 h,放入干燥器中冷却至室温后收集分别负载了碳酸钠和乙酸钠的褐煤备用。
1.2 实验装置及步骤
实验装置如图1所示。

图1 实验装置
用负载了不同浓度乙酸钠的褐煤与水蒸气进行气化重整反应,模拟碱性有机废液与褐煤进行水蒸气重整气化的反应,具体操作步骤如下:首先将称取负载乙酸钠的1 g褐煤样品放入石英管,连接反应系统进行密封后,用高纯氮气对反应系统进行吹扫,氮气流速为0.45 L/min,吹扫反应系统10 min后,以在线气相色谱测量其中的气体组成,确保氧气含量在混合气体中的体积分数不超过0.5%,然后停止通氮气,打开温度控制器开始对反应体系进行加热,加热到反应温度之后,打开注射泵,将水蒸气通入石英管,同时将载气打开,用注射泵控制水蒸气的速度为4 mL/h,连续通入0.5 h;控制氮气的流速为0.15 L/min,并以此为起点开始用在线气相色谱测量反应系统排出的气体组分,反应系统排出的混合气体组分要先经过冷凝器再经过干燥器,以脱除组分中的焦油和水蒸气。气相色谱主要测量组分中的CO,H2,CO2,CH4和N2,氮气除了用作载气,还用来表征产气组分当中其他各种气体的流速,在线气相色谱进行测量的时间间隔为5 min。
用负载了不同浓度碳酸钠的褐煤、未负载催化剂的褐煤分别进行水蒸气气化反应,反应步骤同上,比较三种情况下褐煤的气化特性。
1.3 数据处理方法
1.3.1 单一气体产气计算
根据在线气相色谱当中各种气体的体积分数,计算H2,CO,CH4和CO2的气体总浓度[16-17]。
样品煤产生的气化合成气中单一气体的体积浓度以式(1)计算:
(1)
式中:Ci表示气体的体积分数,%;i表示H2,CO,CH4和CO2中任一气体;t表示实验测量的时间,min;φi表示在线气相色谱中对应气体的体积分数,%;v表示通过实验系统出口处的合成气体积流量,L/min。
气体总体积按照式(2)计算:
(2)
式中:vN2表示通入实验系统中氮气的入口体积流量,L/min;φN2表示氮气在混合气体中的体积分数,%。
1.3.2 碳转化率计算
碳转化率(x)[6,18]按照下式计算:
(3)
式中:x表示气化反应的碳转化率,%;nc表示反应物当中的碳元素的总含量,mol。
1.3.3 均相模型
均相模型[19-21]指煤在气化反应过程中,主要阻力是化学反应阻力,而不是气化剂在煤颗粒内部和表面扩散速率不同产生的阻力,颗粒体积不会影响煤气化反应速率,因此,将均相模型与均相体系进行类比之后,可以将煤气化反应速率表达为:
(4)
式中:t表示时间,min;x表示对应于时间t的碳转化率,%;A表示Arrhenius方程当中的指前因子,无量纲;E表示化学反应活化能,kJ/mol;R表示摩尔气体常数,kJ/(mol·K);T表示绝对温度,K。
1.3.4 缩核模型
缩核模型[21]假设气化剂与煤的气化反应只发生在类似球状的颗粒反应物的表面,主要阻力为气固反应过程当中,气化剂在反应颗粒表面的边界层以及在颗粒外部已经完成气化反应,但剩余的灰层仍覆盖在煤颗粒表面,对气体扩散产生阻力。反应速率的主要影响因素为反应颗粒的表面积以及颗粒中剩余反应物的量,即缩核反应是逐步向内层反应。因此,缩核反应的反应动力学方程可以表示为:

(5)
(6)
式中:t表示时间,min;x表示时间t对应的碳转化率,%;k表示缩核反应的表面反应速率常数,min-1;E表示化学反应活化能,kJ/mol;R表示摩尔气体常数,kJ/(mol·K);T表示绝对温度,K。
2 结果与讨论
2.1 褐煤水蒸气气化产物组成
由在线气相色谱分析可知,褐煤水蒸气气化产物主要有CO2,CO,CH4和H2。负载不同浓度Na2CO3和CH3COONa的褐煤气化产物分布见图2和图3。对比图2和图3可以看出,氢气的体积大致上为CO2产气体积的两倍左右,与MUANGRAT et al[22]实验中氢气和二氧化碳的产气比例基本相符,这是因为负载乙酸钠的褐煤在气化过程中,使用的气化剂水蒸气是过量的。气化反应过程中主要发生以下三类[21-23]反应:

ΔH=131.28 kJ/mol
(7)

ΔH=-41.2 kJ/mol
(8)

ΔH=172.45 kJ/mol
(9)
由以上三个反应式可以看出,水蒸气组分足量或者过量的时候,主要发生的反应为式(7)和式(8),因此在最终结果中,含量最高的组分是氢气和二氧化碳,二者的体积比接近于2∶1。在褐煤的水蒸气重整反应中,还会反生微量的以下反应(见式(10)和式(11)[24])。

ΔH=-74.81 kJ/mol
(10)

ΔH=206.4 kJ/mol
(11)
依据化学反应平衡的移动方向,式(11)的甲烷水蒸气重整反应由于在反应系统中含有的足量水蒸气而导致反应向右侧移动,因此生成的甲烷含量占比接近于0。
由图2a和图3a可以看出,产氢体积随着催化剂负载量的增加先增加后减少;随着温度的升高,产氢量增加。这是因为在褐煤的水蒸气催化重整反应中产生氢气的反应主要为式(7)和式(8),式(7)为吸热反应,升高温度有利于反应平衡向产生氢气的方向移动。式(8)虽然是放热反应,但反应物中的CO是由式(9)中的反应产生,随着温度升高,可能会促进其产生更多的CO。MA et al[23]的研究也证明了此观点。
对比图2d和图3d可以看出,在800 ℃条件下碳酸钠作为催化剂比乙酸钠作为催化剂能获得更高的氢气产量,说明在此温度下,乙酸钠比碳酸钠具有更强的催化作用。
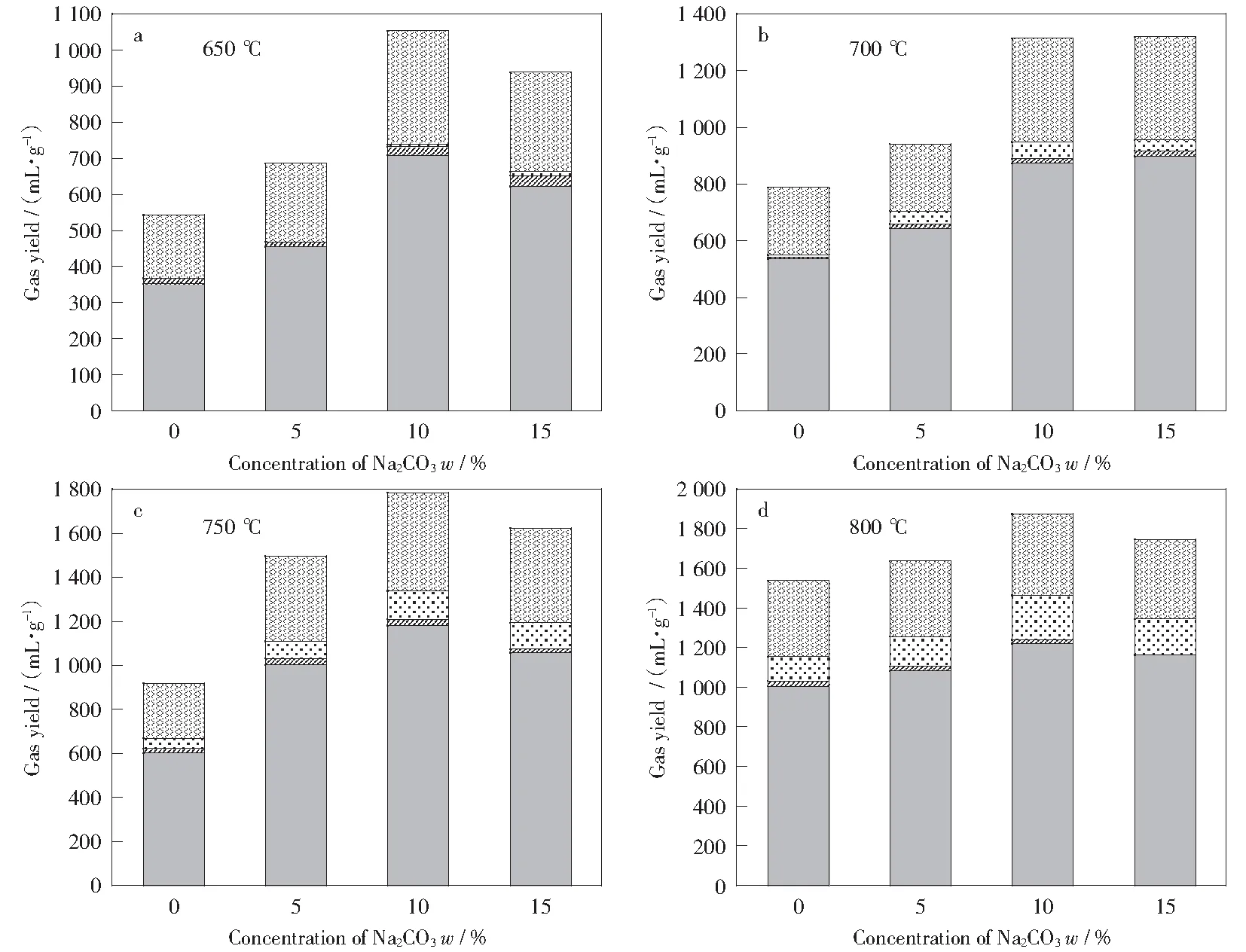
图2 650 ℃~800 ℃条件下负载不同浓度碳酸钠的褐煤产气分布

图3 650 ℃~800 ℃条件下负载不同浓度乙酸钠的褐煤产气分布
2.2 碳转化率随负载催化剂浓度的变化特性
气化温度越高,褐煤中的有机物分解越多,可能会对结果分析产生影响,因此选用700 ℃时的碳转化率进行分析。700 ℃时负载不同浓度碳酸钠和乙酸钠的褐煤气化的碳转化率见图4和图5。由图4可以看出,提高Na2CO3浓度可以提高气化反应速率,最大碳转化率也在提高。MEI et al[14]在实验中也是以Na2CO3作为催化剂,结果与本实验基本吻合。
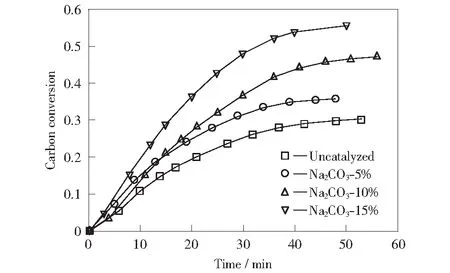
图4 700 ℃时负载碳酸钠浓度对褐煤气化的影响
图5为700 ℃条件下,负载乙酸钠的褐煤在水蒸气气化过程中碳转化率随时间的变化曲线。在负载催化剂浓度为0%~10%区间中,随着负载浓度的增加,催化气化的作用逐渐增强,与蒋友华等[10]在有机钠盐催化无烟煤气化的过程中得到的碳转化率随时间变化的曲线结果相一致。但是,当其中负载乙酸钠的浓度增加到15%时,其碳转化率曲线反而下降,可能是由于在反应体系中的Na元素含量增大,出现了过高浓度的催化剂,堵塞微孔表面,从而导致催化气化效果降低。碳酸钠作为催化剂并没有因为浓度增加而出现抑制现象。
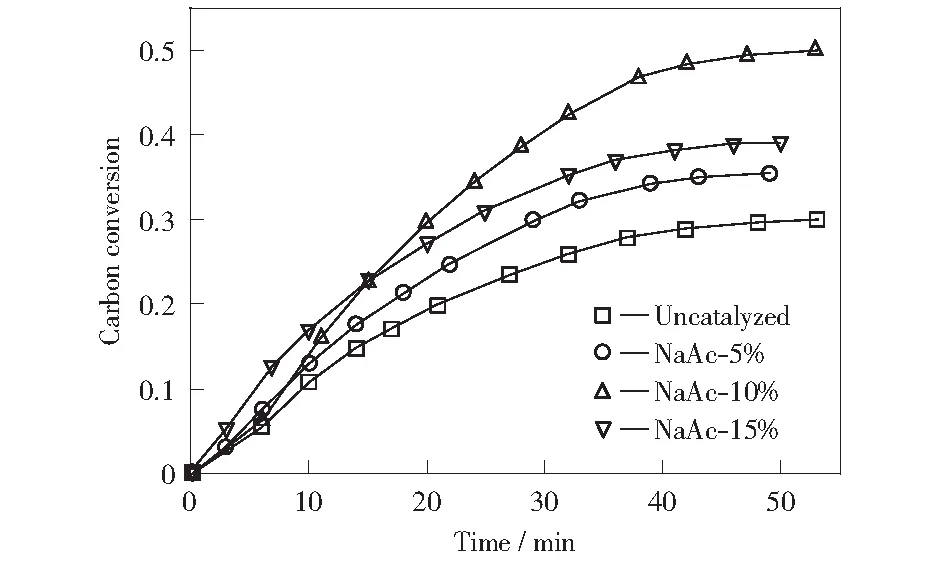
图5 700 ℃时负载乙酸钠浓度对褐煤气化的影响
2.3 碳转化率随温度的变化特性
本研究建立的褐煤供热碱性有机废液气化工艺流程中,主要研究目标是在600 ℃~800 ℃条件下实现最高的气转化效率。由实验结果可知,负载催化剂浓度为15%时,气化转化效率最高,因此选择负载15%乙酸钠的褐煤进行分析,并与无催化对照组进行对比。图6为无催化条件下褐煤碳转化率随温度的变化。由图6可知,碳转化率随着温度的升高而增大,当温度从750 ℃变化到800 ℃时,碳转化率明显提高。WANG et al[25]研究表明,经过处理后的煤焦因不含具有催化作用的成分,在水蒸气气化过程中,只有当温度升到1 000 ℃以上,碳转化率随时间延长才会有明显的提高。而在本实验中使用的褐煤是未经酸洗脱灰处理的褐煤,褐煤中含有碱金属以及碱土金属等具有催化作用的微量成分,因此当温度从750 ℃变化到800 ℃的时候,碳转化率随温度增加有一个较明显的提升。

图6 无催化条件下褐煤碳转化率随温度的变化
图7和图8分别表示负载5%碳酸钠和5%乙酸钠条件下褐煤碳转化率随时间的变化曲线。由图7和图8可知,在650 ℃和700 ℃时,碳转化率的最大值基本相近,表示在此温度区间,褐煤气化反应的主要影响因素为催化剂负载量。由图7可知,以碳酸钠为催化剂的实验中,750 ℃和800 ℃时碳转化率随时间变化的曲线基本相近,表明褐煤的最佳催化气化温度为750 ℃,与KIM et al[26]发现碳酸钾作为催化剂700 ℃是最适宜的实验温度具有相似的结论。在以乙酸钠作为催化剂的水蒸气气化过程中,温度达到800 ℃时,其碳转化率达到90%以上,说明在此条件下乙酸钠具有更高的催化活性。
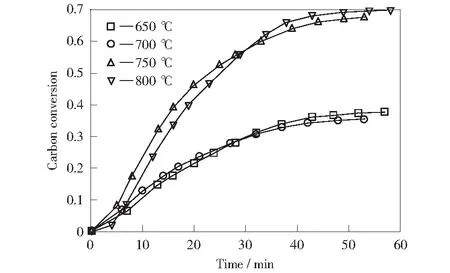
图7 负载15%碳酸钠的褐煤碳转化率随温度的变化
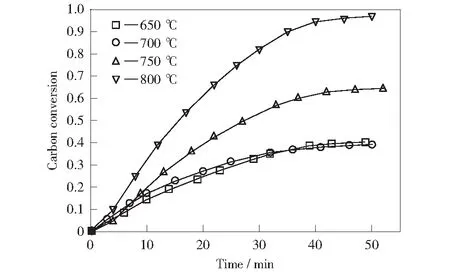
图8 负载15%乙酸钠的褐煤碳转化率随温度的变化
2.4 动力学分析
当乙酸钠的负载浓度为15%时,反应出现抑制现象。若以此条件下的数据作模型,拟合曲线的相关系数不够高。而催化剂负载浓度为10%时,催化效果要明显高于负载浓度为5%的效果。因此,本实验选取10%负载浓度下的数据进行动力学分析。
2.4.1 均相模型
均相模型假设在反应物体系中活性反应中心可以均匀地分布在固体颗粒物内部,反应过程中颗粒的尺寸保持恒定,从而在反应体系中的颗粒物密度会均匀发生变化。对式(4)两侧进行积分得到:
-ln(1-x)=kt
(13)
依据实验数据进行线性回归拟合,拟合结果见图9~图11。
依据图9~图11中数据计算出反应速率常数k以及对应的均方差,结果见表2。
在表2中,本研究得到的反应速率常数与刘洋等[20]得到的准东煤在700 ℃~750 ℃条件下的反应速率常数基本一致,表明实验结果是可信的。并且在相同的温度条件下,负载10%乙酸钠的褐煤比负载10%碳酸钠的褐煤具有更高的反应速率且均高于无催化条件下的反应速率,表明在此条件下乙酸钠的催化效果要优于碳酸钠的催化效果。

图9 无催化条件下均相模型线性拟合

图10 负载10%碳酸钠催化条件下均相模型线性拟合
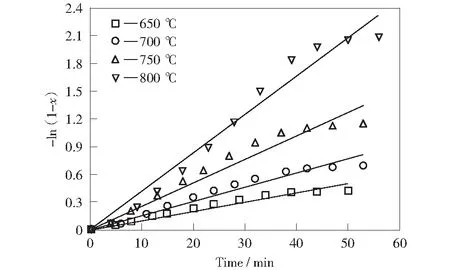
图11 负载10%乙酸钠催化条件下均相模型线性拟合
2.4.2 缩核模型
缩核模型假设气化反应只发生在球形颗粒物表面,影响化学反应速率的主要因素为未反应的反应物的表面积或者反应物的残留量,以化学反应为速率控制步骤,反应级数为2/3。对式(5)积分可以得到:

表2 采用均相模型计算得到的动力学参数和相关系数
3[1-(1-x)1/3]=kt
(14)
依据实验数据进行线性回归拟合,拟合结果见图12~图14。
依据图12~图14中数据求出反应速率常数k以及对应的均方差,结果见表3。
将使用缩核模型计算得出的反应动力学参数与刘洋等[20-21]的研究进行比较。刘洋等[20]的研究温度区间为700 ℃~750 ℃,ZHANG et al[21]研究的温度区间为大于800 ℃,比较后可知,在无催化条件下,本研究得到的反应速率常数与前人的研究结果吻合较好,碱金属催化剂在提高褐煤气化效率上具有明显的效果。
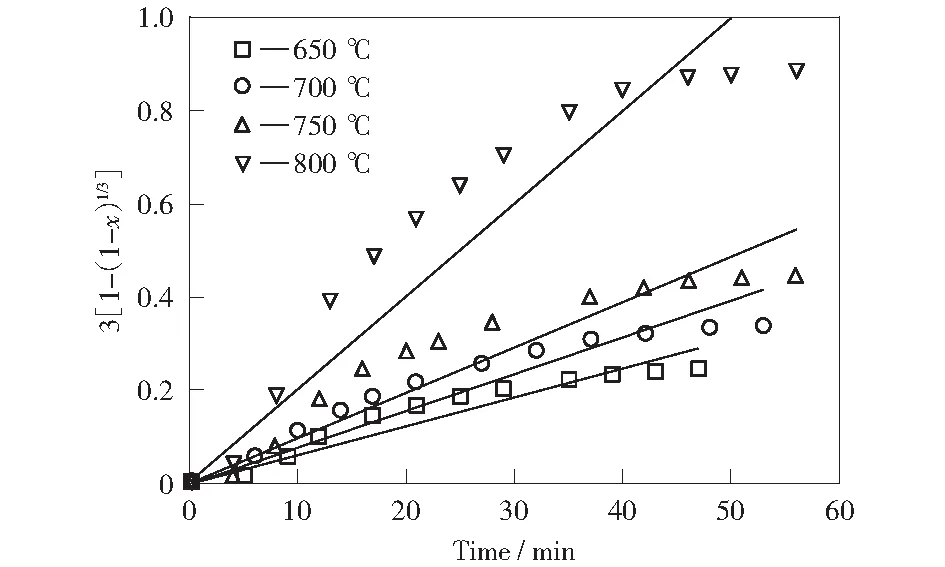
图12 无催化条件下缩核模型线性拟合
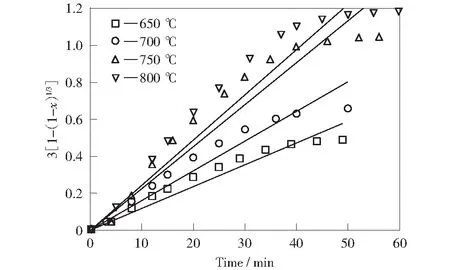
图13 负载10%碳酸钠催化条件下缩核模型线性拟合
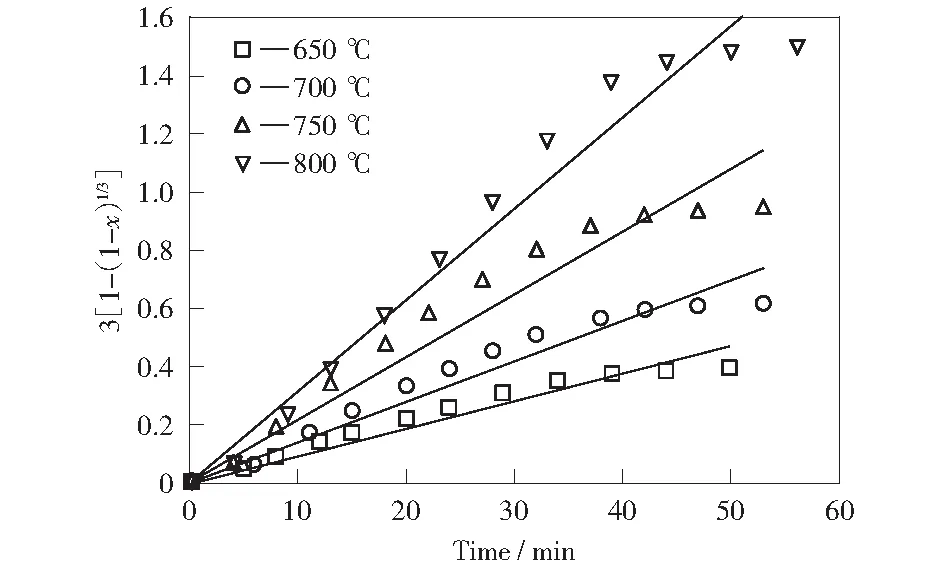
图14 负载10%乙酸钠催化条件下缩核模型线性拟合
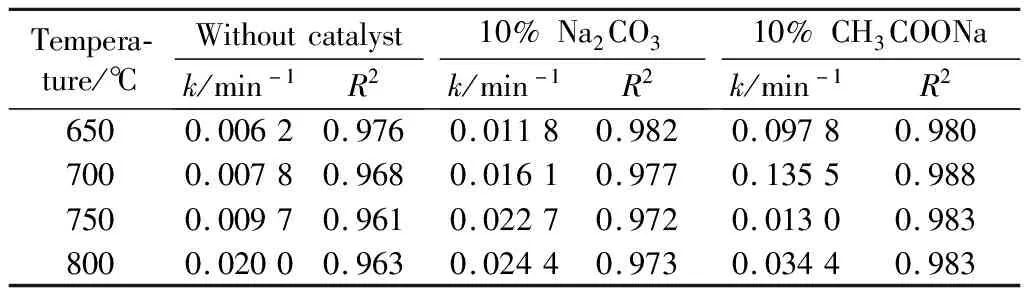
表3 采用缩核模型计算得到的动力学参数和相关系数
3 结 论
1)碳酸钠和乙酸钠作为催化剂对于褐煤水蒸气气化具有明显的催化效果,能够显著提高反应速率和碳转化率。但当乙酸钠的负载量达到15%之后会出现抑制现象,而碳酸钠作为催化剂并没有出现抑制现象。
2)在相同温度或相同催化剂负载浓度的条件下负载乙酸钠的催化效果要优于负载碳酸钠时的催化效果。
3)均相模型和缩合模型都能较好拟合负载乙酸钠和碳酸钠的褐煤水蒸气气化反应,能够得到大于0.97的反应速率回归的相关系数。两种模型均得出:负载10%乙酸钠时褐煤的反应速率大于负载10%碳酸钠时褐煤的反应速率。
