脓毒性休克患者发生急性肾损伤危险因素的Meta分析
2020-03-26闵玉娣权明桃李维维
闵玉娣, 权明桃, 陈 妮, 陈 瑶, 肖 旋, 李维维
(遵义医科大学附属医院护理部, 贵州 遵义 563000)
脓毒性休克(Septic Shock,SS)又称感染性休克,常因病情危重常收治于重症监护室内,具有较高的死亡率[1]。急性肾损伤(Acute Kidney Injury,AKI)是脓毒性休克的常见并发症之一,可显著增加患者住院时长、死亡风险及医疗费用[2]。因此及早识别脓毒性休克患者发生AKI的危险因素,帮助临床医护人员及早进行预防和干预,对于改善患者临床结局至关重要。虽然国内外学者对脓毒症、严重脓毒症、脓毒性休克并发AKI的危险因素进行了研究和总结,但结论不尽相同。因此,本研究采用荟萃分析方法总结脓毒性休克患者AKI的危险因素,探讨AKI高危人群的特征,以期为临床医护人员早期识别和预防提供参考依据。
1 资料与方法
1.1文献检索:中文检索中国生物医学文献数据库、中国知网、万方数据库、维普数据库;英文检索Cochrane、Pubmed、Web of Science、Embase数据库。中文检索式为(脓毒症休克或脓毒性休克或感染性休克)AND(急性肾损伤或肾损伤或肾功能不全或急性肾衰竭)AND(影响因素或危险因素或相关因素或预测因素);英文检索式为(“sepsis shock”OR“septic shock”OR“infectious shock ”OR“infective shock”)AND(“acute kidney injury” OR“acute renal injury”OR“AKI” OR “acute renal failure”OR “acute kindey failure”)AND(“factors” OR “risk factor” OR “influence factor” OR “relevant factor”)。检索时限限制为2018年10月1日。
1.2文献纳入与排除标准:纳入标准:①研究对象年龄≧16岁;②研究类型是病例对照或队列研究;③结局指标为危险因素;④语言是中文或英文。排除标准:①重复发表;②研究对象包含脓毒症或严重脓毒症患者;③动物实验;④无法获取全文;⑤研究数据本研究无法转化应用。
1.3文献筛选与资料提取 :2名研究员独立进行文献筛选的工作,存在不同意见时,由第三方介入评定。将发表年份、研究地点、总样本例数等资料提取至表格中。
1.4文献质量评价:根据Newcastle-Ottawa Scale评价文献质量,涉及研究对象的选择、组间可比性、结果测量等方面,该量表共8个条目总计9分。
1.5统计分析 :采用RevMan5.3进行数据分析。对吸烟、饮酒、高血压等使用比值比(OR),对年龄、APACHEⅡ评分等使用加权均数差(WMD)及95%可信区间(CI)进行描述。若各研究结果间不存在异质性(P>0.1,I2<50%),则采用固定效应模型进行meta分析;若各研究结果间存在异质性(P<0.1,I2≥50%),则采用随机效应模型进行meta分析,以P<0.05为差异有统计学意义。
2 结 果
2.1文献检索结果:共检索出英文1909篇,中文983篇,利用软件去掉重复文献395篇,阅读题目和摘要后纳入158篇,阅读全文后最终纳入9篇文献,其中英文3篇,中文6篇。
2.2纳入文献的基本情况及质量评价:纳入的9篇文献中,2篇为队列研究,7篇为病例对照研究,总人数10142例,病例组6879人,对照组3263人。文献特征及评价结果见表1。
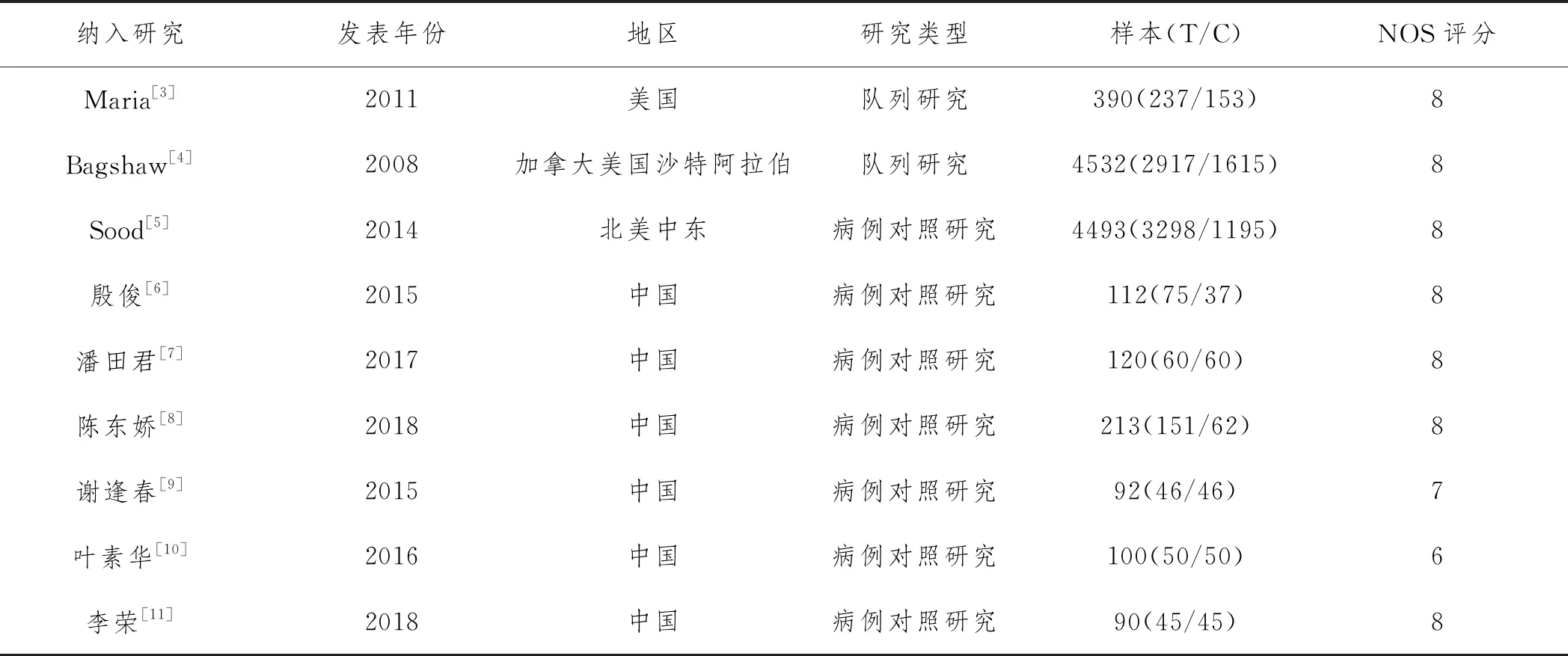
表1 纳入文献的基本情况及质量评价
2.3Meta分析结果
2.3.1年龄:共8个研究[3~5](9752例)分析了年龄与脓毒性休克患者AKI发生的关系,其中1篇队列研究、7篇病例对照研究,将各研究进行合并后存在异质性(P<0.00001,I2=96%)选用随机效应模型进行meta分析,结果显示:年龄不是脓毒性休克患者发生AKI的危险因素[WMD=1.33,95% CI(-1.73,4.38),P=0.39],见图1。

图1 年龄与急性肾损伤发生的森林图
2.3.2吸烟:共6个研究[3,6,7,9~11](904例)对吸烟与脓毒性休克患者AKI发生的关系进行了分析,合并后各研究无异质性(P=0.96,I2=0%),故采用固定效应模型进行meta分析,结果显示:吸烟是脓毒性休克患者发生AKI的危险因素[OR=1.43,95%CI(1.08,1.87),P=0.01],见图2。
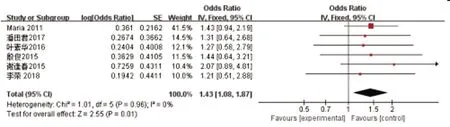
图2 吸烟与急性肾损伤发生的森林图
2.3.3饮酒:共7个研究[3,5~7,7~9](5397例)对饮酒与脓毒性休克患者AKI发生的关系进行了分析,合并后各研究无异质性(P=0.40,I2=4%),选用固定效应模型,结果显示:饮酒不是脓毒性休克患者发生AKI的危险因素[OR=0.90,95% CI(0.77,1.05),P=0.19],见图3。
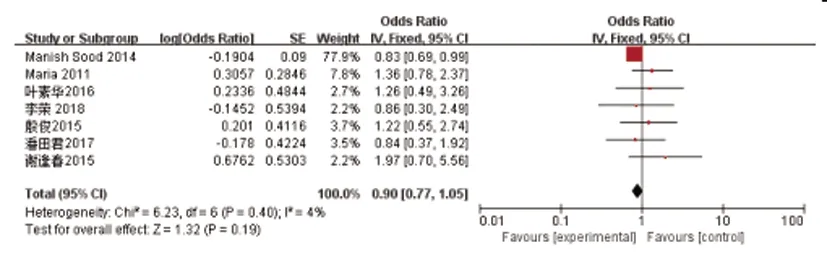
图3 饮酒与急性肾损伤发生的森林图
2.3.4高血压:共7个研究[3,5~7,7~9](5397例)对高血压与脓毒性休克患者AKI发生的关系进行了分析,合并后各研究无异质性(P=0.96,I2=0%),选用固定效应模型,结果显示:高血压与脓毒性休克患者发生AKI存在关系[OR=1.39,95%CI(1.19,1.62),P<0.0001],见图4。
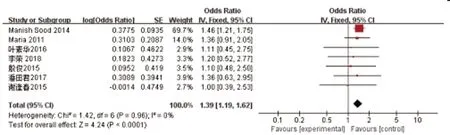
图4 高血压与急性肾损伤发生的森林图
2.3.5糖尿病:共8个研究[4~7,7~9](9752例)对糖尿病与脓毒性休克患者AKI发生的关系进行了分析,合并后不存在无异质性(P=0.49,I2=0%),选用固定效应模型,结果显示:糖尿病是脓毒性休克患者发生AKI的危险因素[OR=1.53,95% CI(1.38,1.69),P<0.00001],见图5。

图5 糖尿病与急性肾损伤发生的森林图
2.3.6机械通气:共8个研究[3,4,6~8](5649例)对机械通气与脓毒性休克患者AKI发生的关系进行了分析。合并后未见异质性(P=0.38,I2=6%),选用固定效应模型,结果显示:机械通气是脓毒性休克患者发生AKI的危险因素[OR=1.30,95% CI(1.13,1.48),P=0.0002],见图6。

图6 机械通气与急性肾损伤发生的森林图
2.3.7升压药≧2种:共5个研究[4,6~8,11](5067例)分析了使用2种及2种以上升压药与脓毒性休克患者AKI发生的关系,合并后各研究有异质性(P=0.0009,I2=79%),选用随机效应模型,结果显示:使用2种及2种以上种类升压药是脓毒性休克患者发生AKI的危险因素[OR=2.51,95% CI(1.35,4.64),P=0.003],见图7。

图7 升压药≧2种与急性肾损伤发生的森林图
2.3.8输血史:共5个研究[3,7,7~9](792例)分析了输血史与脓毒性休克患者AKI发生的关系,合并后各研究有异质性(P=0.05,I2=58%),选用随机效应模型,结果显示:输血史是脓毒性休克患者发生AKI的危险因素[OR=3.55,95%CI(1.82,6.91),P=0.0002],见图8。

图8 输血史与急性肾损伤发生的森林图
2.3.9造影剂:共4个研究[7,7~9](402例)报道了造影剂与脓毒性休克患者AKI发生的关系,4篇病例对照研究合并后无异质性(P=0.95,I2=0%),选择固定效应模型,结果显示:造影剂为脓毒性休克患者发生AKI的危险因素[OR=3.44,95%CI(2.03,5.84),P<0.00001],见图9。

图9 造影剂与急性肾损伤发生的森林图
2.3.10血培养阳性:共5个研究[3~5,7,8](9607例)分析了血培养阳性与脓毒性休克患者AKI发生的关系,合并后存在异质性(P=0.0005,I2=80%)选用随机效应模型,结果显示:血培养阳性是脓毒性休克患者发生AKI的危险因素[OR=1.59,95% CI(1.17,2.15),P=0.003],见图10。
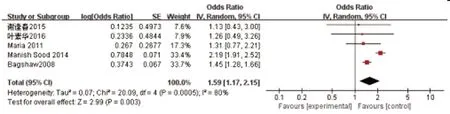
图10 血培养阳性与急性肾损伤发生的森林图
2.3.11APACHEⅡ评分:共6个研究[4,5~9](9540例)对APACHEⅡ评分与脓毒性休克患者AKI发生的关系进行了分析,合并后各研究间可见异质性(P<0.00001,I2=98%)选用随机效应模型,结果显示:高APACHEⅡ评分是脓毒性休克患者发生AKI的危险因素[WMD=1.96,95% CI(1.49,2.43),P<0.00001],见图11。

图11 APACHEⅡ评分与急性肾损伤发生的森林图
2.3.12中心静脉压(CVP):共5个研究[5,7~10](5018例)报道了CVP与脓毒性休克患者AKI发生的关系,5篇均为病例对照研究,合并后各研究间有异质性(P=0.003,I2=71%)选用随机效应模型,结果显示:高CVP是脓毒性休克患者发生AKI的危险因素[WMD=3.55,95% CI(2.89,4.21),P<0.00001],见图12。

图12 CVP与急性肾损伤发生的森林图
2.4发表偏倚评估及敏感性分析:通过饮酒因素进行分析,可见漏斗图左右基本对称,表示纳入研究文献发表偏倚可能性小,见图13。通过对固定和随机效应模型的合并效应量进行比较,可见合并效应值基本一致,表明分析结果稳定可靠,见表2。

图13 饮酒与急性肾损伤发生的漏斗图

表2 敏感性分析结果[OR/WMD(95%)CI]
3 讨 论
脓毒症被定义为由于宿主对感染的有害反应而导致的器官功能障碍[1],最常见的器官障碍之一则是肾脏。脓毒性休克作为脓毒症最严重的一种亚型,对患者器官功能的损害更加明显。尽管越来越多的研究分析了临床风险、病理生物学、治疗方法等相关因素,但由于改善患者AKI的措施仍待验证,因此脓毒症相关急性肾损伤仍然是一个需要重点关注问题,需要进一步研究以减少其对患者带来的不良后果[2]。各种微生物感染机体触发炎症反应,大量炎症细胞浸润和免疫复合物堆积,可直接或间接地造成肾脏损伤。随着年龄的增长对肾脏细胞修复具有重要作用的祖细胞和干细胞的增殖能力逐渐下降[10],但可能由于本meta分析纳入研究中脓毒性休克患者年龄均值较大有关,未显示出年龄对脓毒性休克患者发生AKI的意义;烟草中的化学物质具有多种损伤效应,可直接影响肾脏血流动力学、刺激副交感神经,该研究已在动物试验中得到证实[11];潘田君[7]通过分析一项病例对照研究发现,有高血压及糖尿病的患者更容易发生AKI,这可能与高血压引起的肾小动脉硬化,影响肾脏血流,严重者可导致肾功能衰竭有关;同样高血糖状态会使肾小球呈现高滤过状态,使得肾小球压力显著增加,加速肾脏损害[12];机械通气可增加胸腔内的压力,导致静脉回流减少,降低心输出量及肾灌注;此外机械通气还会引发促炎反应,改变神经体液系统等影响肾小球滤过功能,引起或促进AKI的发生发展[2];叶素华[8]通过一项病例对照研究发现使用造影剂及有输血史的患者更容易发生AKI,这可能与造影剂可直接对肾小管上皮细胞产生毒性作用,而血液中的免疫产物堆积引起肾小管阻塞等损害肾功能有关;急性生理与慢性健康评分Ⅱ(Acute Physiology And Chronic Health Evaluation Ⅱ,APACHEⅡ)是评估患者病情危重程度的工具,高APACHEⅡ评分则提示患者的临床预后较差,是脓毒性休克患者发生AKI的危险因素[9];此外,研究发现较高水平的中心静脉压(Central Venous Pressure,CVP)可使AKI的发病率和死亡率升高,而较低中心静脉压可使AKI的发生率下降[13],这可能与低中心静脉压可使肾脏灌注间接增加,从而改善肾脏功能有关。综上所述,既往临床上常采用肌酐、尿量等指标帮助临床医护人员诊断AKI,但各项指标在不同的病理生理状态下表达情况不尽相同,且受到各家医院开展检查项目的制约以及结果获得的滞后性,无法较好的指导医护人员对AKI发生做出及时的预判并进行早期预警防范。本研究meta分析结果显示吸烟、高血压、糖尿病、机械通气、升压药≧2种、输血史、造影剂、血培养阳性、高APACHEⅡ、高中心静脉压是脓毒性休克患者AKI的危险因素,提醒临床医护人员治疗及护理具有以上因素的脓毒性休克患者时,应考虑AKI的发生,以做好预防及观察。
本研究存在以下局限性:本次纳入的研究对象种族、病例数量、研究工具、研究地域存在差异,部分危险因素合并后存在一定的异质性。根据本Meta分析结果显示饮酒尚不能证明饮酒是脓毒性休克患者并发AKI的危险因素,需进一步的探讨。
