土壤化学反硝化及N2O产生机理研究进展
2020-03-17赖睿特张克强杨涵博
颜 青, 赖睿特, 张克强, 杨涵博, 王 风
农业农村部环境保护科研监测所, 天津 300191
N2O作为一种重要的温室气体,性质稳定,可以长时间存在于大气中,同时它还是氮氧化物之一,间接影响臭氧的消耗[1]. 虽然N2O对全球总辐射的贡献率仅占6%[2],其浓度和增长速率也都低于CO2和CH4,但N2O单位分子增温潜力分别是CO2、CH4的296、23倍[3],当大气中其浓度增加1倍时,将会导致全球升温0.3 ℃[4]. 农田土壤对全球N2O的排放具有重要贡献,WANG等[5]发现,矿物氮肥的施用已经使农田土壤成为N2O排放的主要来源. Thomson等[6]认为,全球N2O排放总量中约有23来自土壤,土壤N2O的产生又主要归因于农业生产. Griffis等[7]发现,农业系统中约4%的人为氮以N2O的形式返回大气层. 土壤作为重要的N2O排放源对大气温室气体浓度有不可忽视的影响,因而土壤氮素转化产生N2O的作用途径需要进一步探索. 但以往的研究主要集中在生物途径的氮素转化产生N2O,而非生物途径对土壤氮素转化起到的作用及其影响因素却鲜见报道[8-9]. 近年来,越来越多的研究发现,除了微生物作用以及酶反应以外,非生物学途径对于N2O的产生有重要意义,如图1所示,土壤化学反硝化作为一种非生物氮素转化过程,与N2O的排放有着密切联系. 关于化学反硝化过程的研究可以追溯到20世纪60年代甚至更早[8]. 研究表明,在酸性和中性条件下化学反硝化的产物以NO和N2O为主,碱性条件下则以N2和NH4+为主[10];在反应条件上,化学反硝化通常只有在低pH下才被认为是N2O的产生源,不过该过程N2O产生量比NO或N2少,也远小于硝化或反硝化过程N2O产生量[11]. 不同非生物过程因作用机制的差异会导致其对土壤N2O产生的贡献相差较大,马兰等[12]研究发现,NH2OH处理的封丘旱地潮土在培养7 d后,N2O累积排放量约为添加等量NO2--N处理的74倍. 与生物反硝化和硝化等途径相比,化学反硝化N2O产生量通常较小,但是在酸性或酸化土壤中发生化学反硝化的可能性及其对NO和N2O排放的贡献却是不容忽视的[13]. 该文综述了20世纪80年代以来土壤化学反硝化的作用机制,以及pH、反应底物浓度、有机质和温度等环境要素对化学反硝化影响的研究进展,并提出下一步的重点研究方向,以期为今后抑制化学反硝化生成N2O提供参考.
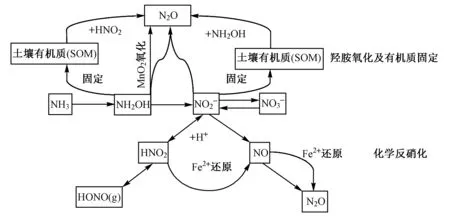
图1 非生物学途径产生N2O的过程[14]Fig.1 Process of N2O production by abiotic pathways[14]
1 土壤化学反硝化的机理与途径
虽然N2O产生的化学途径已经被发现近一个世纪,但其研究往往被忽视[8-9]. Clément等[15]根据氮的电子得失和反应对象不同,将氮素化学转化划分为3种作用,即化学固定、化学硝化和化学反硝化. 化学反硝化是指硝化过程中产生的羟胺(NH2OH)和亚硝酸盐(NO2-)进行化学分解,或者由有机物或Fe2+等物质将土壤中的高价氮还原成低价氮的过程[8,13,16],其产物主要包括NO、N2O和N2,甚至还有NH4+[8]. 目前对于化学反硝化的发生机理缺少统一的规定和理解,NO3-被还原、NH2OH的化学氧化和NO2-的还原均与化学反硝化密切相关,但其具体机理尚未定论. 化学反硝化主要发生在酸性或一些阴冷的森林土壤中[17]. 在反应特点上,与生物硝化或反硝化作用相比,化学反硝化具有反应速率快、不依赖压力等优势. 此外,某些化学还原剂能够在一定条件下通过反硝化作用获得比生物方法更多的N2O反应产物[18].
1.1 化学反硝化中N2O的产生机理
Bremner[11]指出,NH2OH和NO2-作为硝化作用的中间产物,均可以通过化学途径产生N2O. NH2OH和NO2-的化学分解产生N2O,这也通常被认为是化学反硝化的一种特殊形式. Stüven等[19]发现,NH2OH既是硝化细菌细胞的选择性抑制剂,又是还原NO2-为NO和N2O的强还原剂,但是目前对于羟胺反应是否被归纳为化学反硝化机理尚未达成共识. 化学反硝化的另一个重要反应底物是NO2-,王敬国[20]指出,氮素的化学转化必须要有NO2-的积累. 由于进一步氧化受到抑制而积累的NO2-,其化学分解主要包括自分解和与氨基酸反应两种形式:①NO2-自分解只有在pH<5下才能进行,而且随pH的升高而降低,自分解的产物主要是NO2和NO;②NO2-与a-氨基酸R-NH2反应,产物为N2[21].
1.2 化学反硝化途径
化学反硝化的作用底物NO3-、NO2-和NH2OH是土壤氮素转化过程中的产物或中间产物,它们同样参与生物硝化和反硝化过程. 但在化学反硝化过程中主要考虑这些物质发生的化学反应,主要包括NO3-、NO2-和NH2OH的化学分解. NO3-的化学分解主要由Fe2+或有机物作电子供体参与完成;NH2OH化学分解主要指其与Fe3+反应;NO2-的化学分解包括自分解及其与Fe2+、有机物R-NH2反应等,上述反应途径归纳于图2.
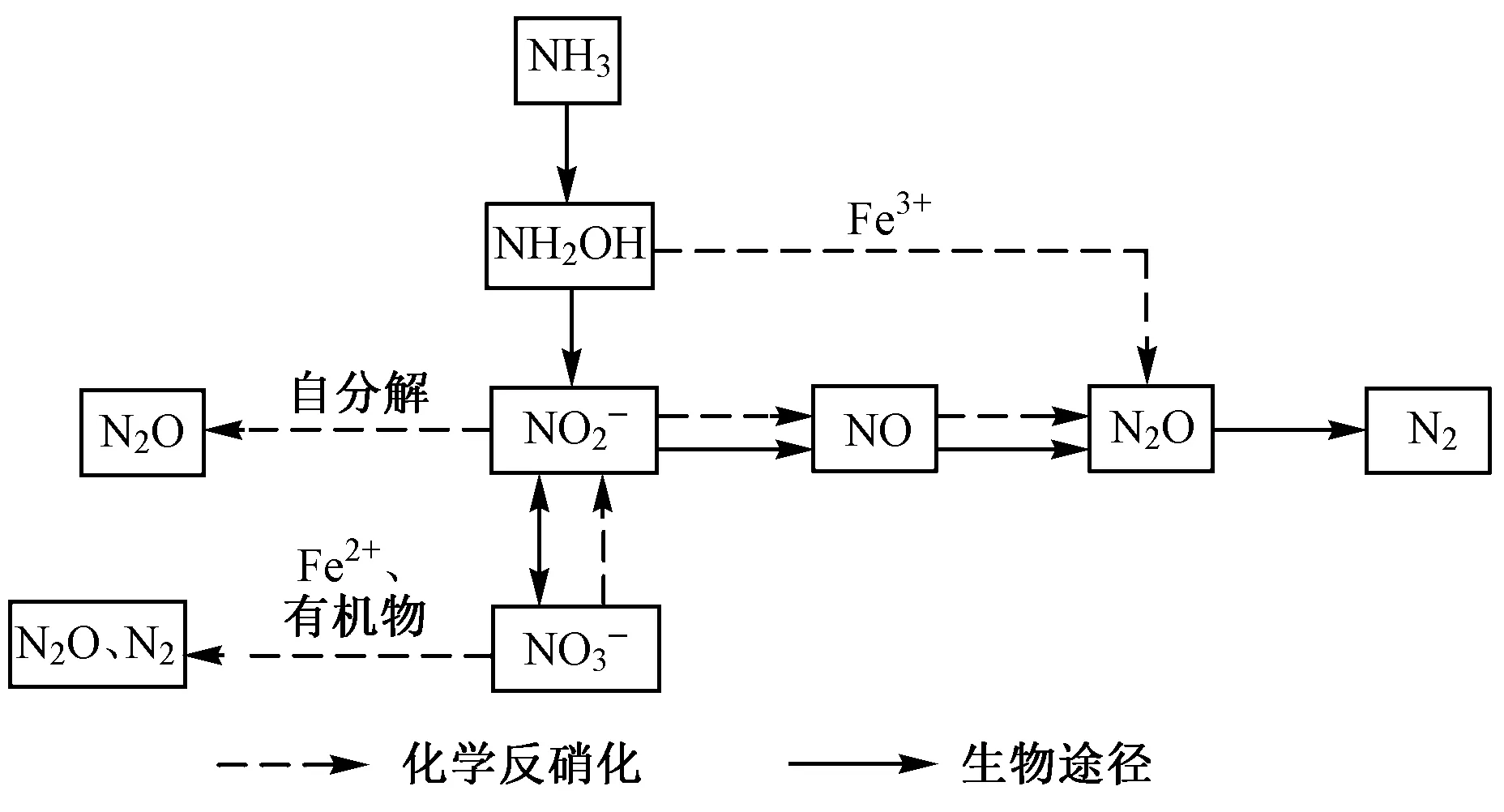
图2 土壤化学反硝化机制与转化途径Fig.2 Mechanism and transformation pathways of soil chemical denitrification
2 Fe对土壤化学反硝化的作用机制
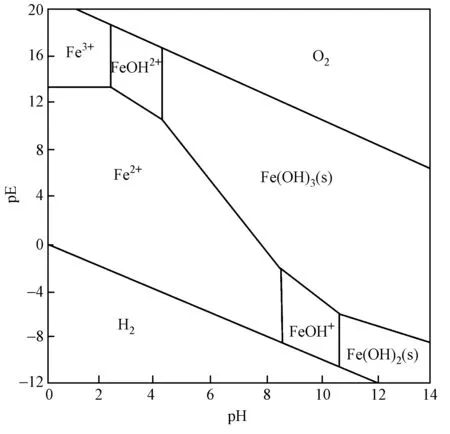
图3 Fe的pE-pH稳定性相图[8]Fig.3 Phase diagrams of soluble and solid forms of Fe under a range of redox potential and pH conditions[8]
自然环境中土壤Fe主要以Fe2+和Fe3+两种价态存在,其存在形式取决于土壤pH和pE(见图3),当处于Fe3+稳定区条件时,Fe2+将电子转移到高价氮将其还原,同时由于失电子Fe2+被氧化为Fe3+而稳定存在;当处于Fe2+稳定区条件时,Fe3+从NH2OH得到电子还原为Fe2+稳定存在,同时使NH2OH氧化. 邱轩等[22]发现,含铁矿物可以通过电子传递影响微生物代谢,从而对碳和氮的转化循环产生影响. 操家顺等[23]在研究反硝化系统除磷时发现,Fe3+会影响细菌的酶活性. Fe元素不仅影响生物途径中的氮素转化,对非生物过程同样有密切作用. Dalal等[24]发现了Fe对非生物过程的特殊影响,即在有机质或Fe2+等还原剂作用下,NO2-和NO3-被还原生成N2O的非生物过程. Fe参与的化学反硝化主要体现在Fe2+还原NO3-和NO2-,以及Fe3+与NH2OH反应两个方面.
2.1 Fe2+还原高价氮
NO3-在碱性条件下可以被Fe2+还原,主要还原产物是NH4+;而NO2-在酸性和碱性条件下均可被Fe2+还原,主要还原产物有N2、N2O、NH4+等(见表1).
2.1.1NO3-的还原
Fe2+作为还原剂可以与NO3-反应. Ratering等[25]研究在水稻土中添加NO3-对剖面Fe2+和Fe3+分布特征的对照试验中,发现NO3-依赖于Fe2+. Matocha等[26]发现,天然土壤中Fe2+在添加NO3-后立即被氧化,该现象表明了Fe2+与NO3-发生氧化还原反应的可能性,Straub等[27]在纯培养和浓缩培养条件下观察到了这一过程,并以式(1)进行描述:
10Fe2+(aq)+2NO3-+24H2O→
10Fe(OH)3(s)+N2(g)+18H+
(1)
2.1.2NO2-的还原
近年来,NO2-与Fe2+相关反应的研究逐渐深入. Samarkin等[10]发现,非生物N2O的产生是由于Fe2+氧化与NO2-还原的耦合. Cleemput等[28]也提出,NO2-可与铁离子或有机物发生反应,当pH<4时Fe2+促进NO2-分解,而pH呈中性时Fe2+与NO2-的反应速率较慢,但仍然意义重大[29-30]. 也有研究[19]认为,土壤中Fe2+和有机物质可通过减少O2以促进NO2-转化为N2O. Klueglein等[31]发现,NO2-可以与Fe2+发生快速的化学反应,如式(2)[32]所示:
2NO2-+4Fe2++5H2O→
4FeOOH+N2O+6H+
(2)
表1 不同类型Fe2+还原NO2-NO3-产物比较[18]
Table 1 Comparison of NO2-NO3- reduced by different forms of Fe2+[18]
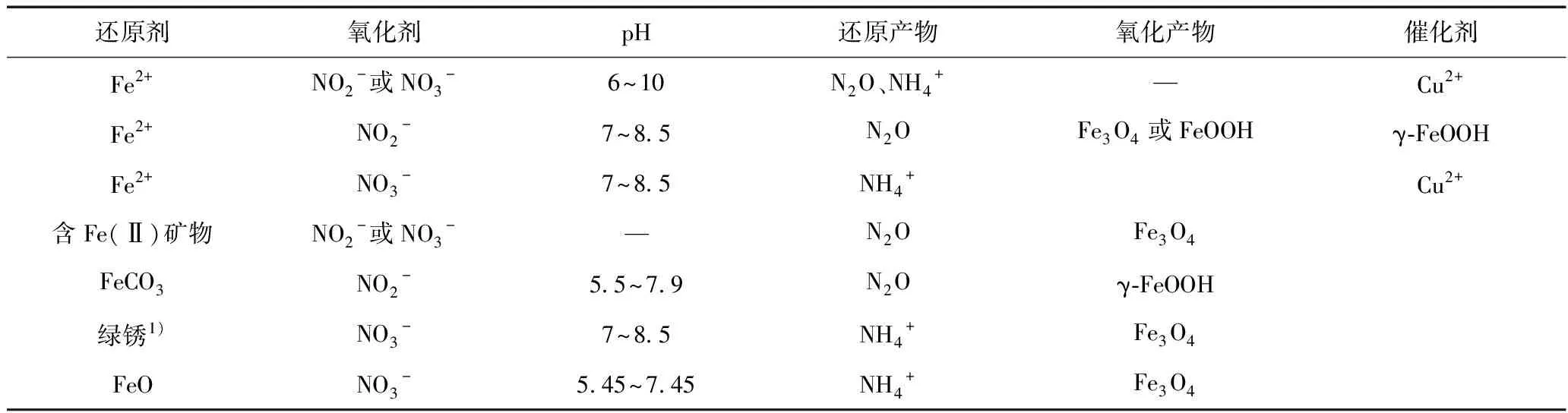
表1 不同类型Fe2+还原NO2-NO3-产物比较[18]
还原剂氧化剂pH还原产物氧化产物催化剂Fe2+NO2-或NO3-6~10N2O、NH4+—Cu2+Fe2+NO2-7~8.5N2OFe3O4或FeOOHγ-FeOOHFe2+NO3-7~8.5NH4+Cu2+含Fe(Ⅱ)矿物NO2-或NO3-—N2OFe3O4FeCO3NO2-5.5~7.9N2Oγ-FeOOH绿锈1)NO3-7~8.5NH4+Fe3O4FeONO3-5.45~7.45NH4+Fe3O4
注:1) 绿锈(green rusts,GRs)是近年来最新研究的一类含有Fe的不稳定化合物.
NO2-除与Fe2+发生氧化还原反应以外,其自分解产生N2O的过程也与Fe有关. Hecke等[33]发现,底层土壤中的Fe2+和Cu+能促进NO2-的化学分解. 随pH的降低,HNO2分解加速,气体产物NO2和NO因活性极强,可以快速将Fe2+氧化为Fe3+[34],产生的HNO进一步分解后,以N2O为N的最终形态,如式(3)~(7)所示:
NO2-+H+→HNO2
(3)
2HNO2→NO2+NO+H2O
(4)
NO2+2Fe2++2H+→2Fe3++NO+H2O
(5)
NO+Fe2++H+→Fe3++HNO
(6)
2HNO→N2O+H2O
(7)
2.2 Fe与羟胺的反应
NH2OH能够与土壤中Fe3+或Mn4+进行化学反应并产生N2O[9,35-36]. 影响Fe与NH2OH反应的主要因素有C/N、温度、反应物浓度、pH等. Heil等[37]发现,土壤C/N可以影响NH2OH反应生成N2O,并得到在相同NH2OH用量下C/N越低、生成的N2O越多的结论. Zhu-Barker等[9]发现,Fe3+氧化NH2OH的速率随温度的升高而增加. 酸性条件下,当Fe3+浓度高于NH2OH浓度时,二者反应的主要产物是N2O[38],Fe3+浓度低于NH2OH浓度时的主要产物是N2[39]. 马兰等[12]也发现,NH2OH在酸性条件下比在碱性条件下更稳定,pH<5.95虽然不利于N2O的产生,但该条件下N2O为主要气态产物[19].
3 NH4+和有机物参与的化学反硝化
3.1 NH4+
在光照或高温高压环境中,NO3-在碱性条件下可以与NH3发生反应,在酸性条件下可以与NH4+发生反应,产物是N2、NO或N2O. 吴德礼等[18]发现,当存在Cl-时,HNO3与H+反应的产物NO2+会与Cl-合成NO2Cl,NO2Cl若与NH4+反应则生成N2O,若与NH3反应则生成N2. 由于酸性条件下有更多的NH4+,因此得出N2ON2(二者物质的量的比)随酸度的增加而增大的结论,反应过程如式(8)~(14)[18]所示:
NO2Cl的生成:
HNO3+H+→H2NO3+→NO2++H2O
(8)
Cl-+NO2+→NO2Cl
(9)
NO2Cl与NH4+反应:
NO2Cl+NH4+→{O2N-NH3}++H++Cl-(10)
{O2N-NH3}+→N2O+H3O+
(11)
NO2Cl与NH3反应:
3NO2Cl+3NH3→3NH2Cl+3NO2-+3H+(12)
3NH2Cl→N2+NH4++3Cl-+2H+
(13)
3NO2-+3NH4+→3N2+6H2O
(14)
3.2 有机物
NO2-可以与土壤中的腐殖酸、黄腐酸、木质素结构单元和酚类化合物反应生成N2、N2O和CH3ONO[40]以及NO[41-42],且随温度升高[9]、pH降低或有机物质增加[41],反应速率显著增加. Davidson等[43]提出土壤“铁轮假设”,认为有机质还原Fe3+为Fe2+后,可还原NO3-为NO2-,NO2-进而与酚类化合物反应形成硝基和亚硝基酚,从而固定土壤中的NO3-. 王敬国[20]将有机质与NO2-反应的过程归纳为式(15):
NO2-+有机质→硝基苯酚类→醌肟化合物→
N2、N2O、NO和NO2等
(15)
4 化学反硝化的主要影响因素
4.1 土壤pH
化学反硝化在较高的pH下反应更彻底,气体产物倾向于以N2形式排放,且pH对于NH2OH和NO2-非生物转化的影响趋势截然相反.
在微生物活性较低或灭菌条件下化学反硝化起主导作用,该条件下较高的pH有利于促进化学反硝化,因为化学反硝化是产H+的过程,较低的pH会抑制反应的正向进行[44],碱性环境更利于化学反硝化进行,而且使高价态无机氮更倾向于最终转化成N2. Buresh等[30]在不同pH下研究NO3-与Fe2+的氧化还原反应时发现,NO3-的还原速率和气体产物均随pH的升高而逐渐增加. pH也是土壤NH2OH和NO2--N非生物过程产生N2O的关键影响因子,添加NH2OH处理中非生物过程产生的N2O占排放总量的比例与土壤pH呈显著正相关,添加NO2--N处理中二者则呈显著负相关,说明NO2--N在酸性土壤中可能主要通过非生物过程产生N2O[45],而在碱性土壤中主要通过生物过程;NH2OH则与之相反[12].
土壤N2O排放量与pH呈负相关,且pH会影响气体产物比例. 低pH下,尽管反硝化活性低,但N2O的释放比例较高. 在pH为3.87的酸性土壤中,N2O成为反硝化的唯一终产物[20]. pH通过改变产物转化速率而影响化学反硝化气体产物的比例,在酸性条件下主要气体产物是NO和N2O,而在碱性条件下主要气体产物是N2. 酸性土壤中NON2O(二者物质的量的比,下同)较高,是因为低pH下NO向N2O、N2O向N2的转化速率均显著低于高pH条件下,因而随着pH的降低,NON2O与N2ON2逐渐增大[46](见图4).
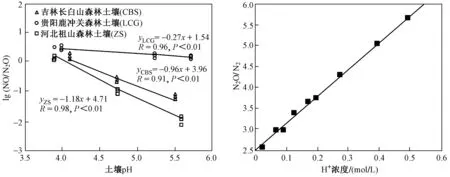
图4 土壤pH与NON2O、N2ON2的关系[18,47]Fig.4 Relationship between soil pH, NON2O and N2ON2[18,47]
4.2 反应底物浓度
化学反硝化的反应底物主要包括NO3-和NO2-形态的高价氮,化学反硝化反应速率和气体产物NO、N2O的产生量均与初始底物浓度呈正相关. Kampschreur等[48]发现,NO2-的增加可以提高化学反硝化过程中NO和N2O的产生量. 另外,反应底物浓度也会影响化学反硝化的气体产物比. Samarkin等[10]在研究南极维多利亚南部的高盐湖DJP(Don Juan Pond)土壤时发现,DJP盐水中含有较高浓度的NO3-、NO2-和NH4+,而且其周围的石质耕层土壤来源于富Fe(Ⅱ)-富铁白云石的风化作用,试验证明,NO3-、NO2-浓度高的卤水与土壤中含铁矿物的反应是产生N2O的主要原因,而且N2O生成速率与初始反应底物浓度成正比.
底物浓度较高会促进化学反硝化产生NO、N2O的现象可能归因于pH. 胡波等[49]在研究氮沉降对酸雨区森林土壤影响时发现,氮沉降量的增加会降低土壤pH. 土壤中高价氮主要源于氮肥,氮肥的大量施用使大气氮素沉降呈迅猛增加的趋势,一旦进入土壤会引起pH降低,酸性条件下化学反硝化气体产物以NO、N2O为主,表现为促进NO、N2O的排放.
底物浓度在一定范围内会促进N2O生成,超过该范围则会出现抑制. 如陈思等[50]在研究黑土与潮土时发现,当添加低浓度(200 mgkg)硝态氮时,与对照组相比,N2O排放通量分别增加了849%和676%;添加高浓度(500 mgkg)硝态氮时,N2O排放通量则受到显著抑制. 但是对于化学反硝化受底物浓度影响的浓度极限以及是否出现抑制现象等问题仍然有待进一步探究.
4.3 有机质
有机质的存在有利于化学反硝化发生,土壤中有机质通过其还原性反应和自身分解影响化学反硝化:①有机质直接参与化学反硝化反应. Verhaegen等[51]发现,NO2-与土壤有机质反应生成有机氮化合物; Cleemput等[29]发现,NO2-可与土壤腐殖质中的酚类物质反应生成有机氮亚硝基化合物,且随着有机质含量和土壤酸度的增加而增加. ②有机物自身发生分解和电离,使pH-pE环境改变,从而间接影响化学反硝化过程[8]. CN作为土壤有机质质量的指标,是评价NH2OH氧化生成N2O的预测指标,而Heil等[37]在研究NH2OH的化学氧化时发现,NH2OH用量相同时,较低的CN更利于N2O的产生.
4.4 固相界面及金属离子
固相界面和某些过渡金属离子(如Cu2+)的存在可以促进化学反硝化的进行. TAI等[52]发现,在严格厌氧条件下水溶液中的NO2-与Fe2+基本不发生反应,但在加入金属氧化物、氢氧化物、碳酸盐等固相物质后,NO和N2O生成速率显著提高. Fe3+与固相物质表面形成的活性Fe2+的表面形态,促进了其与NO2-的反应.
某些过渡金属离子(如Cu2+)也可以加速Fe2+与NO3-的反应[30,33]. Buresh等[30]发现,Fe2+与NO3-的反应在Cu2+的催化下能较快进行. 在没有Cu2+等化学催化剂的情况下,Fe2+溶液还原NO3-的速度很慢,NO3-的还原率可忽略不计[53];而在有Cu2+存在的体系中,pH为8.0下,24 h内有61%的硝态氮通过非生物过程被Fe2+还原成了含氮气体产物[30]. Cu2+的存在除促进反应速率外,还会影响化学反硝化产物分布[18,54]. Cu2+的加入会降低产物中N2ON2,Cu2+可能催化N2O进一步被还原为N2. Cleemput等[28]发现,在pH为6~8时,Cu2+对Fe2+存在下的NO2-稳定性产生一定影响.
4.5 温度
高温不仅可以刺激非生物途径N2O产生,随着温度的升高,其N2O产生速率甚至较生物过程更高[37],同时高温也会抑制生物途径N2O产生. 虽然化学反硝化适应的温度范围还没有得到准确证明,但是研究指出,50 ℃对于化学反硝化作用的意义重大,如Malhi等[55-56]认为,温度高于50 ℃时化学反硝化可能成为主要作用过程. Heil等[37]发现,在灭菌土壤中,50 ℃时NH2OH非生物氧化会产生更多的N2O. 添加尿素的酸性土壤中N2O排放量随温度升高而增加,并且非生物的化学过程是土壤中N2O排放的主导途径;而有机肥处理的土壤中N2O排放量随温度升高而降低. 在尿素处理的土壤中,N2O在40 ℃下的排放总量显著高于在20 和30 ℃下的排放量[57].
虽然pH、底物浓度、有机质、固相界面、Cu2+、温度因素对土壤化学反硝化产生N2O的大体影响趋势已经明确,但是单个影响因素对N2O产生显著促进或抑制作用的极值点还缺少详细研究,多种影响因素的影响强弱程度和交互作用对土壤化学反硝化产生N2O的研究也不足,可以考虑利用控制变量法、相关性分析等方法进行下一步研究.
5 结论
a) 在土壤酸性较强或其他不利于微生物和酶活性的环境中,化学反硝化可能占据重要地位,其作用途径主要包括NO3-、NO2-和NH2OH的化学分解.
b) 不同形态Fe参与化学反硝化生成N2O的途径不同,主要包括Fe2+还原NO2-和NO3-,Fe3+氧化NH2OH.
c) 化学反硝化主要受pH、底物浓度、有机质、固相界面、Cu2+、温度等因素的影响. 较高的pH更有利于化学反硝化的发生,但不利于N2O的排放;底物浓度越高,化学反硝化速率越大,气体产物NO和N2O的产生量越大;有机质、固相界面、Cu2+的存在有利于化学反硝化进行;温度升高会刺激N2O非生物途径生成,50 ℃对于化学反硝化意义特殊.
6 研究展望
a) 加强化学反硝化的作用机理方面的基础性研究. 化学反硝化的边界还没有形成共识,有学者认为化学反硝化仅指NO3-被还原的过程,也有学者将NH2OH的化学氧化和NO2-还原都归纳为化学反硝化. 化学反硝化各途径作用机理的发生条件及限制因素还需要进一步阐释. 典型耕作土壤化学反硝化N2O的产生量基础数据尚需积累,以揭示化学反硝化对于土壤N2O排放的贡献.
b) 加强多因素综合影响下化学反硝化强度及N2O产生特征方面的应用性研究. 在已初步明确的pH、底物浓度、有机质、固相界面、Cu2+、温度对土壤化学反硝化N2O产生特征基础上,进一步明确单一影响因素对N2O产生显著促进或抑制作用的极限条件. 同时,着重加强土壤化学反硝化产生N2O的多因素综合影响效果和交互作用.
c) 拓展与实践化学反硝化在控制土壤N2O产生的现实作用. 在化学反硝化发生的适宜区域,特别是南方酸雨侵蚀区、高原极寒地区、森林土壤等区域,如在酸雨腐蚀地区通过人为调控来限制铁矿物等与高价氮、羟胺的化学反应,减缓其反应速率或加大其反应程度,从而达到限制N2O生成或促进N2O继续转化的目的.
参考文献(References):
[1] 戴树桂.环境化学[M].北京:高等教育出版社,1997.
[2] 常思琦,王东启,俞琳,等.上海城市河流温室气体排放特征及其影响因素[J].环境科学研究,2015,28(9):1375-1381.
CHANG Siqi,WANG Dongqi,YU Lin,etal.Greenhouse gas emission characteristics from urban rivers in Shanghai[J].Research of Environmental Sciences,2015,28(9):1375-1381.
[3] WU Dong,WANG Chao,DOLFING J,etal.Short tests to couple N2O emission mitigation and nitrogen removal strategies for landfill leachate recirculation[J].Science of the Total Environment,2015,512513(15):19-25.
2017年,药品加成全部取消后,上海十院通过医疗服务项目价格调整的补偿率为99%,基本能够实现足额弥补。如考虑到医疗器械价格调整,实际补偿率为68%。受此影响,骨科、心脏外科、普外科等手术科室,由于业务特性对材料的依存度较高,在取消药品加成和医疗器械价格的调整后平均补偿率仅为47%。
[4] 徐文彬.概论N2O大气浓度演变及其大气化学[J].地质地球化学,1999,27(3):74-80.
XU Wenbin.Variations in atmospheric concentration of N2O and its atmospheric chemistry[J].Geology-Geochemistry,1999,27(3):74-80.
[5] WANG Cheng,LU Haohao,DONG Da,etal.Insight into the effects of biochar on manure composting:evidence supporting the relationship between N2O emission and denitrifying community[J].Environmental Science & Technology,2013,47(13):7341-7349.
[6] THOMSON A J,GIANNOPOULOS G,PRETTY J,etal.Biological sources and sinks of nitrous oxide and strategies to mitigate emissions[J].Philosophical Transactions of the Royal Society B:Biological Sciences,2012,367(1593):1157-1168.
[7] GRIFFIS T J,LEE X,BAKER J M,etal.Reconciling the differences between top-down and bottom-up estimates of nitrous oxide emissions for the U. S. Corn Belt[J].Global Biogeochemical Cycles,2013,27(3):746-754.
[8] 王娅静,刘晶,郭景恒.铁作用下土壤氮素化学转化过程的研究进展[J].中国农业大学学报,2014,19(2):95-99.
WANG Yajing,LIU Jing,GUO Jingheng.Chemical transformation of soil nitrogen under the influence of iron:a review[J].Journal of China Agricultural University,2014,19(2):95-99.
[9] ZHU-BARKER X,CAVAZOS A R,OSTROM N E,etal.The importance of abiotic reactions for nitrous oxide production[J].Biogeochemistry,2015,126(3):251-267.
[10] SAMARKIN V A,MADIGAN M T,BOWLES M W,etal.Abiotic nitrous oxide emission from the hypersaline Don Juan Pond in Antarctica[J].Nature Geoscience,2010,3(5):341-344.
[11] BREMNER J M.Sources of nitrous oxide in soils[J].Nutrient Cycling in Agroecosystems,1997,49(1):7-16.
[12] 马兰,李晓波,李博伦,等.土壤中羟胺和亚硝态氮非生物过程对N2O排放的贡献[J].土壤学报,2016,53(5):1181-1190.
MA Lan,LI Xiaobo,LI Bolun,etal.Contributions of abiotic processes driven by hydroxylamine and nitrite to N2O emission in six different types of soils in China[J].Acta Pedologica Sinica,2016,53(5):1181-1190.
[13] 蔡延江,丁维新,项剑.土壤N2O和NO产生机制研究进展[J].土壤,2012,44(5):712-718.
CAI Yanjiang,DING Weixin,XIANG Jian.Mechanisms of nitrous oxide and nitric oxide production in soils:a review[J].Soils,2012,44(5):712-718.
[14] 曹文超.设施菜田土壤硝化、反硝化N2O产生特征及影响因素[D].北京:中国农业大学,2017.
[15] CLÉMENT J,SHRESTHA J,EHRENFELD J G,etal.Ammonium oxidation coupled to dissimilatory reduction of iron under anoxic conditions in wetland soils[J].Soil Biology and Biochemistry,2005,37(12):2323-2328.
[16] 黄树辉,吕军.农田土壤N2O排放研究进展[J].土壤通报,2004,35(4):516-522.
HUANG Shuhui,LU Jun.Research progress in nitrous oxide emissions from agricultural soil[J].Chinese Journal of Soil Science,2004,35(4):516-522.
[17] 梁东丽.黄土性土壤氮素氧化亚氮气态损失及其影响因素的研究[D].杨凌:西北农林科技大学,2003.
[18] 吴德礼,傅旻瑜,马鲁铭.生物及化学反硝化过程中N2O的产生与控制[J].化学进展,2012,24(10):2054-2061.
WU Deli,FU Minyu,MA Luming.Nitrous oxide emission and control in biological and chemical denitrification[J].Progress in Chemistry,2012,24(10):2054-2061.
[19] STÜVEN R,VOLLMER M,BOCK E.The impact of organic matter on nitric oxide formation byNitrosomonaseuropaea[J].Archives of Microbiology,1992,158(6):439-443.
[20] 王敬国.土壤氮素的转化过程中温室效应气体的释放和吸收[J].环境科学研究,1993,6(5):47-51.
WANG Jingguo.Biological production and fluxes of N2O and NO in soils[J].Research of Environmental Sciences,1993,6(5):47-51.
[21] 钟玲玲.关于土壤中氮素转化规律的研究[J].北方环境,2002(3):50-53.
[22] 邱轩,石良.微生物和含铁矿物之间的电子交换[J].化学学报,2017,75(6):583-593.
QIU Xuan,SHI Liang.Electrical interplay between microorganisms and iron-bearing minerals[J].Acta Chimica Sinica,2017,75(6):583-593.
[23] 操家顺,谢玉洁,方芳,等.Fe3+对反硝化系统除磷效果及微生物产物的影响[J].环境科学研究,2015,28(1):125-133.
CAO Jiashun,XIE Yujie,FANG Fang,etal.Influences of Fe3+on phosphorus removal and microbial products in denitrifying phosphorus removal system[J].Research of Environmental Sciences,2015,28(1):125-133.
[24] DALAL R C,WANG Weijin,ROBERTSON G P,etal.Nitrous oxide emission from Australian agricultural lands and mitigation options:a review[J].Australian Journal of Soil Research,2003,41(2):165-195.
[25] RATERING S,SCHNELL S.Nitrate-dependent iron (Ⅱ) oxidation in paddy soil[J].Environmental Microbiology,2001,3(2):100-109.
[26] MATOCHA C J,DHAKAL P,PYZOLA S M.The role of abiotic and coupled bioticabiotic mineral controlled redox processes in nitrate reduction[J].Advances in Agronomy,2012,115:181-214.
[27] STRAUB K L,BENZ M,SCHINK B,etal.Anaerobic,nitrate-dependent microbial oxidation of ferrous iron[J].Applied and Environmental Microbiology,1996,62(4):1458-1460.
[28] CLEEMPUT O V,SAMATER A H.Nitrite in soils:accumulation and role in the formation of gaseous N compounds[J].Fertilizer Research,1995,45(1):81-89.
[29] CLEEMPUT O V,BAERT L.Nitrite stability influenced by iron compounds[J].Soil Biology and Biochemistry,1983,15(2):137-140.
[30] BURESH R J,MORAGHAN J T.Chemical reduction of nitrate by ferrous iron[J].Journal of Environmental Quality,1976,5(3):320-325.
[31] KLUEGLEIN N,KAPPLER A.Abiotic oxidation of Fe(Ⅱ) by reactive nitrogen species in cultures of the nitrate-reducing Fe(Ⅱ) oxidizerAcidovoraxsp.BoFeN1-questioning the existence of enzymatic Fe(Ⅱ) oxidation[J].Geobiology,2013,11(2):180-190.
[32] 李爽,李晓敏,李芳柏.Fe(Ⅱ)对反硝化过程及其功能微生物群落的影响[J].中国环境科学,2018,38(1):263-274.
LI Shuang,LI Xiaomin,LI Fangbai.Effect of Fe(Ⅱ) on denitrification and associated functional microbial communities[J].China Environmental Science,2018,38(1):263-274.
[33] HECKE K V,CLEEMPUT O V,BAERT L.Chemo-denitrification of nitrate-polluted water[J].Environmental Pollution,1990,63(3):261-274.
[34] BONNER F T,PEARSALL K A.Aqueous nitrosyliron(Ⅱ) chemistry:1.reduction of nitrite and nitric oxide by iron(Ⅱ) and (Trioxodinitrato) iron(Ⅱ) in acetate buffer.Intermediacy of nitrosyl hydride[J].Inorganic Chemistry,1982,21(5):1973-1978.
[35] SCHREIBER F,WUNDERLIN P,UDERT K M,etal.Nitric oxide and nitrous oxide turnover in natural and engineered microbial communities:biological pathways,chemical reactions,and novel technologies[J].Frontiers in Microbiology,2012,3(372):1-24.
[36] BREMNER J M,BLACKMER A M,WARING S A.Formation of nitrous oxide and dinitrogen by chemical decomposition of hydroxylamine in soils[J].Soil Biology and Biochemistry,1980,12(3):263-269.
[37] HEIL J,LIU Shurong,VEREECKEN H,etal.Abiotic nitrous oxide production from hydroxylamine in soils and their dependence on soil properties[J].Soil Biology and Biochemistry,2015,84:107-115.
[38] BRAY W C,SIMPSON M E,MACKENZIE A A.The volumetric determination of hydroxylamine[J].Journal of the American Chemical Society,1919,41(9):1363-1378.
[39] BENGTSSON G,FRONAEUS S,BENGTSSON-KLOO L.The kinetics and mechanism of oxidation of hydroxylamine by iron(Ⅲ)[J].Journal of the Chemical Society:Dalton Transactions,2002(12):2548-2552.
[40] STEVENSON F J,SWABY R J.Nitrosation of soil organic matter:I.nature of gases evolved during nitrous acid treatment of lignins and humic substances[J].Soil Science Society of America Journal,1964,28(6):773-778.
[41] BLACKMER A M,CERRATO M E.Soil properties affecting formation of nitric oxide by chemical reactions of nitrite[J].Soil Science Society of America Journal,1986,50(5):1215-1218.
[42] CHRISTIANSON C B,CHO C M.Chemical denitrification of nitrite in frozen soils[J].Soil Science Society of America Journal,1983,47(1):38-42.
[43] DAVIDSON E A,CHOROVER J,DAIL D B.A mechanism of abiotic immobilization of nitrate in forest ecosystems:the ferrous wheel hypothesis[J].Global Change Biology,2003,9(2):228-236.
[44] HANSEN H C B,GULDBERG S,ERBS M,etal.Kinetics of nitrate reduction by green rusts:effects of interlayer anion and Fe(Ⅱ):Fe(Ⅲ) ratio[J].Applied Clay Science,2001,18(1):81-91.
[45] VENTEREA R T.Nitrite-driven nitrous oxide production under aerobic soil conditions:kinetics and biochemical controls[J].Global Change Biology,2007,13(8):1798-1809.
[46] 卢晋晶.土壤pH对化学反硝化气体产物及其组分比的影响[D].北京:中国农业大学,2012.
[47] 王娅静.基于数据整合和实验模拟研究土壤pH对N2O和NO排放的影响[D].北京:中国农业大学,2018.
[48] KAMPSCHREUR M J,KLEEREBEZEM R,de Vet W W J M,etal.Reduced iron induced nitric oxide and nitrous oxide emission[J].Water Research,2011,45(18):5945-5952.
[49] 胡波,王云琦,王玉杰,等.模拟氮沉降对土壤酸化及土壤酸缓冲能力的影响[J].环境科学研究,2015,28(3):418-424.
HU Bo,WANG Yunqi,WANG Yujie,etal.Effects of simulated nitrogen deposition on soil acidification and soil buffering capacity[J].Research of Environmental Sciences,2015,28(3):418-424.
[50] 陈思,张克强,麻晓越,等.外源硝态氮对典型耕作土壤冻结过程N2O排放的影响[J].环境科学研究,2014,27(6):635-641.
CHEN Si,ZHANG Keqiang,MA Xiaoyue,etal.Effects of nitrate nitrogen application on N2O emissions from three types of soil during freezing process[J].Research of Environmental Sciences,2014,27(6):635-641.
[51] VERHAEGEN K,CLEEMPUT O V,VERSTRAETE W.Nitrification mediated nitrosation of organics and effects on soil microbial biomass[J].Biological Wastes,1988,26(4):235-245.
[52] TAI Yuanliang,DEMPSEY B A.Nitrite reduction with hydrous ferric oxide and Fe(Ⅱ):stoichiometry,rate,and mechanism[J].Water Research,2009,43(2):546-552.
[53] OTTLEY C J,DAVISON W,EDMUNDS W M.Chemical catalysis of nitrate reduction by iron(Ⅱ)[J].Geochimica et Cosmochimica Acta,1997,61(9):1819-1828.
[54] MORAGHAN J T,BURESH R J.Chemical reduction of nitrite and nitrous oxide by ferrous iron[J].Soil Science Society of America Journal,1977,41(1):47-50.
[55] MALHI S S,MCGILL W B,NYBORG M.Nitrate losses in soils:effect of temperature,moisture and substrate concentration[J].Soil Biology and Biochemistry,1990,22(6):733-737.
[56] 吕海霞.影响土壤反硝化作用的因素[J].河南农业,2015(17):15.
[57] 徐小亚.增温和干旱对土壤N2O排放和相关微生物的影响[D].杭州:浙江大学,2017.
