肺源性急性呼吸窘迫综合征患者预后影响因素研究
2020-03-09陈伟宋立强
陈伟,宋立强
急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)是一组以肺水肿和轻微肺不张为病理特征、以低氧血症为主要临床表现的临床综合征,其病死率高达40%[1]。ARDS 的致病因素较多,患者间个体差异较大[2],且其早期诊断率较低,进而导致ARDS 患者病死率居高不下,已成为目前临床诊治难点[3]。而探究ARDS 的发病原因及寻找精准评价、预测患者预后的临床标志物非常重要。本研究旨在分析肺源性ARDS 患者预后的影响因素,现报道如下。
1 对象与方法
1.1 研究对象 选取2017 年3 月—2019 年3 月空军军医大学西京医院呼吸与危重医学科收治的肺源性ARDS患者167 例,ARDS 的诊断符合柏林标准[4],且发病原因均为肺炎。根据预后将所有患者分为生存组72 例和死亡组95 例。排除标准:(1)合并血液系统疾病、风湿性疾病、凝血功能障碍者;(2)合并肿瘤者;(3)临床资料不完整者。本研究经空军军医大学西京医院医学伦理委员会审核批准,所有患者知情并签署知情同意书。
1.2 研究方法 回顾性分析167 例患者病历资料并由本院呼吸科监护室医生共同审阅,记录所有患者的临床资料及入院24 h 内实验室检查指标,其中临床资料包括年龄、性别、体质指数(BMI)、吸烟史、既往史(包括手术史及高血压、冠心病、脓毒症、其他疾病病史)、慢性气道疾病发生情况〔包括支气管哮喘、慢性阻塞性肺疾病(COPD)及哮喘-慢性阻塞性肺疾病重叠综合征(ACOS)〕、急性生理学与慢性健康状况评分系统Ⅱ(APACHE Ⅱ)评分、住院时间及住院花费。支气管哮喘诊断参照2014 哮喘全球防治倡议(GINA)中的相关诊断标准[5],COPD 诊断参照《慢性阻塞性肺疾病诊治指南(2013 年修订版)》[6]中的相关诊断标准,ACOS 诊断参照慢性阻塞性肺疾病全球倡议(GOLD)和GINA 提出的相关诊断标准[7]。实验室检查指标主要包括炎性指标〔包括白介素6(interleukin-6,IL-6)、肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、C 反应蛋白(C-reactive protein,CRP)及降钙素原(procalcitonin,PCT)〕、肾功能指标〔主要包括血肌酐(serum creatinine,Scr)〕、心肺功能指标〔包括脑钠肽前体(pro brain natriuretic precursor,proBNP)、乳酸、氧合指数(OI)、心肌肌钙蛋白T(cardiac troponin T,cTnT)、心肌肌钙蛋白I(cardiac troponin I,cTnI)〕和凝血功能指标〔包括凝血酶原时间(prothrombin time,PT)和活化部分凝血活酶时间(activated partial thromboplastin time,APTT)〕。
1.3 统计学方法 采用SPSS 22.0 统计软件进行数据处理,符合正态分布的计量资料以表示,采用两独立样本t 检验,不符合正态分布的计量资料以M(QR)表示,组间比较采用Wilcoxon 秩和检验;计数资料分析采用χ2检验;肺源性ARDS 患者预后的影响因素分析采用多因素Logistic 回归分析;绘制受试者工作特征(receiver operating characteristic curve,ROC)曲线以评价OI、APTT 对肺源性ARDS 患者预后的预测价值。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者临床资料比较 两组患者年龄、男性比例、体质指数(BMI)、吸烟史、手术史、高血压病史、脓毒症病史、其他疾病病史及ACOS 发生率比较,差异无统计学意义(P>0.05);死亡组患者中有冠心病病史者所占比例、支气管哮喘发生率低于生存组,COPD 发生率、APACHE Ⅱ评分高于生存组,住院时间长于生存组,住院花费多于生存组,差异有统计学意义(P<0.05,见表1)。
2.2 两组患者实验室检查指标比较 两组患者IL-6、乳酸、cTnI 及PT 比较,差异无统计学意义(P>0.05);死亡组患者TNF-α、CRP、PCT、Scr、proBNP、cTnT高于生存组,OI 低于生存组,APTT 长于生存组,差异有统计学意义(P<0.05,见表2)。
2.3 肺源性ARDS 患者预后影响因素的多因素Logistic回归分析 将表1~2 中有统计学差异的指标作为自变量,将预后作为因变量(变量赋值见表3)进行多因素Logistic 回归分析,结果显示,OI 是肺源性ARDS 患者预后的保护因素,APTT 是肺源性ARDS 患者预后的危险因素(P<0.05,见表4)。
2.4 OI、APTT 对肺源性ARDS 患者预后的预测价值ROC 曲线显示,OI 预测肺源性ARDS 患者预后的曲线下面积为0.732〔95%CI(0.647,0.816)〕,最佳临界值为179.85 mm Hg,灵敏度为61.5%,特异度为73.5%;APTT 预测肺源性ARDS 患者预后的曲线下面积为0.855〔95%CI(0.793,0.916)〕,最佳临界值为61.79 s,灵敏度为70.9%,特异度为87.2%,见图1。

表1 两组患者临床资料比较Table 1 Comparison of clinical data between the two groups
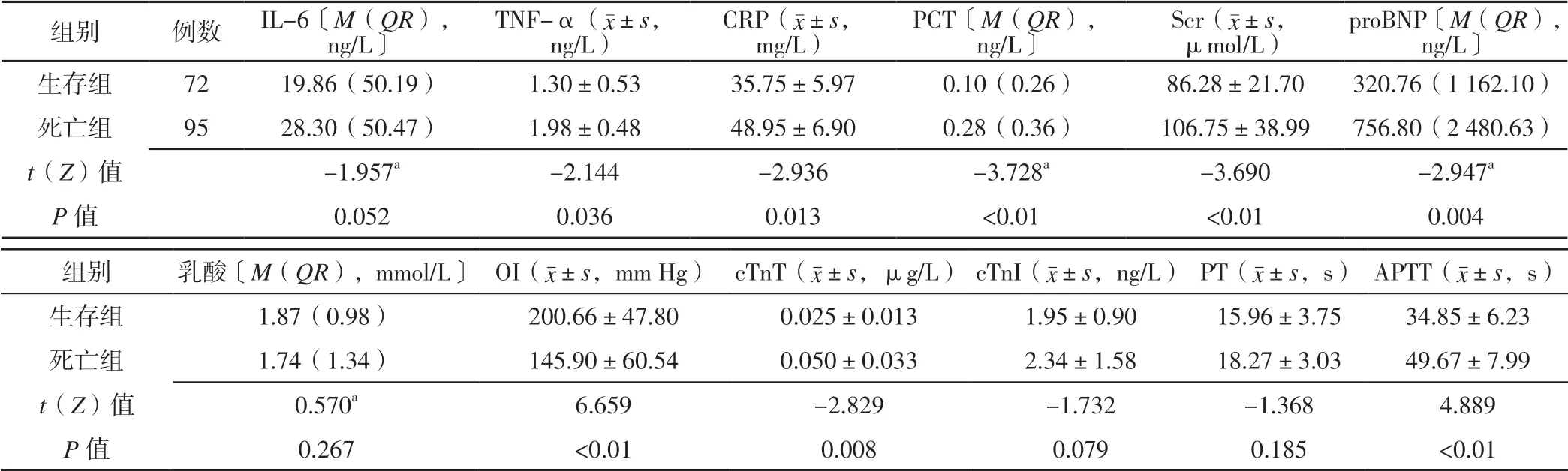
表2 两组患者实验室检查指标比较Table 2 Comparison of laboratory examination results between the two groups

表4 肺源性ARDS 患者预后影响因素的多因素的Logistic 回归分析Table 4 Multivariate Logistic regression analysis on influencing factors of prognosis in patients with pulmonary ARDS
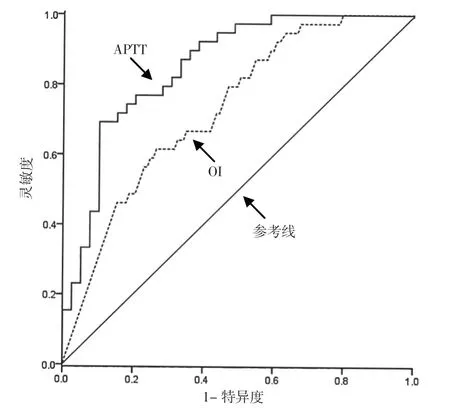
图1 OI、APTT 预测肺源性ARDS 预后的ROC 曲线Figure 1 ROC curve for predictive value of OI and APTT in predicting the prognosis in patients with pulmonary ARDS
3 讨论
近年越来越多的学者认为,ARDS 的发病机制主要涉及过度炎性反应、血管内皮功能损伤、抗凝机制异常等[8],此外有学者开始从基因组学、代谢组学等方面探究ARDS 的发病机制[9],但ARDS 病程发展快、发病原因多样,导致患者缺乏个体化治疗方法。
ARDS 根据致病原因分为肺源性ARDS 和非肺源性ARDS,其中肺源性ARDS 主要与严重的肺上皮细胞损伤有关,而非肺源性ADRS 则主要表现为严重的内皮细胞损伤[10];此外,肺源性ARDS 和非肺源性ARDS 患者预后的预测因子亦不同[11]。本研究以肺源性ARDS 为研究对象,结果显示,死亡组患者COPD 发生率高于生存组,但支气管哮喘发生率低于生存组,与AZOULAY 等[12]研究结果表明合并COPD 的ARDS 患者病死率反而较低相矛盾;而COPD 与支气管哮喘的病理过程不同可能是两者合并ARDS 后死亡率不同的原因之一。COPD 与支气管哮喘虽均具有气流受限特征,但支气管哮喘患者吸入支气管扩张剂后第1 秒用力呼气容积(FEV1)改善率常>12%,即支气管舒张试验(+);而多数COPD 患者吸入支气管扩张剂后FEV1改善率常<12%。支气管哮喘与气道慢性炎症有关,部分患者气流阻塞是可逆转的[13];COPD 属于下呼吸道慢性炎性反应,其多伴有小气道功能受损和弥散功能下降,气流受限常呈渐进性发展,并伴有气道高反应性[14]。COPD 与ARDS 的炎性反应机制相似,二者均有中性粒细胞介导的白介素8(IL-8)、IL-6、TNF-α 释放的炎性反应过程[15-16],这可能导致炎性作用叠加;而支气管哮喘主要以嗜酸细胞介导的炎性反应为主,这可能是合并COPD 患者病死率更高的原因之一。
目前,临床较认可ARDS 的主要发病机制为炎性反应严重失衡加重肺泡上皮/内皮组织损伤[17],其中TNF-α 参与诱导细胞因子表达及损伤肺泡毛细血管屏障[18],PCT 是临床上可反映炎性反应严重程度的常用指标[19]。本研究结果显示,死亡组患者TNF-α、CRP、PCT 高于生存组,提示肺源性ARDS 患者预后与炎性反应严重程度有关,与既往研究结果相一致[20-21]。
OI 是ARDS 诊断和分级的主要指标,低氧血症是ARDS 的主要临床表现之一。本研究结果显示,OI 是肺源性ARDS 患者预后的保护因素,且OI 预测肺源性ARDS 患者预后的曲线下面积为0.732,与既往研究结果相一致[22]。APTT 能反映内源性凝血功能[23]。ARDS 凝血功能异常表现为肺泡腔纤维蛋白沉积,分析其原因可能与过度炎性反应诱导纤溶损伤有关[24]。本研究结果显示,APTT 是肺源性ARDS 患者预后的危险因素,且APTT 预测肺源性ARDS 患者预后的曲线下面积为0.855,分析其可能原因主要如下:(1)APTT 是血小板减少症的高危因素之一[25],而血小板减少又与肺源性ARDS 患者预后密切相关[26-27];(2)肺源性ARDS 患者全身凝血纤溶系统异常[28];(3)本研究纳入的研究对象均为肺源性ARDS,且76.65%的患者合并慢性气道疾病,而慢性气道疾病患者急性加重期常处于高凝状态[29-30]。
综上所述,OI、APTT 是肺源性ARDS 患者预后的独立影响因素,OI<179.85 mm Hg、APTT>61.79 s 的肺源性ARDS 患者死亡风险较高;但本研究样本量较小且未对ARDS 严重程度进行分层分析,今后仍需扩大样本量、增加时间截点,以寻找能有效预测ARDS 患者预后的影响因素。
作者贡献:陈伟进行文章的构思与设计,数据收集、整理、分析,结果分析与解释,并负责撰写论文;宋立强进行研究的实施与可行性分析,负责文章的质量控制及审校,并对文章整体负责,监督管理。
本文无利益冲突。
