DSA引导下经皮胃造瘘术治疗食管癌伴吞咽困难
2020-01-09文秋月胡鸿涛黎海亮
王 谭,文秋月,胡鸿涛,黎海亮
(郑州大学附属肿瘤医院 河南省肿瘤医院放射介入科,河南 郑州 450008)
食管癌是常见恶性肿瘤之一,在我国的发病率和死亡率均居世界首位[1],常由于吞咽困难、严重肿瘤负荷及放射和化学治疗后严重不良反应导致发生营养不良。X线引导下经皮胃造瘘术(percutaneous radiologic gastrostomy, PRG)是指在X线设备引导下将胃造瘘管自腹部体表插入至胃腔内,以提供肠内营养,从而改善吞咽困难患者的营养状态,增强免疫功能,加强治疗信心,提高生活质量[2];但该技术少见用于治疗食管癌患者。本研究观察DSA引导下PRG治疗食管癌伴吞咽困难的有效性及安全性。
1 资料与方法
1.1 一般资料 回顾性分析2016年3月—2018年11月我院收治的194例食管癌并吞咽困难患者,男153例,女41例,年龄42~88岁,平均(67.0±10.4)岁;TNM分期Ⅱ~Ⅲ期33例、Ⅳ期161例。纳入标准:①经病理检查明确诊断食管癌;②吞咽功能障碍评分>2分(无吞咽困难0分,硬性固体食物吞咽困难1分,仅能吞咽软食2分,仅能进流食3分,完全不能吞咽4分[3]);③预计生存时间>30天。排除标准:①恶病质;②妊娠;③过度肥胖[体质量指数(body mass index, BMI)>40 kg/m2]。
根据是否行PRG将患者分为2组。PRG组80例,男60例,女20例,平均年龄(66.6±10.4)岁;非PRG组114例,男93例,女21例,平均年龄(67.1±10.5)岁。
1.2 仪器与方法 采用Siemens Artis Zeego DSA机为引导设备。术前行消化道造影、上腹部CT或MRI,判断腹腔脏器位置关系和食管狭窄程度。嘱患者术前禁食、水12 h,术前0.5~1.0 h常规肌内注射山莨菪碱(5~10 mg)。
嘱患者仰卧,行表面麻醉口、咽、食管。PRG组:于X线透视下将导丝、导管引入胃腔内,而后沿导管注入500~1 000 ml空气充盈胃腔。行C臂CT扫描,确定穿刺点、穿刺角度和深度,在透视下用鲋田式胃壁固定器在预定穿刺处垂直穿刺,注入对比剂证实其进入胃腔后固定胃壁。行C臂CT扫描后设计穿刺针道,以携带可撕脱导引鞘的16F穿刺针穿刺,然后拔除穿刺针,保留鞘管,经鞘管注入对比剂确认其位于胃腔,之后经鞘管引入15F胃造瘘管,经尾端注入对比剂证实其进入胃腔,而后向气囊内注入生理盐水4 ml,见图1。术后禁食、水24 h,复查造影确认造瘘管位置正常、无对比剂外漏等并发症后,经造瘘管灌注无渣流食。非PRG组:嘱患者在透视下口服泛影葡胺进行食管造影,确定食管狭窄部位,标记狭窄段上下端。将导丝通过食管引入胃腔内,而后沿导丝将支架置入器引入食管腔,准确定位后后拉外鞘,使支架释放、膨胀并留置于食管狭窄处,上下端分别覆盖狭窄上下端2 cm以上,然后撤出支架置入器。再次口服泛影葡胺食管造影,确认支架位置正确。术后2 h可进无渣流食,2天后若无特殊不适可进半流食,3~4天后可进软食,不可进过硬食物。术后1周复查食管造影,明确支架有无移位。
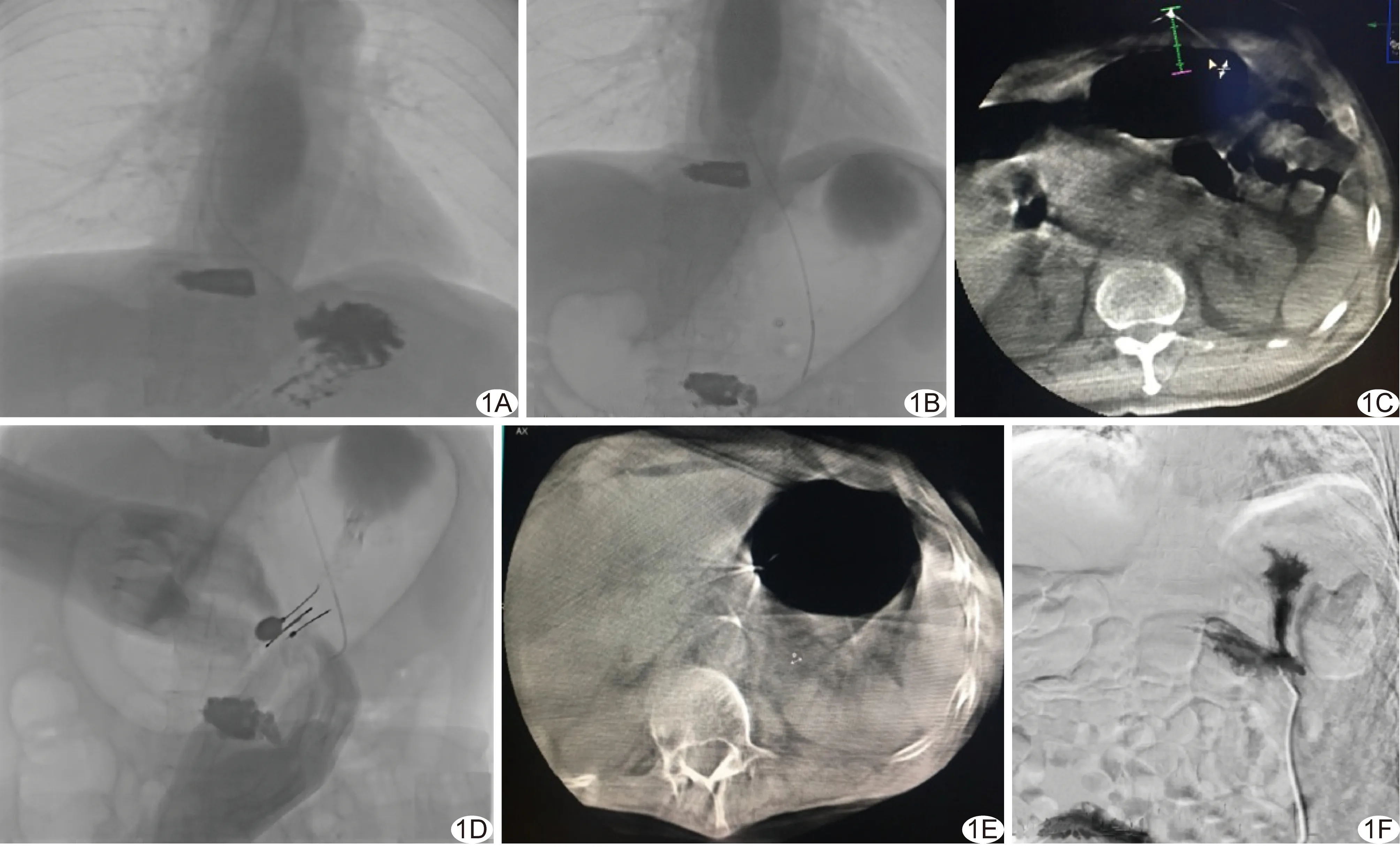
图1 患者男,65岁,食管癌并发吞咽困难,DSA引导下PRG行肠内营养 A.透视下将导丝、导管引入胃腔内; B.沿导管注入500~1 000 ml空气充盈胃腔; C.行C臂CT扫描,确定穿刺点、穿刺角度和深度; D.透视下以胃壁固定针在预定穿刺处垂直刺入,注入对比剂证实在胃腔内后固定胃壁; E.行C臂CT扫描设计穿刺针道; F.经造瘘管尾端注入对比剂证实进入胃腔,而后向气囊注入4 ml生理盐水
对2组患者均于术后进行饮食教育。以患者吞咽困难前正常饮食量、饮食结构和饱腹感为参考,采用主食、蔬菜、水果、肉食搭配,少食多餐原则制定饮食量,2组进食参考量均为非流食状态下150~400 g/天。
1.3 相关指标观察 术前及术后1个月检测2组患者BMI及血清白蛋白、前白蛋白、血红蛋白水平,并统计随访期内吸入性肺炎、消化道出血、食管-气管瘘、食管-纵隔瘘、腹泻及便秘等不良反应。截止随访日期为2019年8月20日。
1.4 统计学分析 采用SPSS 22.0统计分析软件。2组患者年龄、BMI及血清白蛋白、前白蛋白、血红蛋白等计量资料均符合正态分布,以±s表示,组间比较采用t检验;两组性别、肿瘤分期、吞咽困难评分等计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2组患者性别、年龄、肿瘤分期、狭窄食管长度、美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)行为状态评分、吞咽困难评分、组织学分型、化学治疗及放射治疗差异均无统计学意义(P均>0.05),见表1。2组患者术前BMI及血清白蛋白、前白蛋白、血红蛋白水平差异均无统计学意义(P均>0.05),术后1个月PRG组血清白蛋白(t=4.696,P<0.001)、前白蛋白(t=2.163,P=0.032)及血红蛋白水平均高于非PRG组(t=2.362,P=0.020);2组术后1个月血清白蛋白、前白蛋白、血红蛋白水平均低于术前(P均<0.05),见表2。
随访期内,PRG组吸入性肺炎、食管-气管瘘发生率均低于非PRG组(P均<0.05);2组消化道出血、食管-纵隔瘘、便秘及腹泻发生率差异均无统计学意义(P均>0.05),见表3。

表1 2组患者基线资料比较
表2 2组患者术前及术后1个月营养指标比较(±s)

表2 2组患者术前及术后1个月营养指标比较(±s)
组别BMI(kg/m2)白蛋白(g/L)前白蛋白(g/L)血红蛋白(g/L)PRG组(n=80) 术前20.06±1.5436.18±2.840.31±0.60125.00±6.30 术后1个月19.76±1.1334.03±4.95∗0.26±0.05∗113.20±6.30∗ t值0.6172.7455.2577.367 P值0.5380.007<0.001<0.001非PRG组(n=114) 术前19.67±0.5537.11±3.000.30±0.60127.10±6.27 术后1个月19.47±0.5531.11±3.000.24±0.06110.10±6.27 t值2.73115.066-8.10020.476 P值0.007<0.001<0.001<0.001
注:*:与非PRG组相同时间点比较,P<0.05

表3 2组患者术后1个月内不良反应比较[例(%)]
3 讨论
进行性吞咽困难是食管癌患者的主要临床症状[4],导致患者对营养物质摄入不足,加之肿瘤负荷对营养需求增加,使大部分食管癌患者发生营养不良,降低其对放射及化学治疗的耐受性,影响患者总生存期[5]。
目前静脉营养及肠内营养是营养支持治疗的主要方法。与肠外静脉营养相比,肠内营养支持能够促进胃肠道蠕动,调节肠道菌群并预防肠源性感染,故当患者需长期营养支持时,多推荐采用肠内营养[6-7]。PRG是吞咽困难患者肠内营养的常用方法[8],技术成功率较高[9-10],临床应用逐渐广泛,但为有创手术,而食管癌伴吞咽困难患者对各种治疗的耐受性均较差,故对其进行PRG的研究较少。
本研究观察PRG对食管癌伴吞咽困难的治疗效果及安全性,结果显示,术后1个月PRG组血清白蛋白、前白蛋白及血红蛋白水平均高于非PRG组,原因可能是PRG后进食不受患者本人情绪或食欲影响,通过造瘘管更好地补给了肠内营养,使其营养状态相对较好,治疗耐受性较高,控制肿瘤进展效果较佳,而有效控制肿瘤又能降低营养成分的消耗。本研究PRG组患者术后1个月时BMI高于非PRG组,但差异无统计学意义,原因可能为随访时间过短。与PRG组比较,非PRG组吸入性肺炎和食管-气管瘘的发生率显著升高,原因可能包括:①由于食管严重狭窄,经口进食后食物下行不利,易反流,从而引起呛咳,导致吸入性肺炎;②既往研究[11-13]报道,置入食管支架后,随着放射及化学治疗的作用、进食不当及肿瘤进展,支架易移位、再狭窄,尤其是在贲门狭窄部位置入支架后,胃酸反流不受约束,使吸入性肺炎的发生率显著增加;③对于溃疡型食管癌患者,若置入支架,食管蠕动与之长期摩擦势必加重食管壁损伤,且放射及化学治疗的不良反应均易导致食管瘘发生。PRG术后患者较少发生疼痛,且管外口位于腹壁,不影响患者外观形象和心理状况,不会严重影响患者的食欲状况和治疗积极性;管内口位于胃腔,未破坏贲门部生理结构,且与食管壁不接触,不会加重食管壁损伤,故胃食管反流和食管瘘的发生率相对较低。MIN等[14]报道,食管癌患者PRG后不良反应发生率为18.8%(除便秘和腹泻外),本研究PRG组术后1个月不良反应发生率为12.50%(10/80, 除便秘和腹泻外),较文献[14]报道降低,原因可能在于对患者及家属着重强调在补充肠内营养过程中应少量多次注入,不可一次注入过多饮食,亦可能与本研究随访时间较短有关。
综上所述,应用PRG行肠内营养支持治疗食管癌合并吞咽困难患者安全性高,疗效肯定,值得临床推广应用。但本研究仅为单中心回顾性观察,难免存在统计学偏倚,有待进一步完善。
