聚乙二醇干扰素α-2a联合替诺福韦治疗HBV/HCV重叠感染患者的疗效及影响因素分析
2020-01-08
目前乙型肝炎病毒(HBV)感染及丙型肝炎病毒(HCV)感染在全球范围内呈流行趋势,已逐渐成为严重威胁人类健康的主要传染病[1]。随着人们生活方式的改变,临床上HBV/HCV重叠感染的现象变得十分普遍,当患者出现HBV/HCV重叠感染时,可促进慢性肝病的进展及癌变[2]。有研究指出,与单纯感染HBV或HCV的患者相比较,重叠感染患者的肝细胞及肝功能损伤更为严重,重叠感染还将显著升高患者发生肝硬化及肝细胞癌的风险[3]。HBV与HCV之间并没有交叉免疫作用,因此在对HBV/HCV重叠感染患者的治疗过程中,要同时监测HBV和HCV的转阴情况,以便更大程度地清除患者体内的HBV和HCV,从而降低甚至阻断进一步发展成为各种慢性肝病及癌变的风险[4]。本研究选取66例HBV/HCV重叠感染患者,分别采用替诺福韦单药及替诺福韦联合聚乙二醇干扰素α-2a这两种治疗方案,现将结果报道如下。
1 资料与方法
1.1 一般资料
选取2016年10月至2018年12月四川省巴中市中心医院收治的66例HBV/HCV重叠感染患者作为研究对象,按随机数表法分为研究组和对照组,每组各33例。
纳入标准:(1)治疗前HBV-DNA、HCV-RNA定量检测水平均≥6 lg copy/mL;(2)入组前无相关抗病毒治疗史;(3)入组前6个月内未应用可能影响机体免疫功能的相关药物;(4)年龄为20~65岁;(5)患者及家属均知情并签署同意书。
排除标准:(1)合并人类免疫缺陷病毒(HIV)感染者;(2)合并其他类型肝炎病毒感染者;(3)合并肾、肺、心等脏器功能不全者;(4)合并精神异常者;(5)合并肝硬化失代偿期者;(6)哺乳期或妊娠期女性;(7)有干扰素使用禁忌证者。
对照组共33例,年龄为20~65岁,平均年龄(41.9±1.6)岁,其中男性24例,女性9例;研究组共33例,年龄为20~65岁,平均年龄(42.1±1.7)岁,其中男性22例,女性11例。两组患者的性别、年龄差异无统计学意义(P>0.05),具有可比性。本研究获得医院医学伦理委员会批准。
1.2 治疗方法
对照组应用替诺福韦(由成都倍特药业有限公司生产,国药准字H20163436)治疗。每日1次,每次300 mg,饭后温水送服,6个月为1个疗程,共2个疗程[5]。
研究组应用替诺福韦联合聚乙二醇干扰素α-2a(由厦门特宝生物工程股份有限公司生产,国药准字S20160001)治疗。替诺福韦的用法及用量与对照组相同。聚乙二醇干扰素α-2a 1周1次,每次180 μg,皮下注射,6个月为1个疗程,共2个疗程[6]。
1.3 观察指标
观察比较两组治疗后6个月、12个月时HBV-DNA及HCV-RNA的转阴情况。观察比较两组治疗前及治疗后12个月时丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、谷氨酰转肽酶(GGT)、总胆红素(TBil)水平变化。在治疗前及治疗后12个月时,取两组12 h空腹静脉血约4 mL,应用全自动生化分析仪对两组的肝功能指标进行检测。观察比较两组治疗前及治疗后12个月时HBV-DNA和HCV-RNA的定量水平变化。在治疗前及治疗后12个月时,取两组12 h空腹静脉血约4 mL,使用荧光探针技术分别检测两组患者HBV-DNA、HCV-RNA的定量水平。观察两组在治疗过程中的不良反应发生情况。观察影响HBV/HCV重叠感染患者疗效的相关因素。
1.4 统计学处理
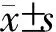
2 结果
2.1 两组治疗后6个月、12个月时HBV-DNA及HCV-DNA的转阴情况
治疗后6个月时,两组的HCV-RNA转阴率差异无统计学意义(P>0.05);治疗后12个月时,研究组的HCV-RNA转阴率高于对照组,差异有统计学意义(P<0.05)。治疗后6个月和12个月时,研究组的HBV-DNA转阴率均高于对照组,差异均有统计学意义(P均<0.05)。详见表1。
2.2 两组治疗前及治疗后12个月时的肝功能指标变化
治疗前,两组的GGT、AST、ALT、TBil水平差异均无统计学意义(P均>0.05)。治疗后12个月时,研究组的GGT、AST、ALT、TBil水平均低于对照组,差异均有统计学意义(P均<0.05)。详见表2。
表1 两组治疗后6个月、12个月时HBV-DNA及HCV-RNA的转阴情况/例(%)
注:“—”表示无数据

表2 两组治疗前及治疗后12个月时的各项肝功能指标变化()
注:与同组治疗前相比,aP<0.05;与对照组治疗后相比,bP<0.05
2.3 两组治疗前及治疗后12个月时HBV-DNA及HCV-RNA的定量水平变化
治疗前,两组的HBV-DNA及HCV-RNA定量水平差异均无统计学意义(P均>0.05)。治疗后12个月时,研究组HBV-DNA及HCV-RNA的定量水平均低于对照组,差异均有统计学意义(P均<0.05)。详见表3。
2.4 两组在治疗过程中的不良反应发生情况
两组在治疗过程中的不良反应发生情况差异无统计学意义(P>0.05),详见表4。
2.5 影响HBV/HCV重叠感染患者疗效的相关因素
依据两组接受治疗前的一般资料及相应治疗后的转阴情况,分析影响HBV/HCV重叠感染患者疗效的相关影响因素。结果提示,性别、平均年龄、治疗前的HBV-DNA及HCV-RNA定量水平是影响HBV/HCV重叠感染患者疗效的相关独立因素,详见表5。

表3 两组治疗前及治疗后12个月时HBV-DNA及HCV-RNA的定量水平变化()/lg copy·mL-1
注:“—”表示无数据
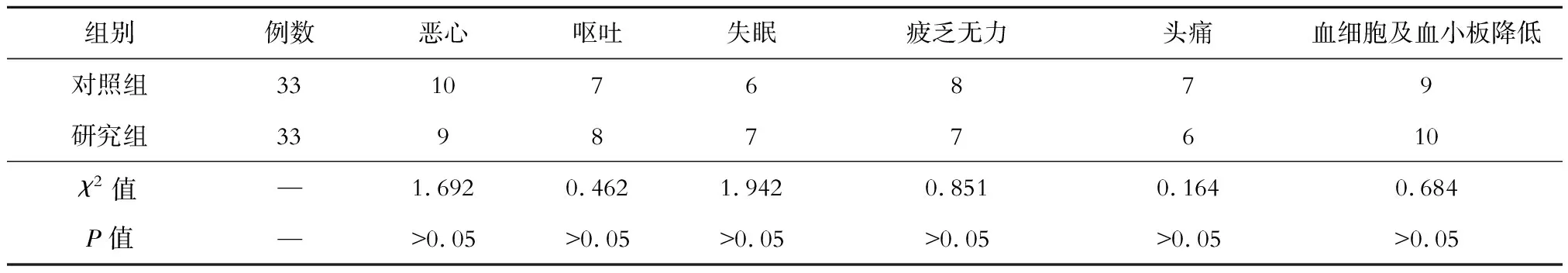
表4 两组在治疗过程中的不良反应发生情况/例
注:“—”表示无数据
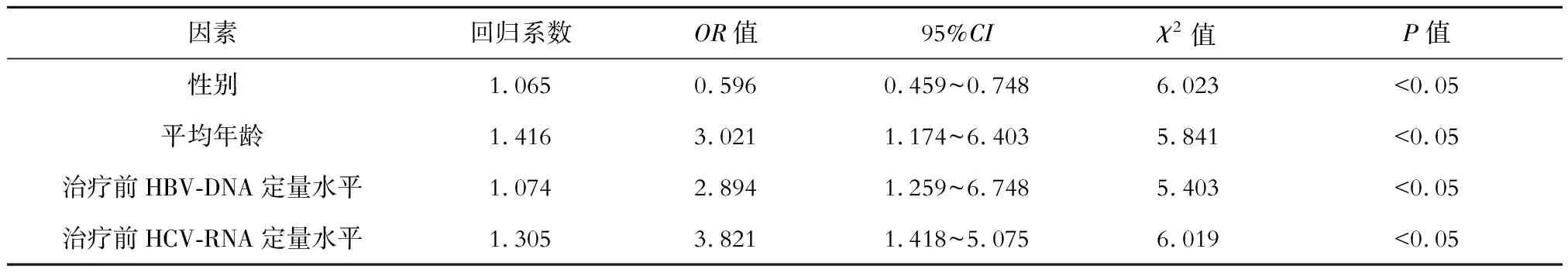
表5 影响HBV/HCV重叠感染患者疗效的相关多因素分析结果
3 讨论
替诺福韦是属于单磷酸腺苷的一种无环核苷(酸)类似物,与临床上常用的阿德福韦酯十分相似[7]。替诺福韦的作用机制主要是通过在细胞中被磷酸化,形成带有药理活性的代谢性产物——替诺福韦二磷酸,其可以使患者体内的病毒DNA复制而产生竞争性的阻滞作用,是目前临床上抗病毒效能较强的药物,且耐药屏障较高[8]。欧盟委员会(EC)和美国食品药品管理局(FDA)分别在2008年4月和8月批准替诺福韦在其辖区内可用于进行相关的抗病毒治疗,替诺福韦被推荐为临床一线抗病毒用药[9]。研究证实,替诺福韦对肝硬化及乙型肝炎患者均具有较好的远期疗效,且安全性较高[10]。有国外研究表明,替诺福韦在治疗出现核苷酸类药物(如阿德福韦酯、拉米夫定等)耐药反应的患者时,其抗病毒效果同样显著,且患者耐受性较好,不良反应较少[11]。
干扰素属于一种糖蛋白类物质,是机体在响应不同病毒等刺激因素时分泌的[12]。干扰素目前已广泛应用于免疫调节、抗纤维化、抗病毒及抗肿瘤治疗等。在治疗HBV/HCV重叠感染患者时,干扰素可以与机体的肝细胞膜接触,在细胞中生成一种具有特异性的蛋白类物质[13]。此外,干扰素还能够提高机体中T淋巴细胞水平,从而有效清除肝细胞中的肝炎病毒。但干扰素在临床上治疗肝炎时,对血药浓度的要求较高,必须使血药浓度持久稳定才能达到理想的抗病毒效果。传统干扰素的临床半衰期较短,同时在患者体内维持有效血药浓度的时间也较短,在用药后24 h左右,机体中干扰素的血药浓度就会降至低水平[14]。聚乙二醇干扰素α-2a通过将聚乙二醇与干扰素α-2a进行共价结合,既能够有效增加相对分子质量,还能形成新的分支组织结构,延长机体的吸收时间,增加其在患者机体中的稳定性,延长半衰期及有效血药浓度持续时间,从而增强其在肝脏中的抗病毒效果,提高临床疗效。
对于HBV/HCV重叠感染的患者,单一使用干扰素或核苷酸类药物进行抗病毒治疗时,因患者体内存在两种病毒,其相互作用会直接影响药物疗效,应答率显著低于单独感染HBV或HCV的患者[15]。因此,选择半衰期更长的聚乙二醇干扰素α-2a联合替诺福韦进行抗病毒治疗,可提高对重叠感染患者的临床疗效。本研究结果显示,治疗后研究组的转阴率及肝功能指标均优于对照组(P均<0.05),提示聚乙二醇干扰素α-2a联合替诺福韦能显著提高HBV/HCV重叠感染患者的临床疗效。
综上所述,应用聚乙二醇干扰素α-2a联合替诺福韦治疗HBV/HCV重叠感染患者,可显著提高患者的HBV-DNA及HCV-RNA转阴率,改善患者的肝功能指标;治疗前,患者的HBV-DNA及HCV-RNA的定量水平越低,预示药物对患者的疗效越理想。
