溶胶凝胶法制备nAl/CuO纳米复合材料
2020-01-01王新新熊继军杜拴丽陈晓勇
王新新,熊继军,杜拴丽,陈晓勇,
(1.中北大学 化学工程与技术学院,山西 太原 030051;2.中北大学 仪器与电子学院,山西 太原 030051)
亚稳态分子间混合物(MIC)是一种反应快、放热高、钝感安全的高性能含能材料,是各国大力发展的国防领域技术之一[1]。在众多MIC体系中,纳米铝(nAl)/CuO复合含能材料是最具代表性的MIC材料[2]。由于溶胶-凝胶技术(sol-gel)能对组分进行精确控制,进而使组分密度可控且混合均匀,故多采用该法制备nAl/CuO纳米含能材料[3-5]。然而文献报道价态低于+3价的金属离子与环氧化物易形成沉淀而难以凝胶[6-7],且传统sol-gel法制备nAl/CuO MIC时,多在酸性环境下进行,凝胶条件较难控制,容易导致混合效果不好。为此,本文发展了弱碱性环境下的nAl/CuO MIC的sol-gel制备技术。弱碱性环境能促进Cu盐的水解和环氧丙烷的开环,并可快速凝胶从而减缓nAl的沉降,进而改善nAl在CuO中分散。
1 实验部分
1.1 材料与仪器
纳米铝(nAl,粒径100 nm),上海超威纳米材料有限公司,买来即用,无进一步处理;三水合硝酸铜[Cu(NO3)2·3H2O,纯度>99.5%]、无水乙醇、十二烷基磺酸钠、尿素、环氧丙烷均为分析纯;去离子水,实验室自制。
DY2103QT超声波清洗仪;DF-101S集热式恒温加热磁力搅拌器;FD-1A-50真空冷冻干燥机;1503VP扫描电子显微镜(SEM);NETZSCH STA 449C(TG)高量程DSC;TENSOR 27红外光谱分析仪(FTIR);D8 Advance X射线衍射仪(XRD)。
1.2 nAl/CuO复合材料的制备
称取一定量的十二烷基磺酸钠、尿素与5 mL去离子水置于三口瓶中,在50 ℃的恒温水浴锅中以350 r/s搅拌1 h,测其pH在7~8之间显弱碱性;将Cu(NO3)2·3H2O分散在3 mL无水乙醇中,置于超声水浴中超声30 min后滴加入三口瓶中;取5 mL环氧丙烷滴加入三口瓶中,260 r/s搅拌20 min。取纳米铝粉(nAl)将其分散在3 mL无水乙醇中,密闭后置于超声水浴中超声10 min后滴加入三口瓶中;搅拌1 h后取出密封。在冰箱中静置,即得湿凝胶。
在冰箱中静置老化数天后,将凝胶置于真空冷冻干燥机中进行冷冻干燥,即得nAl/CuO复合材料。
1.3 nAl/CuO复合材料的表征
使用扫描电子显微镜(SEM)表征nAl/CuO纳米含能材料形貌结构;使用高量程DSC表征nAl/CuO纳米含能材料能量释放特性,温度范围为25~800 ℃,升温速率为20 ℃/min。使用红外光谱分析仪FTIR对n-Al-CuO结构进行表征。使用X射线衍射仪(XRD)(CuO Kaγ=0.154 18 nm)表征nAl/CuO纳米含能材料的结构组成。
2 结果与讨论
2.1 nAl/CuO复合材料的湿凝胶
图1是酸、碱条件下nAl/CuO复合体系湿凝胶的光学照片(试剂瓶躺倒拍照是为了直观展示弱碱性环境下CuO凝胶制备成功)。

图1 酸(上)、碱(下)环境中制备的 nAl/CuO体系湿凝胶
由图1可知,酸性环境中制备的nAl/CuO复合体系的湿凝胶清晰的展示了分层现象,瓶底黑色部分显然是nAl沉淀,而黑色沉淀之上是CuO凝胶,因此说明酸性条件下sol-gel法制备的nAl/CuO体系是不稳定的,nAl与CuO凝胶的“亲和”性差,不利于nAl与CuO的分散。而碱性条件下sol-gel法制备的nAl/CuO体系(图1下)中黑色物质均匀的分散在CuO凝胶中(试剂瓶中上部没有单独纯净的CuO蓝色凝胶层),nAl很好地悬浮在CuO凝胶中,在观察时间内并没有出现nAl沉淀现象。说明碱性条件下的sol-gel技术有利于改善nAl与CuO的混合和分散。
2.2 nAl/CuO纳米复合材料形貌分析
为进一步考察材料结构和直观观察nAl在CuO基体的分散性,使用SEM观察了所得nAl/CuO纳米复合材料的表面形貌,结果见图2。

图2 nAl/CuO纳米复合材料的SEM图
由图2可知,nAl/CuO纳米复合材料呈现出明显的凝胶网络结构,球形纳米铝粒子的尺寸在50 nm 左右,均匀的镶嵌在凝胶网络结构中。nAl粒子表面吸附了大量的微细CuO颗粒,表明CuO凝胶对nAl粒子进行了较好的包覆,这种包覆有利于氧化剂与还原剂的快速放能反应。同时发现体系内存在大量的溶胶孔洞,孔洞结构使nAl/CuO纳米复合材料具有极大的比表面积,进而使体系具有更高的反应活性。
2.3 nAl/CuO复合材料的红外光谱分析
nAl/CuO复合材料的FTIR谱图见图3。
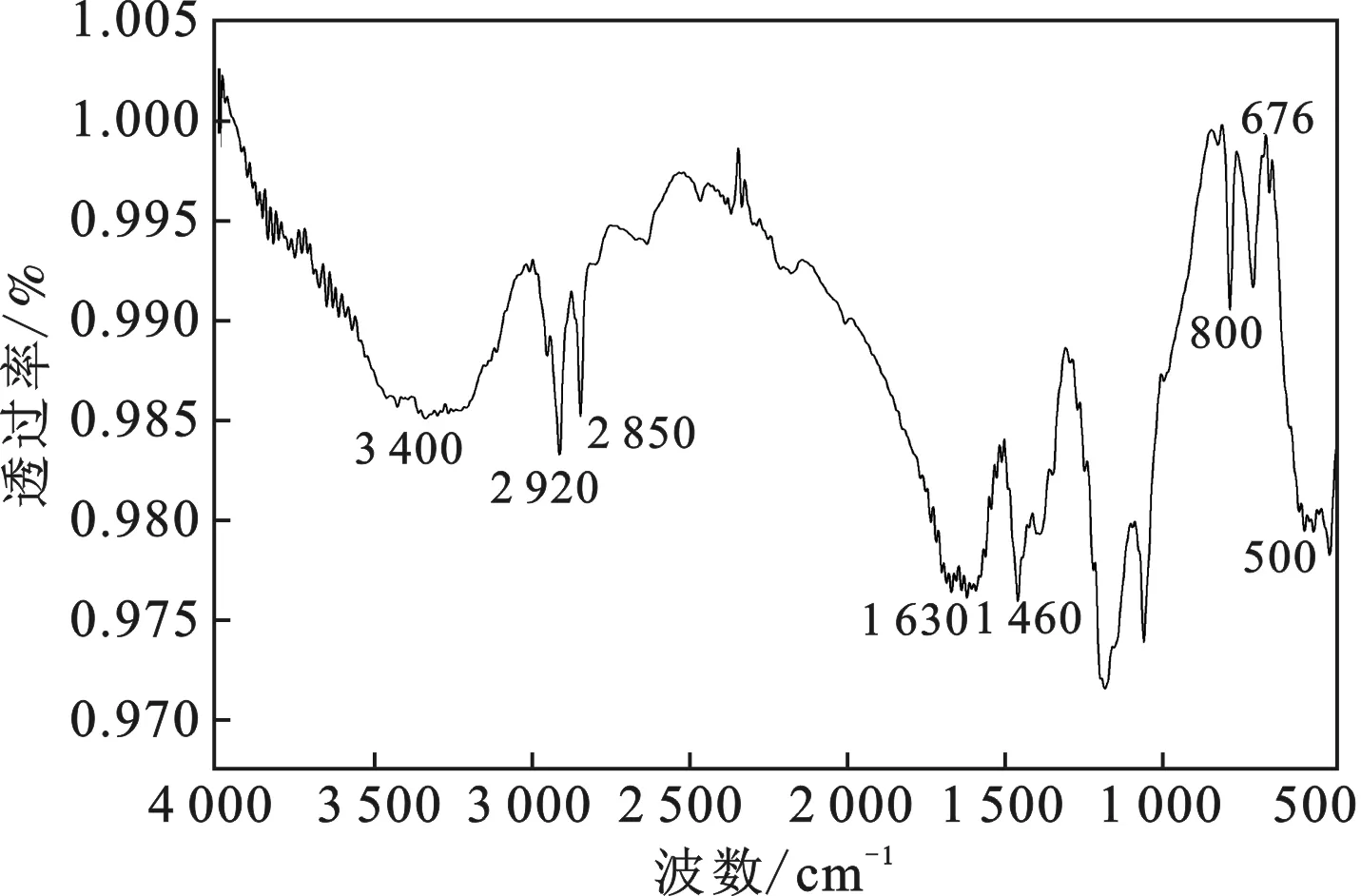
图3 nAl/CuO纳米复合材料的红外光谱
由图3可知,在3 400,1 630 cm-1波数附近都显示出较强吸收峰,表明复合材料中仍含有微量的水。这是由于复合材料在冻干过程中,水、乙醇等有机溶剂并未完全除去[8]。而在1 000~1 500 cm-1的强特征吸收峰是由于N—O键振动引起的,在2 920,2 850,1 460 cm-1处的吸收峰是由于表面活性剂的饱和碳C—H伸缩振动引起的,这表明表面活性剂对原料进行了较好的包覆,从而引起吸收峰位置的偏移。而800 cm-1波数以下,主要为铜氧键的吸收峰,其中676,500 cm-1为Cu—O键的伸缩振动[9]。这凝胶体系中证明CuO前驱体的存在,即所制得的干凝胶由nAl/CuO组成。为进一步支持这一论证我们对所制干凝胶结构进行了X射线衍射。
2.4 nAl/CuO复合材料的成分分析
nAl/CuO复合材料的XRD谱图见图4。

图4 nAl/CuO纳米复合材料的XRD图
由图4可知,由于22.18,35.5°处衍射峰太强导致其他衍射峰强度变得过弱,故在插图中放大了部分曲线。当 2θ角为38.43,44.64,65.04,78.2°处出现了Al的特征衍射峰,分别对应铝面心结构的(111)、 (200)、 (220)和(311)晶面(PDF:04-0787),证明原料铝粉为典型的立方晶系。样品的XRD图谱中包含有一些弥散较宽的衍射峰和尖锐的衍射峰。由谢乐公式可知,当衍射峰较弥散时该样品具有细小的纳米结构。对比CuO材料的标准图谱可知,在2θ为 32.47,35.5,38.79,48.90,53.46,58.24,61.55,66.31,68.13,72.52,75.16°处分别出现对应于单斜晶型CuO(JCPDS号:05-0661)结构 (110)、(111)、(111)、(202)、(020)、(202)、 (113)、(311)、(220)、(311)、(222)衍射晶面的衍射峰,对应CuO凝胶特征衍射峰晶型较为完整[10]。
2.5 nAl/CuO纳米复合材料能量特性分析
nAl/CuO纳米复合材料的热分析是在惰性气体N2气氛下以20 ℃/min的升温速率进行的,由图5可知,该反应放热峰较多,487 ℃以下的吸、放热峰表明所制备nAl/CuO纳米复合材料中仍存在一些未除净的有机杂质,这与红外光谱中所得结论完全相符。反应起始温度为487 ℃,且存在一个主要放热峰在578 ℃左右,说明反应多在固-固相完成。经计算放热量为1 018 J/g,是理论反应热(4 077 J/g[11])的25%,相比自组装[11]、球磨[12]、溅射[13]等方法制备的nAl/CuO体系放热量仍有一些差距,但sol-gel方法制备过程更加安全、低成本、分散均匀。

图5 nAl/CuO纳米复合材料的DSC热行为曲线
3 结论
在弱碱性环境下制备了高反应活性的nAl/CuO纳米复合材料,并用FTIR、XRD、SEM 及DSC对nAl/CuO纳米复合材料进行了表征。结果显示,相比酸性sol-gel体系,在碱性催化剂环境下nAl/CuO纳米复合材料可快速凝胶且凝胶体系混合均一,SEM观察具有明显的纳米级别的分散水平与凝胶网络结构;DSC测试放热量为1 018 J/g。该结果可以为sol-gel法制备nAl/CuO纳米含能材料提供新思路和数据支撑。
