基于相图原理定量预测(Mg1-x-yBaxSry)1.95SiO4∶0.05Eu系列荧光粉的结构和发光性能
2019-12-20孙传耀高明远
汪 雨,罗 岚,2*,郭 锐,孙传耀,高明远
(1. 南昌大学 材料科学与工程学院,江西 南昌 330001;2. 南昌大学 江西省轻质高强结构材料重点实验室,江西 南昌 330001)
1 引 言
稀土离子掺杂正硅酸盐荧光粉性状优良、结构稳定、化学和热稳定性好,且原料广泛、制备工艺简单,是具有较高经济价值和社会价值的荧光粉[1-3]。Poort、Barry等最早研究了Eu掺杂的正硅酸盐体系,发现荧光粉有着较大可见光发射范围,可覆盖蓝色到黄色可见光[4-6]。正硅酸盐随碱土离子种类及配比的不同,可以有多种物相,如Ba2SiO4、α-Sr2SiO4、β-Mg2SiO4是正交相,β-Sr2SiO4是单斜相,γ-Mg2SiO4是立方相[7-9]。M3MgSi2O8(M=Ba,Sr, Ca)荧光粉由于M离子种类不同可以是单斜或三斜晶系[10-12];且随着烧成温度不同,物相组成有着极大的变化,例如,正硅酸钙Ca2SiO4随着温度的不同组分可发生三斜α-Ca2SiO4(1 400 ℃)、正交高温α′H-Ca2SiO4、正交低温α′L-Ca2SiO4、单斜β-Ca2SiO4(βH,βL)、正交γ-Ca2SiO4五种晶型转变[13]。利用烧成温度和二元碱土离子调配来控制正硅酸盐荧光粉的物相组成,进而调控其发光性能研究较多,但对基于多元碱土离子配比调控物相及其发光性能的研究较少。本文在1 200 ℃制备了(Mg1-x-yBaxSry)1.95SiO4∶0.05Eu系列荧光粉,系统地研究了随着三元碱土离子配比变化其正硅酸盐物相组成、发光性能的变化规律;借鉴相图建立方法由样品发射光谱得出了CIE色像散点并基于散点分布建立 (Mg1-x-yBaxSry)1.95SiO4∶0.05Eu三元色像图,优选高效荧光粉;同时探讨单相区和混合相区发光性能的变化内在机制,建立组分-结构-发光性能关联。
2 实 验
2.1 (Mg1-x-yBaxSry)1.95SiO∶0.05Eu粉体制备
采用高温固相法制备(Mg1-x-yBaxSry)1.95SiO4∶0.05Eu荧光粉末(总计44个样品),其中包括3个二元碱土离子配比系列(Mg2SiO4-Sr2SiO4、Ba2SiO4-Sr2SiO4、Mg2SiO4-Ba2SiO4)、3个三元碱土离子配比系列(Ba分别保持0.2、0.6不变而Mg/Sr比连续变化,Mg/Sr比保持1/4不变而Ba含量连续变化)、以及若干散点样品如(Ba0.65Sr0.35)1.95SiO4∶0.05Eu、(Mg0.35Ba0.65)1.95SiO4∶0.05Eu、(Ba0.68-Sr0.12Mg0.2)1.95SiO4∶0.05Eu、(Ba0.67Mg0.13Sr0.2)1.95-SiO4∶0.05Eu。其制备过程为:按照化学计量比称量BaCO3、MgCO3、SrCO3、SiO2(天津市大茂化学试剂厂,分析纯)、Eu2O3等原料,混合BaF2(0.7%)和碳粉(3%),在刚玉坩埚中充分研磨,20 ℃/min升温至1 200 ℃保温3 h,随后随炉冷却,研磨得到对应粉末样品。
2.2 结构和性能表征
采用PANalytical X射线衍射仪(Cu-Kα源,步长0.001°,每步滞留时间1 s)进行X射线衍射(X-ray diffraction,XRD)分析。选用PE公司的FS F-4500荧光光谱仪对样品进行光谱分析(Photoluminescence spectrum,PL)测试,并由发射光谱计算得到CIE值(Commission International DE L’elairage)进而得到发光色像示意图。利用WFH-203B型三用紫外分析仪对样品254 nm和365 nm激发下的荧光发射进行观察,同时数码相机记录样品发光状态。采用Hamamatsu公司的C9920-02G量子效率测量仪测量其量子效率(Absolute PL quantum yields,QE)。
3 结果与讨论
3.1 结构分析
3.1.1 物相组成
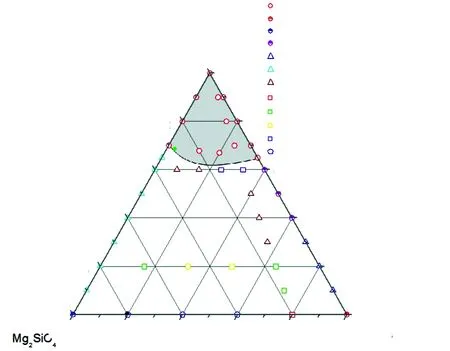
1 200 ℃煅烧得到(Mg1-x-yBaxSry)2SiO4中二元和三元系列粉末的相组成如图1(其中,圆形标注为单相区,半填充圆形为双相区,三角形为三相区,方形为四相区,五边形为五相区,且形状相同颜色不同代表相数目相同但相组成不同)和表1所示。(Mg1-x-yBaxSry)2SiO4涉及的物相有γ-Mg2SiO4、β-Mg2SiO4、MgSr3Si2O8、Ba2SiO4、α-Sr2SiO4、β-Sr2SiO4六种(对应的晶体结构信息如表2所示),其中γ-Mg2SiO4、β-Mg2SiO4、MgSr3Si2O8相中的Mg离子配位数较少,其对应的位点的空间较小,发生Eu离子取代后不利于大半径的Eu2+(0.135 nm,CN=10)而利于小半径的Eu3+(0.095 nm,CN=6 )存在。由物相分析可知(图1),(Mg1-x-yBaxSry)1.95SiO4∶0.05Eu粉末相组成随着组元变化存在渐变性,即端点出发物相组成数目逐渐增多,且物相组元含量呈逐渐减少或逐渐增多的连续变化;在富Ba端形成了Ba2SiO4单相相区。为进一步确定单相区的范围,对(Ba0.65Sr0.35)2SiO4、(Mg0.35Ba0.65)2SiO4、(Ba0.68Sr0.12Mg0.2)2SiO4、(Ba0.67Mg0.13Sr0.2)2SiO44个散点进行物相分析,其中(Mg0.35Ba0.65)2SiO4为Ba2SiO4、β-Mg2SiO4、γ-Mg2SiO4混合物,其余3个样品均为单一Ba2SiO4相,由此得出如灰色标识的Ba2SiO4单相区(单一Mg2+或Sr2+的固溶度为30%和35%)。

图1 (Mg1-x-yBaxSry)2SiO4相图
Fig.1 Phase diagram of (Mg1-x-yBaxSry)2SiO4powder(Carbon 3%, BaF20.7%, 1 200 ℃/3 h)
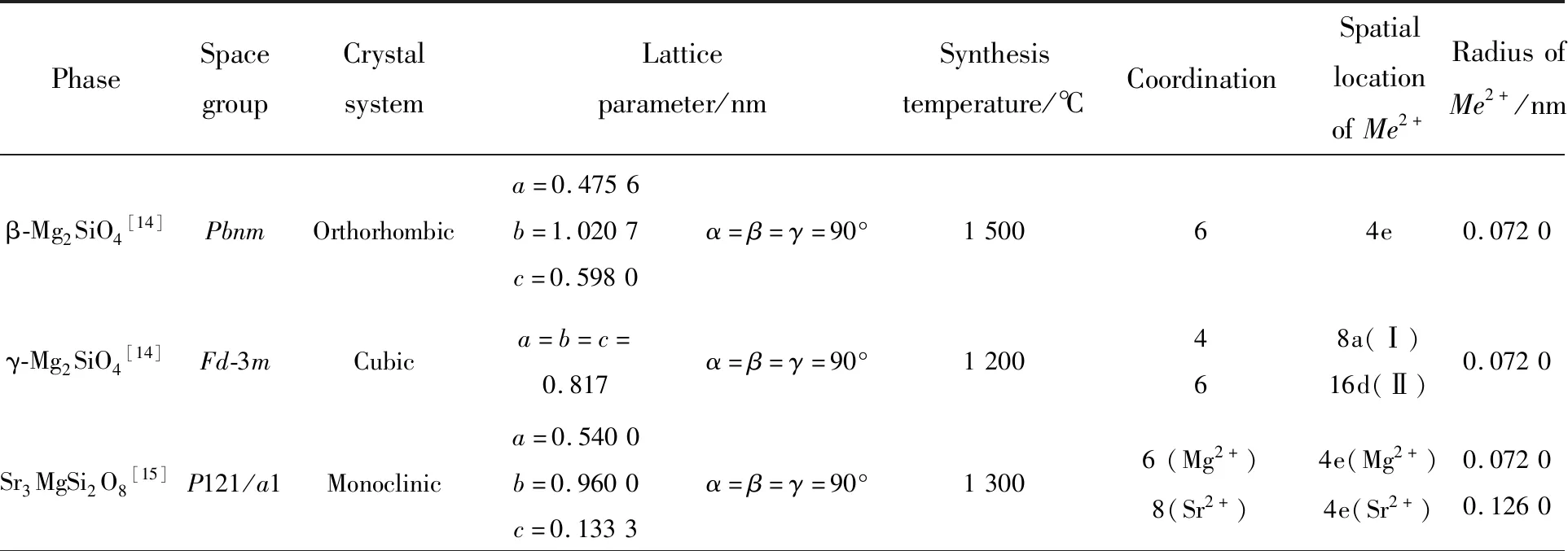
表1 (Mg1-x-yBaxSry)2SiO4粉末中物相结构及其发光性能
Tab.1 (Mg1-x-yBaxSry)2SiO4powder phase composition information and its luminescent properties(Carbon 3%, BaF20.7%, 1 200 ℃/3 h)

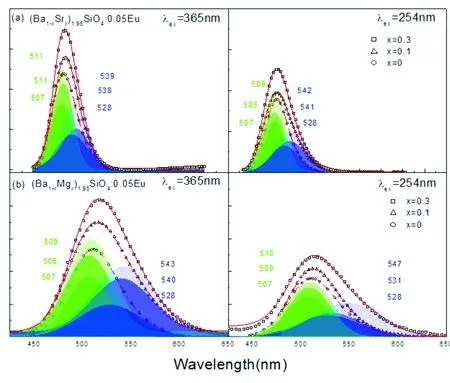
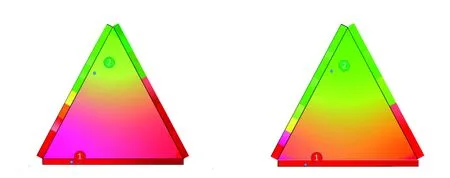
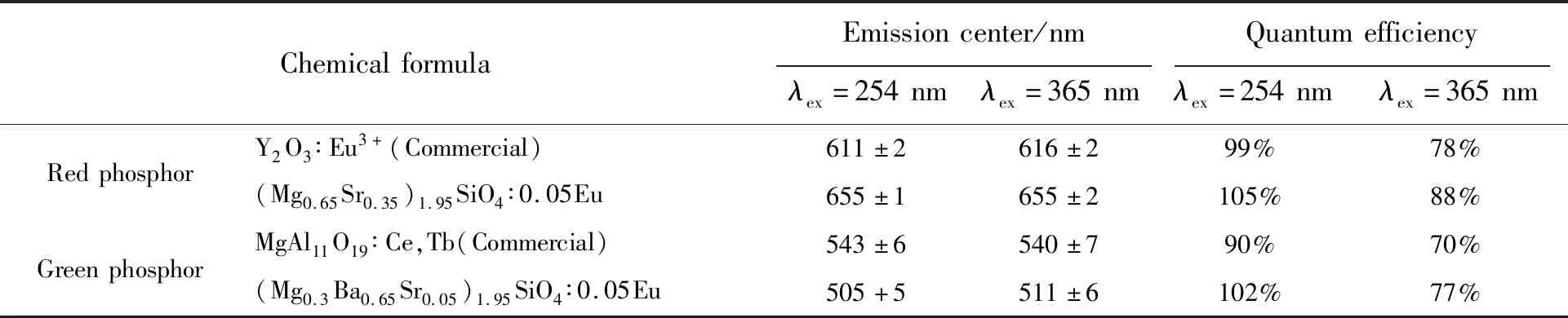
CompositionPhasetransformationLuminecsecnceunderUVlightexcitaionofpowderdopedwithEuion254nm365nm(Mg1-xBax)2SiO4(x=0,0.1,0.2,0.3,0.4,0.5,0.6,0.65,0.7,0.8,0.9,1)β-Mg2SiO4、γ-Mg2SiO4(x=0)→Ba2SiO4、β-Mg2SiO4、γ-Mg2SiO4(0 表1(续) 表2 (Mg1-x-yBaxSry)2SiO4粉末物相结构信息 表2(续) 3.1.2 富钡端单相区结构分析 进一步分析组元对单相区晶体结构的影响(如图2所示)。基于衍射峰位,利用布拉格方程(λ=2dsinθ)和晶面间距计算公式: (1) 可得对应粉末的晶格参数a、b、c值,如表3所示。由表3可知,单相区随着Sr、Mg增加,晶格常数略有减小,且对b影响较大(xSr=0.1、xMg=0.1相比x=0,a值变化不明显,b变化约为0.41%、0.45%,而c变化为0.27%、0.29%)。由Ba2SiO4相晶体结构可知,碱土离子占据2个4c位置,其中位置Ⅰ为10配位沿c轴与硅氧四面体形成链状,而位置Ⅱ为9配位沿着b轴与硅氧四面体成链[19],由晶格计算结果可知小半径的Mg2+、Sr2+(rBa2+(0.134 nm,CN=6)rEu2+(0.112 nm,CN=6)=rSr2+(0.112 nm,CN=6)rMg2+(0.072 nm,MCN=6)[20])固溶时取代9配位的Ba2+(Ⅱ)的倾向更大。此外,衍射峰的半峰宽(Full width at half maxima,FWHM)可以定性表示粉末的结晶状况,即半峰宽越窄结晶程度越高,由单相区粉末的衍射数据可见,随着Mg2+、Sr2+固溶,结晶度变好。 图2 Ba2SiO4相(Ba1-xMex)1.95SiO4∶0.05Eu(Me=Mg或 Sr)粉末的XRD图 Fig.2 XRD patterns of Ba2SiO4-phase (Ba1-xMex)1.95SiO4∶0.05Eu(Me=Mg or Sr) powders(Carbon 3%, BaF20.7%,1 200 ℃/3 h) 由上述分析可知,(Mg1-x-yBaxSry)2SiO4粉末按相组成可分为混合物区和富钡单相区;混合物相区越靠近端点相组成越简单且随着组元增加相组成越复杂;单相区在富钡端,即为Ba2SiO4单相,随着小半径的Mg2+、Sr2+固溶,晶格参数减小,结晶状态变好;相组成随着组元呈现渐变性。此外,粉末主要涉及6种物相,且含镁物相其对应碱土离子配位空间较小,Eu离子取代后倾向形成+3价;Ba2SiO4晶体结构中当Mg2+、Sr2+取代Ba2+时,倾向于9配位的Ba2+(Ⅱ)位置。 表3 Ba2SiO4相(Ba1-xMex)1.95SiO4∶0.05Eu(Me=Mg or Sr)粉末的结构参数 Tab.3 Structural parameters of Ba2SiO4-phase (Ba1-xMex)1.95SiO4∶0.05Eu(Me=Mg or Sr) powders(Carbon 3%, BaF20.7%, 1 200 ℃/3 h) Composition(121)(112)(130)a/nmb/nmc/nmV/nm3FWHM(200)(Ba0.65Mg0.35)2SiO426.07529.63330.4210.57921.01890.74910.44210.108(Ba0.9Mg0.1)2SiO426.06829.61330.4400.57941.01950.74950.44270.146(Ba0.65Sr0.35)2SiO426.14029.58030.4200.57931.01850.74910.44200.129(Ba0.9Sr0.1)2SiO426.10129.66030.4480.57961.01970.74970.44310.148Ba2SiO428.25529.59923.6640.58201.02190.75170.44700.150(Ba0.68Sr0.12Mg0.2)2SiO426.07629.63230.4220.57941.01910.75110.44360.125(Ba0.67Mg0.13Sr0.2)2SiO426.00929.62230.4990.57951.01930.75120.44370.124标准Ba2SiO426.09629.66130.4400.58051.02000.74990.4440 3.2.1 紫外激发和发射光谱分析 对粉末进行荧光光谱分析(图3),由发射光谱计算得到其对应的CIE值并得出其对应色像示意图(图4中彩色条)。对粉末进行紫外发光照相记录,如图4所示。二元组分样品中:(Mg1-xBax)1.95SiO4∶0.05Eu存在Eu3+红光发射(595 nm的5D0→7F1跃迁和615 nm的5D0→7F2跃迁发射)和Eu2+(510 nm的4fn→4fn-15d),随着x的增大红光发射渐弱绿光渐强(粉末中β-Mg2SiO4和γ-Mg2SiO4逐渐减少而Ba2SiO4相逐渐增多(表1);β-Mg2SiO4和γ-Mg2SiO4相中碱土离子配位数较小不利于Eu2+,而Ba2SiO4相碱土离子配位数较大有利于Eu2+(表2)),荧光粉由红变绿转变点为x254nm≥0.5、x365nm≥0.3;(Ba1-ySry)1.95SiO4∶0.05Eu随着y的增大绿光发射渐弱红光渐强(粉末中β-Sr2SiO4逐渐增加,α-Sr2SiO4和Ba2SiO4相逐渐减少(表1);β-Sr2SiO4碱土离子配位数较小不利于Eu2+,而α-Sr2SiO4和Ba2SiO4相碱土离子配位数较大有利于Eu2+(表2)),荧光由绿变红的转变点y254nm0.6、y365nm0.4,且荧光粉总体亮度相比(Mg1-xBax)1.95SiO4∶0.05Eu暗一些;(Mg1-ySry)1.95-SiO4∶0.05Eu随着体系中y的减少红色荧光逐渐由暗红变为亮红(γ-Mg2SiO4、β-Mg2SiO4增加,α-Sr2SiO4、β-Sr2SiO4减少(表1);由于β-Mg2SiO4和γ-Mg2SiO4中Mg2+为4配位和6配位,α-Sr2SiO4和β-Sr2SiO4中Sr2+为9、10配位(表2)),荧光强度先减小后增大,当y=0.2时(Mg0.8Sr0.2)1.95SiO4∶0.05Eu最亮。三元组分样品中:(Ba0.2SryMg0.8-y)1.95SiO4∶0.05Eu均为红色荧光粉,随着y值增大亮度降低,其原因与(Mg1-y-Sry)1.95SiO4:0.05Eu类似;(Ba0.6Mg0.4-ySry)1.95-SiO4∶0.05Eu在245 nm激发下随着Sr离子增加逐渐由绿变红(y254nm≥0.32为红色),365 nm激发下均为绿色;(Bax(Mg0.2Sr0.8)1-x)1.95SiO4∶0.05Eu随着x的减小(α-Sr2SiO4、β-Sr2SiO4、β-Mg2SiO4、 Sr3MgSi2O8逐渐增加,Ba2SiO4逐渐减少,如表1所示)逐渐由绿变红(在Ba2SiO4单相区内粉末均为绿色荧光粉;混合物相区则随着Sr、Mg增加荧光粉由绿变红(随着Mg、Sr增加碱土离子配位空间逐渐减小,不利于Eu2+,故Eu2+/Eu3+比值逐渐减小,粉末由绿变红),当x254nm≥0.2、x365nm≥0.3为绿色荧光粉。 3.2.2 富钡端单相区荧光粉精细发射光谱分析 进一步探究了Ba2SiO4相荧光粉光谱的特性,其精细光谱分析如图5所示。基于Van Uiltert提出的发射峰与发光中心的关系式: (2) 图3 (Mg1-x-yBaxSry)1.95SiO4∶0.05Eu系列荧光粉的荧光光谱 Fig.3 Photoluminescent spectra of (Mg1-x-yBaxSry)1.95SiO4∶0.05Eu(carbon powder 3%, BaF20.7%, 1 200 ℃/3 h) 图4 (Mg1-x-yBaxSry)1.95SiO4∶0.05Eu系列荧光粉的紫外激发发光照相记录及CIE图 Fig.4 Photos and CIE sketch of (Mg1-x-yBaxSry)1.95SiO4∶0.05Eu under UV light excitation and CIE sketch(Carbon powder 3%, BaF20.7%, 1 200 ℃/3 h) 表4 Eu2+在Ba2SiO4中不同格位的Uiltert公式的计算值 Tab.4 Calculated emission peak values of Eu2+at different lattice sites in Ba2SiO4crystal by Uiltert eqution Q∗/cm-1nrBa2+/nmE/cm-1λcalc/nmBa(Ⅰ)Ba(Ⅱ)340001090.15200.14702206120927453478 由(Mg1-x-yBaxSry)1.95SiO4∶0.05Eu光谱性能分析可知,Ba2SiO4相区荧光粉均为绿色荧光粉,且随着Sr2+、Mg2+固溶绿色荧光亮度逐渐增大(精细光谱表明Sr2+、Mg2+固溶有促进Eu2+离子进入高发光效率的格位的效果);单相区外的样品点随着Ba含量减少,荧光粉紫外激发荧光颜色逐渐由绿变红(混合物相中Eu离子配位空间逐渐减小,Eu逐渐以Eu3+离子形式存在),且随着Sr2+增加变化更快;Mg2SiO4-Sr2SiO4二元系列为红色荧光粉,颜色由红变成浅红。总体上荧光粉紫外激发颜色和亮度随组元呈现渐变性,单相区(富Ba端)和混合相区组元和发光性能之间的关联分别是:Sr2+、Mg2+固溶度导致结晶度、Eu2+取代位置倾向发生渐变进而导致单相区粉末光谱的渐变;在混合相区中相组成的渐变导致光谱渐变。借鉴相图建立方法,由样品发射光谱得出CIE色像,并由散点分布建立三元发光色像图如图6所示。从图6中可看出随着组元变化其发光性能的变化,据此优选出绿色荧光粉样品点组分为(Mg0.3Ba0.65Sr0.05)1.95SiO4∶0.05Eu,红色荧光粉组分为(Mg0.65Sr0.35)1.95SiO4∶0.05Eu,其粉末与商业荧光粉性能对比如表6所示。 图5 Ba2SiO4相(Ba1-xMex)1.95SiO4∶0.05Eu(Me=Mg或Sr)荧光粉精细发射谱(散点为实验数据,红线为拟合总结果,绿线为Eu(Ⅰ)拟合,蓝线为Eu(Ⅱ)拟合) Fig.5 High resolution emission spectra of Ba2SiO4-phase (Ba1-xMex)1.95SiO4∶0.05Eu powder(black points for expermental data, red line for the fitting, green line for Eu(Ⅰ) fitting, blue line for Eu(Ⅱ) fitting)(Carbon powderx%, BaF20.7%, 1 200 ℃/3 h) 表5 Ba2SiO4相(Ba1-xMex)1.95SiO4∶0.05Eu(Me=Mg or Sr)发射谱数据 Tab.5 Data of Ba2SiO4-phase (Ba1-xMex)1.95SiO4∶0.05Eu high-resolution emission spectrum(Carbon powder 3%, BaF20.7%, 1 200 ℃/3 h) CompositonUnder365nmexcitaionUnder254nmexcitaionMaincenter/nmCenter1/center2/nmIntegralarearatioMaincenter/nmCenter1/center2/nmIntegralarearatioBa1.95SiO4∶0.05Eu511507/5281.11506507/5281.12(Mg0.1Ba0.9)1.95SiO4∶0.05Eu513506/5401.25510509/5311.21(Mg0.3Ba0.7)1.95SiO4∶0.05Eu519509/5431.28515510/5471.58Ba1.95SiO4∶0.05Eu511507/5281.11506507/5281.12(Ba0.7Sr0.3)1.95SiO4∶0.05Eu517511/5381.37507505/5411.39(Ba0.9Sr0.1)1.95SiO4∶0.05Eu512511/5391.31509509/5421.36 图6 (Mg1-x-yBaxSry)1.95SiO4∶0.05Eu 254 nm(a)和365 nm(b)发光示意图。 Fig.6 CIE sketch of (Mg1-x-yBaxSry)1.95SiO4∶0.05Eu under 254 nm(a),365 nm(b) UV light excitation(Carbon powder 3%, BaF20.7%,1 200 ℃/3 h). 表6 样品与商用荧光粉对比 本文采用高温固相法在1 200 ℃保温3 h制备了(Mg1-x-yBaxSry)1.95SiO4∶0.05Eu荧光粉:3个二元碱土离子配比系列、3个三元碱土离子配比系列、若干散点,共计44个样品,通过分析其物相组成和光谱性能(PL谱、CIE值、紫外发光照相记录),得出组分-结构-发光性能关联。实验结果表明,(Mg1-x-y-BaxSry)1.95SiO4∶0.05Eu体系中物相组成随着组分变化存在渐变性(由端点出发,物相组元数目逐渐增多,且物相组元含量是逐渐减少或增多的连续变化);在富Ba端形成了Ba2SiO4单相相区(Sr最大量含量为35%、Mg为30%),随着Sr2+、Mg2+固溶,结晶程度提高,且Mg2+、Sr2+倾向取代9配位的Ba2+(II);Eu2+进入Ba2SiO4晶体结构以取代的方式进入。光谱分析发现(Mg1-x-yBaxSry)1.95SiO4∶0.05Eu荧光粉在紫外激发下其颜色和亮度呈现渐变性;Ba2SiO4相荧光粉均为绿色荧光粉且随着Sr2+、Mg2+固溶的增加荧光亮度逐渐增大(精细光谱表明单相区内Sr2+、Mg2+有促进Eu2+离子进入高发光效率的Ba2+(I)格位的效果);Mg2SiO4-Sr2SiO4二元系列为红色荧光粉;单相区外的样品粉末随着Ba减少,荧光粉紫外激发荧光颜色逐渐由绿变红(此时混合物中Eu离子配位空间逐渐减小,Eu逐渐以Eu3+离子形式存在)。(Mg1-x-yBaxSry)1.95SiO4∶0.05Eu系列荧光粉的结构、发光性能随组分渐变而呈现渐变性,其中单相区(富Ba端)和混合相区组元与发光性能之间的关联分别是:Sr2+、Mg2+固溶度导致结晶度、Eu2+取代位置倾向发生渐变进而导致光谱的渐变;在混合相区中相组成的渐变,导致光谱渐变。借鉴相图建立方法,由样品发射光谱得出CIE色像,并由散点分布建立三元发光色像图,在此基础上优选出绿色和红色荧光粉样品点(如(Mg0.3-Ba0.65Sr0.05)1.95SiO4∶0.05Eu和(Mg0.65Sr0.35)1.95SiO4∶0.05Eu),其优良的结晶性能和发光性能得到验证。由此可见,基于相图原理建立三元色像图,是系统高效地研发多元发光材料性能的有效手段。


3.2 光谱分析
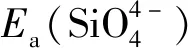




4 结 论
