过氧化氢干化学检测方法的实验研究
2019-09-10刘传志宫平侯玥
刘传志 宫平 侯玥

摘 要:目的:采用次血红素六肽(DhHP-6)催化H2O2氧化4-氨基安替吡啉-氯代苯酚显色体系,建立了以反射光检测为原理的H2O2干化学测定方法。方法:实验采用TiO2和聚乳酸微球为试剂载体,通过试剂分层包埋制备H2O2干化学检测片,考察了方法的反应线性、精密度和准确度及与国标方法的相关性。结果:H2O2干化学测定方法响应的线性范围为2.0~20mg/L;H2O2浓度3.9mg/L和15.5mg/L的变异系数(CV)和加标回收率分别在3.2%~3.5%和98.2%~102.2%;与国家标准方法比较相关系数r=0.998 5;13例样品中的H2O2浓度在1.05~18.26mg/L;与国标方法之间的两组数据经统计差异不显著(P>0.05)。结论:该方法快速、准确、灵敏,适合测定食品中过氧化氢的残留。
关键词:过氧化氢;次血红素六肽;模拟酶;干化学
中图分类号:R446.1 文献标识码:A 文章编号:1003-5168(2019)17-0124-04
Abstract: Objective To catalyze the oxidation of 4-aminoantipyrine-chlorophenol by H2O2 with subhemoglobin hexapeptide (DhHP-6), and establish a dry chemical method for H2O2 determination based on the principle of reflected light detection. Methods TiO2 and polylactic acid polymer microspheres were used as reagent carriers to prepare H2O2 dry chemical detection tablets by layered entrapment. The linearity, precision and accuracy of the method and the correlation with the national standard method were investigated. Results The linear range of response of H2O2 dry chemical assay was 2.0~20mg/L; the coefficient of variation (CV) and spiked recoveries of H2O2 concentrations of 3.9mg/L and 15.5mg/L were 3.2%~3.5% and 98.2%~102.2%, respectively. The correlation coefficient with the national standard method was r=0.9985; the concentration of H2O2 in 13 samples was between 1.05 and 18.26mg/L; the statistical difference between the two groups was not significant (P>0.05). Conclusion This method is fast, accurate and sensitive, and is suitable for the determination of residual hydrogen peroxide in food.
Keywords: Hydrogen peroxide;Deuterohemin-Ala His Thr Val Glu Lys;mimetic enzyme;dry chemistry
1 研究背景
過氧化氢(H2O2)作为强氧化物,在食品工业、制药工业等领域具有广泛的应用[1,2]。因此,快速、简便和准确检测H2O2的浓度十分重要。目前,常用的检测H2O2的方法有比色法、滴定法、化学发光和电化学检测[3,4]等。这些方法均需要较大型的仪器及在实验室内进行测量,不适合进行现场即时检验。其中,基于酶的比色分析方法具有成本低、选择性高、操作简单、灵敏度高等特点。然而,酶的保质期短、易变性,加之其对操作环境变化的敏感性,使其应用受到了限制[5]。
因此,课题组在传统比色分析的基础之上,根据次血红素六肽(DhHP-6)具有过氧化氢酶的催化特性[6],建立了一种快速检测H2O2的干化学方法,使其能实现现场实时检测H2O2的功能,并与国家标准《食品中过氧化氢残留量的测定》(GB 5009.226—2016)[7]使用的钛盐比色法进行比对分析。实验显示,该方法具有操作简单、快速、准确的特点。
2 过氧化氢检测卡的材料及制作
2.1 反应原理
H2O2在DhHP-6的催化下产生氧自由基(O-),O-通过氧化4-AAP-氯代苯酚体系显色。
2H2O2+4-AAP-氯代苯酚 DhHP-6[→]4H2O+亚醌胺(红色)
反应后显色浓度与H2O2含量成正比,可通过漫反射光电比色进行定量分析[8]。
2.2 材料
二氧化钛(TiO2);聚乳酸高分子微球;DhHP-6;4-AAP-氯代苯酚;聚酯胶片;磷酸盐缓冲液;聚乙烯醇水溶性粘合剂;表面活化剂;高压喷枪。
2.3 制作方法
第一,按比例将聚乳酸高分子微球、DhHP-6、4-AAP-氯代苯酚、磷酸盐缓冲液、表面活化剂和水溶性粘合剂按重量比16∶0.015∶0.085∶0.3∶0.05∶0.5进行混合,使用高压喷枪将此混合物均匀地喷涂在聚酯胶片上,使之形成具有一定厚度、可容纳一定体积液体的试剂层,所有的化学反应和显色均在此完成。
第二,试剂层干燥后,按比例将TiO2粘合剂进行混合,喷涂在试剂层上,形成扩散层。干燥后,完成H2O2干化学检测片的制作。将其剪裁成7mm×7mm的正方形,置入检测卡底内,形成H2O2干化学检测卡。
3 过氧化氢检测卡的性能验证
3.1 H2O2干化学测定方法的建立
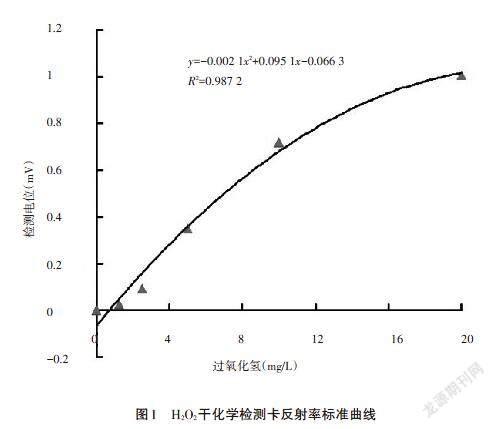
3.1.1 标准曲线。将3.0%的H2O2稀释成浓度为1.25、2.5、5.0、10.0、20.0mg/L备用。分别取10μL不同浓度H2O2的标本液体,将其均匀地加在H2O2干化学检测卡中,蒸馏水做空白对照,置于具有25℃恒温功能的漫反射光电比色仪上10min,测定结果以电位值(mV)表示,以空白对照干片测定值为基准值减去其他各测定值,得出各对应过氧化氢浓度的检测相对值,建立标准曲线。H2O2干化学检测卡标准曲线如图1所示,在2.0~20.0mg/L范围内线性较好,[R2]=0.987 2。
3.1.2 样本测定。取13份未知浓度H2O2样品,按检测方法测定相对值,在标准曲线上查找对应的过氧化氢浓度。
3.2 方法的精密度和准确度实验
在过氧化氢浓度为3.9mg/L和15.5mg/L两份样品中,添加3.0mg/L的H2O2,观察干化学检测卡方法的精密度和准确度。使用H2O2干化学检测卡(批号:2019003)加样10μL,各测定10次,结果如表1所示。两个浓度H2O2检测精密度分别为3.5%和3.2%,准确度分别为98.2%和102.2%。
3.3 过氧化氢检测卡与国家标准的比对实验
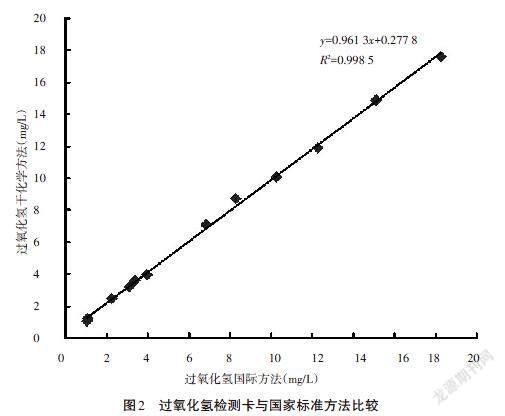
分别用国家标准方法《食品安全国家标准 食品中过氧化氢残留量的测定》(GB 5009.226—2016)的钛盐比色法和过氧化氢干化学检测卡对13份不同同浓度的过氧化氢进行测定,观察过氧化氢干化学检测方法与国家标准方法的相关性,结果采用SPSS.20统计软件对两方法进行配对t检验分析,结果如图2所示。
实验结果显示,国标方法与氧化氢干化学检测方法的两组数据经配对t检验统计,差异不显著([t0.09<t0.05(24)=2.064],P>0.05),相关系数为0.998 5,证明过氧化氢干化学分析方法与国家标准方法具有较好的相关性。
4 讨论
目前,对食品安全、环境污染等监测已趋向于现场快速检测[9]。其中,采用干化学(Dry Chemistry)检测是主要应用方式,在食品安全、环境污染和临床化学等检测中具有较大的应用的空间[10-12]。刘丹[13]、杨惠宇[14]通过将生化试剂固定在高分子膜载体上来制备干片,制备的干片包括血红蛋白干片、白蛋白干片、总蛋白干片。本文制备的H2O2干化学检测卡是基于反射光度法原理,以二氧化钛(TiO2)和聚乳酸高分子微球为试剂载体,通过试剂分层包埋制备干片,实现了过氧化氢的快速、灵敏检测。
与国家标准的比对实验相关系数为0.998 5,证明该方法具有较好的灵敏度和精密度,为过氧化氢的快速检测提供了一种新方法。
参考文献:
[1] Zhu J, Nie W, Wang Q, et al. In situ growth of copper oxide-graphite carbon nitride nanocomposites with peroxidase-mimicking activity for electrocatalytic and colorimetric detection of hydrogen peroxide[J]. Carbon, 2018(129):29–37.
[2] He J, Sunarso J, Zhu Y,et al. High-performance non-enzymatic perovskite sensor for hydrogen peroxide and glucose electrochemical detection[J]. Sens Actuators B Chem, 2017(244):482–491.
[3] Dhara K, Ramachandran T, Nair B G, et al. Au nanoparticles decorated reduced graphene oxide for the fabrication of disposable nonenzymatic hydrogen peroxide sensor[J]. Sensors & Actuators B Chemical, 2014(195):197-205.
[4] Hooch Antink W, Choi Y, Seong K, et al. Simple synthesis of CuO/Ag nanocomposite electrode using precursor ink for non-enzymatic electrochemical hydrogen peroxide sensing[J]. Sens Actuators B Chem, 2018(255):1995–2001.
[5]Zhang N, Sheng Q, Zhou Y, et al. Synthesis of FeOOH@PDA-Ag nanocomposites and their application for electrochemical sensing of hydrogen peroxide[J]. Journal of Electroanalytical Chemistry, 2016(781):315–321.
[6]侯玥,董占梅,马野,等.DhHP-6替代过氧化物酶在葡萄糖检测中的应用[J].长春理工大学学报(自然科学版),2016(3):139–142.
[7]中华人民共和国国家卫生和计划生育委员会.食品中过氧化氢残留量的测定:GB5009.226—2016[S].
[8]石鑫,刘传志,宫平,等.基于次血红素六肽的过氧化氢灵敏比色方法[J]应用化学,2019(7):849-853.
[9]Krska R,Molinelli A.Rapid Test Strips for Analysis of Mycotoxins in Food and Feed[J].Anal Bioanal Chem, 2009(1):67–71.
[10]Bowden R G,Kingery P M,Long L.Precision of a Dry-chemistry Method of Lipid Screening [J]. Public Health,2006(6):572–576.
[11]Flatland B,Breickner L C,Fry M M.Analytical Performance of a Dry Chemistry Analyzer Designed for in-clinic Use[J].Vet Clin Pathol,2014(2):206–217.
[12]Arimoto S,Kamei A,Yasukawa T,et al.Development of Highly Sensitive Electrochemical Measurement on Dry Chemistry Measuring Electrode Potential Shift[J]. Electrochim Acta,2013(108):776–780.
[13]劉丹.干式生化分析方法的建立及其方法学评价[D] .长春:长春理工大学,2014.
[14]杨惠宇,张昊,徐美玲,等.干式生化膜片的制备及其应用[J].应用化学,2015(8):963–968.
