卵巢癌胃转移1例及文献复习
2019-09-02李卫民徐湘江韩雪高志远杨广栋李胜水
李卫民,徐湘江,韩雪,高志远,杨广栋,李胜水
作者单位:沧州市中西医结合医院,a消化科,b病理科,河北 沧州 061001
卵巢癌胃转移罕见,病史、影像及CA125能为诊断提供线索,确诊则需要病理及免疫组化,现将发现的1例卵巢癌胃转移病例报告如下。
1 临床资料
病人,女性,63岁。主诉因腹胀、消瘦1个月于2016年9月18日入住沧州市中西医结合医院。病人1个月前无诱因出现腹胀,进食后加重,体质量减轻约4 kg,无其他伴随症状。既往40年前“左下肢骨髓炎”手术治疗。查体:生命体征正常。浅表淋巴结无肿大,无贫血貌,巩膜无黄染,心、肺未见异常,上腹压痛,下腹饱满,腹部未见其他异常。直肠指检未及异常。2016年9月16日门诊胃镜:食管及贲门未见异常。胃底穹窿局部黏膜充血,胃体、胃角黏膜光滑,胃窦前壁及部分大、小弯侧见一巨大隆起肿物突入胃腔,致胃窦腔隙严重狭窄,镜端不能通过,肿物表面黏膜光滑、色泽正常。换超细胃镜延后壁进镜抵达幽门,幽门开闭自然,十二指肠球部黏膜光整、大弯侧饱满隆起,球降移行部管腔走形偏移、管壁柔软、镜端通过顺利,降段未见异常。考虑胃窦部黏膜下肿物可能,建议超声内镜进一步检查。入院后查血肿瘤标志物:糖类抗原(CA-125)158.3 U/mL、人附睾蛋白4(HE4)>1 500.0 pmol/L、促胃液素释放肽前体(PRO-GRP)60.5 pg/mL、非小细胞肺癌相关抗原(CYFRA21-1)13.32 ng/mL均增高,甲胎蛋白(AFP)、癌胚抗原(CEA)、糖类抗原(CA199)、糖类抗原(CA-199)、糖类抗原(CA 72-4)、糖类抗原(CA-153)、铁蛋白(FER)、神经元特异性烯醇化酶(NSE)、鳞状上皮细胞癌抗原(SCC)均正常。血清乳酸脱氢酶(LDH)310 U/L、α-羟丁酸脱氢酶(HBDH)277 U/L,前白蛋白(PA)146.0 mL/L,磷(PHOS)1.5 mmol/L,其他等生化指标正常。结核抗体阴性。胸部CT未见异常。腹盆腔CT:胃窦部大弯侧软组织肿块影,边界尚清晰,密度均匀,约7.8 cm×3.7 cm,增强呈明显强化。双侧附件区多发囊实性病灶,内见分隔,增强实性部分明显强化。腹腔大量液体密度影。盆腔未见游离液体、气体密度影。腹膜不规则增厚,腹膜后多发小淋巴结。肝、胆、胰腺、双肾未见异常。超声:左侧附件区约5.7 cm×5.0 cm囊性包块,形态规则,边界不清,内见线状强回声分隔,局部囊壁较厚,周边见血流信号;右侧附件区约7.3 cm×5.3 cm杂乱回声包块,形态不规则,边界不清,回声不均匀,局部呈无回声区,内可见血流信号;子宫、宫颈未见异常,盆腔未见积液。考虑胃黏膜下肿物、卵巢占位,于超声引导下右侧卵巢肿物穿刺,病理诊断:(盆腔肿物穿刺)癌,免疫组化结果显示MC(+)、CK7(+)、CA-125(+),CEA(-)、CR(-),Ki-67(+约15%),诊断为腺癌,考虑为卵巢浆液性腺癌(图1,2)。超声胃镜显示:胃窦、体交界小弯侧见一实性低回声肿物,形态规则,边界清楚,包膜完整,内部回声欠均匀,内部未探及明显血流信号,肿物与胃壁肌层回声延续。超声胃镜引导下ECHO-19穿刺针穿刺肿物组织,快速病理找到癌细胞(图3),病理诊断:(胃部细针穿刺)癌,结合免疫组化结果CK-low(+)、CK7(+)、CA125(+),CEA(-)、TTF-1(-)、WT1(-)、CR(-),诊断为腺癌,考虑转移性,符合卵巢来源(图4)。补做免疫组化,结果显示CDX2(-)。
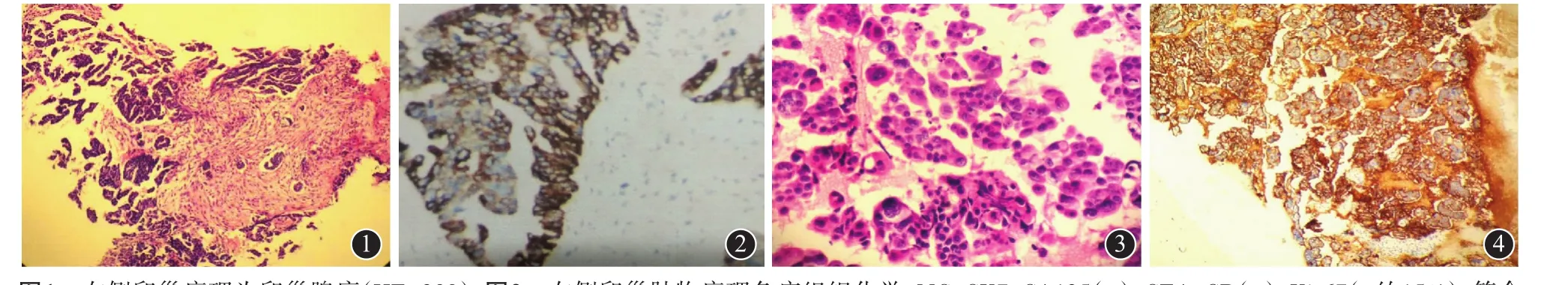
图1 右侧卵巢病理为卵巢腺癌(HE×200);图2 右侧卵巢肿物病理免疫组织化学:MC、CK7、CA125(+),CEA、CR(-),Ki-67(+约15%),符合卵巢浆液性腺癌(免疫组织化学×200);图3 幽门部肿块病理找到癌细胞(HE×200);图4 幽门部肿块免疫组织化学:CK-low、CK7、CA125(+),CEA、TTF-1、WT1、CR(-),提示转移性腺癌,符合卵巢来源(免疫组织化学×200)
综合病人病史及右侧卵巢肿物及胃窦肿块病理,诊断为卵巢浆液性腺癌胃转移、腹膜转移,给予紫杉醇+顺铂3周方案化疗,自2016年9月21日至2017年3月20日化疗8个周期后病情进展,期间第4周期时病情缓解,但家属及病人拒绝手术。自2017年4月30日至2017年9月10日改为依托泊苷第1~10天3周方案化疗,4个周期后病情稳定,2017年10月18日第5个周期后病情再度进展。2017年11月1日手术发现腹膜广泛转移,闭腹,2017年11月10日行卡铂+紫杉醇化疗,现病情稳定。
2 讨论
胃癌继发卵巢转移(Krukenberg肿瘤)已被广泛认知,而卵巢癌继发胃转移是罕见的,查阅文献仅有个例报道。发生胃转移的卵巢癌病理又以浆液性腺癌居多[1-4]。此类癌肿转移发生机制尚未明确。影像及CA125能为诊断提供线索,确诊则需要病理及免疫组化。Kang等[4]于2008年报道的首例原发性卵巢癌出现胃受累,是以CT增强扫描显胃窦部局灶性溃疡,黏膜下肿块提示为头绪,术后病理明确诊断的。CA125的测定对鉴别卵巢原发性癌和来源于胃肠道的卵巢转移性癌有重要意义[5]:CA125在卵巢转移性癌中低表达,当CK7阳性时有两种可能:(1)卵巢原发癌、(2)胃来源的卵巢转移性癌。因为虽然CK7在卵巢原发癌100%表达,在肠道来源的卵巢转移性癌阴性,但在胃来源的卵巢转移性癌50%表达,此时如果CA125阳性则支持卵巢原发癌,如果CA125阴性则支持胃来源的卵巢转移性癌。3例无其他复发部位的卵巢癌胃转移病例[1,6],是在卵巢癌切除史背景下,CA125增高提示复发,正电子发射断层扫描发现受累胃壁后经病理证实。周江蛟等总结了9例卵巢癌胃转移个案,仅1例诊断卵巢癌同时发现胃转移,其他就诊时发现胃壁肿物,既往有卵巢癌病史,尤其当CA125高于正常范围时,应当考虑卵巢癌胃转移可能[7]。Kim等[8]探讨了腹腔镜手术对卵巢转移胃癌的治疗可行性。Brieau等[9]则论述了化疗方案FOLFOX或FOLFIRI方案敏感性、有效性。
由于卵巢癌胃转移罕见,目前未有诊疗共识具体涉及其预后、转归。本例病人胃黏膜下肿物与卵巢肿物同时发现,需明确两处病灶关系是一种肿瘤转移还是不同的两种肿瘤,如果是转移,原发肿瘤是胃还是卵巢。因胃镜下胃内肿物表面黏膜光滑、色泽正常,提示源于黏膜下,与胃癌转移至卵巢的Krukenberg肿瘤表现不符,后经超声内镜引导细针穿刺胃壁及卵巢肿瘤穿刺结合免疫组化确诊,病理为卵巢癌浆液性腺癌,我们应用紫杉醇+顺铂3周方案化疗一度病情缓解,之后更换依托泊苷第1~10天3周方案化疗前4周期同样有效,或许为该病诊疗积累些许经验。通过回顾本病例及复习相关资料,提示对同时发现的不同系统肿瘤一定要结合临床特征、肿瘤标志物、明确落实相应病灶病理,才能不漏掉少见病例,提高诊疗精准性。
(本文图1~4见插图9-3)
