抗中性粒细胞胞浆抗体阴性肉芽肿性多血管炎1例报告并文献复习
2019-08-14陈虹吴兰雁郑广宁林梅
陈虹 吴兰雁 郑广宁 林梅
口腔疾病研究国家重点实验室 国家口腔疾病临床医学研究中心四川大学华西口腔医院口腔黏膜病科 成都 610041
肉芽肿性多血管炎(granulomatosis with polyangiitis,GPA)原称韦格纳肉芽肿病(Wegener’s granulomatosis,WG),是一种以坏死性肉芽肿性血管炎为主要特征的全身性疾病,为少见的自身免疫性疾病[1-2]。GPA的临床表现复杂、多变,早期诊断困难,易被误诊或漏诊,而病情进展比较迅速,如得不到及时的治疗,病死率高。GPA最常累及鼻黏膜、肺及肾脏[3-4],口腔症状仅出现在5%~10%患者中,其中以草莓状牙龈为首发临床症状更是罕见[5]。现回顾性分析四川大学华西口腔医院接诊的1例以草莓状牙龈为主诉的抗中性粒细胞胞浆抗体(anti-neutrophil cytoplasmic antibody,ANCA)阴性GPA病例的临床病理特点,并复习相关文献,加深对本病的认识。
1 临床资料
1.1 基本情况及病史
患者,男性,50岁,藏族。2014年9月因“左上颌牙龈及右下颌牙龈红肿14个月”就诊。在四川大学华西口腔医院就诊14个月前,患者无明显诱因出现左上颌牙龈及右下颌牙龈红肿,随后范围逐渐扩大,并出现疼痛及左上牙松动;2个月前到当地医院就诊,拔除B3—6,并切取左上颌牙龈组织进行活组织检查,显示牙龈黏膜慢性炎症伴糜烂。
1.2 初诊情况
患者到四川大学华西口腔医院就诊时,除乙型肝炎(乙肝表面抗原、乙肝e抗体、乙肝核心抗体3项阳性,即小三阳)外,否认其余特殊病史;否认体重下降、发烧、咳嗽、呼吸困难、胸痛或任何尿路症状等全身症状。临床检查显示:A2—B2颊侧牙龈、前庭沟及上唇内侧黏膜充血发红、肉芽增生、肿胀,表面有不规则溃疡,触痛明显;在C2—5颊侧及舌侧牙龈可见颗粒状红色增生,C45颊侧及舌侧牙龈间杂白色点状颗粒状病损(草莓状外观)(图1 A、B)。A1—5松动度为Ⅰ°,B12松动度为Ⅱ°,口腔卫生状况欠佳;右鼻根部有压痛,右鼻前庭黏膜见糜烂,鼻根部皮肤见数个点状糜烂面。辅助检查显示:A2—B2颊侧牙龈的真菌涂片为阳性(+)。实验室检查显示:血常规、血糖、肝肾功、感染标志物的部分结果详见表1,ANCA检测均为阴性。
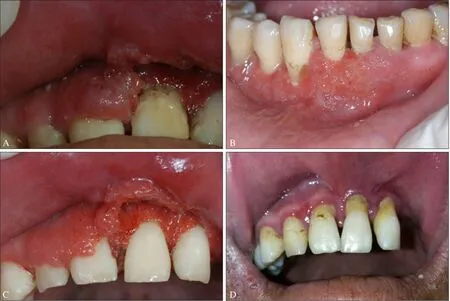
图 1 初诊及复诊时患者的口内表现Fig 1 Intraoral photograph at the initial, second consultation and followed for three years
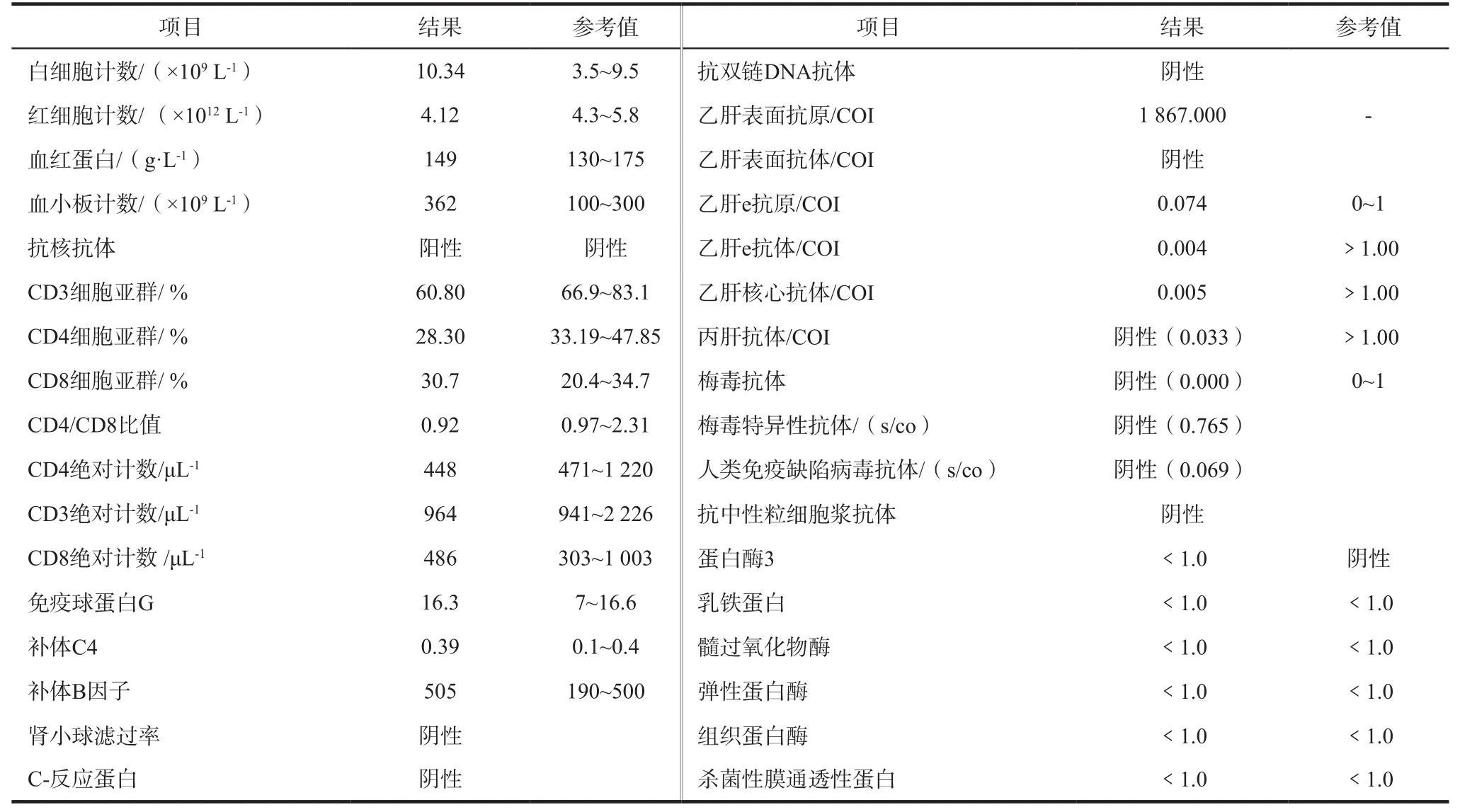
表 1 实验室检查结果Tab 1 The results of laboratory test
初步处理:1)局部抗菌消炎(全口牙周冲洗,氯己定、口炎颗粒及氟康唑等药物治疗),待炎症感染情况改善后进行活组织检查;2)建议检查以下项目:颌面部全景片、锥形束计算机断层扫描(cone beam computed tomography,CBCT)、胸部CT、腹部B超;3)建议患者于耳鼻喉科、感染科就诊,排查相关疾病。
1.3 复诊情况
2014年10月患者携检查报告复诊,诉口内症状减轻,疼痛明显缓解。
临床症状如图1C所示,红肿有所改善;复查口内黏膜真菌涂片均为阴性。
所携带的颌面部全景片及CBCT显示:B3—7缺失,剩余牙槽嵴底平;右上颌窦密度增加,内侧腔壁骨质不连续;鼻泪管内壁骨质不光滑,涎管壁带状密度增高;右侧下颌骨骨纹理紊乱,骨髓腔变小,骨质密度增高,边界不清楚;右侧颌骨较对侧膨隆,左下颌骨颊侧也有类似改变。经放射科专家会诊认为:右侧上颌窦腔充满软性密度结构,内壁骨质溶解吸收,通连下鼻甲;鼻泪管内壁骨质不光滑,涎管壁带状密度增高,存在上颌窦炎及筛窦炎(图2A~D)。鼻部CT显示:右侧上颌窦、筛窦炎症、鼻部软组织稍肿胀(图2E~F)。胸部CT、腹部B超均未显示明显异常。
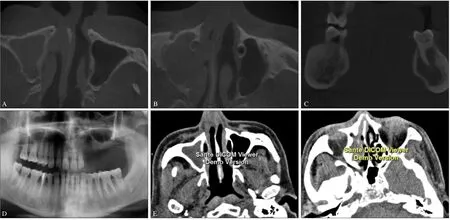
图 2 病例的全景片、CBCT及鼻部CTFig 2 X-ray, CBCT and nasal CT of the patient
在四川大学华西口腔医院颌面外科再次切取左上唇内侧牙龈红肿糜烂及增生物进行活组织检查,结果显示:牙龈黏膜灶性坏死、炎性肉芽组织形成及血管炎(图3)。
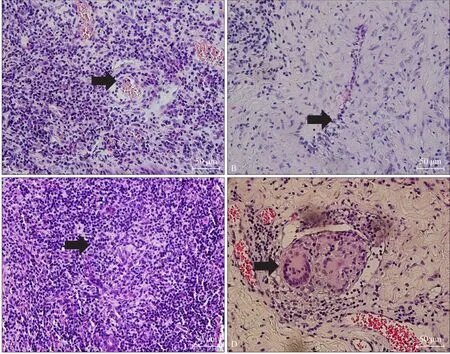
图 3 牙龈活组织检查 苏木精-伊红染色Fig 3 Photomicrograph of the gingivae Hematoxylin-eosin staining
此外,免疫组织化学检查显示:免疫球蛋白(immunoglobulin,Ig)G4为阴性,梅毒螺旋体(Treponema pallidum)为阴性;原位杂交实验显示:Epstein-Barr病毒编码核糖核酸(Epstein-Barr virus-encoded RNA,EBER)为阴性;抗酸染色以及Warthin-Starry染色均为阴性,磷钨酸苏木精(phosphotungstic acid hematoxylin,PTAH)染色为阴性;结核分枝杆菌DNA/聚合酶链式反应(polymerase chain reaction,PCR)检测未查见确切结核分枝杆菌DNA片段。
结合病理、实验室检查及临床表现,诊断为局限性GPA,肾脏暂未受累。局部消炎处理,维护口腔卫生;建议患者到华西医院耳鼻喉科病理确诊鼻部病损,并到风湿免疫科进行系统治疗。
患者拒绝接受鼻窦病损组织的活组织检查,后回当地继续治疗。电话随访3年,患者牙龈处溃疡消失(图1D,图片由患者家属提供),自诉嗅觉丧失,余无明显异常。
2 讨论
GPA临床较少见,发病率平均为1/30 000~1/50 000,其中97%的患者是高加索人,亚洲人发病较罕见[5-6];该病从儿童到老年人均可发生,但中老年人多发,40~50岁是本病的好发年龄[7-8]。GPA患者临床表现复杂,口腔黏膜表现亦多样,常为坏死性肉芽肿性溃疡,好发于舌、腭、咽等处黏膜;牙龈的草莓样增生也有发生[9];极少数患者会出现唾液腺炎[10]。口内坏死组织脱落可导致骨组织暴露,破坏牙槽骨,使牙齿松动,拔牙创不愈合等[10]。也有文献[11]指出,该病口腔表现进程为:起初为轻度鼻塞和牙龈炎,继而出现黏膜破溃,亦可破坏鼻中隔和硬腭,甚至穿通面部。口腔可以作为GPA的先兆表现部位,及时认清这些容易被混淆的口腔损害,有助于临床医生进行GPA早期诊断,从而为该病的治疗与预后提供良好的基础。
GPA早期诊断难度较大,易被误诊或漏诊。目前GPA诊断仍采用1990年美国风湿病学院[12]的标准:1)鼻或口腔炎症。痛性或无痛性口腔溃疡,脓性或血性鼻腔分泌物。2)X线胸片异常。胸片示结节、固定浸润病灶或空洞。3)尿沉渣异常。显微镜观察显示血尿(每高倍视野中红细胞超过5个)或出现红细胞管型。4)病理性肉芽肿性炎性改变。动脉壁或动脉周围或血管(动脉或微动脉)外区有中性粒细胞浸润。符合其中2条或2条以上时,可诊断为GPA。而本病例符合第1及第4条标准,遂可明确诊断。
ANCA作为与血管炎相关的自身抗体,其特异性与敏感性均较好,可帮助诊断GPA。其中,PR3-ANCA及c-ANCA虽然不是GPA的诊断标准,但对于该病的特异性和敏感性高达90%以上,显著提高了GPA的诊断正确率[13]。若ANCA均为阴性,也不能完全排除GPA。当GPA处于早期阶段时,ANCA可不升高。
病理表现作为GPA诊断的金标准,但是血管炎在不同器官以及疾病的不同发展阶段的病理表现亦有差异,病理表现可能缺乏特异性,或出现假阴性,从而干扰临床判断[14]。因此,临床实践中可能常有早期因血清ANCA阴性及病理检查表现不典型的GPA病例,临床医生需寻找各种蛛丝马迹,综合考虑,多科会诊,尽早进行临床诊断显得尤为重要。
一般来说,GPA预后较差,尤其是未经治疗的GPA患者,平均生存期仅5个月。在这些患者中,82%的患者1年内死亡,2年内死亡率高达90%以上,死因多为严重感染、呼吸衰竭或(和)肾衰竭。在以上严重损害出现前,明确诊断并积极治疗是十分有意义的。及时用药是治疗GPA的关键,一旦组织坏死就不可逆。治疗通常可分为3期,即诱导缓解期、维持缓解期和控制复发期。目前循证医学研究证实,细胞毒性药物(如环磷酰胺)与糖皮质激素联合治疗GPA非常有效,可明显、快速缓解病情。此外,足够的治疗疗程也是非常重要的,特别是肾脏受累及(或)严重呼吸系统疾病的患者,疗程不应少于18个月。在以上严重损害出现前,明确诊断并积极治疗是十分有意义的。口腔可以作为GPA的先兆表现部位,及时认清这些容易被混淆的口腔损害,有助于临床医生进行GPA早期诊断,从而为该病的治疗与预后提供良好的基础。本例GPA患者在病灶较局限时及时诊断、治疗,病情相对稳定,没有出现重要脏器功能的严重损害,严密随访,这些可能是患者长期随访3年预后仍较好的原因。
