卵母细胞滑面内质网聚集体对临床结局和早期出生结局的影响
2019-07-30王雪肖亚玲孙正怡甄璟然郁琦邓成艳周远征王含必
王雪,肖亚玲,孙正怡,甄璟然,郁琦,邓成艳,周远征,王含必
(中国医学科学院 北京协和医学院 北京协和医院妇科内分泌与生殖中心,北京 100730)
在辅助生殖技术中,患者的妊娠结局取决于胚胎的质量好坏,而胚胎发育潜能与卵母细胞质量息息相关,因此对卵母细胞形态和发育潜能进行正确评估非常重要。通常卵母细胞的评估方法是基于胞浆外和胞浆内的一些特征进行的,包括极体形态、卵周间隙、折射体、胞内颗粒、空泡和滑面内质网等[1]。在正常卵母细胞中滑面内质网呈多个、分散的球形聚集模式,周围由线粒体包绕[2]。而卵母细胞内滑面内质网聚集(Smooth endoplasmic reticulum clusters,sERC)是卵母细胞胞浆内的一种异常滑面内质网聚集体,以单个大聚集体模式聚集[3],表现为圆形、 扁平且清晰的盘状物,直径约为10~18 mm[4]。目前国内外学者已对sERC做了很多相关研究,但在辅助生殖过程中是否可以移植含sERC的卵母细胞发育而来的胚胎还无明确结论。
尽管2011年的欧洲人类生殖与胚胎学学会(Alpha/ESHRE)专家共识建议丢弃含sERC的卵母细胞[1],但是各个中心对含有sERC的卵母细胞的处理仍然缺乏统一的认识。最近欧洲一项多中心的调查显示,48%(56/118)的中心受Alpha/ESHRE共识的影响,改变了对含sERC卵母细胞的态度,但是仅仅有14%的中心在ICSI之前丢弃含sERC的卵母细胞,43%的中心并没有丢弃含SERC的卵母细胞,但是也没有登记和随访新生儿数据[5]。因此,当受sERC影响的卵母细胞没有丢弃时,记录胚胎的发育情况和对新生儿随访,并将这些数据进行发表是非常重要的。只有通过分析这些数据才能更好地明确卵母细胞的这些形态学异常是否与文献中记录的先天异常有关。因此,本中心进行了此前瞻性的观察性研究,对近2年出现含sERC卵母细胞的胚胎发育情况及临床和新生儿结局进行统计分析,追踪含sERC卵母细胞的移植预后,试图为含sERC卵母细胞的可用性问题增添新的证据。
资料与方法
一、研究对象与分组
收集2016年12月至2018年8月在我院生殖中心进行ICSI助孕治疗的患者纳入研究。按照本中心的常规操作,无额外操作,所有患者均签署知情同意书。本研究纳入标准为:(1)进行ICSI操作的患者;(2)新鲜取卵周期。排除标准为:(1)进行常规IVF的患者;(2)男方为睾丸穿刺取精或副睾穿刺取精的患者;(3)进行植入前遗传学诊断或筛查的患者。
根据患者获卵时卵母细胞中是否出现sERC,分为sERC+周期组(A组)和sERC-周期组(B组),A组即该周期每个人所获得的卵母细胞中至少出现1个sERC卵母细胞,共80个周期,B组即所获得的卵母细胞中均未出现sERC,共1 492个周期。A组中再根据卵母细胞是否出现sERC,进一步分为sERC+卵母细胞组(A1组,共140个)和sERC-卵母细胞组(A2组,共416个)。再根据所移植的胚胎是否来源于sERC卵母细胞,分为Ⅰ组:所移植胚胎全部来源于sERC+卵母细胞;Ⅱ组:所移植胚胎中的1枚胚胎来源于sERC+卵母细胞,1枚来源于sERC-卵母细胞;Ⅲ组:所移植胚胎均来源于sERC-卵母细胞。
二、研究方法
1.控制性促排卵和取卵:所有患者的促排方案按照本中心的常规进行,主要是GnRH激动剂长方案和GnRH拮抗剂方案,使用卵泡刺激素(FSH,果纳芬,默克雪兰诺,瑞士)进行卵巢刺激。当主导卵泡直径达到18~20 mm时,注射人绒毛膜促性腺激素(HCG,艾泽,默克雪兰诺,瑞士),38 h后进行阴道超声引导的卵泡穿刺来获取卵母细胞。
2.卵母细胞sERC的评估及ICSI操作:获取卵母细胞后2 h左右用透明质酸酶消化颗粒细胞,拆除卵母细胞周围颗粒细胞,放置培养箱培养2 h左右进行ICSI操作。ICSI时,在倒置显微镜下评估每一个卵母细胞的形态,并记录相关数据。在高倍镜下,胞浆内大的sERC表现为圆形、扁平且清晰的盘状物,与空泡相似,但sERC内无液体,折光性相对较弱,两者易于鉴别[6-7]。在ICSI操作时应尽量避免将精子注射到sERC内。
3.胚胎培养、评估和临床判断:ICSI后18~20 h观察原核情况,若出现2个原核(2PN)判断为正常受精。取卵后第3日进行胚胎的形态学评估,根据卵裂球的数目、大小、形态及碎片的状态进行评分,挑选质量最好的两枚胚胎进行移植,如不能移植则将两枚胚胎进行冷冻保存,其余所有胚胎均进行囊胚培养,在取卵后第5日或6日观察囊胚形成情况,并根据Gardner评分法[8]进行评分,挑选内细胞团质量达到A或B级的囊胚进行冷冻,C级的囊胚放弃,滋养细胞层的质量不限。冷冻操作方法按照本中心的常规进行。移植后25~30 d超声检查,可见胎囊并有胎心搏动者判断为临床妊娠.
4.观察指标:胚胎相关的测量指标包括:(1)受精率=受精数/MⅡ卵母细胞数×100%;(2)优质胚胎率=优质胚胎数/卵裂数×100%;(3)囊胚形成率=囊胚数/(卵裂数-移植数-卵裂期冷冻数)×100%;(4)种植率=着床胚胎数/移植胚胎数×100%。临床相关的测量指标包括:(1)临床妊娠率=临床妊娠例数/移植周期数×100%;(2)流产率=流产例数/临床妊娠例数×100%。(3)活产率=随访获得活产的总例数/移植周期数×100%。新生儿的数据包括:孕周、出生体重、体长、性别、出生时的畸形情况。
三、统计方法

结 果
本研究共纳入1 435例患者,共1 572个ICSI周期,其中出现sERC的周期为80个周期,即sERC+周期组(A组);sERC-周期组(B组)为1 492个周期。至少出现1个sERC卵母细胞的周期发生率为5.1%。总共纳入分析的MⅡ卵母细胞为6 759个,其中存在sERC的卵母细胞为140个,发生率为2.1%。A组中,sERC卵母细胞的发生率为34.6%。
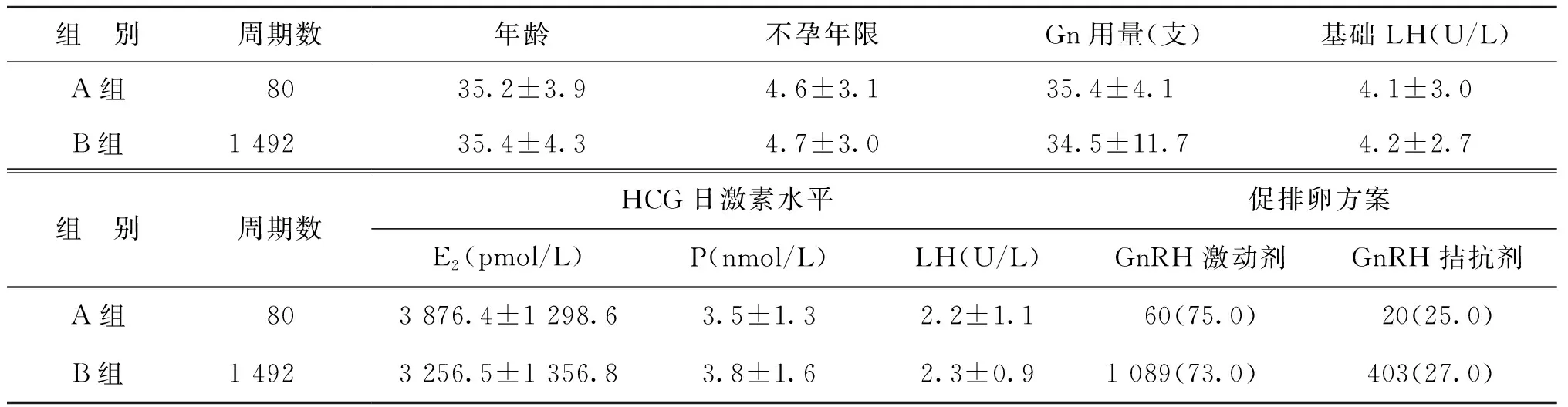
一、A、B两组一般情况比较
两组的年龄、不孕年限和Gn用量比较均无显著性差异(P>0.05)。A组HCG日E2水平略高于B组,但尚无显著性差异(P>0.05);两组的促排卵方案比较亦无显著性差异(P>0.05)(表1)。
二、A、B两组的胚胎发育指标和临床情况比较
A组获卵数、成熟卵率和受精率略高于B组,但均无显著性差异(P>0.05);A组的囊胚形成率显著低于B组(P<0.05);两组的种植率、临床妊娠率、流产率和活产率比较亦无显著性差异(P>0.05)(表2)。
三、A、B两组的新生儿结局的比较
由于2018年移植的患者尚有部分未分娩,所以分娩结局只分析至2018年5月底的数据。A组的新生儿出生体重略低于B组,且A组的早产率略高于B组,但两者比较均无显著性差异(P>0.05);两组的出生缺陷率比较亦无显著性差异(P>0.05)(表3)。

组 别周期数年龄不孕年限Gn用量(支)基础LH(U/L)A组8035.2±3.94.6±3.135.4±4.14.1±3.0B组1 49235.4±4.34.7±3.034.5±11.74.2±2.7组 别周期数HCG日激素水平促排卵方案E2(pmol/L)P(nmol/L)LH(U/L)GnRH激动剂GnRH拮抗剂A组803 876.4±1 298.63.5±1.32.2±1.160(75.0)20(25.0)B组1 4923 256.5±1 356.83.8±1.62.3±0.91 089(73.0)403(27.0)


组 别周期数获卵数成熟卵率受精率优胚率A组807.8±3.888.1(556/631)91.0(506/556)12.3(62/505)B组1 4927.2±4.786.2(9 289/10 776)89.4(8 306/9 289)9.7(807/8 283)组 别周期数囊胚形成率种植率临床妊娠率流产率活产率A组8028.7(104/363)*23.3(28/120)35.9(23/64)10.5(2/19)28.5(16/56)B组1 49233.7(1 968/5 838)26.1(574/2 201)39.6(468/1 181)22.0(91/414)29.9(312/1 045)
注:与B组比较,*P<0.05;获卵数、成熟卵率、受精率、优胚率、囊胚形成率、种植率和临床妊娠率按照总移植人数计算(2016~2018年);由于2018年移植的患者目前尚有部分未分娩,故流产率和出生率按照截至2018年5月底前移植的人数计算
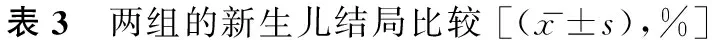

组 别分娩周期数性别比(男/女)出生体重(g)双胎率出生缺陷率早产率A组160.67(8/12)2 706.0±551.525.0(4/16)025.0(4/16)B组3131.05(192/183)2 942.0±628.519.8(62/313)0.6(2/313)16.9(53/313)
四、A组中A1组和A2组的胚胎发育情况比较
A组80个sERC+周期中共获得140个sERC+卵母细胞(A1组),416个sERC-卵母细胞(A2组)。其中A1组的受精率、囊胚形成率显著低于A2组(P<0.05),A1组的优质胚胎率有低于A2组的趋势,但尚无显著性差异(P>0.05)(表4)。

表4 A1组和A2组的胚胎发育情况比较 (%)
注:与A2组比较,*P<0.05
五、新鲜移植sERC+卵母细胞的临床结局比较
在A组中,只有2个周期全部进行两枚sERC+卵母细胞来源的胚胎移植,有2个周期只有1枚胚胎可移植,且都是sERC+卵母细胞来源,在这4个周期(Ⅰ组)中只有1枚胚胎着床,且成功分娩。10个周期(Ⅱ组)进行sERC+/sERC-卵母细胞来源的胚胎移植,其中4例获得临床妊娠,已经随访的2例患者均已分娩。50个周期(Ⅲ组)进行sERC-卵母细胞来源的胚胎移植,其中18例获得临床妊娠。3组的种植率和临床妊娠率比较无显著性差异(P均>0.05),3组均未出生畸形儿(表5)。
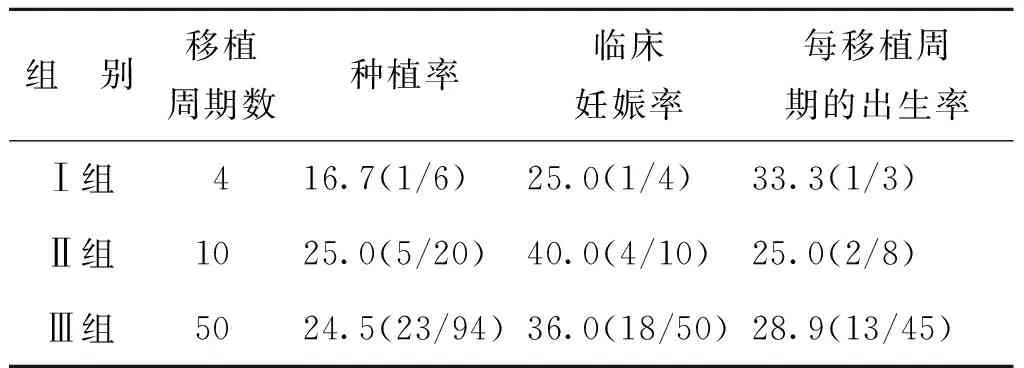
表5 不同sERC+、sERC-卵母细胞来源胚胎的临床结局(%)
注:移植周期数、种植率、临床妊娠率按照总移植人数计算(2016~2018年);由于2018年移植的患者目前尚有部分未分娩,故出生率和畸形率按照截至2018年5月底前移植的人数计算
讨 论
既往文献报道在促排卵周期中,sERC的发生率为5.4%~23.1%不等[9-10]。在本研究中,至少出现一个sERC卵母细胞的周期发生率为5.1%。sERC的观察取决于观察者的经验水平和所应用显微镜,可以在光学显微镜下观察到一些直径较大的sERC,而一些较小的sERC却不容易被发现。迄今为止sERC的形成原因尚不清楚,有研究显示sERC的形成可能是由于卵巢过度刺激造成的,认为HCG日E2水平与sERC的形成有显著相关性[6]。在本研究中我们发现尽管A组获得的卵母细胞数略高于B组,HCG日E2水平略高于B组,但组间比较均无显著性差异。另有研究发现在培养过程中sERC体积会增大,认为所有sERC之间或小sERC之间存在连接,其可以在卵母细胞中形成较大的sERC;以及提前出现的LH峰会引起MⅡ卵母细胞出现sERC,认为sERC是卵巢促排卵过程中激发LH之前胞浆过度成熟的标志,其可能是胞浆过熟的一个表现[10]。
关于sERC对胚胎发育影响的争议较大。在本研究中,我们发现A组与B组的受精率和优胚率相似,组间比较无显著性差异,这与之前一些研究结论[9,11-13]相似。但也与一些研究结论相反,有学者认为在正常生理情况下,滑面内质网会释放钙离子,其在卵母细胞成熟、受精和早期胚胎发育阶段发挥关键作用,而sERC的异常分布类型可能会参与钙离子信号的异常调节,导致sERC+周期组的受精率显著下降[14-16]。在本研究中我们还发现A组的囊胚形成率显著降低,这与Ebner等[17]的研究结论一致。我们根据A组内卵母细胞是否存在sERC进行分组,并对两亚组进行比较,发现A1组的受精率显著低于A2组,将胚胎培养至Day5~6时,A1组的囊胚形成率显著低于A2组,这与之前一些研究结论[6,11]相似。尽管在受精后第3天胚胎的发育速率与正常卵母细胞相比并无显著性差异,但sERC+卵母细胞的囊胚发育更慢一些,而且有研究显示囊胚的扩张程度和孵化状态都受sERC的影响,sERC+卵母细胞来源的囊胚的内细胞团(Inner cell mass,ICM)质量更差一些,sERC能够使ICM质量下降35%[18]。最近Otsuki等[10]进行了一项Time-lapse的研究,记录并比较了sERC+卵母细胞的分裂过程,他们发现sERC+组卵母细胞的有丝分裂或减数分裂错误率显著高于非sERC卵母细胞。如果在有丝分裂或减数分裂期间发生卵裂失败就会导致胚胎染色体异常。一旦卵裂失败的细胞发育为滋养细胞,就会出现胎盘异常;如果这些细胞发育为ICM,会导致进一步的卵裂失败,反过来会引起非整倍体。总之,从这些结论中我们很难总结sERC是否会影响Day3的胚胎质量,而且囊胚形成率低的原因还不是很清楚,还有待于进一步研究。
在本研究中,我们发现A组与B组的种植率、临床妊娠率相似,组间比较无显著性差异,这与Hattori 等[12]的研究结论相似。由于2018年移植的患者中还有部分没有分娩,因此在统计妊娠结局时我们只统计至2018年5月底,在有分娩结局的患者中,我们发现A组的出生体重略低和早产率略高,分析原因可能是因为A组双胎较多造成的,与sERC本身的关系可能不大。我们还分析了A组内,单纯移植sERC+卵母细胞、移植sERC+/sERC-和完全sERC-卵母细胞的出生结局。在日常工作中,由于考虑到sERC对胚胎及出生结局的影响尚不确切,我们会优先移植非sERC卵母细胞来源的胚胎,因此移植sERC卵母细胞来源胚胎的周期数较少,仅有4个周期完全移植sERC来源的胚胎,有1例活产,胎儿未见异常。10个周期移植了至少1枚sERC+卵母细胞来源的胚胎,在随访的4个妊娠周期中有2例分娩,胎儿未见异常,这与Mateizel等[9]的研究结论相一致,他们发现移植来源于显著sERC卵母细胞的胚胎后可以生育正常无畸形的孩子;该研究纳入了394个sERC+周期,81例活产,sERC+卵组与sERC-组的新生儿畸形率无显著差异。同样Itoi等[13]也未发现移植sERC+卵母细胞来源的囊胚后,新生儿的结局与sERC-组有统计学差异。尽管本研究的数据有限,但也支持这样的结论,因为在这些来源于sERC+卵母细胞出生的孩子中,并没有发现异常。既往有一些研究提示sERC可能与较差的临床结局和新生儿结局相关:Otsuki等[6]的研究显示sERC+周期组的临床妊娠率降低,而生化妊娠率升高;Ebner等[17]认为移植sERC卵母细胞来源的胚胎更容易发生早产和低出生体重;还有研究发现移植sERC卵母细胞来源的胚胎后发生新生儿先天异常的比例增加,如Beckwith-Wiedmann综合征、心血管畸形和多发畸形的发生率大大增加[6,16,19];最近还有文献报道了1个来源于sERC+卵母细胞的复杂的染色体异常[20]。但是复习文献,我们知道与自然周期相比,ART操作后出生的孩子更容易发生印记缺陷[21],所以很难判断印记缺陷是否是由sERC造成。而且不同研究间的差异也可能是由于设计方案、样本量大小、卵巢刺激方案、人群变异或其他因素的不同而造成。就本研究而言,移植sERC卵母细胞来源的胚胎后可以出生正常孩子,但也存在一些疑虑,即出生时正常能否代表将来的发育正常。因此,对sERC卵母细胞来源的孩子还需要进行长期随访,关注发育过程是否有异常。
总之,在辅助生殖过程中,sERC+卵母细胞的安全性问题还有待于进一步商榷,对于获卵数少的患者,如果采纳Alpha共识,完全丢弃sERC+卵母细胞,那么患者的周期取消率会显著增加。因此,对于胚胎数量少和仅有sERC+卵母细胞来源胚胎的患者来讲,在充分知情同意的前提下,可以考虑移植sERC+卵母细胞来源的胚胎。在将来,sERC形成的分子机制以及sERC对卵母细胞和胚胎的影响还有待于进一步研究,对sERC卵母细胞来源的新生儿的安全性还需要进行多中心的长期随访研究。
