胎儿肺囊性病变的磁共振表现
2019-06-19周刚范路萍尹秋凤刘明汪登斌
周刚, 范路萍, 尹秋凤, 刘明, 汪登斌
胎儿肺囊性病变是肺组织胚胎发育异常引起的先天性肺病变,发病率约4.15∶10 000[1],主要分为先天性肺气道畸形(congenital pulmonary airway malformation,CPAM)、肺隔离症(pulmonary sequestration,PS)、支气管源性囊肿(bronchogenic cyst,BC)和先天性支气管闭锁(congenital bronchial atresia,CBA)等。产前超声为首选的影像学检查,但超声受软组织分辨率低、孕妇和胎儿等因素的限制。随着快速MRI序列的发展,胎儿MRI凭借其视野广阔、软组织分辨率高的优势在胎儿肺囊性病变的诊断中发挥着重要作用,成为超声重要的补充检查。笔者回顾性分析30例产前诊断为胎儿肺囊性病变的资料,分析病变的MRI表现,旨在提高胎儿肺囊性病变的诊断水平。
材料与方法
1.一般资料
搜集本院从2010年6月-2018年4月产前诊断为胎儿肺囊性病变的孕妇30例,年龄24~37岁,平均年龄(28.40±3.28)岁;胎儿孕周为21~39.29周,平均(26.65±4.98)周(从孕妇的末次月经开始推算)。本组病例为本院或外院产前超声发现胎儿肺部病变,为更清晰显示病变及进一步明确诊断肺病变,于1周内在我院行胎儿MRI检查。
2.检查方法
采用GE Signa 3.0T/Philips 3.0T MRI扫描系统,体线圈。孕妇仰卧,足先进。不予以镇静剂。做胎儿横断面、矢状面、冠状面多切面扫描。采用两种快速类T2WI扫描序列,主要序列为快速稳态场回波序列,部分运用单次激发快速自旋回波序列;快速T1WI扫描序列,快速翻转恢复运动抑制序列。快速稳态场回波序列扫描参数:翻转50°,带宽125,TR 5.1~5.5 ms,TE 1.5~1.8 ms,矩阵224×224,采集次数2,层厚6 mm,间隔0.5 mm,视野38 cm×38 cm。单次激发快速自旋回波序列扫描参数:带宽20.83,TR 4000 ms,TE 30.8 ms,矩阵320×224,采集次数0~1,层厚7 mm,间隔0,视野42 cm×30 cm。快速翻转恢复运动抑制序列扫描参数: 翻转角20°,带宽15.63,TR 7.7 ms,TE 4.2 ms,矩阵256×160,层厚6.5 mm,间隔0.5 mm,视野36 cm×27 cm。扫描层数根据胎儿大小定。所有序列扫描时间不超过10 min。
3.图像分析
根据随访结果对病变进行分类,由2名有高级职称的放射科医师对图像进行回顾性分析,分析了病变的位置、形态、大小、信号特征、是否发现体循环供血及纵隔有无移位等。
结 果
1.产前磁共振表现及诊断
30例病变MRI表现为快速稳态场回波序列或单次激发快速自旋回波序列高信号、快速翻转恢复运动抑制序列低信号。
经产后手术病理证实的16例病灶中,左肺8例,右肺6例,纵隔2例,其中2例纵隔病灶产前MRI定位诊断为右肺。
先天性肺气道畸形:7例产前定位、定性诊断均准确,左肺3例,右肺4例;上叶3例,下叶4例。4例边缘呈分叶状,见多个大小不一的囊,较大的囊长径>0.5 cm,囊内信号均匀,其中1例患侧肺饱满且纵隔左移;1例呈类圆形,长径>0.5 cm,边缘光整,内部信号欠均匀,见小条状稍低信号及一枚小囊状更高信号,心脏右移;1例为单囊,呈类圆形,长径>0.5 cm,边缘光整,内部信号均匀(图1);1例呈团块状,实性为主,边缘尚光整,内部信号尚均匀;7例均未见体循环血管分支进入病灶。
肺隔离症:产前定位准确,4例均为左肺下叶。3例定性诊断正确,MRI表现为团块状,边缘光整,均可见体循环(降主动脉)分支进入病灶(图2),2例内部信号均匀,1例内见囊样更高信号,其中1例心脏稍右移;1例误诊为先天性肺气道畸形,MRI表现为多枚囊状高信号,形态不规则,未见明显体循环分支进入病灶。
支气管源性囊肿:3例产前诊断均为先天性肺气道畸形。2例产前定位准确,其中1例位于左肺,MRI表现为左肺增大,见多发大小不一病灶,部分边缘呈分叶状,内部信号尚均匀;另1例位于右肺上叶,MRI表现为团状,边缘欠光整,内部见管状低信号及小囊状更高信号。1例定位错误,产前定位于右肺上叶,手术中定位于上纵隔偏右侧,MRI表现为类圆形,边缘光整,内部信号均匀,其内侧缘与气管关系密切(图3);3例均未见体循环血管分支进入病灶,纵隔均未见受压移位。
先天性支气管闭锁:产前定位准确,位于右肺下叶,而定性诊断误诊为先天性肺气道畸形,呈团状,边缘光整,内部信号均匀,未见体循环血管分支进入病灶,纵隔未见移位(图4)。

图1 右肺下叶先天性肺气道畸形。孕35+6周。胎儿MRI示右肺下叶脊柱旁类椭圆形异常信号灶(箭),最大截面大小约3.6cm×2.4cm,快速稳态场回波序列呈高信号,内部信号均匀,边缘光整,与正常肺组织分界清。 图2 左肺下叶肺隔离症。孕24+5周。胎儿MRI冠状面示左肺下叶团状异常信号灶(白箭),单次激发快速自旋回波序列呈高信号,与正常肺组织分界清,可见起自胸主动脉的分支血管进入病变(黑箭)。图3 纵隔型支气管源性囊肿。孕24+5周。a) 胎儿MRI示右肺上叶区类圆形异常信号灶(黑箭),单次激发快速自旋回波序列呈均匀高信号,形态规则,边缘光整,与气管关系密切(白箭); b) 出生后4d行胸部CT平扫示纵隔偏右侧类圆形低密度灶(箭),形态规则,边缘光整,内部密度均匀,平扫CT值为1HU; c) 胸部增强CT示病灶增强后未见强化; d) 胸部CT冠状面三维重建示病灶内侧紧贴气管(箭)。
淋巴管畸形:产前误诊为右肺中下叶先天性肺气道畸形,病灶形态不规则,边缘不光整,向纵隔内胸腺前后间隙延伸,纵隔向左移(图5)。
产前超声随访中消失的3例病灶2例定位于左肺下叶,1例定位于右肺上叶,MRI均诊断为先天性肺气道畸形。2例为单囊,呈类圆形,边缘光整,内部信号均匀;1例表现为左肺下叶信号异常增高,边缘光整,内可见管状更低信号及两枚小囊状更高信号,肺结构完整,经回顾性分析,考虑先天性肺叶液体过载可能(图6)。3例病灶均未见体循环血管分支进入病灶,纵隔未见受压移位。3例病灶在之后的产前超声随访中均未见显示(检查时间分别为孕30周、孕32周、孕30周)。
随访中病灶未消失且未行手术治疗的11例左侧8例,右侧3例。2例尚未出生,病变呈团块状,边缘光整,内部信号均匀,分别可见腹主动脉及降主动脉的分支进入病灶内,MRI诊断为肺隔离症。9例已出生,1例表现为右肺体积增大,呈异常高信号,内部信号不均匀,见多发大小不一的囊状更高信号灶及起自腹主动脉的分支血管进入病变,MRI诊断为先天性肺气道畸形合并肺隔离症(图7)。1例诊断为左侧胸腔积液伴左肺受压,未提及肺囊性病变。余7例病例MRI均诊断为先天性肺气道畸形,2例呈类圆形,边缘光整,内部信号均匀;4例边缘呈分叶状,见数个囊状更高信号;1例呈片状,边缘光整,内部信号均匀;7例均未见体循环血管分支进入病灶,纵隔均未见受压移位。
2.产前MRI诊断、产前超声诊断与术后病理结果比较
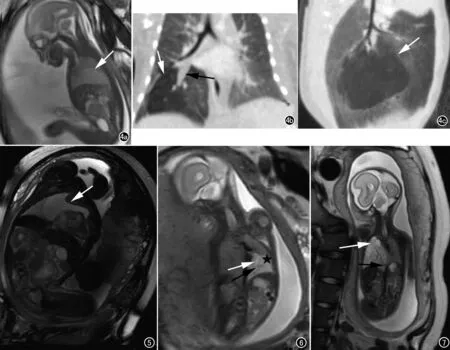
图4 右肺下叶先天性支气管闭锁。孕25周。a) 胎儿MRI示右肺下叶团状异常信号灶(箭),快速稳态场回波序列呈高信号,内部信号尚均匀,形态不规则,与正常肺组织分界清; b) 出生后1d行胸部CT平扫冠状面三维重建示右肺下叶内基底段肺气肿表现(白箭),近肺门处见粘液栓(黑箭); c) 矢状面三维重建示右肺下叶内基底段肺气肿表现(白箭)。 图5 纵隔内大囊型淋巴管畸形。孕37周。胎儿MRI冠状面单次激发快速自旋回波序列示纵隔内单房囊性病变,呈高信号,病变边缘不光整,内侧紧贴心脏,纵隔及心影受压左移,病变主要位于右侧胸腔,部分延伸入左侧胸腔,呈爬行性生长表现。 图6 左肺下叶先天性肺叶液体过载可能。孕24+3周。胎儿MRI冠状面单次激发快速自旋回波序列示左肺下叶信号增高(星),边缘光整,内见条状更低信号(黑箭)及小囊状更高信号(白箭),肺结构完整,未见体循环分支血管进入病灶。孕30周时行超声检查左肺下叶未发现病灶。 图7 右肺先天性肺气道畸形合并肺隔离症。孕23周。胎儿MRI冠状面单次激发快速自旋回波序列示右肺体积增大,呈异常高信号,内部信号不均匀,多发大小不一的囊状更高信号灶(白箭)及起自腹主动脉的分支血管进入病变(黑箭)。
回顾性分析经手术治疗病例的临床资料,以术后病理结果为标准,分别计算产前MRI诊断、纠正后MRI诊断及产前超声诊断的定位准确率及定性准确率(表1)。纠正后MRI诊断为知晓病理诊断后回顾性分析病变的影像表现,纠正了1例纵隔型支气管源性囊肿和1例纵隔内淋巴管畸形的产前MRI诊断。
讨 论
胎儿肺囊性病变为前肠、肺气道和血管的畸形和发育异常的疾病,包括先天性肺气道畸形、肺隔离症、支气管源性囊肿和先天性支气管闭锁等。超声因其安全、实用、经济为胎儿首选的影像学检查,但存在一定局限,如检查视野偏小、软组织分辨率低,而且当孕妇有子宫肌瘤、羊水过少、肥胖、多胎和胎儿体位不佳、肋骨遮挡等情况时,胎儿显示不清楚,容易漏诊、误诊。

表1 胎儿肺囊性病变的产前诊断与病理结果对比
胎儿MRI具有视野广阔、软组织分辨率高、可进行多平面扫描的优势,且不受孕妇体质、胎儿体位影响,能清晰显示病变的位置、范围、内部情况及与正常肺组织、纵隔的关系等。
1.经手术证实的胎儿肺囊性病变的诊断及MRI表现
先天性肺气道畸形以前称为先天性囊性腺瘤样畸形(congenital cystic adenomatoid malformation,CCAM),是胎儿最常见的肺部病变,大多学者认为其发病机制是肺芽的发育异常导致局部支气管过度生长[2]。其发生率双肺相仿,多为单侧单叶,多叶及双肺累及较罕见[3]。本组病例中右肺发生率高于左肺;7例均为单侧单叶。目前依据其临床病理特征将其分为5型[4-5],其中Ⅰ-Ⅲ型相当于经典的STocker分型,不同类型的先天性肺气道畸形在MRI上有不同的表现。0型表现为实性病变,Ⅲ型表现为小囊或实性病变;Ⅰ型、Ⅱ型及Ⅳ型表现为大囊(囊腔直径≥0.5 cm)或大囊合并小囊(大囊囊腔直径≥0.5 cm)。MRI诊断根据其影像特征并结合超声分型,按囊的大小可将其简单分为大囊型(最大囊直径≥0.5 cm)和微囊型(最大囊直径<0.5 mm)。大囊型表现为快速翻转恢复运动抑制序列呈低信号、快速稳态场回波序列呈高信号的病变,形态多不规则,内部有单发或多发大小不一的囊,信号较周围病变组织高或呈等信号,可见快速稳态场回波序列呈低信号的囊壁;微囊型表现为实质性[6]。本组病例中6例为大囊型(4例多囊,边缘呈分叶状;2例单囊,边缘光整);1例微囊型,实性为主,内部信号均匀,未见囊状更高信号。本组病例根据MRI表现产前均准确诊断,而且胎儿MRI能多切面显示病变内囊的影像特征,为先天性肺气道畸形的分型提供依据。其中1例产前MRI及超声、产后术后病理诊断均为左肺下叶先天性肺气道畸形,但其产后行MRI检查可见降主动脉发出分支进入病变,不排除存在先天性肺气道畸形合并肺隔离症,但因其为外院手术,未取得手术病理切片进一步分析。
肺隔离症是由于胚胎的前原肠、额外发育的支气管肺芽接受体循环供血而形成的无功能肺组织团块,好发于左肺下叶。在所有胎儿肺囊性病变中,肺隔离症是唯一由体循环供血的病变,因此,发现有起自体循环动脉分支的血管进入病变是诊断关键征象[7]。快速稳态场回波序列(SSFP)实质为T2/T1加权梯度回波图像,心脏四腔和大血管结构为高信号;单次激发快速自旋回波序列(single shot FSE)实质为重T2W自旋回波图像,血管为低信号,气道为高信号,能更好地发现是否有体循环分支进入病变从而明确诊断肺隔离症。本组病例3例可见体循环分支进入病变,产前均正确诊断;而对于供血动脉较小的肺隔离症在MRI上较难发现,也易误诊。本组病例1例未发现体循环分支进入病变,误诊为先天性肺气道畸形,而产前超声及产后胸部CT增强检查均可见体循环分支进入病变,均提示为肺隔离症,因此结合产前超声、产后可予以胸部增强CT或MRI检查,可提高诊断准确率。
支气管源性囊肿可发生在前肠发育路径中的任何部位,若发生于胚胎发育早期,囊肿多位于肺外纵隔部位;若发生于胚胎发育后期,则多位于肺内[8]。根据发生部位可以分为纵隔型(占多数[9])、肺内型和异位型。MRI除了能显示病变的位置、形态、信号外,还能较好地显示病变与气管或支气管的毗邻关系,此为诊断的提示性征像,如果支气管源性囊肿未与气道毗邻,或囊肿较大而毗邻关系复杂时,诊断较为困难[10]。本组病例3例在产前MRI及超声均误诊为先天性肺气道畸形,其中1例位于纵隔内,呈类圆形,边缘光整,冠状面可见病变内侧紧贴气管,提示为支气管源性囊肿;另2例形态不规则,边缘不光整,内部见数个囊状更高信号,未发现与气管或支气管确切的毗邻关系,与先天性肺气道畸形鉴别困难。
先天性支气管闭锁是一种罕见的胎儿肺畸形,常见累及的支气管为段间支气管及亚段间支气管[11],其发病机制有学者认为是支气管芽在孕5~6周胚胎早期因缺血而停止发育,导致支气管局部闭锁或狭窄;也有学者认为是在孕16周后,发育完成的支气管因为缺血或炎症引起的瘢痕导致支气管闭锁[12-13]。闭锁发生于主支气管或叶支气管为中央型,多见于右肺,预后较差;闭锁发生于段或亚段支气管为外周型,多见于左肺上叶和右肺下叶的段支气管,预后较好[14]。闭锁支气管近端与上呼吸道相通,远端扩张并充满液体,从属的肺组织膨胀,文献报道其产前MRI的典型表现为在异常增大、信号异常增高的患肺肺门侧可见高信号的囊腔影[15]。本例右肺下叶内基底段支气管闭锁在胎儿MRI能发现右肺下叶病变,但并未观察到文献所报道的典型表现,产前诊断是困难的。
在经手术病理证实的胎儿肺囊性病变的产前诊断中,MRI的产前定位诊断准确率和产前超声的相同,产前定性诊断准确率高于超声,而且MRI能提供更多信息。MRI能更直观显示先天性肺气道畸形病变内部囊的特点,在分型方面较超声更有优势;能多切面观察病变是否有来自于体循环分支的血管,超声彩色多普勒血流显象也能追溯血管来源,但血管的显示对超声仪器及操作检查者的经验有很高的要求,超声与MRI联合应用可优势互补;对于纵隔内病变的定位是优于超声的;对于病变与气管、支气管关系的显示优于超声;能观察到支气管闭锁的部位及肺组织的病变范围,对于分型及分析其预后有一定帮助;此外,MRI还能测量剩余正常肺组织体积、肺发育的成熟度等情况[16-17]。
2.产前超声随访中消失的胎儿肺囊性病变的诊断及MRI表现
关于胎儿肺部病变的自然退化或消失的报道主要为先天性肺气道畸形和肺隔离症,3例随访中消失的病灶,产前MRI及超声均未发现有体循环分支血管进入其内,2例呈类圆形,边缘光整,内部信号均匀,排除肺隔离症后,根据笔者的经验和MRI表现特征,认为先天性肺气道畸形可能性比较大。另外1例表现为左肺下叶信号增高,边缘光整,内见条状更低信号及小囊状更高信号,肺结构完整,产前MRI及超声均未见体循环分支血管进入病灶,不符合先天性肺气道畸形或肺隔离症MRI表现,文献报道在鉴别胎儿肺部自然退化或消失的病变应考虑先天性肺叶液体过载(congenital lobar fluid overload,CLFO),它可能是由于短暂的粘液堵塞或外因性原因压迫导致气道的单向活瓣作用导致液体受限于肺叶内,产前超声有时很难与微囊型先天性肺气道畸形鉴别,而MRI能更好显示肺内完整的结构和肺门血管因液体过载受拉伸的特点[18],对其诊断有独特的优势。本例的MRI表现符合文献所报道的先天性肺叶液体过载。
3.随访中未消失且未行手术治疗的胎儿肺囊性病变的诊断及MRI表现
2例尚未出生,根据产前MRI及超声诊断为肺隔离症。9例已出生,目前情况可,无明显的呼吸系统症状,未选择手术治疗;其中7例诊断为先天性肺气道畸形,1例产前超声诊断为左侧胸腔积液和左肺下叶肺隔离症,而MRI诊断为左侧胸腔积液伴左肺受压,并未提及左肺肿块。胎儿胸腔积液为液体聚集于单侧或双侧胸膜腔内的异常,胎儿胸腔积液超声或MRI均可明确诊断,胎儿MRI的冠状面可更直观地显示肺组织受压的程度及纵隔、心脏的移位的情况。胸腔积液会导致患侧肺组织受压、信号不均匀,较容易遗漏患侧肺组织的其他病变。此外,1例由腹主动脉分支供血的右肺囊性病变内可见多发较大更高信号的囊,为先天性肺气道畸形合并肺隔离症的典型表现。
常见的胎儿肺囊性病变的发病机制相似[19],磁共振表现也相似,尤其是当病变表现不典型或混合出现时,诊断不易。此外,在产前诊断为胎儿肺囊性病变的病例中,1例经手术证实为淋巴管畸形(lymphatic malformation,LM)。它是淋巴管发育异常或某些原因引起淋巴液排出障碍,淋巴液的潴留导致淋巴管扩张、增生而形成[20],常见的发生部位是颈部(75%)、腋部(20%)、腹膜后、腹腔内器官(2%)、四肢和骨骼(2%),纵隔的发生率不足1%[21]。本例为大囊单房的囊性病变,内部信号均匀,产前误诊为先天性肺气道畸形,但是回顾性分析,可见病灶形态不规则,边缘不光整,向纵隔内胸腺前后间隙延伸,提示为发生于纵隔内的囊性病变,需要考虑淋巴管畸形的诊断。淋巴管畸形治疗方法的选择受发病部位、深度、发病年龄、病变类型(大囊型或微囊型)及对于周围正常组织的影响等多种因素影响[22],与超声相比胎儿磁共振能更好地显示淋巴管畸形的发生部位、形态及在组织间隙爬行性生长这一特征性表现,给定性诊断和治疗方案的选择提供重要信息。
总之,胎儿MRI有助于胎儿肺囊性病变的定性诊断,可作为胎儿超声有效的补充手段,为临床处理提供重要信息。文献报道先天性肺气道畸形有自限性,部分可能与胸膜肺母细胞瘤的发生具有相关性[23]。本研究存在不足之处如样本较小;部分患儿在外院手术,未取得病理图像;一些病例未手术治疗,缺乏手术病理;缺乏长期随访观察等。
