黑北凹地富钾地下卤水自然蒸发实验研究
2019-06-15彭玲玲魏学斌赵为永穆延宗王云生
彭玲玲 ,魏学斌 ,赵为永 ,刘 颖 ,穆延宗 ,乜 贞 ,王云生
[1.中国地质科学院矿产资源研究所,自然资源部盐湖资源与环境重点实验室,北京100037;2.中国地质大学(北京);3.中国石油青海油田分公司勘探开发研究院]
黑北凹地位于柴达木西北地区阿尔金山山前冲洪积扇群上,梁中凹地北东方向,察汗斯拉图以西。近年来,在梁中凹地-黑北凹地-察汗斯拉图一带发现大量砂砾石层型孔隙卤水,该卤水储量巨大,富水性较强,水位埋藏浅[1],易抽取且抽取过程不易结盐。与南翼山等背斜构造第三系油田水富含B、Li、Br、I等不同[2-4],黑北凹地砂砾石层型孔隙卤水化学组成简单,特征为高Na,富含K,低B、Li的氯化物型卤水。根据研究结果,此种类型卤水为高山融水溶滤N2地层中的盐类而形成的溶滤型卤水[5]。卤水中NaCl含量达到单独开采工业品位,KCl达到边界品位,由于地下卤水储量巨大,有望成为中国钾盐生产后备基地。现场蒸发实验对卤水中有用元素的可利用性、生产工艺及后期工业化生产有着重要的指导作用[6]。笔者以黑北凹地地下卤水为研究对象,借鉴前人对其他盐湖卤水蒸发实验研究的经验[7-11],通过夏季小型现场蒸发实验,探究了卤水在蒸发浓缩过程中各元素的富集浓缩变化规律及析盐规律。
1 实验部分
1.1 实验原料
卤水取自黑ZK02井。初始卤水物化参数见表1。

表1 黑北凹地黑ZK02井卤水物化参数
1.2 实验方法
蒸发实验在黑北凹地现场进行,蒸发初始所用容器为5个口径为50 cm、深度为20 cm的塑料盆。取卤水127.9 kg分置于5个蒸发容器中,卤水深度为13 cm。将装置放置在自然条件下蒸发,定期测定大气的温度、湿度,卤水的温度、密度、pH、蒸发量等物理参数;及时进行固液分离,并分别准确称量分离后的固体、液体质量,分别取固体、液体样品进行化学分析。为控制蒸发速度,蒸发过程中逐渐减少容器的个数,使卤水深度保持在10 cm以上,当卤水深度较浅时进行合并继续蒸发。固、液分离频率根据卤水蒸发速率与析盐速率而定,直到最终无法进行固液分离为止。
1.3 分析方法
由中国科学院青海盐湖研究所盐湖化学分析测试部进行液、固相样品的分析测试[12]:Na+、Ca2+、Mg2+、K+、B2O3用等离子光谱仪分析;Sr2+、Li+用等离子质谱仪分析;Cl-用以铬酸钾为指示剂的硝酸银容量法分析;SO42-用盐酸联苯胺容量法分析;矿物种类鉴定用Rigaku MiniFlex 600型X射线衍射仪和JSM-5610LV型扫描电镜-能谱仪分析;每日常规测量中pH使用PHB-4型便携式pH计测量,湿度使用WS2080A型温湿度计测量,密度使用漂浮式比重计测量。
1.4 实验结果
蒸发实验从2014年8月9日开始,10月5日结束。期间进行了16次固、液分离,由于9月22日进行第13次固、液分离之后卤水浓度过大,固样难以晾干,并且会随着温度的变化在半固体与固体之间转化,故不再取固样进行溶解测试。蒸发实验观测数据见表2,固、液样品分析数据见表3、表4。根据配矿理论将分析数据进行配矿[13],结果见表5。

表2 蒸发实验观测数据

表3 固样化学组成

表4 液样化学组成

表5 固相中各盐类质量分数 %
2 数据处理与分析
2.1 相图分析
黑北凹地地下卤水中的阴离子主要为Cl-,阳离子主要为 Na+、Ca2+、Mg2+、K+等,其卤水类型按其化学性质分类为氯化物型,在蒸发实验中前期Ca基本不以矿物析出,因此可以采用K+,Na+,Mg2+∥Cl--H2O(25℃)四元介稳相图;在实验后期,Ca浓缩富集,达到饱和后以CaCl2·6H2O矿物析出,因此可以选用 Na+,Mg2+,Ca2+∥Cl--H2O(25 ℃)四元介稳相图。根据整个蒸发过程中的固、液相中的离子组成及计算出的相图指数,绘得卤水蒸发结晶路线,见图1。从图1可以看出,液相初始点位于NaCl相区,随着蒸发的进行液相点逐渐向KCl相区和远离NaCl相点的位置移动,直到HL8点到达NaCl与KCl共饱线,沿此共饱线向石盐、钾石盐、光卤石共饱点移动,因此共饱点为不稳定共饱点,之后随着蒸发液相点沿石盐与光卤石共饱线移动,最终蒸干于石盐、光卤石、水氯镁石共饱点。对应的固相点最初由NaCl相区缓慢朝KCl相区移动,这是由于卤水中的离子以Na+、Cl-占绝对优势,导致蒸发初始阶段析出物以NaCl为主,所以在相图中显示为长时间处于NaCl相区,HS8点之后固相点迅速进入KCl相区,与液相点对比可知,液相点在HL8点到达NaCl、KCl共饱线,之后向石盐、钾石盐、光卤石共饱点移动,说明在HL8点之前液相中的K不断浓缩,而析出的固相以NaCl为主,到HL8点之后液相中的KCl开始析出。在石盐、钾石盐、光卤石共饱点钾石盐开始溶解,而石盐和光卤石共饱析出,至钾石盐回溶完成后,液相点随蒸发沿石盐、光卤石共饱线移动,在此相图中最终蒸干于石盐、光卤石、水氯镁石共饱点。结合相图及蒸发记录可知,在卤水密度达到1.307 g/cm3,或者体积浓缩至原卤体积的5.13%时,KCl便开始大量析出。

图1 K+,Na+,Mg2+∥Cl--H2O(25 ℃)介稳相图中固液相的变化趋势
2.2 矿物析出次序
图2 为固体样品 HS6、HS9、HS11、HS14 的扫描电镜-能谱仪分析结果;图3为固体样品HS6的XRD分析结果。从图2、图3可以将实验过程中盐类的析出分为 4 个系列:1)石盐(HS1~HS6);2)石盐+光卤石(HS7~HS10);3)石盐+光卤石+水氯镁石(HS11~HS13);4)石盐+光卤石+水氯镁石+南极石(HS14)。
2.3 离子富集规律分析
实验用卤水中Na+、Cl-基本达到饱和,在卤水蒸发初始即有大量固相析出,而且析出的固相中石盐质量分数可达98.68%。由蒸发记录(表2)及固相配矿结果(表5)可知,第七次固液分离后成卤率已达8.17%,固相中石盐质量分数仍高达90%以上,第八次固液分离后成卤率为5.59%,固相中石盐质量分数有所下降(为79.01%),其后的数次分离固相中石盐含量迅速下降。其他离子则经历了较长时间的富集过程,而后才开始成盐析出,这种结果印证了前述原卤离子含量单一的特征。
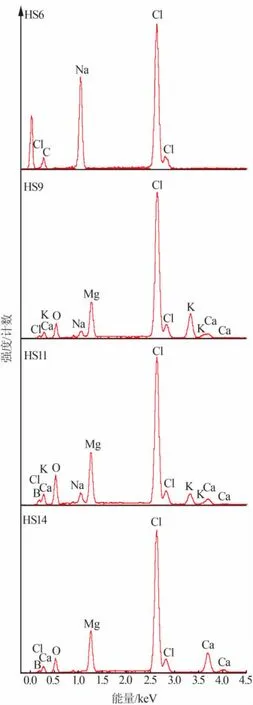
图2 HS6、HS9、HS11、HS14 样品扫描电镜能谱分析结果

图3 HS6样品XRD谱图
图4为固相中KCl质量分数与液相中K+质量浓度随着成卤率的变化趋势。从图4看出,蒸发初期液相中K+质量浓度缓慢增加,曲线较为平缓,从HL0到HL3成卤率从100%降低到33.27%,但是液相中K+质量浓度只从2.603 g/L增加到5.673 g/L,仅增加至2.2倍,但是当到达HL3点之后,即成卤率达到33.27%之后,K+在液相中的富集速率逐渐加快,曲线斜率明显增大,直到HL8点即成卤率达到5.59%时,液相中K+质量浓度达到极大值21.060g/L,之后便迅速下降;与液相中K+质量浓度相对应,固相中KCl质量分数在HS7点之前近乎于零,说明在HS7点之前,即成卤率到达8.17%之前,液相中K+浓度一直未达到饱和,固相中微量的KCl含量来源于母液夹带,HS7点之后,固相中的KCl含量迅速增加,直到HS9点,即成卤率为4.14%时,固相中KCl质量分数达到极大值31.92%,之后便迅速降低,说明该卤水中的钾盐在此阶段集中析出。固相中KCl质量分数从迅速增加到降低的过程,与液相中的K+含量先短暂增加到极大值点后又迅速降低的变化规律相吻合。

图4 固相中KCl质量分数、液相中K+质量浓度随成卤率的变化规律
图5为Mg在固、液相中的含量随成卤率的变化趋势。从图5看出,前期液相中Mg2+质量浓度变化趋势与K+类似,都是经历了较长时间的缓慢增加过程,在HL3点之前,即成卤率达到33.27%之前,曲线十分平缓,液相中Mg2+质量浓度只从6.075 g/L增加到14.920 g/L,仅增加至2.5倍,HL3点之后液相中Mg2+富集速率迅速增加,曲线斜率明显增大,直到HL16点,液相中Mg2+质量浓度达到极大值73.090g/L,从HL11到HL16,液相中Mg2+含量出现小幅的上下波动,说明其存在蒸发浓缩与析盐之间的一个平衡状态;固相中的Mg2+质量分数,在HS4点之前,即成卤率达到22.52%之前,Mg2+质量分数增加一直较为缓慢,曲线平缓并且略有波动,说明此时固相中的Mg2+来源主要为母液夹带,从HS4点之后,固相中的Mg2+富集速率开始逐渐加快,曲线的斜率逐渐增大,直到HS12,固相中的Mg2+质量分数达到极大值8.339%。

图5 Mg在固、液相中的含量随成卤率的变化规律

图6 Li、B2O3在液相中的质量浓度随成卤率的变化规律
图6为液相中Li、B2O3随成卤率的变化趋势。从图6可以看出,二者在液相中随着成卤率的降低一直处于富集阶段,HL6点之前,卤量较大,Li、B2O3浓度低,蒸发浓缩速率较慢,HL6点之后,成卤率达到12.24%,二者开始迅速富集,但是最终并未出现下降趋势。从固样分析结果(表3)来看,随着成卤率的降低,Li、B2O3在固样中的质量分数并未出现大幅增长,说明其在整个蒸发过程中并未以盐的形式析出。根据浓缩倍数关系,在整个蒸发过程中,卤水浓缩了322.6倍,B2O3浓缩了393.9倍,而Li只浓缩了81.8倍,考虑到测试误差及实验过程中的母液夹带及损失,B2O3在整个蒸发过程中的富集倍数与卤水相符,而Li在蒸发过程中出现了损失,究竟以何种方式损失,还有待后续查证。
2.4 pH及密度变化规律分析
在蒸发实验过程中,连续测定了每次固液分离时卤水的pH及密度,根据测定结果绘制其随成卤率的变化规律见图7。从图7可以看出,随着成卤率的降低,pH及密度都呈现出规律性的变化:卤水pH不断降低,而密度不断增高,pH由初始的6.45降低到最终的2.03,密度由初始的1.200 g/cm3增加到最终的1.400 g/cm3。pH与密度的斜率(绝对值)均在HL8点开始迅速增大,其下降或上升速度明显加快,而此点正好对应KCl大量析出的点,因此此次实验pH及密度的变化规律可以做为卤水制卤过程的控制指标,可为后期卤水提钾实验和盐田实验提供相关数据支撑。

图7 pH及密度随成卤率的变化规律
3 结论
通过黑北凹地富钾卤水自然蒸发实验,可以得出以下结论:1)黑北凹地砂砾石层型孔隙卤水中Na、Cl离子含量远高于其他离子,在蒸发结晶过程中,经过了较长时间的石盐析出阶段,达到钾盐析出阶段,其析盐顺序为石盐—光卤石—水氯镁石—南极石;2)黑北凹地地下卤水在晒制过程中,其蒸发结晶路线与 K+、Na+、Mg2+∥Cl--H2O(25 ℃)介稳相图相符,原始卤水位于氯化钠相区,最终蒸干于石盐、光卤石、水氯镁石共饱点;3)黑北凹地地下卤水在蒸发过程中,钾以光卤石矿物析出,当成卤率达到5.59%时,光卤石开始大量析出,且有一钾盐的集中析出阶段,便于钾盐的提取利用;4)B2O3、Li在整个蒸发过程中一直在卤水中浓缩富集,没有结晶析出,其最终质量浓度分别为5.79 g/L与180 mg/L,B2O3浓缩了393.9倍,而Li只浓缩了81.8倍;5)蒸发过程中,卤水的pH、密度数据直观反映了卤水的蒸发进度,可作为后续制卤阶段指示指标。
