锂离子掺杂对 Na2CaSiO4:Eu3+红色荧光粉能量增强作用研究
2019-04-12隆金桥刘真珍刘晓风郑丽雪黄珍华
隆金桥,刘真珍,颜 锦,刘晓风,郑丽雪,黄珍华
(1.百色学院化学与环境工程学院,广西百色533000;2.百色学院信息工程学院)
红色荧光粉作为三基色白光LED灯的组成部分而得到了广泛的研究。在已经研究的红色荧光粉中,报道最多的是Eu3+掺杂红色荧光粉。Eu3+掺杂红色荧光粉的特点是可被近紫外光及蓝光所激发,且发射光谱为线状光谱,故色度较纯、流明效率较高,其缺点是由于在近紫外光区及蓝光区的激发光谱也是线状光谱,不存在较宽的激发光谱,因此它的发光效率不高。为了得到发光性能良好的红色荧光粉,国内外有不少学者进行了相关的研究[1-4]。例如在LiYSiO4:Ce3+,Tb3+,Eu3+[1]、NaCaGaSi2O7:Eu3+,Li+[2]等荧光粉中,均获得了既增宽又增强的激发光谱以及增强了的线状发射光谱。
硅酸盐具有结构稳定、合成成本低、能被紫外或蓝光激发等特点,在防水、耐热、耐腐蚀等方面的性能表现优越,被广泛应用于节能灯、白光发光二极管(LED)、显示器等领域,引起研究者的极大关注[2-4]。目前见报道的以硅酸盐为基质的红色荧光粉有如下 几 个 体 系 :NaCaGaSi2O7:Eu3+,Li+[2]、Na2CaSiO4:Eu3+[3]、Sr2SiO4:0.03 Eu3+[4]等。 这些荧光粉均获得了既增宽又增强的激发光谱以及增强了的线状发射光谱。本文研究的红色荧光粉 Na2CaSiO4:Eu3+,Li+体系以前还未见报道。本文采用高温固相合成法合成了Eu3+、Li+掺杂Na2CaSiO4的红色荧光粉,用XRD和PL对荧光粉进行表征,并对Eu3+、Li+掺杂浓度对荧光粉发光性的影响进行研究。
1 实验
1.1 试剂及仪器
硝酸铕[Eu(NO3)3,纯度为 99.99%];硅酸钠、硝酸锂和碳酸钙,均为AR。
F-7000型荧光分光光度计;Rigaku D/max 2500V型X射线粉末衍射仪。
1.2 荧光粉的制备
1.2.1 30 mmol Na2Ca1-xSiO4:xEu3+的制备
按 n(Na)∶n(Ca)∶n(Si)∶n(Eu)=2∶(1-x)∶1∶x 准确称取硅酸钠、碳酸钙置于玛瑙研钵中,加入1 mmol/mL的硝酸铕溶液(x=0.04、0.08、0.12、0.16、0.20、0.24)。充分研磨30min,转入瓷坩埚,再放入烘箱中于105℃条件下烘3 h,冷却后研磨得到产物前驱体。将前驱体转入瓷坩埚,在马弗炉中300℃下煅烧3 h,再升温至850℃煅烧4 h,降温后取出产品,自然冷却,研磨即得白色Na2CaSiO4:Eu3+系列荧光粉。
1.2.2 30 mmol Na2Ca0.84SiO4:0.16Eu3+,yLi+的制备
按 n(Na)∶n(Ca)∶n(Si)∶n(Eu)∶n(Li)=2∶0.84∶1∶0.16∶y准确称取硅酸钠、碳酸钙置于玛瑙研钵中,加入1 mmol/mL的硝酸铕溶液,再加入1 mmol/mL硝 酸 锂 溶 液 (y=0.08、0.10、0.12、0.14、0.16)。 然 后按1.2.1的步骤进行,可得系列荧光粉Na2CaSiO4:Eu3+,Li+。
1.3 荧光粉的表征
XRD的测定:运用Rigaku D/max 2500V型X射线粉末衍射仪进行,铜靶 Kα衍射、波长 λ为0.154 060 nm、扫描范围为 5~70°、步长为 0.026°、每步扫描时间为20 s。
荧光光谱测定:运用F-7000型荧光分光光度计对荧光粉进行光谱测量。光源为氘灯、扫描速率为1 200 nm/min、激发光狭缝为2.5 nm、发射光狭缝为2.5 nm、工作电压为700 V。
2 结果与讨论
2.1 XRD分析
图1 为 Na2CaSiO4:Eu3+和 Na2CaSiO4:Eu3+,Li+的XRD谱图。由图1可知,荧光粉Na2CaSiO4:Eu3+和Na2CaSiO4:Eu3+,Li+的衍射峰和标准卡 PDF#73-1726的衍射峰相吻合,没有出现Eu3+和Li+的衍射峰。说明掺杂少量的Eu3+和Li+后,合成出的荧光粉仍为纯相。标准卡PDF#73-1726 Na2CaSiO4属于立方晶系结构,Z=4,空间群为P213,晶格参数a=b=c=0.748 nm。Na2CaSiO4:Eu3+的晶格参数 a=b=c=0.749 nm,Na2CaSiO4:Eu3+,Li+的晶格参数 a=b=c=0.747 nm。 这些参数发生了变化都说明Eu3+和Li+已经进入荧光粉的晶格中。根据离子电负性标度,Ca2+电负性值为1.160,Na+电负性值为 1.024,Eu3+电负性值为 1.433,Li+电负性值为 1.009[5]。根据文献[6-7]描述,掺杂离子容易取代电负性相近的离子,所以Li+会优先取代Na+的位置,Eu3+会优先取代Ca2+的位置。
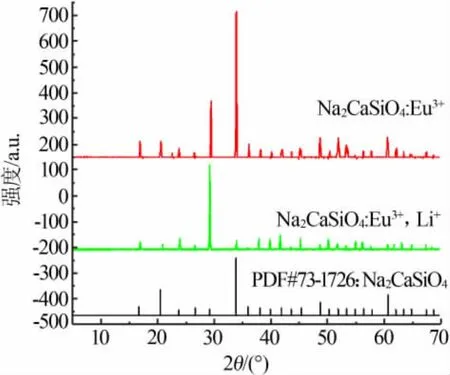
图1 850 ℃焙烧 4 h 的 Na2CaSiO4:0.16Eu3+和Na2CaSiO4:0.16Eu3+,0.12Li+的 XRD 谱图
2.2 Na2CaSiO4:0.16Eu3+的光谱特征
图2为 Na2CaSiO4:0.16Eu3+的光谱特征峰,在350~550 nm区间为监测波为614 nm的荧光粉Na2CaSiO4:0.16Eu3+的激发峰,它们均源自于Eu3+离子的7F0—5L6、7F0—5D2和7F0—5D1的跃迁。 这些峰的位置分别位于 394、464、534 nm 处,其中 464、534 nm处比在394 nm处弱得多,说明Na2CaSiO4:0.16Eu3+荧光粉可用于紫外光激发的LED灯当中。图2的发射光谱可知,在394、464 nm分别激发下,荧光粉的发射光谱形貌大致相同,都存在4个发射峰,分别位于 590、614、646、696 nm 左右。 它们都属于 Eu3+的5D0—7FJ(J=1、2、3、4)跃迁。 但是 394 nm 激发的发射光谱比464 nm激发的发射光谱要强,这就再一次证明该荧光粉能更好地被紫外光有效激发。本课题所开展的 Na2CaSiO4:0.16Eu3+荧光粉主发射峰处在614 nm,是属于5D0—7F2磁偶极跃迁所对应的发射峰,发红色光。原因是在Na2CaSiO4:0.16Eu3+荧光粉晶体中Eu3+取代了半径和电负性相当的Ca2+的位置,使 Eu3+不处在 Na2CaSiO4的中心,对称性弱[8],红色发光增强。
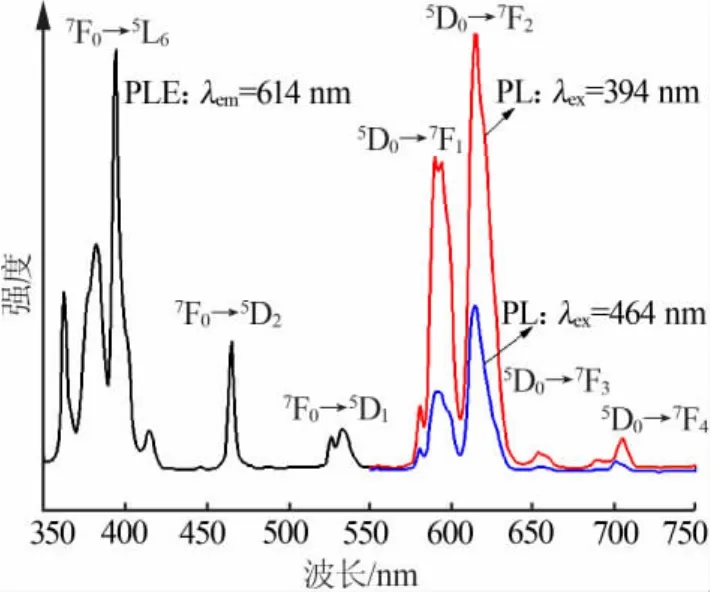
图2 Na2CaSiO4:0.16Eu3+样品的荧光光谱图
2.3 Eu3+之间能量传递方式及荧光猝灭研究
图3 为 Na2CaSiO4:xEu3+(x=0.04~0.24)的发射光谱。由图3可知,掺杂不同浓度的Eu3+时,样品的发射光强度随着Eu3+掺杂浓度的增加而增强。当Eu3+的掺杂量x达到0.16时,发光强度达到最大,继续增加Eu3+浓度发光强度迅速降低,出现浓度猝灭现象。这是由于在晶体内当Eu3+离子的用量增大时,激活剂Eu3+之间的距离缩短,使Eu3+之间电子的无辐射能量传递几率增强,发射几率变小,使发光强度减弱。文献[9]报道,离子之间能量传递的临界距离(RC)可以表示为:
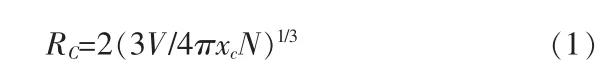
式中:xc为发光强度最大时的稀土含量(硝酸铕与Na2CaSiO4物质的量比);N为晶胞中可被激活离子替换的阳离子晶格位置数;V为晶胞体积。对于Na2CaSiO4:Eu3+荧光粉来说,xc=0.16、N=4、V=0.420 nm3。将上述参数带入式(1),可以计算出临界距离RC≈1.083 nm。RC≥0.5 nm,说明Eu3+的浓度猝灭过程是多极矩相互作用引起的。
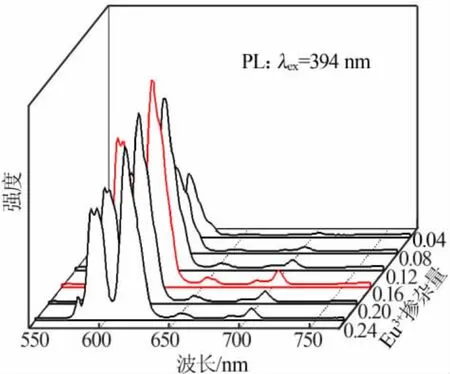
图3 Na2CaSiO4:xEu3+(x=0.04~0.24 )的发射光谱
稀土离子之间是通过能级匹配来实现能量转移的。文献[10-11]的研究已经证实,Eu3+的发光强度I与掺杂浓度C之间存在如下线性关系:

式中:C为Eu3+掺杂浓度;F为材料系数 (同一基质为常数);d=3(为能量传递维数);S表示离子间的相互作用(S=6、8、10分别对应于电偶极-电偶极、电偶极-电多极、电多极-电多极的多极矩相互作用)。根据(2)式对不同Eu3+掺杂浓度的数据进行线性拟合,得到线性方程Y=2.403-1.453X,斜率为-1.453,计算得 S=4.359>3,结合(1)和(2)式结果,可以认为在Na2CaSiO4:Eu3+荧光粉中,引起 Eu3+浓度猝灭效应的能量传递方式主要为电偶极-电偶极相互作用。
2.4 Li+对 Na2CaSiO4:0.16Eu3+发光性能的影响
图4a 是 Na2CaSiO4:0.16Eu3+和 Na2CaSiO4:0.16Eu3+,0.12Li+的激发和发射光谱图。图4b是Na2CaSiO4:0.16Eu3+,yLi+(y=0.08~0.16)产品在监测波长λex=394 nm时的发射光谱图。
由图4a可知,掺入Li+后荧光粉激发和发射光谱图峰的位置、峰的形状很相似,都增强了激发和发射光谱的强度,但发射光谱增强的强度大于激发光谱增强的强度,激发光谱是掺杂前的1.25倍,发射光谱是掺杂前的1.61倍。根据XRD的检测结果,Li+进入Na2CaSiO4晶体中,除了起到电荷补偿剂的作用外,还使Na2CaSiO4晶胞参数发生变化,晶体体积变小,晶体场环境发生变化,这种变化促进了基质Na2CaSiO4与激活离子Eu3+之间的能量传递,从而使Li+掺杂 Na2CaSiO4:0.16Eu3+荧光粉的发光强度得到了提高。另外,适量浓度的Li+掺入发光材料能够提高晶格中的氧空位浓度,使晶体场对称性降低,促进能量转移,从而发光强度增加,本实验结果与文献[12]报道是一致的。

图4 Na2CaSiO4:0.16Eu3+和 Na2CaSiO4:0.16Eu3+,0.12Li+的激发和发射光谱图(a);Na2CaSiO4:0.16Eu3+,yLi+不同Li+浓度发射光谱图(b)
由图4b可知,Li+的掺杂可以有效提高荧光粉的发光强度,Li+掺杂浓度不同发光强度不同,Li+掺杂量y为0.12时,发光最强。少量的掺杂起到电荷补偿和增加晶体中的氧空位作用,促使发光增强。当Li+掺杂量大于0.12时,过多的掺杂将破坏基质Na2CaSiO4的晶格,引起发光强度降低。本实验确定最佳Li+掺杂量为0.12。
2.5 色坐标分析
图5 为 Na2CaSiO4:0.16Eu3+和 Na2CaSiO4:0.16Eu3+,0.12Li+的色坐标图。分别取 Na2CaSiO4:0.16Eu3+和Na2CaSiO4:0.16Eu3+,0.12Li+的发射光谱的数据,经过GoCIE计算得到发射光谱的色坐标值均为x=0.65,y=0.35,比 Sr2SiO4:0.03Eu3+体系(0.60,0.39)[4]要好,与标准的红光色坐标(0.67,0.33)很接近。Li+掺杂前后两荧光粉的色坐标值一样,说明Li+掺杂入荧光粉Na2CaSiO4:0.16Eu3+后,对荧光粉的发光起到增敏作用,对电荷跃迁没有选择性增强,即对5D0—7F1和5D0—7F2增敏作用一致,从掺杂前后的R值变化(R前=1.47,R后=1.51)也可说明这一点。

图5 Na2CaSiO4:0.16Eu3+和 Na2CaSiO4:0.16Eu3+,0.12Li+的色坐标图
3 结论
1)采用高温固相法合成一系列 Eu3+,Li+掺杂Na2CaSiO4红色荧光粉,该荧光粉晶体结构为立方晶系,掺杂Eu3+,Li+后的荧光粉晶胞参数与标准卡相比发生了变化,说明Eu3+,Li+已经进入晶格中。根据离子电负性标度,Li+(1.009)与 Na+(1.024)电负性相近,Eu3+(1.433)与 Ca2+(1.160)电负性相近,掺杂 Li+会优先取代Na+的位置,Eu3+会优先取代Ca2+的位置。2)荧光粉随Eu3+,Li+掺杂浓度的增加,发光强度逐渐增大,当Eu3+掺杂量为0.16时,荧光粉Na2CaSiO4:Eu3+的发光达到最大值。Li+的掺杂对Na2CaSiO4:Eu3+荧光粉具有增敏作用。当Li+掺杂量为0.12时,此时的发射光谱的强度是掺杂前的1.61倍。荧光粉掺杂Li+能起到电荷补偿和增加氧空位作用,使晶格产生畸变,促使荧光粉发光强度增大。
