上皮样滋养细胞肿瘤4例临床分析
2019-04-03邵世清张红霞王社莲张永艳
邵世清,黄 贵, 田 君,张红霞,王社莲,张永艳
1) 河南大学淮河医院妇产科 河南开封 475000 2) 河南大学淮河医院病理科 河南开封 475000
上皮样滋养细胞肿瘤(epitheliodtrophoblastictumor,ETT)是一种非常罕见的特殊类型滋养细胞肿瘤,迄今国内外仅有100余例的报道,占整个妊娠滋养细胞疾病的1.39%~2.00%[1],其发病机制尚不明确,可发生肺、阴道、附件、盆壁、肾等多个部位的转移[2],具有癌的特征。有研究[3]表明ETT组织中含有来自父源的新等位基因和Y染色体基因位点,提示ETT来源于妊娠而非自身。为了提高对该疾病的认识,现收集河南大学淮河医院妇产科诊治的4例ETT患者资料,对其临床特征、病理特点、免疫表型特点、治疗及预后进行总结,报道如下。
1 病例资料
1.1一般资料4例均于2000年5月至2017年8月被河南大学淮河医院收治,入院后常规进行病史采集、体格检查、实验室检查及影像学检查。4例的基本资料见表1。其中1例发生阔韧带转移。
1.2影像学检查彩超(图1A)示:病灶位于子宫下段,包块边界清晰,其周边具有低回声晕带,常见周边型血流分布,呈环形,内部血流稀少或无显示。MRI(图1B)示边界清晰的异常信号影,T1WI等信号或稍低,T2WI以稍高或等信号为主;增强扫描表现为轻度均匀或不均匀强化,内可见出血、坏死或囊变。

表1 4例ETT患者的基本资料
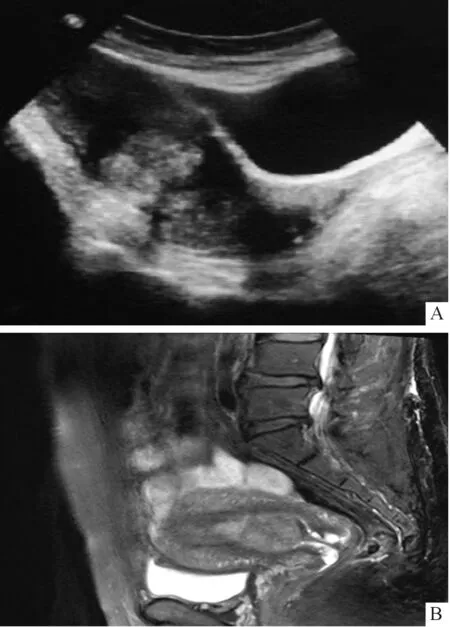
A:彩超;B:MRI
1.3病理表现2例通过诊刮取得标本,另2例通过宫腔镜检查取得标本。 病理科常规给予HE染色及免疫组化染色,确诊为ETT。采用国际妇产科联盟(FIGO)滋养细胞肿瘤解剖分期和预后评分系统(2000年)[4]进行病理分期,病例1~4分别为4、5、4、7期。
4例病灶均位于子宫下段或宫颈处,病灶直径3~6 cm,位于肌壁间,向宫腔突出,呈菜花状或结节状,质地偏软,肿瘤切面灰黄或灰褐色,伴局部出血坏死,可呈囊实性或海绵状。镜下可见统一的单核中间滋养层细胞,呈巢状或条索状分布,可见嗜酸性玻璃样物质沉积和细胞坏死,其围绕肿瘤细胞形成大小不等的肿瘤细胞岛,形成特征性的“地图状”坏死。肿瘤细胞中等大小,核卵圆形或圆形,染色较深,核仁小,易见核分裂象。多数肿瘤细胞胞质透明,少数为嗜双色性;少部分肿瘤细胞胞质丰富,嗜酸性,核较大,染色深。肿瘤细胞巢中或肿瘤细胞之间表现出上皮样细胞生长的特点。
免疫组化染色结果(图2)显示,细胞角蛋白(AE 1、3、7和18)、上皮性钙黏附蛋白(E-cadherin)、表皮生长因子受体(EGFR) 和上皮膜抗原(EMA)、CD10、人类白细胞抗原G(human leukocyte antigen G,HLA-G)、P63均呈弥漫性阳性;少部分肿瘤细胞HCG阳性表达,黑色素瘤细胞黏附分子(Mel-CAM)、胎盘碱性磷酸酶(placental alkaline phosphatase,PLAP)、人胎盘催乳素(hPL)呈局灶阳性表达;Ki-67指数为10%~25%。

A:上皮样滋养细胞(HE);B:EGFR;C:hPL;D:HCG;E:P63;F:Ki-67
1.4治疗4例患者均无生育要求。与患者及家属详细沟通病情后,给予腹腔镜全子宫切除术。手术均由经验丰富的医师实施,均顺利完成。4例患者术后均恢复良好,术后1~2周开始化疗。1例患者首先给予MTX单药化疗,肌内注射MTX 0.4 mg/(kg·d),连续5 d, 2个疗程;血β-HCG下降不理想,改为EMA-CO方案化疗2个疗程,血HCG降至正常,继续巩固1个疗程,共3个疗程。余3例术后均采用EMA-CO方案化疗3~5个疗程。EMA-CO联合方案:第1天, VP16静脉注射100 mg/m2,Act-D静脉注射0.5 mg,MTX静脉注射100 mg/m2,MTX静脉滴注200 mg/m2持续12 h;第2天, VP16静脉滴注100 mg/m2,Act-D静脉注射0.5 mg;第2天, 四氢叶酸(CF)静脉注射15 mg,从静脉注射MTX开始24 h后给药,每12 h 1次,共2次;第4~7天无用药;第8天,VCR静脉注射1.0 mg/m2, CTX静脉注射600 mg/m2。
1.5随访出院后3个月第1次随访,以后每6个月随访1次,3 a后每年随访1次直至终生。随访内容有询问病史(包括腹痛、咳嗽、咯血等症状),妇科检查,血β-HCG检测,必要时行盆腔超声、X线胸片或CT检查。4例均无复发,无死亡。
2 讨论
ETT由Shih等[5]于1998年首次报道并命名,2003 年WHO将 ETT列入女性生殖系统肿瘤分类之中。ETT多见于育龄期女性,Keser等[6]报道ETT发病年龄为15~48岁(平均36.1岁),通常在妊娠后1~18 a(平均 6.2 a)发病。本组4例发病年龄32~46岁,距前次妊娠时间8~118个月。有文献[7]报道,ETT患者中继发于足月妊娠、自然流产、葡萄胎的比例分别为67%、16%、16%,Shen等[8]报道转移率为25%;本组4例符合上述特点。ETT患者主要临床表现为异常阴道出血;当出现转移后会出现相应的临床症状,如下腹疼痛等,同时伴有β-HCG轻度升高,与胎盘部位滋养细胞肿瘤(placental sitetrophoblastic tumor,PSTT)表现相似,但远不及绒毛膜癌(choriocarcinoma,CC)患者的β-HCG水平高。有文献[9]报道初次就诊时约69%的患者β-HCG小于2 500 IU/L,本组血β-HCG值为188.6~3 320.8 IU/L。从上述分析可以看出,ETT缺乏特异性临床表现,诊断比较困难,容易误诊为不全流产、CC、PSTT等。因此,应尽早通过诊刮或宫腔镜检查取材进行病理检查。
ETT是由绒毛膜型中间滋养叶细胞构成,肿瘤呈膨胀式生长,呈“地图状”或“岛屿状”排列,肿瘤细胞围绕血管壁,一般不侵犯血管壁;上皮性标志物AE(1、3、7和18)、E-cadherin、EGFR、EMA和CD10等均呈弥漫性阳性表达,滋养细胞标志物HCG、hPL、PLAP、Mel-CAM、P63等呈局灶性阳性表达,HLA-G呈强阳性表达,Ki-67指数为10%~25%。CC显微镜下可见滋养叶细胞、中间型滋养叶细胞和合体滋养叶细胞排列成巢状或条索状,肿瘤细胞异型性明显,核分裂相明显,肿瘤内无间质和血管,伴有明显出血、坏死;HCG呈强阳性表达,P63 和hPL则呈阴性表达[10],Ki-67指数大于50%[11]。PSTT显微镜下可见由形态单一的胎盘中间滋养叶细胞组成,肿瘤细胞体积较大,呈浸润性生长,呈条索状、片状或岛屿状排列,多向肌壁间浸润性生长,常侵犯血管壁;HCG 呈阳性表达, h PL呈弥漫阳性表达,P63阴性[12],Ki-67指数相对较低(15%~25%)[11]。
ETT是类似于PSTT的低度恶性肿瘤,发病率较低,生长缓慢,但很多病例具有较强的侵袭性及致命性的临床表现。目前人们对其发病机制及生物学行为了解较少,仍缺乏统一规范的诊疗方案。通常采用手术为主、化疗为辅的治疗措施。对于解剖分期Ⅰ期、年轻有生育要求者,可行刮宫或局部病灶剔除术,保留子宫;若无生育要求,可行全子宫切除术,目前不常规考虑切除卵巢,不常规进行淋巴结清扫。对于Ⅱ~Ⅳ期患者,需给予全子宫切除及盆腹腔可疑病灶切除,是否有必要行盆腔淋巴结清扫仍有争议。化疗在ETT治疗中的价值尚不确定,ETT化疗指征也不明确,但对有高危因素的患者化疗是必要的。有研究[13]认为,发病时间距末次妊娠时间大于2 a,浸润深度,坏死组织占肿瘤比例,高倍镜下核分裂象大于6/10 等为 ETT 的高危因素等。目前尚无统一化疗方案,有文献[14]报道的联合化疗方案有EMA-CO、EMA-EP及FAEV等。谢辛等[4]认为术后HCG正常后,低危患者至少巩固化疗1个疗程,通常共2~3个疗程;高危患者继续化疗3个疗程,其中第一疗程必须为联合化疗。本组3例术后采用EMA-CO联合方案,1例MTX单药化疗失败后改EMA-CO方案,均治愈,提示EMA-CO联合方案在ETT治疗方面有一定优势。也有研究者[15]认为,手术联合术后化疗与单独手术相比,并不能使患者获益。对于ETT术后化疗与否、化疗的指征、化疗方案的选择,以及化疗效果的评价均有待进一步总结。
