甲醇合成反应过程的模拟与优化
2019-03-22张秋利李凤英
张秋利,罗 敏,李凤英
(1.西安建筑科技大学冶金工程学院,陕西 西安,710055;2.陕西省冶金工程技术研究中心,陕西 西安,710055)
甲醇是一种重要的有机化工基础原料和优质清洁能源,可用于合成燃料、烯烃、汽油、二甲醚、聚甲氧基二甲醚等众多化学品[1]。近年来,我国煤制甲醇行业发展迅速,并将煤化工、石油化工和天然气化工等结合起来,促进了产品的优质化和多元化,缓解了我国石油资源不足的问题,促进了能源的高效、清洁、低碳利用[2]。全球的甲醇需求迅速增长,而且中国也已成为世界上重要的甲醇生产和消费大国,甲醇行业在国民经济中所占的比重也越来越大[3,4]。因此,甲醇生产规模的扩大和市场竞争的加剧,客观上对甲醇生产技术进步提出更高要求,其生产过程中每个环节的改进,尤其是在工艺节能、优化方面都会产生很大的经济效益。
工业甲醇的生产过程由三个基本步骤组成:合成气制备、合成气转化、粗甲醇精馏。其中,合成气的主要成分是H2、CO和CO2,在理想条件下生产甲醇的合成气应满足n(H2-CO2)/n(CO+CO2)=2,而实际的甲醇工业中最佳值略大于2。按合成压力不同,甲醇的生产方法主要分为:高压合成法和低压合成法。本文选取低压法进行甲醇合成模拟,催化剂为广泛应用的铜基催化剂。Graaf等[5]对铜基催化剂的甲醇合成反应的本征动力学进行探索,提出了Langmuir-Hinshelwood-Hougen-Watson(L-H-H-W)型动力学方程。在Graaf的研究基础上,李建伟等[6]采用传统方法建立了C302催化剂上的甲醇合成反应的速率模型,并通过实验测量C302催化剂上的甲醇合成反应的动力学数据,得到了六种模型的参数估值,然后利用F统计量、复相关指数和反应器出口处CO和CO2浓度模型的预测值与实测值的相对偏差相结合的方式,严格地对六种动力学模型的适定性进行检验。在工业应用中,蒋小川等[7]对C302催化剂上的六种具备不同结构的合成反应动力学模型进行了实际应用的验证,得出结论:在六种模型中有三种C302催化剂上的甲醇合成的动力学模型与实际工业应用是比较吻合的。陈鹏等[8]基于LH-H-W模型在压力为5MPa、温度为185~225℃、不同的原料气组成的条件下,实验测得选用C306催化剂进行甲醇合成的合成反应的动力学数据,经计算得出结论:在低温段185~215℃范围内,C306催化剂上的合成反应速率比C302催化剂的速率要大,温度高于213℃,则C302催化剂优于C306催化剂。马宏方等[9]基于L-H-H-W动力学模型通过实验和计算,得到了催化剂为C307时甲醇合成反应的本征动力学模型。
目前工业生产中普遍采用C302催化剂,其动力学模型有了较多的研究,但是基于动力学的模型,其合成过程的具体工艺参数需要进一步优化。因此本文选择C302为催化剂,进行甲醇低压合成的工艺流程模拟,并分析温度、压力、分流比和催化剂填充密度对甲醇合成反应的影响,为工业制甲醇生产工艺的设计与优化奠定理论基础。
1 甲醇合成反应及动力学方程
合成甲醇的原料有很多,主要有煤、天然气、焦炉煤气、沼气等[10]。其中焦炉煤气是焦炭生产过程的副产品挥发性物质,它富含 H2、CH4、CO、CO2和 N2,以及小分子碳氢化合物[11]。以焦炉煤气为原料制取甲醇的工艺过程具有能耗低、污染小、投资成本低、原料成本低、市场竞争力强、抗风险能力强等优点。同时,高效清洁利用焦炉煤气可缓解国内能源短缺的问题,并可减少环境污染[12]。Li等[13]分别对焦炉煤气、煤炭和天然气三种原料制甲醇的路线进行了经济分析和比较,发现焦炉煤气路线受环境的影响要比煤低,且焦炉煤气路线的生产成本也低于煤炭和天然气路线。本文选用焦炉煤气为原料制甲醇,其生产流程[14]分为四个阶段:预处理(加压至2.5MPa);净化(精脱硫工段,总硫体积分数脱至0.1×10-6以下);CH4转化(氧化为CO和H2,氢碳比符合基本要求);合成甲醇(得到粗甲醇);精馏(制取贮存精甲醇)。
甲醇合成过程发生的主要反应如下:
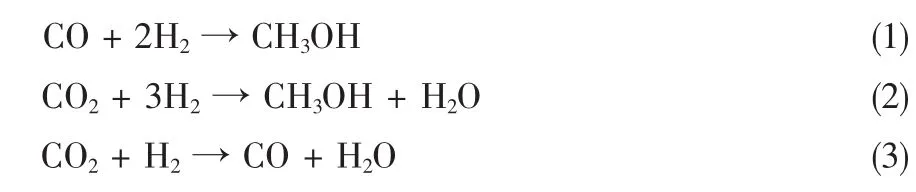
以上反应中主反应有3个,但其中只有2个为独立的化学反应,本设计选用反应(1)和(2)为独立化学反应。在低压条件下,采用C302铜基催化剂对CO和CO2加氢生产甲醇的反应(1)和(2)的过程动力学符合LHHW型双速率本征动力学模型,其动力学方程如式(4)和(5)。
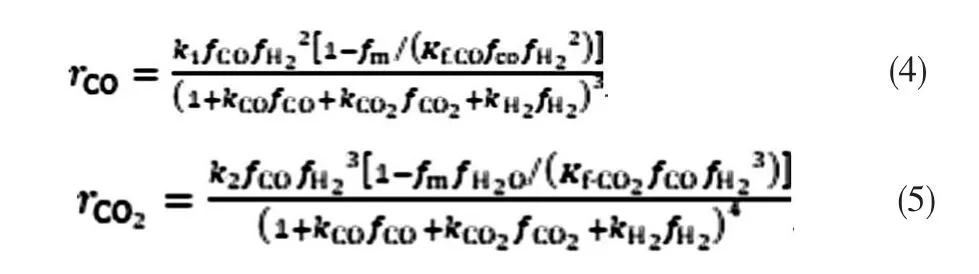
式中:rCO-CO的反应速率;rCO2-CO2的反应速率;ki-反应速率常数;fi-组分i的逸度,由SHBWR状态方程计算,MPa;Ki-组分 i的吸附平衡常数;Kf1,Kf2-分别是反应1和反应2以逸度表示的平衡常数。
各参数值为:
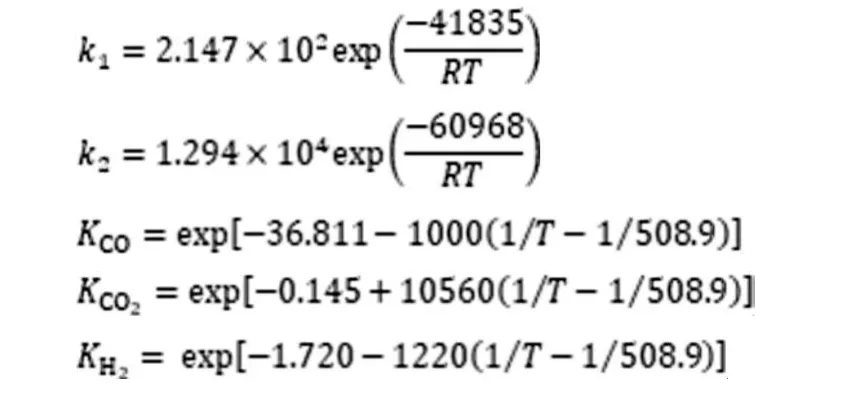
式中:R-理想气体常数,8.314J/(mol·K);T-温度,K。
该甲醇合成的双速率方程是在 5MPa,215~260℃的工业生产条件下,选择C302催化剂进行甲醇合成实验而得到的,并成功用于大型甲醇合成反应器的模拟设计[15]。因此本文对甲醇合成的过程的模拟使用该速率方程。
2 甲醇合成的模拟
结合焦炉煤气制甲醇的生产工艺,进行甲醇合成反应过程的模拟,其流程图如图1所示。来自转化工段的转化气1进入压缩机C1001与循环气混合加压至5.0MPa,再经预热器E1001预热至200℃后进入合成反应器R1001发生反应。从合成塔出来的气体4经冷却器E1002降温至40℃,然后送入闪蒸罐V1001,将未反应的合成气分离出来,气体7经分流器分流一部分气体8至压缩机,循环回合成系统。闪蒸罐V1001分离出来的粗甲醇6送去精馏工段。其中,反应器R1001选择的是平推流反应器,其管长为12.2m、管径为0.0375m;闪蒸罐V1001塔顶部分气体循环回压缩机,压缩后进入甲醇合成塔,因此在此处设置一个分流器控制循环气量,经8号线回流至压缩机。其中8号线中返回的气体所占7号线气体的比例即为分流比。各个模块的结构参数与工艺操作参数的具体设定如表1所示。转化气流量取3000m3/h,其组成如表2所示。
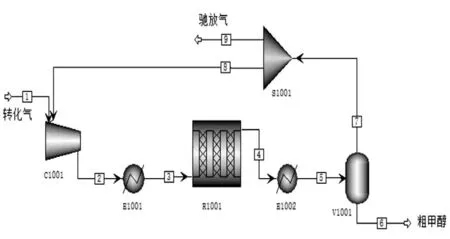
图1 甲醇合成模拟流程图

表1 各模块的结构参数与工艺操作参数
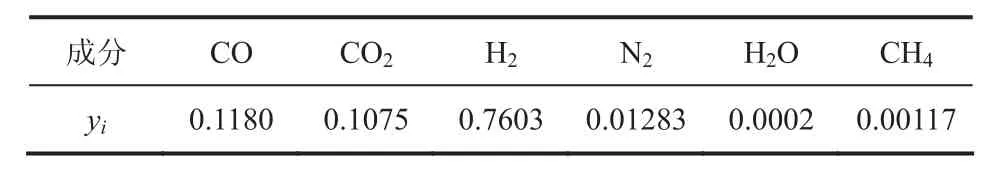
表2 转化气的主要成分
经模拟计算得到的反应器出塔气体成分与粗甲醇成分如表3所示,反应器内沿物料流动方向上的温度与热分布如图2所示,反应器内不同位置的物质组成如图3所示。
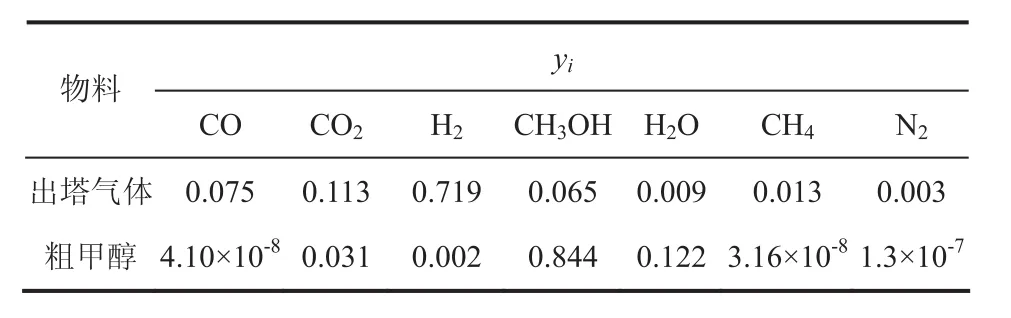
表3 反应器出塔气体与粗甲醇成分
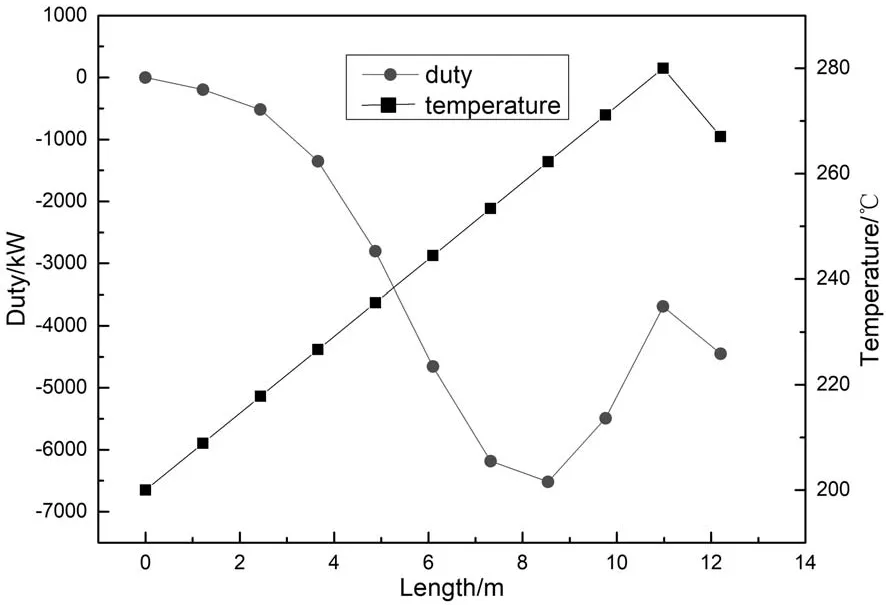
图2 反应器内不同位置的热分布
由图2可知,反应器内不同位置的温度明显不同,由于甲醇合成反应是放热反应,不同位置的反应程度不同,热负荷的总体变化趋势为先下降后上升。图中在8.6m处的温度为256℃,此处放出热量最大,为-6519.07085kW,说明此处的反应最剧烈。
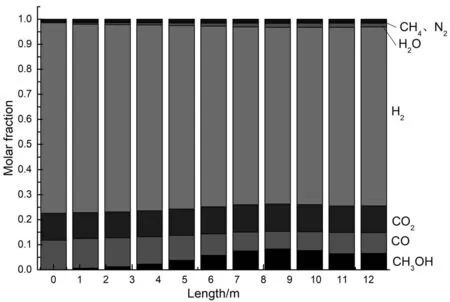
图3 反应器内不同位置的物质组成
从图3中可以看出,CH3OH含量明显增加,CO、CO2、H2含量减少,H2O 也有小幅度的增加,CH4和N2含量不变。
选取参考文献[6]的几组值对本文甲醇合成反应动力学模拟的结果进行验证。模拟条件与文献条件一致,条件如表4所示,反应器出口H2、CO和CO2的物质的量分数模拟值与文献值的对比见表5。
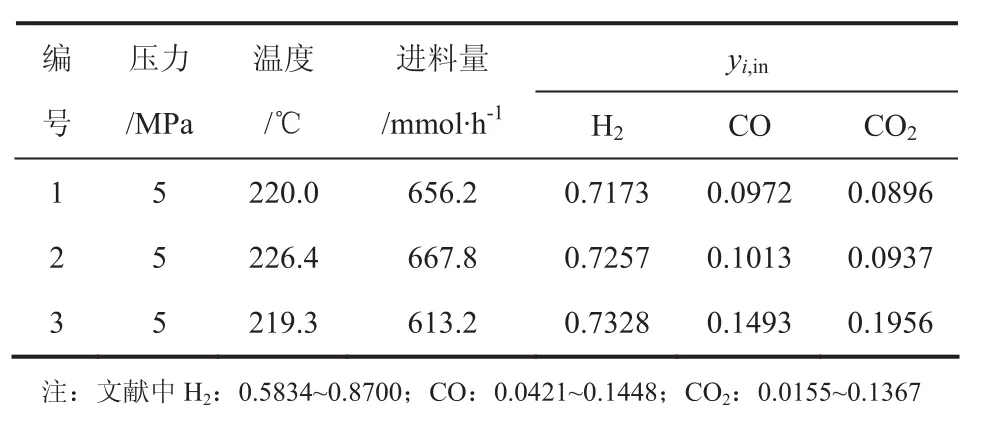
表4 模拟条件
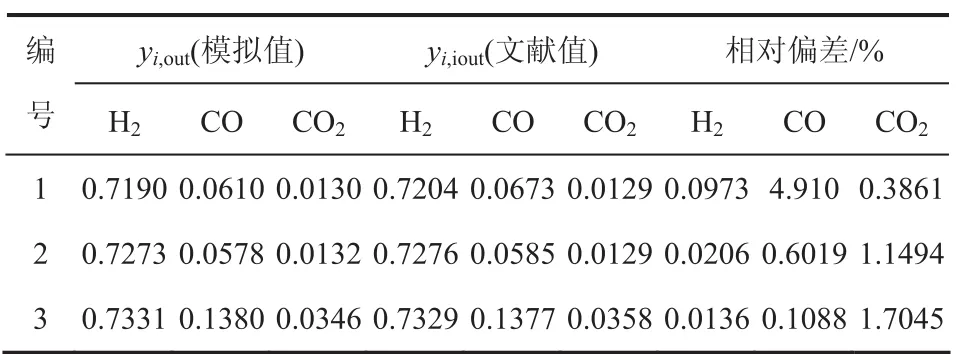
表5 模拟值与文献值的对比
由表5可知,三组模拟结果中H2、CO和CO2的物质的量分数与文献值相对偏差较小,所以本文设计的甲醇合成模拟过程是可行的。
3 甲醇合成过程的优化
在甲醇合成过程中,反应温度、压力、分流比等操作参数是影响甲醇产率的重要因素,为了提高甲醇产率,得到较优的工艺操作条件,本文采用灵敏度分析法进行了参数优化研究。灵敏度分析法是研究分析系统输出对系统参数变化的敏感程度的方法。
3.1 反应温度和压力的影响
在分流比、催化剂填充密度不变的条件下,改变反应压力和反应温度时,出塔气中甲醇的物质的量分数变化曲线见图4。
从图4中可以看出,当甲醇合成反应的压力越高时,甲醇的含量越大。从甲醇合成反应的化学方程式中可以看出合成甲醇是体积减小的反应,也就是说,压力越高对甲醇合成反应的进行越有利。反应温度在200~250℃之间时,甲醇含量随温度升高而增大,在250℃之后,甲醇含量随温度升高而减少。
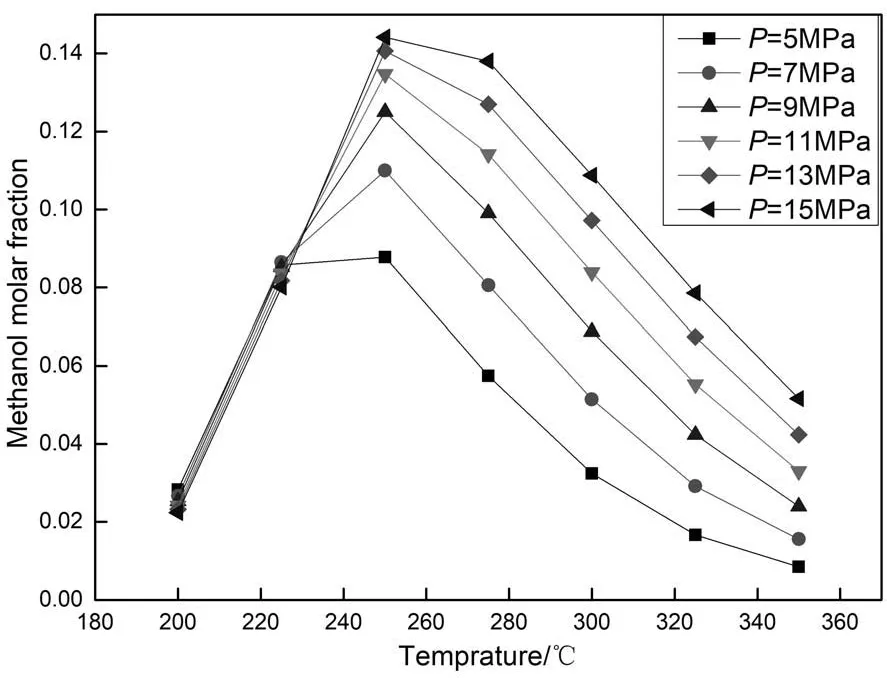
图4 反应温度和压力对出塔气甲醇含量的影响
CO和CO2的反应速率常数分别为:
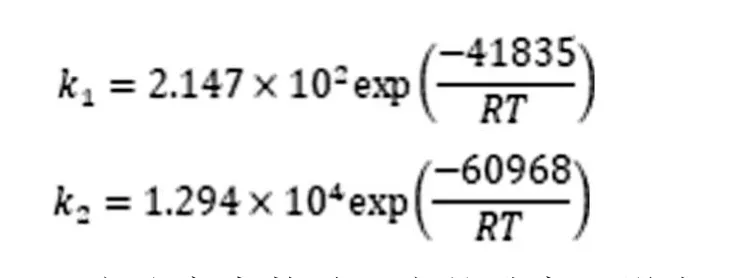
反应速率常数随温度的升高而增大,但是甲醇合成反应是放热反应,反应的平衡常数随着温度的升高而减小。当温度低于250℃时,反应速率常数的增大对反应影响较大,所以甲醇产量随温度升高而增大;温度高于250℃时,反应的平衡常数的减小对反应影响较大,所以甲醇产量随温度升高而减少。因此甲醇合成的最佳反应温度为250℃。
3.2 分流比的影响
为了提高原料气利用率和降低废气排放,反应器排出的气体经闪蒸罐分离出甲醇后,将剩下的气体其中的一部分循环至压缩机,与新鲜转化气进行混合并加压预热后,进入反应塔合成甲醇。但是由于循环气中含有大量的CO、CO2和H2,少量的N2、H2O、CH4和微量的CH3OH, 其中 CO、CO2和 H2这三种气体是甲醇合成反应的反应物,其循环会改变反应物的流量,影响合成反应,循环气体量由分流比控制,分流比对甲醇流量及含量的影响曲线如图5所示。
从图5中可以看出,甲醇含量随分流比的增大而减小,甲醇总流量随着分流比的增大而增加。结合图6可知,当分流比小于0.6时,随着分流比增加,CO含量逐渐减少,H2含量逐渐增加,CO2含量基本不变。当分流比在0.6之后继续增加时,CO2含量开始减少,分流比增加到0.7时,CO2含量的减少愈加明显,CO2是合成甲醇的重要气体,因此,分流比可在0.6~0.7之间选择。图6中,CO和H2的变化曲线有一个交点,交点处的分流比为0.68,此处n(H2-CO2)/n(CO+CO2)=2.2,符合合成气的条件,所以选择0.68为最佳分流比。
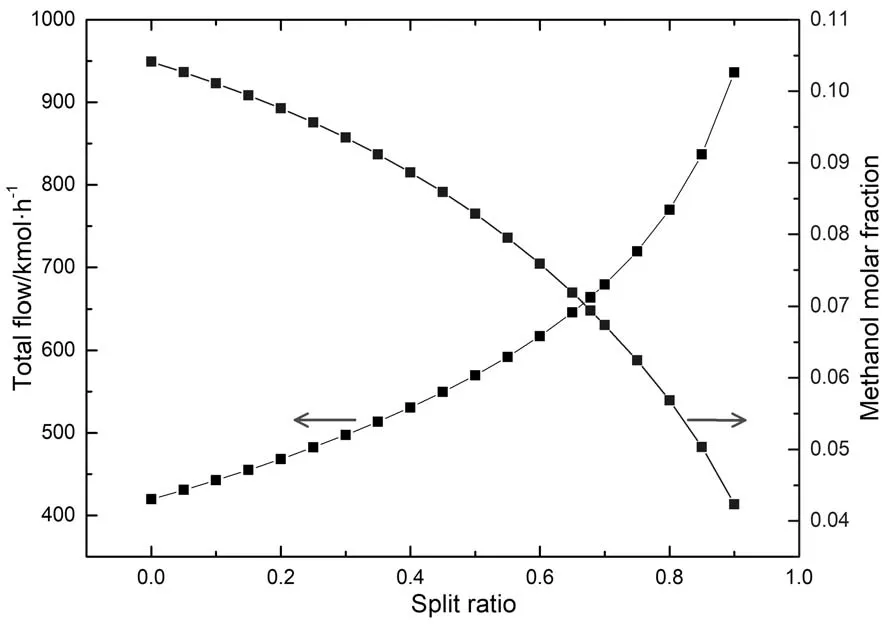
图5 分流比对甲醇总流量和甲醇含量的影响
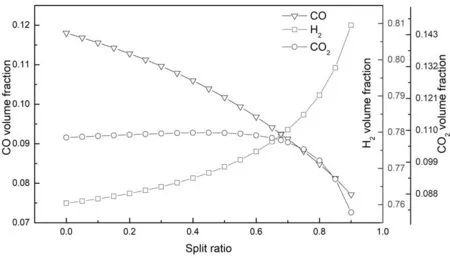
图 6 分流比对合成气中的CO、CO2和H2体积分数的影响
3.3 催化剂填充量的影响
催化剂是甲醇合成反应的载体,催化剂填充密度直接影响了反应气体与其的接触面积,因此填充密度对反应过程有很大影响,模拟得出催化剂填充密度对甲醇流量影响结果如图7所示。
从图7中看出,催化剂填充密度在800~1400kg/m3时,甲醇流量随填充密度的增大而增加,这是因为随着填充密度的增大,合成气的接触面积增大,分子相互碰撞发生反应的几率增大,所以产生的甲醇越多;当催化剂填充密度达到1400kg/m3之后再继续增大时,甲醇产量几乎没有明显变化,这是因为继续增大密度使比表面积减小、空隙减小、压力降增大,合成气较难通过床层,同时合成气的接触面积减小,导致甲醇流量减小。因此,甲醇合成反应催化剂的最佳填充密度为1400kg/m3。
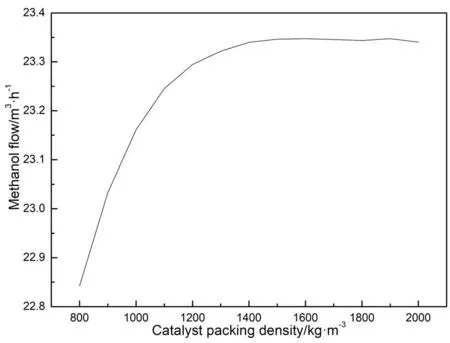
图7 催化剂填充密度对流量的影响
图8表示,当反应器结构参数不变的情况下,在压力为5.0MPa、温度为250℃、分流比为0.68、催化剂填充密度为1400kg/m3的操作条件下,该反应器的甲醇年产量和产率随焦炉煤气流量的变化趋势。从图中可以看到,当焦炉煤气的进料流量从2000m3/h增加到5500m3/h时,甲醇年产量随之增加,甲醇产率呈现阶梯递减。焦炉煤气流量为2100m3/h时,年产为15万t,出口气甲醇的物质的量分数(即甲醇产率)为0.078;流量为2800m3/h时,年产为20万t,甲醇产率为0.077;流量为3500m3/h时,年产为25万t,甲醇产率为0.075;流量为4300m3/h时,年产为30万t,甲醇产率为0.073;流量为5100m3/h时,年产为35万t,甲醇产率为0.070。
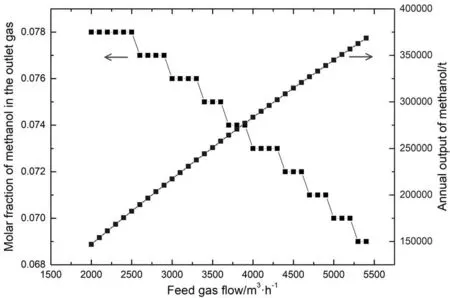
图8 甲醇年产量和产率与进料量的关系
4 结论
本文采用LHHW动力学模型,以焦炉煤气为原料,建立了甲醇合成反应过程的模拟流程,采用C302铜基催化剂,在反应温度为220℃、反应压力为5.0MPa、焦炉煤气流量为3000m3/h时,模拟研究得出反应器内热负荷分布、组成分布与甲醇产率,模拟结果与文献相符。采用灵敏度分析法进行优化研究,得出较优工艺操作参数为:反应温度为250℃、分流比为0.68、催化剂填充密度为1400kg/m3。
