中重度OSAHS患者日间过度嗜睡的影响因素研究
2019-01-23邵川董肖琦陈益女张亮屠金晶余碧芸汤耀东
邵川 董肖琦 陈益女 张亮 屠金晶 余碧芸 汤耀东
阻塞性睡眠呼吸暂停低通气综合征(obstructive sleep apnea hypopnea syndrome,OSAHS)以夜间反复出现上呼吸道阻塞/塌陷、慢性间歇低氧和睡眠片段化为特征[1]。日间过度嗜睡(excessive daytime sleepiness,EDS)是中重度OSAHS患者的常见症状,是引发交通事故、职业事故的重要原因[2-3],也与患者认知障碍有关[4]。因此EDS严重影响患者的生活质量,甚至生命健康[5-6]。然而临床上并非每例中重度OSAHS患者均有EDS,导致EDS的具体机制目前尚未阐明。先前有研究提示,OSAHS患者的EDS可能与睡眠结构紊乱相关[7],也有研究提示EDS可能与夜间低氧相关[8]。本研究根据ESS评分将中重度OSASH患者分为有EDS组和无EDS组,通过比较两组患者夜间低氧和睡眠结构相关参数的差异,分析中重度OSASH患者EDS的可能影响因素,现报道如下。
1 对象和方法
1.1 对象 选择2016年1月至2017年6月本院呼吸科经整夜多导睡眠监测(polysomnography,PSG)诊断的男性中重度 OSAHS成年患者272例,年龄24~81(44.94±10.85)岁。OSAHS的诊断和严重程度分级依据美国睡眠医学会(American association of sleep medicine,AASM)标准[9],以呼吸暂停低通气指数(apnea-hypopnea index,AHI)≥15和≥30且以阻塞性事件为主分别诊断为中度和重度OSAHS。排除标准:(1)之前接受过 OSAHS诊治的患者;(2)合并肥胖低通气综合征、慢性阻塞性肺病、充血性心力衰竭等疾病;(3)有精神疾病或长期服用镇静催眠药物者;(4)习惯性吸烟或饮酒者;(5)其他情况:如行分夜PSG监测的患者、PSG监测时间不足7h和资料不齐全者等。
1.2 方法
1.2.1 临床资料采集 记录患者的基本信息,包括性别、年龄、身高、体重、入睡前脉搏氧饱和度(SpO2)和相关病史,如合并症和既往史等。根据身高、体重计算BMI。患者在睡眠医师指导下独立填写Epworth嗜睡量表(epworth sleepiness scale,ESS)[10],ESS>10 分认为存在EDS。
1.2.2 多导睡眠图的判读 整夜多导睡眠图的判读依据AASM评分手册[11]。睡眠效率=总睡眠时间(total sleep time,TST)/卧床时间(time in bed,TIB)×100%,每一睡眠分期所占的比例,即N1期、N2期、N3期和REM期,分别用该期睡眠时间占TST的百分比表示。氧减饱和指数(oxygen desaturation index,ODI)为平均每小时睡眠时间出现SpO2下降≥3%的次数。此外PSG参数还包括夜间最低SpO2、平均SpO2、氧饱和度低于90%的时间占睡眠时间的百分比(saturation impair time below 90%,SIT90)。
1.3 统计学处理 采用SPSS 22.0统计软件,计量资料用表示,组间比较采用Mann-Whitney U检验;采用logistic回归进行多因素分析。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者基本资料比较 ESS>10分(ESS组)95例,ESS≤10分(无ESS组)177例。两组患者年龄、BMI、AHI、清醒 SpO2比较、差异均无统计学意义(均P>.05),见表 1。

表1 两组患者基本资料比较
2.2 两组患者夜间低氧情况比较 见表2。
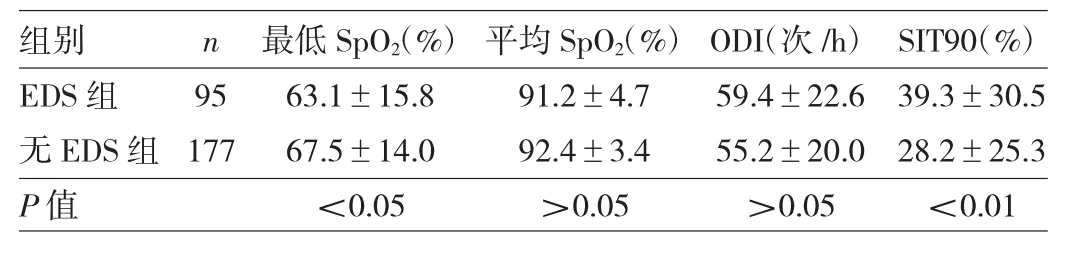
表2 两组患者夜间低氧情况比较
由表2可见,EDS组最低SpO2低于无EDS组(P<0.05),SIT90 高于无 EDS 组(P<0.01);两组平均 SpO2、ODI差异均无统计学意义(均P>0.05)。
2.3 两组患者睡眠结构比较 见表3。
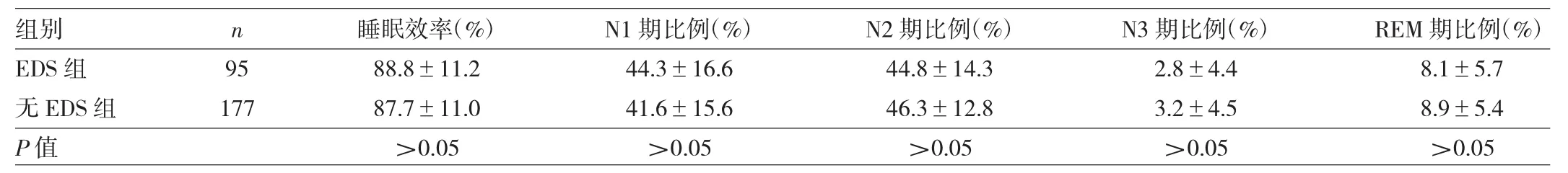
表3 两组患者睡眠结构比较
由表3可见,两组患者的睡眠效率、N1期、N2期、N3期和REM期比例比较,差异均无统计学意义(均P>0.05)。
2.4 影响EDS的多因素分析 见表4。
由表4可见,SIT90是EDS的独立影响因素(P<0.05)。
3 讨论
虽然EDS是中重度OSAHS患者的常见临床表现,但并非每例中重度OSAHS患者都有EDS。关于OSAHS患者EDS的机制目前尚未阐明,之前已有一些研究提示EDS可能与睡眠结构紊乱或夜间低氧有关,但也有研究对这两种观点提出异议[7-8,12]。另外有研究认为夜间低氧和睡眠片段化均为EDS的独立影响因素[13]。为了进一步研究EDS的可能影响因素,笔者根据ESS评分将中重度OSAHS患者分为EDS组和无EDS组,从睡眠结构和夜间低氧两方面比较两组患者的差异,探讨引起EDS的可能原因。本研究对研究对象进行了严格筛选,入选不合并严重心肺疾病和神经、精神疾病的中重度OSAHS患者,考虑到睡眠结构存在性别差异,本研究只入选男性患者,从而避免了性别这个混杂因素。此外两组均有较大的样本量,避免了年龄和AHI的干扰。
本研究发现EDS者夜间最低SpO2较无EDS者更低,且SpO2低于90%的时间更长,多因素回归分析结果显示SIT90可能是EDS的一个影响因素,而夜间最低SpO2差异无统计学意义,可能与夜间最低SpO2同时受到其他多种因素的影响有关。SIT90是评估患者夜间低氧情况的一个客观指标。基于此研究,笔者认为夜间低氧是EDS的重要因素。之前Mediano等[8]的研究发现EDS者夜间最低SpO2、平均 SpO2较无EDS的患者更低,他认为夜间低氧是EDS的重要决定因素,这与本研究结果相似,同时研究发现EDS者睡眠效率更高,而本研究为差异无统计学意义,笔者认为这可能与入选患者的疾病严重程度以及种族不同有关,正如Mediano的研究显示,重度OSAHS患者有较高的睡眠效率,可能是日间嗜睡的结果而不是原因,因为具有严重日间嗜睡的患者一整天都是嗜睡的,包括日间和夜间。
中重度OSAHS患者EDS可能与夜间长期间歇低氧导致神经损伤有关,已有动物研究发现慢性间歇低氧导致与睡眠/觉醒调节相关的神经元细胞丧失,同时还能诱导一氧化氮合酶的产生,后者介导促进觉醒的大脑区域的氧化应激和炎症损伤以及促进睡眠的大脑区域的激活,进而可能导致嗜睡[14]。夜间低氧程度是临床上判断OSAHS病情严重程度的一个重要指标,基于本研究结果和上述提及的动物研究结果,笔者推测夜间低氧是导致EDS的一个重要因素,且EDS可能主要与病情严重程度和病程长短有关。此外,遗传易感性也是一个影响因素[8],但在OSAHS患者中是否有与动物模型类似的生物学机制及相关信号通路可以解释夜间低氧与EDS的关系,目前尚不清楚,需要今后进一步研究探索。
