尿素微胶囊缓/控释肥料制备工艺研究*
2018-11-15杨艳艳韩月云汤建伟化全县
杨艳艳,韩月云,汤建伟,化全县,刘 丽,刘 咏
(郑州大学化工与能源学院,国家钙镁磷复合肥技术研究推广中心,河南郑州450001)
在中国农业生产中,尿素对提高作物产量和产品质量发挥着关键作用。但是尿素易溶于水,施用于土壤后40%~60%的尿素随水土流失,不仅利用率低,也不利于环境保护[1-6]。采用缓控释技术可以有效解决这类问题[7]。传统缓释肥是通过物理方法将聚烯烃、热塑性树脂以及聚氨酯等有机高分子包裹颗粒尿素表面,但此类包膜材料价格较高,难降解,进而对土壤造成危害。壳聚糖(Chitosan,CS)是一种来源广泛的天然生物可降解聚合物,以其廉价性、无毒性和生物可降解性引起研究者的广泛关注[8]。其分子内具有化学性质活泼的氨基与羟基,可以在温和的反应条件下改变其化学性质[9]。因此,壳聚糖可以作为理想的天然缓释载体广泛用于生物医学、制药及农业领域[10-11]。 A.Rattanamanee 等[12]在蚕丝蛋白/明胶水凝胶中添加壳聚糖,通过溶剂挥发法制备缓释尿素。L.Wu等[13]以四氯化碳和丙酮为溶剂,通过转筒造粒法制备了双层包膜尿素颗粒缓释肥,其中壳聚糖为内层,聚丙烯酸高吸水性树脂为外层。这些研究大部分采用物理方法将壳聚糖包裹尿素,难以达到控释效果,且生产成本高。与传统缓释肥料制备方法相比较,采用微胶囊技术制备缓释肥在降低成本、调控养分释放速率方面有很大优势[14-15]。鉴于上述原因,本研究初步探讨采用天然高分子聚合物CS为尿素载体,通过反相乳化-化学交联法制备了尿素微胶囊缓释肥。实验还分别考察了CS浓度、尿素用量、戊二醛用量、乳化剂用量、反应温度以及搅拌速度对制备微胶囊的形态、载肥量以及包封率的影响。通过FT-IR和SEM表征其结构,并探究尿素微胶囊的缓释性能。
1 实验部分
1.1 试剂与仪器
试剂:壳聚糖、对二甲氨基苯甲醛尿素,国药集团化学试剂有限公司提供;异丙醇、戊二醛、液体石蜡、Span-80、冰乙酸、石油醚,均为分析纯,天津市科密欧化学试剂有限公司提供。
仪器:F25-ED型加热制冷循环器、DT1000A型多管架自动平衡离心机、KQ-500DE型数控超声波清洗器、TU-1901型双光束紫外可见分光光度计。
1.2 实验方法
通过反相乳化-化学交联法制备尿素/CS缓释微胶囊。将1 g CS加入体积分数为1%的醋酸水溶液中,60℃下搅拌溶解,静置12 h后,称取一定质量的尿素加入到已配制好的CS溶液中作为水相溶液待用。按照体积比3:1配制石蜡与石油醚混合溶液作为油相待用。将水相分散到油相中,并加入一定量的乳化剂Span-80,使尿素/CS水溶液在油相中形成稳定的W/O体系。以体积分数为50%的戊二醛为交联固化剂,反应3 h后停止并静置一定时间。离心抽滤,回收上层油相。先后分别使用石油醚和异丙醇洗涤,50℃下干燥24 h,得到微胶囊样品。
1.3 结构表征与性能测试
1.3.1 SEM表征
采用JEM-5600LV型扫描电镜对样品做形貌分析。将样品表面喷金处理,实验工作电压为20kV,观察样品的表面结构形态。
1.3.2 FT-IR表征
采用WQL-510型傅立叶变换红外光谱仪对样品做结构分析。以溴化钾压片法制备试样,扫描波长为 400~4 000 cm-1,分辨率为 0.5 cm-1。
1.3.3 载肥量测定
配 制 质 量 浓 度 分 别 为 0.00、0.05、0.10、0.15、0.20、0.25 g/L的尿素标准溶液。加入显色剂对二甲氨基苯甲醛,分别在波段420 nm处用紫外分光仪测定吸光度,并绘制标准曲线[16]。
称取0.2 g微胶囊样品经充分研磨后,样品浸入蒸馏水中至尿素完全释放后过滤。通过紫外分光光度法测定溶液中氮含量。载肥量与包封率按以下公式计算[17]:

式中:ULE为载肥量,%;UCE为包封率,%;m0为加入的尿素总量,g;mC为微胶囊中包封的尿素量,g;mT为微胶囊总质量,g。
1.3.4 微胶囊缓释性能分析
精确称取8份相同质量(0.1 g)的样品,分别置于烧杯中,并分别加入等体积的蒸馏水50mL。在25℃恒温水浴中分别静置不同时间(4、8、12、24、36、48、60、72 h),移取上层清液并测定溶液中的尿素含量。尿素释放率按下式计算:

式中:f为尿素释放率,%;Mt为t时刻尿素释放量,g;M∞为微胶囊中所含尿素总质量,g。
2 结果与讨论
2.1 尿素用量对实验结果的影响
由于尿素用量对载肥量和包封率有着直接影响,本实验分别将不同质量的尿素加入CS溶液中,考察尿素用量对实验结果的影响。称取2 g CS溶于100 mL体积分数为1%的冰醋酸水溶液中,在Span-80和戊二醛体积分数均为3%、转速为900 r/min、反应温度为40℃的条件下制备微胶囊,结果见图1。由图1结果可以看出,在尿素用量为1~6 g时,随着尿素用量的增加,尿素/CS微胶囊的载肥量增加。原因是当体系中尿素含量较低时,CS量过剩;随着尿素量逐渐增加,更多的尿素包埋在CS中,因此载肥量也随之增加。当尿素用量超过6 g并继续增加时,载肥量和包封率逐渐降低。原因是尿素过量造成CS不能完全包裹体系中的尿素,导致形成的微胶囊不完整,载肥量也因此降低。
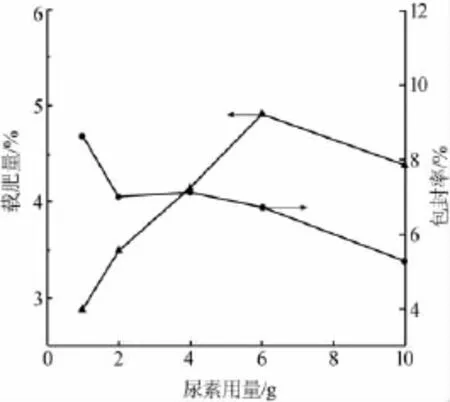
图1 尿素用量对微胶囊载肥量和包封率的影响
2.2 交联剂用量对实验结果的影响
戊二醛含有2个醛基,能在温和条件下与CS分子上的伯氨基和羟基发生反应,在微胶囊内部形成稳定的网络结构。实验分别加入体积分数为1%、2%、3%、4%、5%的戊二醛,其他因素保持不变,考察了交联剂用量对实验结果的影响,结果见图2。由图2可以看出,随着交联剂用量增加,载肥量和包封率相应降低,交联剂达到一定量后,载肥量和包封率变化趋于平缓。原因是交联剂的加入引起微胶囊内部自由体积减少,随交联剂用量增加,交联点之间的分子距离减少,这将进一步降低微胶囊内部的自由体积,使得可以容纳的尿素减少,载肥量和包封率降低[19]。此外在体积分数为2%~3%戊二醛用量的使用范围内,CS的交联点可能达到饱和,此时载肥量和包封率基本保持不变。

图2 戊二醛用量对微胶囊载肥量和包封率的影响
2.3 反应温度对实验结果的影响
反应温度会影响戊二醛和CS分子交联反应程度,进而影响微囊的成型。本实验在加入交联剂后,其他因素保持不变,考察了反应温度分别为30、40、50、60、70℃时对微胶囊载肥量和包封率的影响,结果见图3。由图3可以看出,在30~40℃时,随着温度升高,载肥量和包封率相应降低;当达到一定温度后,载肥量和包封率变化趋于平缓,这与戊二醛用量对载肥量的影响呈现出类似的规律。这是因为当温度升高时,会加剧交联反应的进行,温度越高,交联程度越大;当温度升至一定值时,交联程度达到饱和,此时载肥量变化趋向平缓。

图3 反应温度对微胶囊载肥量和包封率的影响
2.4 搅拌速度对实验结果的影响
实验保持其他因素不变,考察了搅拌速度分别为 600、900、1 200、1 500 r/min 时对微胶囊的载肥量和包封率的影响,结果见图4。由图4可知,随着转速上升,微胶囊的载肥量和包封率都呈现出下降的趋势。其原因是随着搅拌速度提升,液滴均匀分散在油相中,乳化交联后所形成的微胶囊粒径也越来越小,使得微囊比表面积增大,囊壁变薄。此时的微囊在高剪切力作用下易破碎,造成包封率下降;同时如果壁材厚度较小,样品离心抽滤时,胶囊也容易破裂,导致载肥量降低。
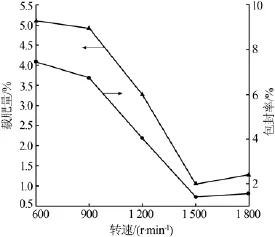
图4 转速对微胶囊载肥量和包封率的影响
2.5 正交试验分析
根据单因素实验的结果,本研究设计了4因素3水平的正交试验,以综合指标即载肥量和包封率的和为筛选指标。正交试验结果见表1。从表1结果可知,影响因素的显著次序由大到小为m(尿素)/m(CS)、反应温度、转速、戊二醛用量。微胶囊的最佳制备条件为 A3B3C1D1,即:m(尿素)/m(CS)=3、戊二醛用量为1.5%(体积分数)、反应温度为30℃、转速为600r/min。实验随后在最佳条件下制备出尿素微胶囊样品,并对其做了FT-IR、SEM结构和形貌表征,以测定微胶囊的缓释性能。

表1 正交试验结果
2.6 FT-IR表征
图5为2.5节最佳条件下制备的尿素微胶囊样品、尿素以及CS原料的红外光谱图。由图5可见,在尿素光谱图中,3 342~3 455 cm-1处有 2个振动峰,应为尿素的特征峰,即N—H键的伸缩振动峰;1 608~1 685 cm-1处的尖锐峰为尿素中C=O双键的伸缩振动特征峰;在微胶囊的光谱图中,3 433 cm-1处的氨基伸缩振动吸收峰变窄效果明显,特征峰强度减弱,将微胶囊光谱图与CS光谱图比较分析,可能是由于交联剂戊二醛的加入,与CS交联后形成Schiff碱的特征峰[20],削弱了 CS 在 1 651 cm-1处的酰胺峰强度,同时在1 623 cm-1处的吸收峰为C=N的伸缩振动峰。而微胶囊光谱图中1 072 cm-1处的羟基变形振动吸收峰减弱,由此证明CS分子中的羟基也同样与交联剂中的醛基发生了交联反应。尿素氨基特征峰吸收强度也减弱了。综合比较3种物质的吸收谱图可知,尿素应该被包埋于CS微胶囊之中。

图 5 尿素(a)、微胶囊(b)和壳聚糖(c)红外光谱图
2.7 SEM表征
图6为2.5节最佳条件下制备的微胶囊样品的SEM形貌照片。由图6可见,粒径小于100 μm的微球应为未包裹尿素的空白CS微胶囊,部分微球形状不规则,出现破损。而成球性良好,颗粒表面光滑且粒径分布在100~130 μm之间的微胶囊应为尿素/壳聚糖微胶囊。这是因为CS包裹尿素后相应体积增加,从而导致粒径增加。

图6 CS微胶囊扫描电镜照片
2.8 微胶囊缓释性能分析
将2.5节最佳条件下制备的微胶囊样品进行不同时间下尿素释放性能的测试,检测0~80 h内尿素的释放情况,结果见图7。由图7可知,尿素释放分为3个阶段:初期阶段(0~12 h),微胶囊中的尿素释放比较快,尿素累积释放率急剧增大,12 h之后释放曲线变得平缓,这是由于微囊表层尿素分子快速溶解产生了突释效果;第二阶段(12~48 h),释放速率主要由溶解扩散作用控制,由于微胶囊表面存在大量的孔隙,水分子可以通过它进入微胶囊的内部并溶解,CS吸水溶胀后成为凝胶态,在微胶囊表面形成凝胶保护层,微胶囊壁厚增加,致使大部分尿素截留在凝胶层中,只能通过扩散作用释放出来,所以释放曲线变得平缓;第三阶段(48~72h),CS分子开始降解,微囊结构开始破坏,此时尿素的释放由CS降解作用主导,尿素释放速率增加,直至72h内完全释放。
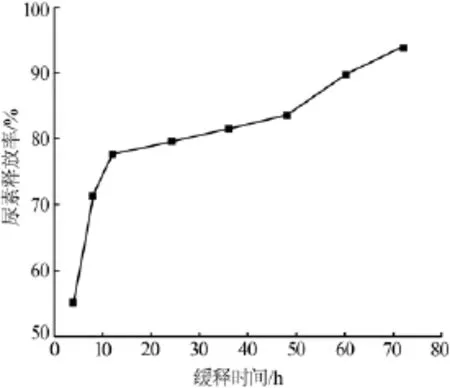
图7 CS微胶囊中尿素释放量随时间的变化曲线
3 总结
1)在制备尿素/CS微胶囊过程中,随着搅拌速度、交联剂戊二醛用量和温度的增加,尿素/CS微胶囊的载肥量呈现下降趋势;而当尿素用量、CS浓度、乳化剂浓度增加时,载肥量和包封率均呈现先增后减趋势。
2)通过单因素结果设计4因素5水平正交试验,得到最优工艺条件:m(尿素)/m(CS)=3、戊二醛用量为1.5%(体积分数)、反应温度为30℃、转速为600 r/min。此条件下制备出的尿素微胶囊成球率高,圆整度好,颗粒表面光滑,粒径分布在100~130 μm之间,载肥量达到11.26%,包封率为15.01%。
3)静水实验表明,尿素呈阶段性释放,且缓释周期可以达到72 h。在缓释肥领域,尿素/CS微胶囊尿素具有潜在的应用价值。
