基于元素周期表中序数规律的巧用
2018-11-08钟舜方
钟舜方
(福建省沙县第一中学 365500)
规律一:元素的周期序数=元素原子的电子层数.通过元素的周期序数可以确定此原子的电子层数,或通过原子的电子层数可以确定此元素的周期序数.
例1 某元素的原子次外层只有两个电子,该元素一定属于( ).
A.第二周期 B.第ⅡA族
C.第三周期 D.第ⅦA族
解析通过次外层可以确定此原子有两个电子层,然后根据周期序数等于元素原子的电子层数可以得出此元素位于第二周期,所以答案为A.
规律二:原子序数的奇数和偶数.
它是指若原子序数为奇数时,主族序数、元素的主要化合价均为奇数;原子序数为偶数时,主族序数、元素的主要化合价均为偶数(除N以外少数元素有多种奇偶价态,较为特殊);零族元素的原子序数均为偶数,元素的化合价可看做为0.
例2 A、B两元素为某周期ⅡA族和ⅢA族元素,若A元素的原子序数为x,则B元素的原子序数可能为( ).
①x+1 ②x+8 ③x+11
④x+18 ⑤x+25 ⑥x+32
A.①③ B.②④ C. ②④⑥ D. ①③⑤
解析由于A位于第ⅡA族元素,所以A元素的原子序数x为偶数;而B位于第ⅢA族元素,所以B元素的原子序数为奇数,不可能为偶数.因此符合要求的只有①③⑤,所以答案为D.
规律三:元素的主族序数=元素原子的最外层电子数=元素的最高化合价=8-∣元素最低负化合价∣.通过其中一个条件就可以确定其它三个量.
例3 某主族元素X的最高价氧化物对应水化物的化学式为H4XO4,它的最高价氧化物的化学式是 ,气态氢化物的化学式是 ,位于第 族.
解析由题可知元素X的最高价含氧酸化学式为H4RO4,再根据正负化合价代数和等于0可以算出元素X的最高化合价为+4,从而分别得出X原子的最外层电子数为4、元素X的最低化合价为-4.所以它的最高价氧化物的化学式是XO2,气态氢化物的化学式是XH4,位于第ⅣA族.
规律四:“T”型、“┻”型关系的序数应用.
在短周期中,直接相邻的“┻”形位置关系的四种元素原子序数关系,如图1;直接相邻的“T”形位置关系的四种元素原子序数关系如图2.
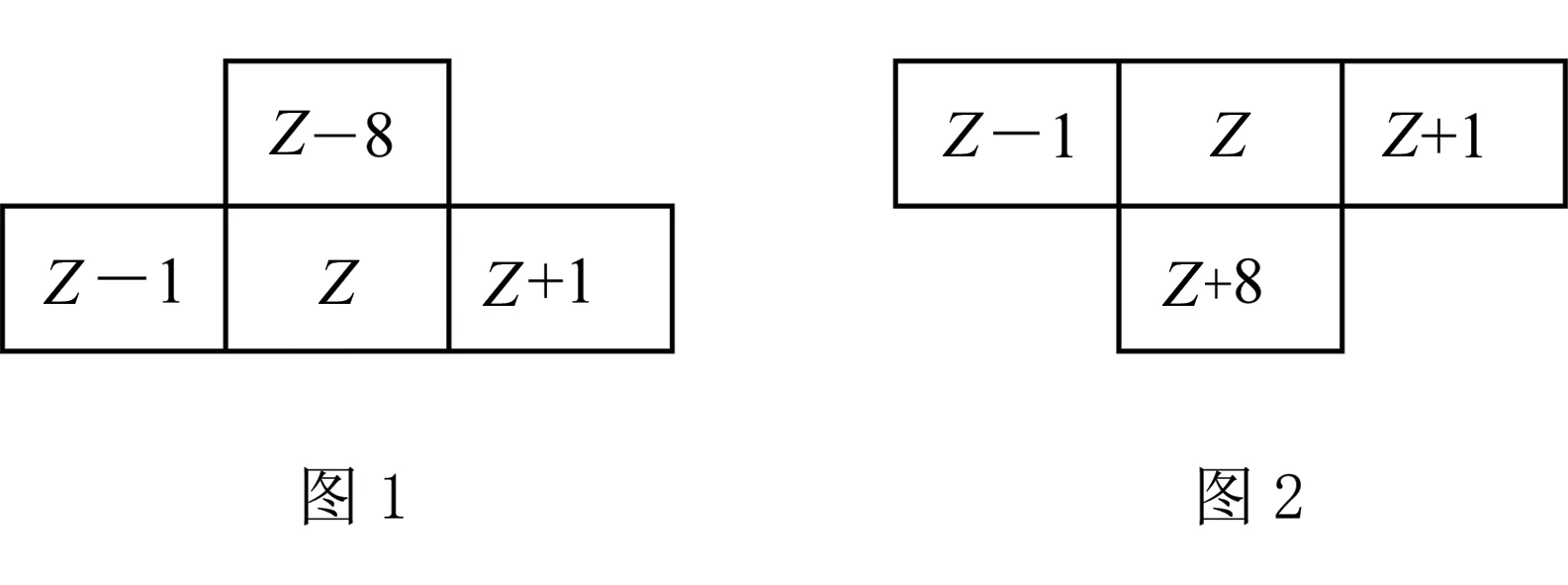
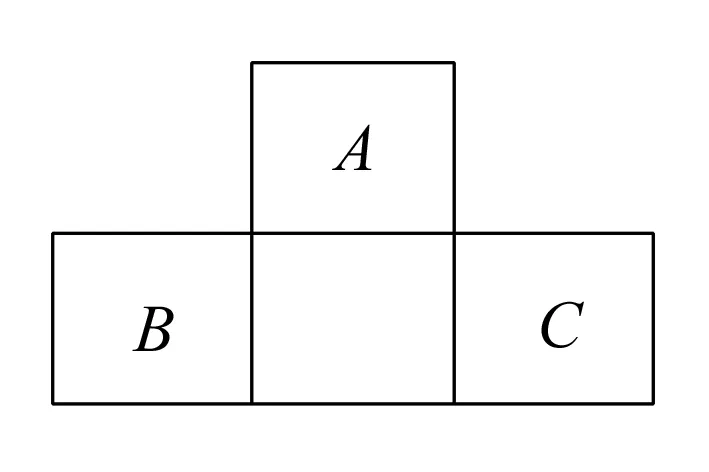
例4 短周期元素A、B、C的位置如图所示,已知B、C两元素所在族序数之和是A元素族序数的2倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C分别是( ).
A.Be、Na、Al B.B、Mg、Si C.O、P、Cl D.C、Al、P
解析这种位置是一种“┻”形关系,所以若B的原子序数为Z,则A和C的原子序数分别为Z-7和Z+2.由题可知:Z+(Z+2)= 4(Z-7)得出Z=15,所以B为P,A为O,C为Cl,因此答案为C.
规律五:同周期主族元素间的原子序数之差值.
在第二周期至第三周期中,其值等于二者间的主族序数之差;在第四周期至第五周期中,其值等于二者间的主族序数之差再加上10;在第六周期至第七周期中,其值等于二者间的主族序数之差再加上24.这是因为第四周期至第七周期里面包括了10个纵行过渡元素,其中第六、七周期的第三纵行中又分别包含了镧系和锕系元素.
例5X、Y同一周期的元素,X位于ⅠA族,Y为ⅣA族元素,它们的原子序数分别是m和n,则m、n的下列关系式不正确的是( ).
A.n=m+3 B.n=m+13
C.n=m+27 D.n=m+10
解析根据规律四可知,在第二周期至第七周期中,同周期内ⅣA族元素的原子序数与ⅠA族元素的原子序数之差分别为3、3、13、13、27、27.所以答案为D.
规律六:主族、0族元素的原子序数与周期内元素种类的关系.
第ⅠA族、ⅡA族下面元素的原子序数等于同主族元素的原子序数加上上面元素所在周期的元素种类.第ⅢA至0族下面元素原子序数,等于同主族元素的原子序数加上下面元素所在周期的元素种类.下面以ⅠA族、0族元素为例说明,其它主族元素同理分析.
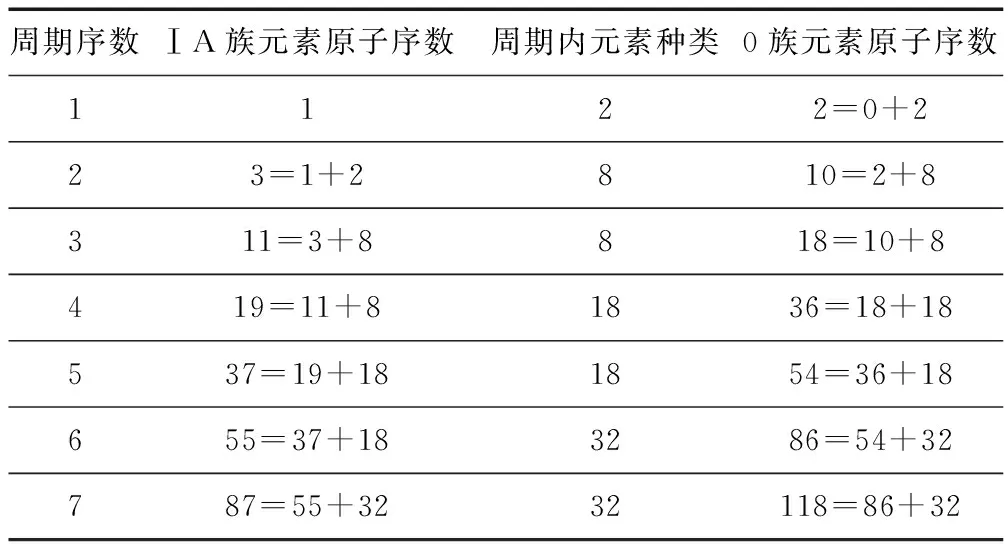
ⅠA族、0族元素的原子序数与周期内元素种类的关系表
例6 同一主族的两种元素的原子序数之差不可能是( ).
A.16 B.26 C.36 D.46
解析根据稀有气体原子序数(2、10、18、36、54、86)可判断同主族两种元素原子序数之差有:18-2=16,36-10=26,54-18=36,所以答案为D.
规律七:稀有气体元素的原子序数与推断元素在周期表中位置之间的应用关系.
首先要记住稀有气体元素的原子序数:2、10、18、36、54、86;其次用元素的原子序数减去比它小且相近的稀有气体元素的原子序数其差值即为该元素所在的纵行数(若其差值大于18则要再减去14才能得到其纵行数);再次根据所学纵行的分布情况(即:第1、2纵行为ⅠA、ⅡA族,第3~7纵行为ⅢB~ⅦB族,第8~10纵行为第Ⅷ族,第11、12纵行为ⅠB、ⅡB族,第13~17纵行为ⅢA~ⅦA族,第18纵行为0族)来确定它的族序数,最后由这种元素的周期数比它相近的原子序数小的稀有气体元素的周期数大1来确定它的周期序数.
例7 现在发现原子序数是115号的元素X,下列说法不正确的是( ).
A.X最高化合价为+5 B.X是非金属元素
C.X位于第七周期第ⅤA族 D.X是金属元素
解析比它小且相近的稀有气体元素的原子序数为86,115-86-14=15即:115号元素位于第15纵行也就是第ⅤA族;由于86号元素位于第六周期,所以115号元素位于第七周期.因此115号元素是金属元素,位于第七周期第ⅤA族,最高化合价为+5,所以答案为B.
