基于Meta分析的复方苦参注射液治疗胃癌的系统评价Δ
2018-10-11郑捷文刘殊羽王凯欢吴嘉瑞段笑娇倪梦蔚
郑捷文,刘殊羽,王凯欢,吴嘉瑞,段笑娇,倪梦蔚
(北京中医药大学中药学院,北京 100102)
胃癌是我国最常见的恶性肿瘤之一,具有较高发病率、转移率和死亡率,多数患者在就诊时已处于进展期,即便实施根治性切除术,局部复发率、淋巴转移率仍较高,因此,复发和转移是治疗失败的重要原因[1]。胃癌属中医“反胃”“噎嗝”“胃脘痛”“症瘕”及“积聚”等病证范畴,中医认为,胃癌是由于脾虚不运,胃失和降,脏腑内虚,毒邪湿痰凝于中焦,气郁血逆,瘀毒内阻,渐而形成积聚[2]。复方苦参注射液是由苦参、白土苓2味中药经加工制成的抗肿瘤类中药注射剂,现代研究结果表明,联合应用复方苦参注射液治疗中晚期胃癌的临床疗效确切,优点明显,可改善疼痛、发热、出血及乏力等临床症状,配合放化疗可减毒增效、抑制肿瘤生长,提高抗肿瘤疗效,增强患者免疫功能[3]。本研究基于文献荟萃分析(Meta分析),全面收集现有临床研究资料,客观评价复方苦参注射液治疗胃癌的疗效及安全性,以期为其临床应用提供依据。
1 资料与方法
1.1 纳入与排除标准
(1)研究类型:复方苦参注射液治疗胃癌的随机对照试验(randomized controlled trial,RCT),凡文献中述及“随机”均纳入,无论是否使用盲法。(2)研究对象:均符合《中国临床肿瘤学会(CSCO)原发性胃癌诊疗指南(2017.V1)》的诊断标准[4];经病理或组织学检查确诊为胃癌的成年患者;有可测量或可评价病灶;接受联合方案化疗或单纯化疗时间≥1个周期;化疗前预计生存期≥2个月;化疗距上次化疗及其他生物治疗时间≥1个月;外周血象及心肺、肝肾功能正常,无化疗禁忌证;年龄、性别、病程、种族及疾病严重程度不限。(3)干预措施:对照组患者采用常规化疗治疗;观察组患者在对照组基础上加用复方苦参注射液,用药剂量、疗程不限,但无配伍中药,无手术等治疗手段辅助,若存在其他并发症等也予以治疗。(4)结局指标:主要结局指标为临床总有效率及生活质量改善情况,次要结局指标为药品不良反应发生情况(白细胞计数降低、胃肠道反应及肝功能异常)。①临床总有效率。参照世界卫生组织关于实体瘤疗效评价评定标准,完全缓解为可见的病变完全消失>1个月;部分缓解为单个病变肿瘤面积缩小≥50%,肿瘤病灶的最大径及其最大垂直径的乘积减少≥50%,维持4周以上;疾病稳定为病情无明显变化至少4周,肿瘤大小估计增大<25%,减少<50%;疾病进展为新病灶出现或原有病变估计增大≥25%[5]。临床总有效率=(完全缓解病例数+部分缓解病例数)/总病例数×100%。②以Karnofsky(KPS)评分标准评定生活质量改善情况,其中上下波动10分以内为稳定,提高10分以上为改善,降低10分以上为降低。③药品不良反应参照1981年世界卫生组织制定的《化疗药物急性及亚急性毒性标准》进行判定[6]。(5)排除标准:研究涉及以下任一项即可排除。①研究对象合并有其他肿瘤者;②对照组干预措施有联合其他中药(中药方剂、中成药及中药注射剂等)治疗,联合放疗、手术等其他西医治疗;③复方苦参注射液用法为非静脉给药;④非临床试验或自身对照研究或随机方法错误的研究;⑤重复发表的研究结果,仅保留发表年份最近,样本量大或信息全面的研究;⑥药品名称、剂量及疗程等数据不完整或数据有误的研究;⑦疗效评价标准不符及无相关结局指标的研究。
1.2 检索策略
计算机检索中国期刊全文数据库(CNKI)、中文科技期刊全文数据库(VIP)、万方数据库、中国生物医学文献数据库(CBM)、PubMed、Embase和the Cochrane Library等数据库,搜集复方苦参注射液联合化疗治疗胃癌的RCT,检索时间为建库至2018年5月1日。采用主题词与自由词结合的方式,中文检索词主要包括“胃癌”“胃肿瘤”“胃部肿瘤”“胃细胞癌”“岩舒注射液”“岩舒”“复方苦参注射液”“复方苦参注射液”及“复方苦参”等,全文检索“随机”;英文检索词主要包括“Stomach Neo-plasms”“Gastric Cancer”“Gastric Carcinoma”“Gastric Neoplasm”“Cancer of Stomach”“Stomach Cancer”“Compound Kushen injection”“Compound matrine”及“Fufangkushen”等。
1.3 文献筛选与资料提取
由2名研究者独立筛选及纳入文献,并提取资料,如有分歧,可以进行讨论或咨询第三方。提取内容包括:纳入研究的基本信息,包括第一作者、发表年份等;研究对象的基本特征,包括观察组和对照组病例数、性别组成、平均年龄、干预措施、药物剂量及疗程等;研究所关注的结局指标和结果测量数据;研究设计类型和偏倚风险评价的关键因素。
1.4 纳入研究的偏倚分析评价
由2名研究者运用Cochrane系统评价员手册5.1.0版“RCT偏倚风险评估工具”[7]对纳入研究进行偏倚风险评价,如遇分歧交由第三方裁定。评价条目包括随机序列生成(选择偏倚)、分配隐藏(选择偏倚)、所有研究参与者和人员采用盲法(执行偏倚)、结果评估的盲法(观察偏倚)、不完整的结果数据(失访偏倚)、选择性报告(报告偏倚)和其他偏倚,每方面内容均有“高风险”“未知风险”和“低风险”3个等级。
1.5 统计学方法
采用Cochrane协作网提供的RevMan 5.3[8]软件统计相关数据,二分类变量指标选用相对危险度(RR)、连续变量采用均数差(MD)为效应指标,均计算95%可信区间(CI)。采用Cochrane Q检验分析各研究间的异质性,并用I2来评价异质性的大小。当P>0.1,I2<50%时,采用固定效应模型进行Meta分析;否则在排除临床异质性的前提下,采用随机效应模型进行Meta分析[9]。如果存在临床或方法学异质性,则采用亚组分析。采用Stata 13.0软件通过逐一排除法进行敏感性分析,以判断结果稳定性。绘制倒漏斗图,分析是否存在发表偏倚。
2 结果
2.1 文献筛选流程
初检出文献359篇,去重、阅读题目及摘要后排除明显不相关文献,共收集复方苦参注射液用于胃癌的临床研究57篇;进一步阅读全文,排除个案研究及不符合纳入标准的文献,最终纳入文献39篇[10-48],均为已发表的中文文献。文献筛选流程见图1。
2.2 纳入文献的基本特征
39篇文献[10-48]共涉及患者3 346例,其中,观察组1 700例,对照组1 646例,两组患者性别、年龄等基线资料的差异均无统计学意义(P>0.05),具有可比性;复方苦参注射液用量12~30 ml,疗程7~42 d。纳入文献的基本特征见表1。
表1纳入文献的基本特征
Tab1Basiccharacteristicsofinvolvedliterature

文献病例数(观察组/对照组)性别(男性/女性)/例平均年龄、范围/岁干预措施观察组对照组疗程结局指标张继军等(2010年)[10]32/3239/2552.30复方苦参注射液20 ml+对照组药物表柔比星+顺铂+氟尿嘧啶21 d×2个周期①②刘永叶等(2017年)[11]34/3443/2545~75复方苦参注射液20 ml+对照组药物奥施康定7 d③王竞等(2016年)[12]27/2523/2963.64复方苦参注射液20 ml+对照组药物氟尿嘧啶+多西他赛21 d×3个周期①袁彩君等(2012年)[13]36/3034/3270.00复方苦参注射液20 ml+对照组药物奥利沙铂+卡培他滨21 d×3个周期①②③张永亮等(2009年)[14]35/3543/2758.50复方苦参注射液30 ml+对照组药物多西他赛+氟尿嘧啶21 d①②③陆彬彬等(2011年)[15]20/2025/1565.50复方苦参注射液20 ml+对照组药物多柔比星+顺铂+氟尿嘧啶28 d×6个周期③王璞(2012年)[16]28/2837/1957.00复方苦参注射液20 ml+对照组药物奥利沙铂+丝裂霉素+氟尿嘧啶+亚叶酸钙21 d×2个周期①②③杨立平等(2014年)[17]39/3941/3763.60复方苦参注射液12 ml+对照组药物氟尿嘧啶+多柔比星+丝裂霉素42 d×3个周期③朱俊等(2015年)[18]34/3445/2250.50复方苦参注射液20 ml+对照组药物多西他赛30 d×3个周期①③罗彬(2013年)[19]90/9089/9155.80复方苦参注射液20 ml+对照组药物多西他赛+顺铂+氟尿嘧啶28 d×4个周期①③张利强等(2010年)[20]34/3439/2954.80复方苦参注射液20 ml+对照组药物奥利沙铂+氟尿嘧啶+亚叶酸钙28 d×6个周期①③刘宽浩等(2014年)[21]77/7586/6659.50复方苦参注射液20 ml+对照组药物奥利沙铂+氟尿嘧啶+亚叶酸钙28 d×4个周期①②③夏国安(2013年)[22]40/3648/2867.60复方苦参注射液20 ml+对照组药物替吉奥14 d×2个周期①③赵月宏等(2014年)[23]30/3043/1747.00复方苦参注射液20 ml+对照组药物多西他赛21 d×(4~6)个周期①③何仁强(2015年)[24]100/100112/8855.70复方苦参注射液30 ml+对照组药物多西他赛21 d×2个周期①③陈健等(2013年)[25]36/3448/2240.50复方苦参注射液20 ml+对照组药物氟尿嘧啶+多西他赛+卡铂21 d×4个周期③黄智芬等(2008年)[26]30/3045/1547.80复方苦参注射液20 ml+对照组药物亚叶酸钙+氟尿嘧啶+顺铂+羟基喜树碱21 d×2个周期①②赵月(2011年)[27]20/2031/1953.20复方苦参注射液20 ml+对照组药物奥利沙铂+亚叶酸钙+氟尿嘧啶21 d×3个周期①②③韩全利等(2011年)[28]39/3944/3454.40复方苦参注射液15 ml+对照组药物奥利沙铂+亚叶酸钙+氟尿嘧啶28 d①③刘书林等(2009年)[29]29/2838/1955.80复方苦参注射液20 ml+对照组药物奥利沙铂+亚叶酸钙+氟尿嘧啶21 d×2个周期①③冯献明等(2013年)[30]52/52——复方苦参注射液20 ml+对照组药物奥利沙铂+亚叶酸钙+氟尿嘧啶21 d①③林春丽等(2011年)[31]43/42—50.40复方苦参注射液20 ml+对照组药物多西他赛+奥利沙铂+氟尿嘧啶21 d×3个周期①②③杨琴(2010年)[32]30/3039/2159.10复方苦参注射液20 ml+对照组药物奥利沙铂+卡培他滨21 d×2个周期③皮庆军(2012年)[33]45/4056/2954.50复方苦参注射液20 ml+对照组药物氟尿嘧啶+顺铂21 d×2个周期②赵航(2016年)[34]48/4853/4359.33复方苦参注射液20 ml+对照组药物氟尿嘧啶42 d②杨秀娥等(2013年)[35]50/5052/4856.50复方苦参注射液30 ml+对照组药物奥利沙铂+亚叶酸钙+氟尿嘧啶21 d×2个周期②郑平(2013年)[36]40/4047/3331~68复方苦参注射液12 ml+对照组药物表柔比星+氟尿嘧啶42 d①③许进秀等(2017年)[37]40/4053/2768.19复方苦参注射液20 ml+对照组药物替吉奥21 d×6个周期①刘迎丽等(2014年)[38]43/4351/3553.58复方苦参注射液20 ml+对照组药物亚叶酸钙+氟尿嘧啶+顺铂21 d×2个周期①③鲁守斌等(2001年)[39]120/100164/5649.70复方苦参注射液20 ml+对照组药物丝裂霉素+氟尿嘧啶+多柔比星21 d×2个周期①②③张克实等(2011年)[40]30/2430/2454.80复方苦参注射液20 ml+对照组药物紫杉醇+氟尿嘧啶21 d×2个周期②张黎(2016年)[41]49/5051/4868.30复方苦参注射液20 ml+对照组药物紫杉醇+氟尿嘧啶21 d×2个周期③杨洁文等(2012年)[42]30/2830/2864.20复方苦参注射液15 ml+对照组药物奥利沙铂+亚叶酸钙+氟尿嘧啶14 d×6个周期①③张强等(2017年)[43]30/3042/1852.00复方苦参注射液20 ml+对照组药物伊立替康+氟尿嘧啶+亚叶酸钙14 d×4个周期①③朴瑛等(2016年)[44]32/3134/29—复方苦参注射液20 ml+对照组药物替吉奥28 d×6个周期③刘龑航等(2010年)[45]83/83118/5872.10复方苦参注射液20 ml+对照组药物奥利沙铂+亚叶酸钙+氟尿嘧啶21 d×4个周期①熊良庚(2008年)[46]37/3448/2351.00复方苦参注射液20 ml+对照组药物紫杉醇+奥利沙铂21 d①③李蓉(2006年)[47]40/40——复方苦参注射液20 ml+对照组药物丝裂霉素+氟尿嘧啶+多柔比星21 d①③张明娟等(2010年)[48]48/4854/4255.90复方苦参注射液20 ml+对照组药物氟尿嘧啶+亚叶酸钙+顺铂(21~28)d×2个周期②③
注:①临床总有效率;②生活质量改善情况;③药品不良反应;“—”表示无相关数据
Note:①clinical efficacy; ②improvement of quality of life; ③adverse drug reactions; “—” means no relevant data
2.3 纳入文献的方法学质量评价
39篇文献[10-48]均只提及随机,但均未描述随机序列产生的具体方法,故分配隐藏均评为“未知风险”;6篇文献[10,12,15,17,26,44]采用随机数字表法,故随机序列产生评为“低风险”,其余33篇未描述随机序列产生的方法,故均评为“未知风险”;均未描述分配隐藏及盲法的实施,故分配隐藏、研究和受试者盲法、结果评价者盲法3项均评为“未知风险”;均无选择性报告,且无病例退出或脱落等问题,数据较完整,故选择性报告及数据完整评为“低风险”,见图2。
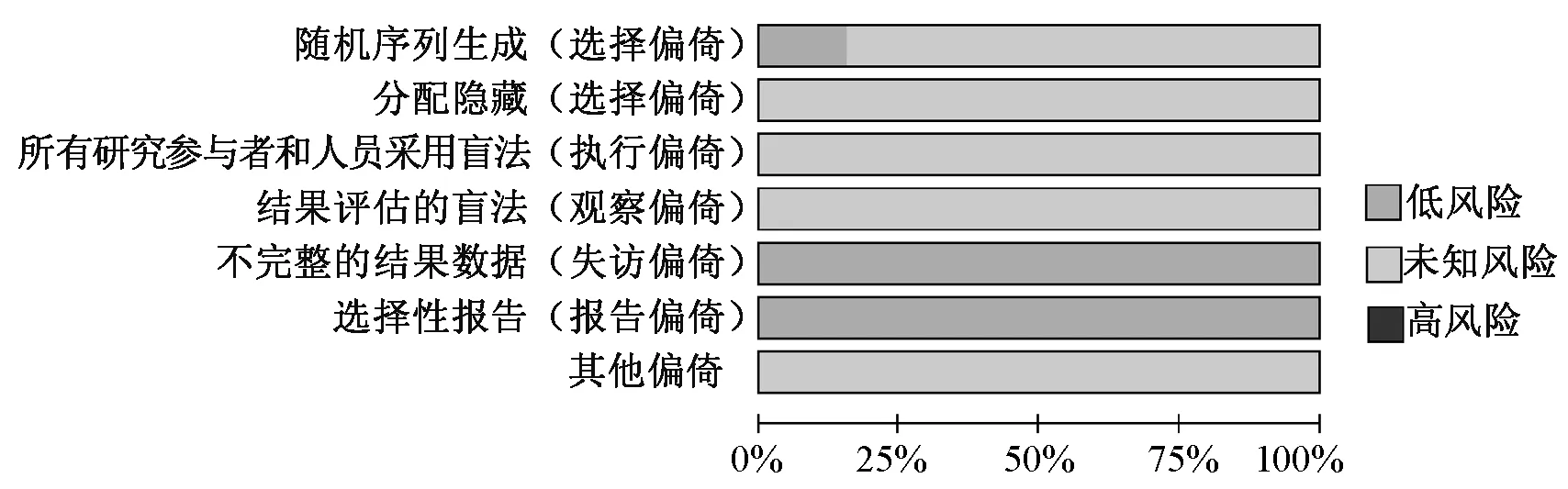
图2 纳入研究的偏倚风险评价结果Fig 2 Risk bias evaluation results
2.4 Meta分析结果
2.4.1 临床总有效率:27篇文献[10,12-14,16,18-24,26-31,36-39,42-43,45,47]报告了临床总有效率,经异质性检验,P>0.1,I2<50%,故采用固定效应模型进行Meta分析。结果显示,观察组患者的临床总有效率明显高于对照组,差异有统计学意义(RR=1.40,95%CI=1.29~1.51,Z=8.16,P<0.000 01),见图3。
2.4.2 生活质量改善情况:14篇文献[10,13-14,16,21,26-27,31,33-35,39-40,48]报告了生活质量改善情况,经异质性检验,P>0.05,I2<50%,故采用固定效应模型进行Meta分析。结果显示,观察组患者的生活质量改善率明显高于对照组,差异有统计学意义(RR=1.74,95%CI=1.53~1.97,Z=8.62,P<0.000 01),见图4。
2.4.3 药品不良反应:(1)白细胞计数降低。21篇文献[13-15,18-19,21-23,27-32,36,38,41,43-44,46-47]报告了白细胞计数降低发生情况,采用随机效应模型进行Meta分析。结果显示,观察组患者白细胞计数降低发生率明显低于对照组,差异有统计学意义(RR=0.63,95%CI=0.55~0.72,Z=6.97,P<0.000 01)。(2)胃肠道反应。27篇文献[11,13-25,28,30-32,36,38,41-44,46-48]报告了胃肠道反应发生情况,采用随机效应模型进行Meta分析。结果显示,观察组患者胃肠道反应发生率明显低于对照组,差异有统计学意义(RR=0.70,95%CI=0.61~0.81,Z=4.97,P<0.000 01)。(3)肝功能异常。16篇文献[13-16,18-24,30-31,44,46-48]报告了肝功能异常发生情况,采用随机效应模型进行Meta分析。结果显示,观察组患者肝功能异常发生率明显低于对照组,差异有统计学意义(RR=0.48,95%CI=0.37~0.62,Z=5.42,P<0.000 01)。
2.5 发表偏倚评估
针对临床总有效率指标绘制倒漏斗图,观察其对称性。结果显示,各研究的点在中线两侧分布不对称,2篇位于左、右侧线上,1篇位于漏斗图右侧线外,表明存在发表偏倚,见图5。
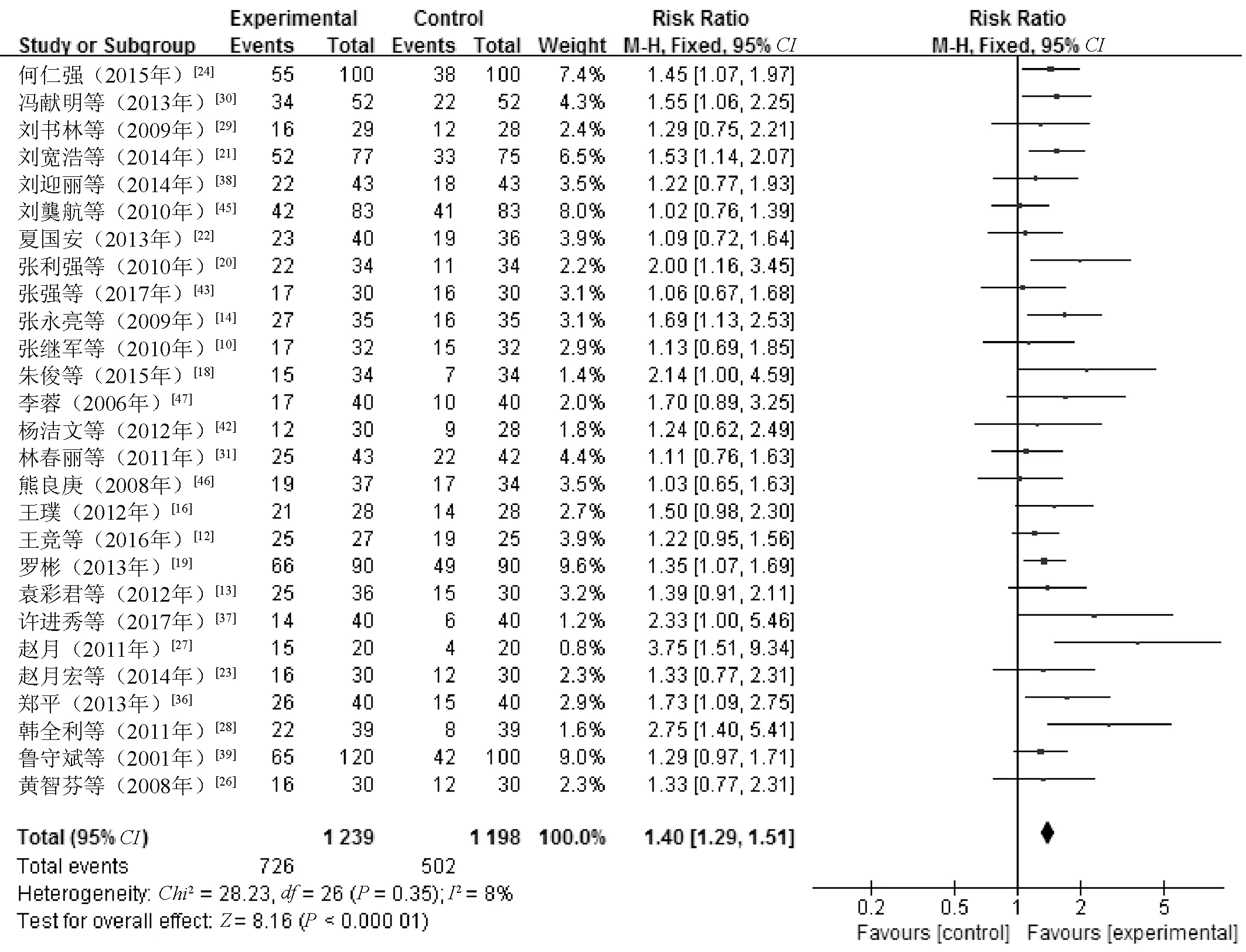
图3 两组患者临床总有效率比较的Meta分析森林图Fig 3 Meta-analysis forest plot of comparison of total clinical effective rate between two groups
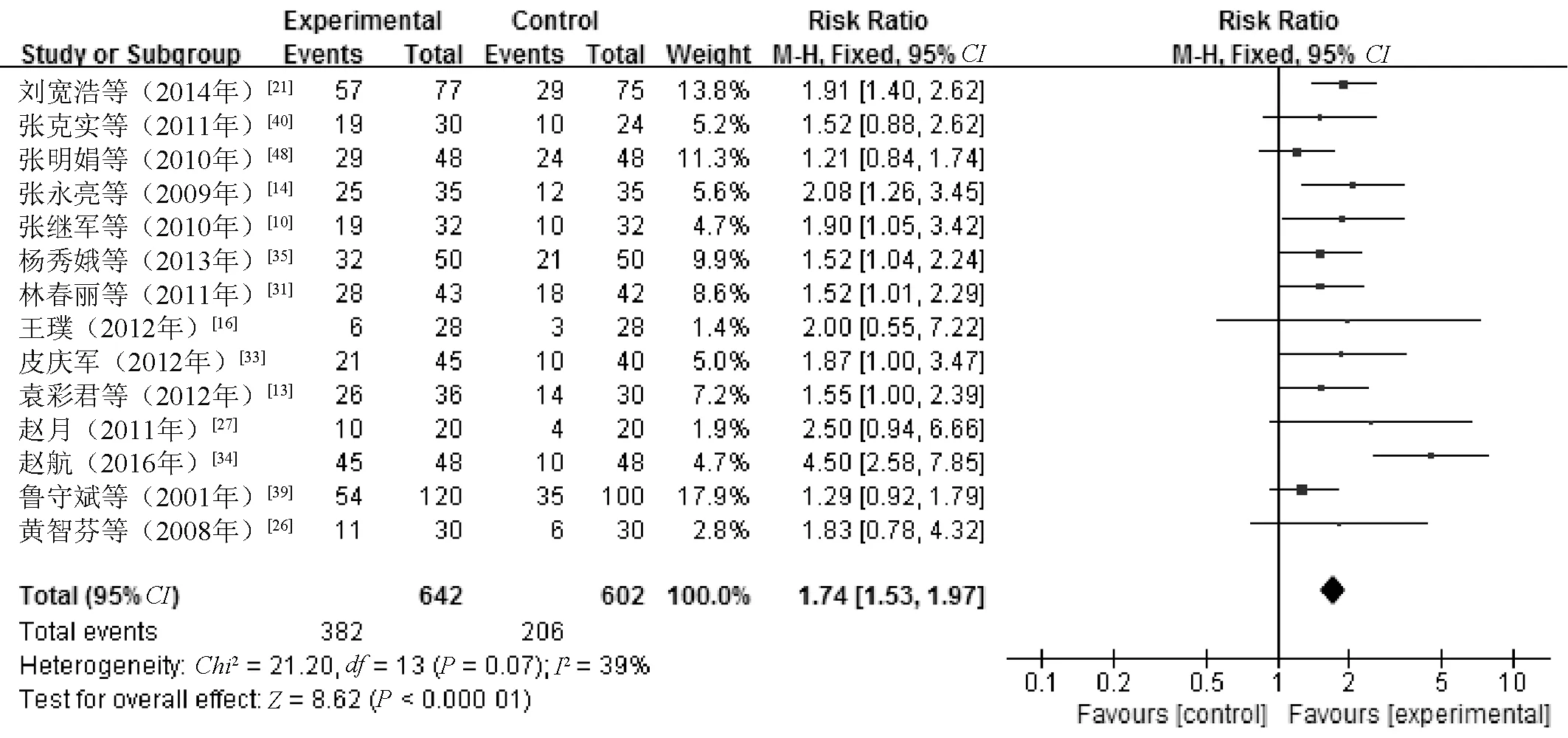
图4 两组患者生活质量改善情况比较的Meta分析森林图Fig 4 Meta-analysis forest plot of comparison of improvement of quality of life between two groups
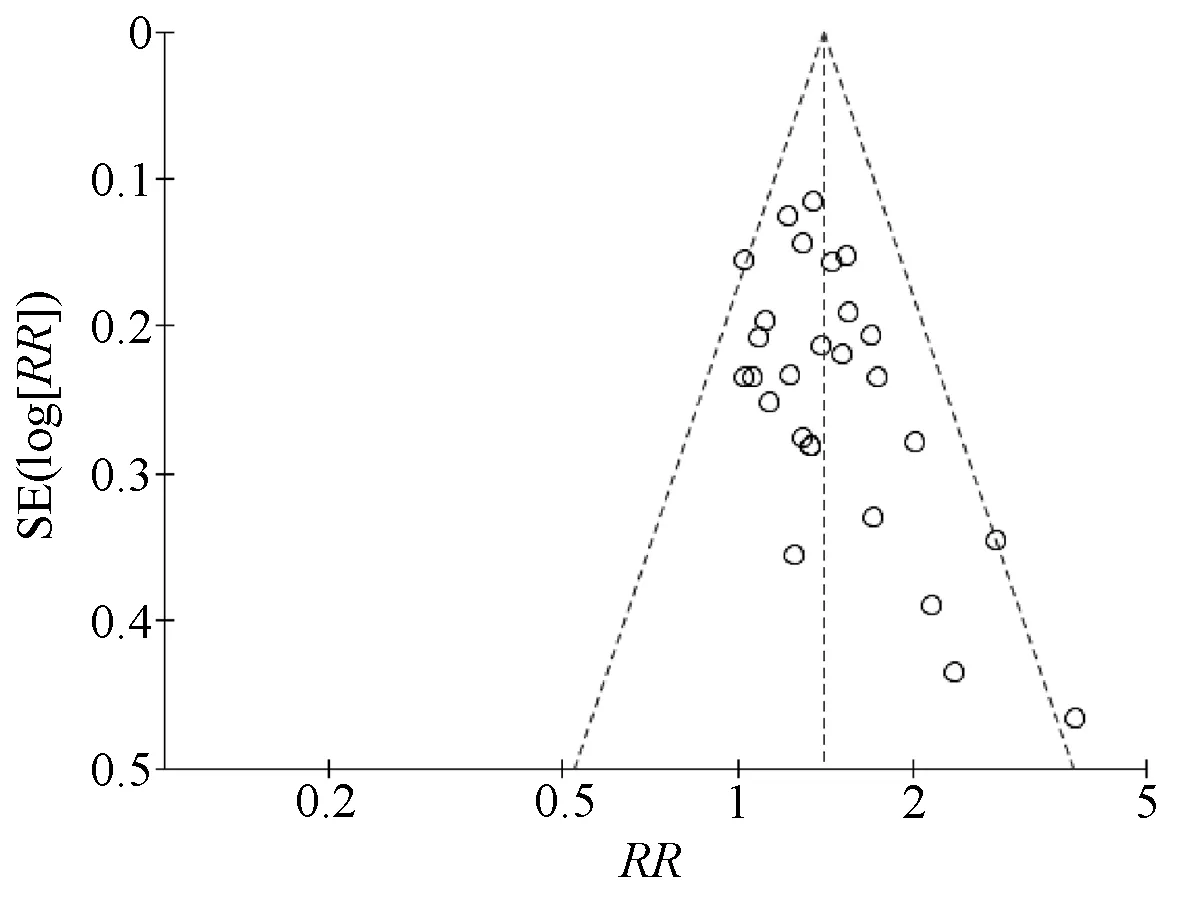
图5 临床总有效率的倒漏斗图Fig 5 Inverted funnel plot of total clinical effective rate
2.6 敏感性分析
针对临床总有效率总体合并效应量运用逐一排除法进行敏感性分析,即每次排除1个研究,对剩余研究重新进行Meta分析,以判断结果稳定性。结果显示,合并效应量未发生质的变化,说明本研究结果相对稳定,见图6。
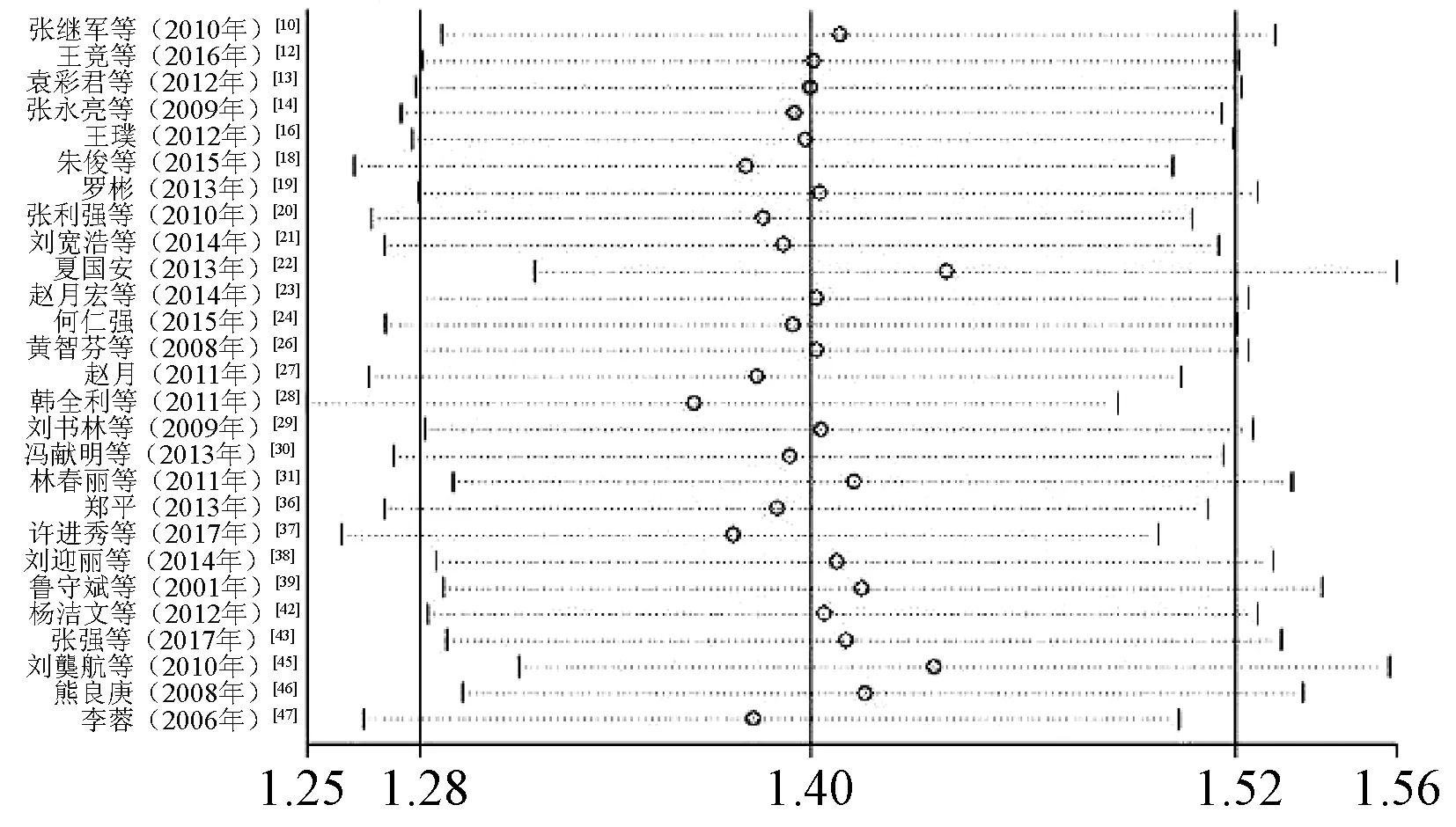
图6 临床总有效率的敏感性分析图Fig 6 Sensitivity analysis of total clinical effective rate
3 讨论
胃癌是我国发病率居第2位、死亡率居第3位的恶性肿瘤。随着外科手术、放射技术的进步以及有效抗肿瘤药的大量研发生产,在提高胃癌治愈率的同时,也产生了许多不良反应,如胃肠道反应、骨髓抑制等,因此,保护机体的免疫功能尤为重要[49]。中医药通过整体调节和辨证论治,能在一定程度上改善症状,提高生活质量,延长生存期,并减轻放化疗的毒性[50]。复方苦参注射液具有抗胃癌细胞增殖的活性,其机制可能与抑制胃癌细胞血管生成因子有关[51],其在临床上的应用日渐广泛。
本研究结果表明,与单纯常规化疗比较,在常规化疗基础上联合应用复方苦参注射液治疗胃癌,可明显提高患者的临床总有效率,明显改善患者的生活质量,明显降低化疗药所致白细胞计数降低、胃肠道反应及肝功能异常等不良反应发生率。
在数据库中共有2篇关于复方苦参注射液治疗胃癌的传统Meta分析[52-53],分别发表于2011、2013年,分别纳入文献10、12篇,均为RCT,分别比较了客观疗效、生活质量改善及不良反应事件发生率。相比较而言,本研究的优势主要体现在以下几点:(1)更新了检索时间且检索较全面,上述2个研究最新检索时间为2013年,而本研究纳入文献中有13篇[11-12,17-18,21,23-24,34,37-38,41,43-44]发表于2013年以后。此外,本研究一方面通过计算机检索国内外数据库,同时检索在研研究和相关学术组织网站,补充其他检索获取RCT的途径;另一方面,检索策略采用主题词和自由词检索相结合的方式,检索词分为胃癌、复方苦参注射液和随机对照研究3个部分。(2)制订了严格的纳入与排除标准,纳入RCT的共同干预措施为化疗,观察组干预措施为在化疗基础上仅加用复方苦参注射液,避免了所纳入文献存在较大的临床异质性。由此可见,本研究所纳入RCT干预措施差异性较小。
同时,本研究也存在一定的局限性:(1)所纳入的大多数研究的方法学质量不高,均为中文文献,仅6篇描述了具体分组方法,其余文献均只提及“随机”,所有文献均未提及使用盲法。(2)对胃癌患者的分期、分型未进行限定,且各研究中化疗药、剂量及疗程也存在一定差异,导致各研究间存在一定的临床异质性;纳入的RCT对生存率及随访情况的报道较少。(3)临床总有效率的倒漏斗图分布不对称,提示纳入文献可能存在发表偏倚,即存在部分阴性结果没有发表等问题。综上,建议临床进行RCT时,不仅应注重随访、报道生存率等终点指标,同时应更加规范治疗胃癌化疗药的剂量、疗程等,切实提高RCT的方法学质量,为临床治疗提供可靠的科学依据。
