铜与稀硝酸反应的实验改进
2018-08-31聂紫娟齐艳娟
聂紫娟 齐艳娟
(长春师范大学化学学院,吉林 长春 130032)
0 引言
铜与稀硝酸反应的演示实验是高一化学必修课中学习一氧化氮、二氧化氮的性质时必做的演示实验。针对该实验,在人教版高中化学教科书中没有提供实验设计,在苏教版和鲁教版高中化学教科书中均设计了实验。运用教科书中的实验装置,进行实验,会发现此实验中存在以下几点问题:
(1)如图1所示,此实验从装置图上看可以发生铜与浓、稀硝酸的反应,进而能观察到产生气体颜色的变化。但实际操作中发现用排水法收集一氧化氮,收集到的气体并不多。
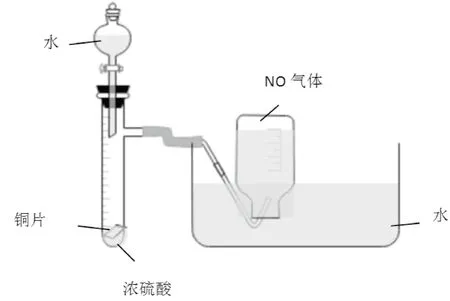
图1
(2)在课堂中进行演示实验时,操作性不强。而且实验现象不明显。
(3)没有对生成的一氧化氮、二氧化氮进行尾气处理。
(4)如图2所示,生成的无色的一氧化氮气体很快就被空气中的氧气氧化成了红棕色的二氧化氮气体,很难观察到一氧化氮慢慢被氧化成二氧化氮的过程。
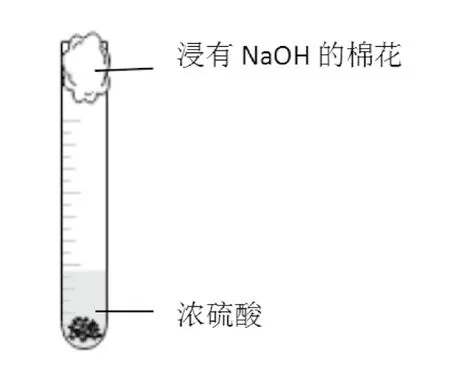
图2
(5)此实验虽然用一块蘸有NaOH的湿棉花团封住试管口,但通过实验发现,湿棉花团的吸收效果并不理想,而且仍有大量的氮氧化物气体逸出。同时试管中的二氧化氮气体无法进行处理。
通过查阅文献发现,已经有很多学者对此实验在教科书的基础上进行了改进。但实验现象不是特别明显。因此本文通过多次试验,对此实验进行了进一步的改进。希望给一线教师进行演示实验提供新方案。
1 实验药品及实验仪器
稀硝酸;铜丝;干燥管,配套的橡胶塞;玻璃管,配套的橡胶管;弹簧夹;试剂瓶,配套单孔橡胶塞;注射器;烧杯,“U”形玻璃管,平配套的橡胶塞。
2 实验原理

3 实验改进装置图
4 实验过程及现象
步骤一:取一个试剂瓶,向其中注满稀硝酸,然后将带有玻璃管的单孔橡胶塞塞进装满稀硝酸的集气瓶口。同时会有少量的稀硝酸被压入玻璃管中。然后再取一支干燥管,如图3所示,进行连接。
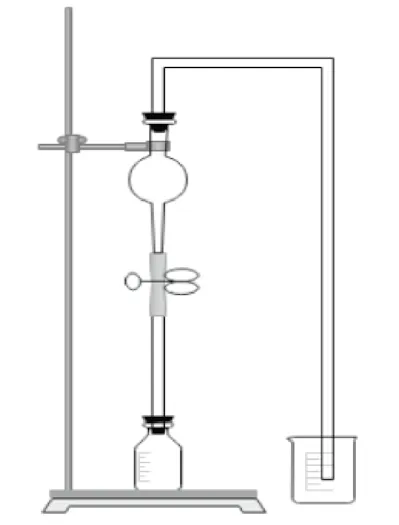
图3 实验改进装置图
步骤二:取一支注射器,然后用注射器将稀硝酸注入玻璃管中,直至稀硝酸淹过乳胶管为止。
步骤三:取2~3根铜丝,将铜丝通过干燥管和玻璃管伸入至试剂瓶的稀硝酸中。然后将带有“U”形玻璃管的单孔橡胶塞塞进干燥管的末端口。“U”形玻璃管插入盛有NaOH溶液的烧杯中,“U”形玻璃管的末端口浸没在NaOH溶液中。使得整个反应在密闭的体系中进行反应。再取一个弹簧夹,将乳胶管夹住。
步骤四:反应一段时间后观察到的现象:
(1)铜丝与稀硝酸反应剧烈,产生大量的无色气泡,溶液变成蓝色,集气瓶和玻璃管中均有无色气泡。
(2)当打开弹簧夹后,可以观察到橡胶管口有红棕色气体产生,而集气瓶和玻璃管中产生的气泡仍为无色气泡。当反应一段时间后玻璃管中有红棕色气体产生(打开弹簧夹后空气进入玻璃管中),而且是从上至下的变化。重复多次实验依然可以观察到这样的现象。
步骤五:反应结束时,NO2通入NaOH溶液中进行尾气处理。
5 注意事项
(1)稀硝酸的浓度:硝酸的浓度以V(浓硝酸65%):V(水)=2∶3为宜。硝酸的浓度偏大,会导致很快产生NO2气体。(2)防止空气进入:试剂瓶中一定要注满稀硝酸,同时玻璃管中也要注满稀硝酸直至淹没橡胶管。(3)“U”形玻璃管的末端一定要浸没在NaOH溶液中。
6 实验改进的优点
(1)实验现象明显。学生能清晰地观察到产生的无色气体NO以及被空气中的氧气氧化后变成红棕色的NO2气体。(2)实验装置简单,在进行课堂演示实验时,易于连接,方便操作。(3)实验中所用到的仪器都是在实验室中用的最基本的仪器,方便实验。(4)整个反应是在密闭的体系中发生反应的,产生的NO在密闭的环境中就被氧化了,能让学生意识到NO易被氧化。(5)学生通过对实验现象的观察,激起学生对本节课学习的兴趣。(6)本实验是在中学化学教材中所提供的演示实验的基础上进行的实验改进。因此,通过此实验可以提高学生的创新意识,同时培养学生的发散思维。(7)设计的实验装置是密闭的,而且反应后有尾气处理,体现了绿色化学的理念。
