锌对神经病理性疼痛小鼠学习记忆障碍及海马DG区脑源性神经营养因子及环磷腺苷效应元件结合蛋白表达的影响
2018-07-18张海燕王月静姚宏波孙丽慧
张海燕 王月静 姚宏波 廉 洁 孙丽慧
(齐齐哈尔医学院组胚教研室,黑龙江 齐齐哈尔 161006)
神经病理性疼痛(NPP)是由于外周或中枢神经系统受到损伤或产生病变而导致的一种慢性疼痛。尽管病因未明,一项针对 275例慢性持续性疼痛患者的认知功能的研究表明,有超过半数的受试者(54%)出现一种以上的认知功能问题,主要症状为难以集中注意力、解决问题和推理能力差、精神错乱、定向力障碍及反应时间长〔1〕。另一项临床研究同样表明,慢性疼痛可能使注意力下降,妨碍记忆的过程〔2〕。动物海马组织与学习记忆及认知功能密切相关,对内源性或外源性环境因素(如高龄、慢性应激等)刺激很敏感,当机体接受慢性应激刺激时,海马结构会被损害进而使其学习记忆能力减退〔3〕。研究发现当动物模型产生NPP时,机体可因为慢性应激而引起相应的学习记忆能力下降〔4〕。锌是我们体内所必需的微量元素,在脑组织中海马的突触泡和苔藓纤维锌含量最高,而该部位与动物的学习记忆密切相关〔5〕。研究发现缺锌动物模型的学习记忆和生长发育显著下降〔6〕。本实验通过在NPP动物模型中添加饲料锌,观察其对NPP所致学习记忆障碍的影响。
1 材料与方法
1.1实验动物 32只雄性健康C57/BL6小鼠(室温饲养,正常饮食水),体重(23±2)g,齐齐哈尔医学院实验动物中心提供,动物生产合格证号:SCXK(黑)2006-0010。
1.2主要试剂 硫酸锌 (福州迈新),脑源性神经营养因子(BDNF)及环磷酸腺苷效应元件结合蛋白(CREB)抗体(Santa公司),免疫组化试剂盒、甲基紫染色剂,二氨基联苯胺(DAB)显色剂(福州迈新),聚偏氟乙烯(PVDF)膜和蛋白Marker (NEB公司),戊巴比妥钠、电化学发光(ECL)试剂盒和胶片(Santa公司),多聚甲醛和酒精等(福州迈新)。
1.3实验器材 1/10 000电子分析天平(上海);JY-ECP3000电泳仪(北京);Olympus万能显微镜和照相机(日本);台式高速离心机(上海);-80℃超低温冰箱(日本);超声波细胞粉碎机(中国);MIVNT显微图像分析系统(中国);半干转印电泳槽 (大连);Mikro22R高速冷冻离心机(德国);低温离心机(北京);电转移槽(北京);化学发光凝胶系统分析仪(上海)。
1.4实验方法
1.4.1NPP小鼠模型制备 首先制作L5-SNT模型,以2%戊巴比妥(50 mg/kg)注射到C57/BL6小鼠腹腔,待其麻醉后,在小鼠背部L4-S1椎体处切开,将左侧椎旁肌肉钝性分离,将L6横突和L5椎板去除,将临近背根神经节的神经结扎,割断神经远端,缝合切口。假手术组切开皮肤分离左侧椎旁肌肉后,只将L6横突及L5椎板去除,神经保留。
1.4.3Morris水迷宫实验 各组模型制备后29 d时行Morris水迷宫实验。实验总时间为5 d,每天9∶00至13∶00 进行训练。隐藏平台潜伏期实验在前4 d进行,随机将动物从非平台所在象限的3个入水点面向池壁放入水中,计算机软件记录动物在60 s内寻找并爬上平台的时间(逃避潜伏期)。如果大鼠在60 s内仍未找到平台,则将其引导至平台并停留15 s,潜伏期计为60 s。第5天为空间探索实验,将动物放入水中自由游泳,记录60 s内在原平台所在象限的游泳时间和路径,分别计算在原平台所在象限游泳时间与路径与总游泳时间和总路径的比值。
1.4.4取材与标本制备 实验结束后,4%硫喷妥钠(50 mg/kg)腹腔注射麻醉各组小鼠,各组小鼠断头取海马组织,一部分放入-80℃冰箱保存,用于Western印迹实验;取另一部分用4%多聚甲醛固定12 h,经石蜡包埋后,制备5 μm厚的石蜡切片。
1.4.5免疫组化检测 石蜡组织切片后,常规脱蜡及水化,高压修复1.5 min。之后滴加3%的过氧化氢10 min;磷酸盐缓冲液(PBS)冲洗后,加入5%BSA封闭30 min,将其去除后放兔抗小鼠多克隆BDNF抗体 (1∶200)及CREB抗体(1∶800),4℃冰箱过夜;次日室温下放置1 h,PBS冲洗后加入二抗(鼠抗兔IgG,1∶200),在37℃恒温箱内孵育30 min;再用PBS冲洗后加入链霉素抗生物素-过氧化物酶孵育10 min;PBS冲洗后用DAB显色,常规脱水、透明和封片。
1.4.6Western印迹检测 海马组织放入EP管内,将组织裂解,测定蛋白浓度,再将混匀的上样缓冲液(5倍)加入,煮沸5 min,静置室温后离心,取上清液;制备分离胶后,进行加样,电泳,转膜,封闭,兔抗小鼠多克隆BDNF抗体 (1∶500)及CREB抗体(1∶800)孵育,在4℃摇床中放置24 h,TBST进行漂洗,二抗(鼠抗兔IgG,1∶5 000)常温孵育2 h,用TBST漂洗,ECL发光,利用X光片进行曝光、显影和定影。
1.5图像分析 用Image-Pro Plus6.0图像分析系统对免疫组化及Western印迹结果进行图像分析。计算平均光密度值(OD)。
1.6统计学方法 应用SPSS13.0软件进行单因素方差分析。
2 结 果
2.1锌对 NPP 小鼠学习记忆能力的影响 Morris水迷宫实验结果显示,与对照组比较,NPP组和Zn-NPP组逃避潜伏期明显延长,原平台所在象限游泳时间/总游泳时间比值和原平台所在象限游泳路径/总路径比值明显降低,差异均有统计学意义(P<0.05);与NPP组比较,Zn-NPP组逃避潜伏期明显缩短,原平台所在象限游泳时间/总游泳时间比值和原平台所在象限游泳路径/总路径比值明显升高,差异均有统计学意义(P<0.05)。见表1。
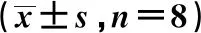
表1 各组水迷宫实验结果
与对照组比较:1)P<0.05;与NPP组比较:2)P<0.05,下表同
2.2免疫组化结果分析 BDNF阳性表达主要在细胞胞质,部分胞核也被着色,而CREB阳性表达部位为细胞核,阳性部位被染成棕褐色,与对照组比较,NPP组和Zn-NPP组阳性表达量显著增加(P<0.05);与NPP组比较,Zn-NPP组阳性表达量均显著降低(P<0.05);见图1,图2,表2。
到目前为止,此类材料主要集中在金属单质类氧化石墨烯复合材料如纳米银-氧化石墨烯复合材料、纳米金-氧化石墨烯复合材料,金属氧化物类氧化石墨烯复合材料如MnO2-氧化石墨烯、ZnO-氧化石墨烯、TiO2-氧化石墨烯复合材料,陶瓷类氧化石墨烯复合材料如SiO2-氧化石墨烯复合材料的研究上。
2.3Western印迹结果分析 与对照组比较,NPP组、Zn-NPP组BDNF、CREB表达量显著增加(P<0.05);与NPP组比较,Zn-NPP组阳性表达量均显著降低(P<0.05);见图3,表3。

图1 各组海马组织DG区BDNF阳性表达(DAB,×400)

图2 各组海马组织DG区CREB阳性表达(DAB,×400)

组别BDNFCREB对照组22.17±3.0616.38±2.51Zn-NPP组34.52±2.181)2)31.09±3.261)2)NPP组56.01±4.091)54.72±3.671)

图3 各组海马DG区的BDNF蛋白表达

组别BDNFCREBNPP组0.87±1.061)1.49±1.571)对照组0.29±1.290.84±1.18Zn-NPP组0.41±1.371)2)1.23±1.461)2)
3 讨 论
锌是体内必需微量元素,参与基因表达、组织修复及记忆形成等生物学过程。海马存在大量游离锌离子,锌离子在突触间隙释放后调控突触后膜受体功能,同时突触后神经元也含有锌离子,调节学习记忆功能,近期研究表明,补锌可使NPP小鼠学习记忆力得到改善,海马区神经元凋亡率显著下降〔7〕,其可能机制与海马区P53蛋白表达改变密切相关,但是否与BDNF及CREB表达改变有关有待于进一步探索。
BDNF在中枢神经系统内广泛分布,如大脑皮层、海马、纹状体、杏仁核等部位都发现有BDNF存在。BDNF 在维持神经元正常的生理功能(如神经元增殖、分化等)、神经的可塑性、突触的连接及促进突触生长等的作用显著〔8,9〕。
当神经系统受到伤害时,BDNF成为感受通路重要的神经递质〔10〕。相关文献结果发现,海马神经元可塑性和功能损伤与BDNF表达变化密切相关〔11〕。其中,当海马组织损伤后,会出现学习记忆力显著下降。研究发现〔12〕,在海马齿状回(DG区)定位后,将BDNF反义寡核苷酸用微量加样器注入小鼠海马DG区,其学习记忆力显著下降,DG区BDNF mRNA表达也显著降低,作用后兴奋性突触后电位也明显降低,这些结果表明海马DG区与BDNF 基因表达在学习记忆过程中作用显著;相似研究发现,在慢性复合应激可引起模型鼠学习记忆的损伤,免疫组化结果发现模型鼠海马内BDNF蛋白表达降低,提示在损害学习记忆增强的慢性复合应激大鼠的学习记忆功能过程中BDNF起关键作用〔13〕。
BDNF在维持海马功能和海马依赖的记忆中发挥着重要作用,其机制可能为,在学习记忆损伤的过程中,BDNF前体被转换成成熟的BDNF,从而增强BDNF信号转导通路,我们推测海马损伤后通过BDNF信号通路来损伤学习记忆;而CREB在通路中的发挥重要作用,其为核转录过程中的关键因子,在多种蛋白激酶(如:PKC、PKA等)的作用下可使其激活;使CREB发生自身磷酸化,此时具备双聚体的CREB与cAMP 反应元件(CRE)目标序列特异性结合,最终可调节多种基因转录功能。前辈发现,维持长时记忆的进程中,CREB起关键作用,其133位丝氨酸可被许多蛋白激酶激活,活化后这些蛋白激酶可转移到细胞核,与 CREB结合并使其磷酸化,最终可促进相关基因的转录〔14〕。本研究提示,补锌改善NPP小鼠认知功能的机制与调节海马DG区神经元BDNF表达有关。
4 参考文献
1McCracken LM,Iverson GL.Predicting complaints of impaired cognitive functioning in patients with chronic pain〔J〕.J Pain Symptom Manage,2001;21:392-6.
2Dick BD,Rashiq S.Disruption of attention and working memory traces in individuals with chronic pain〔J〕.Anesth Analg,2007;104:1223-9.
3Casanova JR,Nishimura M,Swann JW.The effects of early-life seizures on hippocampal dendrite development and later-life learning and memory〔J〕.Brain Res Bull,2014;103:39-48.
4Hu YF,Yang JJ,Hu YP,etal.Involvement of the NMDA receptor in learning and memory in rats with neuropathic pain〔J〕.Eur J Anaesthesiol,2010;27(2):162-8.
5Mirzayi M,Hekmatshoar H.Study of electrical conductivity and memory switching in the zinc-vanadium-phosphate glasses-Physica〔J〕.B Condensed Matter,2013;420:70-3.
6Tahmasebi Boroujeni S,Naghdi N,Shahbazi M,etal.The effect of severe zinc deficiency and zinc supplement on spatial learning and memory〔J〕.Biol Trace Element Res,2009;130(1):48-61.
7王月静,张海燕,廉 洁,等.锌对疼痛后学习记忆障碍小鼠海马神经元P53蛋白表达的影响〔J〕.解剖学报,2015;46(4):455-61.
8Merighi A,Salio C,Ghirri A,etal.BDNF as a pain modulator〔J〕.Prog Neurobiol,2008;85(3):297-317.
9Blugeot A,Rivat C,Bouvier E,etal.Vulnerability to depression:from brain neuroplasticity to identification of biomarkers〔J〕.Neuroscience,2011;31(36):12889-99.
10Li CQ,Xu JM,Liu D,etal.Brain derived neurotrophic factor (BDNF)contributes to the pain hypersensitivity following surgical incision in the rats〔J〕.Mol Pain,2008;4(27):1-11.
11Pezet S,Malcangio M,McMahon SB.BDNF:a neuromodulator in nociceptive pathways〔J〕?Brain Res Brain Res Rev,2002;40(1-3):240-9.
12Ma YL,Wang HL,Wu HC,etal.Brain-derived neurotrophic factor antisense oligonucleotide impairs memory retention and inhibits long-term potentiationin rats〔J〕.Neuroscience,1998;82(4):957-67.
13Tezuka T,Umemori H,Akiyaa T,etal.PSD-95 promotes Fyn mediated tyrosine phorylation of the N methyl-D-aspartate receptor subunit NR2A〔J〕.Proc Natl Acad Sci USA,1999;96:435-40.
14Meng Y,Xu H,Wang R,etal.Impairment of singal transduction pathway on neuronal survival in brains of Alzheimers disease〔J〕.Chin J Pathol,2002;31(6):502-5.
