羟丙基-β-环糊精包合艾纳香挥发油的制备工艺研究
2018-06-22冯树丹李昀桦
易 琼,冯树丹,李昀桦,王 鲁*
(1.贵州大学 贵州省生化工程中心,贵州 贵阳 550025;2.贵州大学 药学院,贵州 贵阳 550025)
艾纳香挥发油是艾纳香植物在精制艾片过程中所产生的一种挥发油物质,许多研究表明艾纳香挥发油具有显著的药理学活性,其抗菌、消炎,镇痛,组织修复等作用显著,发展前景广大[1-3]。其常温为液体,容易挥发,水溶解度小,致使其剂型选择较为局限,生物利用度也不高,制约了其推广应用[4]。因此,针对其现代生物药剂学应用上的不足,寻求一种适用于艾纳香油的新剂型辅料,具有重要的临床意义。有报道利用聚乙二醇为辅料将其制成口含滴丸用于急慢性咽炎的防治[5],但艾纳香挥发油-羟丙基-β-环糊精(HP-β-CD)包合物的制备还未见报道。HP-β-CD是一种水溶性极好(75 g/100ml), 热稳定性好, 且无刺激性、无溶血作用的医用辅料。它可将艾纳香挥发油包合使其固化,增加药物稳定性, 改善药物溶解度,提高其生物利用度,便于加入不同的基质或敷料中制成各种剂型,拓展其应用范围。因此,本实验室以自制黔产的艾纳香油为研究对象,运用新型包合技术,以提高艾纳香油的水溶性和稳定性为目的,采用饱和水溶液法进行正交实验,制备艾纳香挥发油/ HP-β-CD 精包合物,为下一步艾纳香挥发油新制剂的研发提供数据参考。
1 材料与方法
1.1 仪器
JB-3A型磁力搅拌器(上海司乐仪器厂);触点式温度计(上海医用仪器厂);MultiskanGo型全波段酶标仪(Thermo 公司);冷冻干燥机(美国LABCONCO公司);WHF-203B三用紫外分析仪(上海精科实业有限公司)。
1.2 试剂
2-羟丙基-β-环糊精(HP-β-CD)(粉末型,纯度97%)(阿拉丁有限公司);艾纳香挥发油(贵州大学生化工程中心自制);其余试剂均为分析纯。
1.3 方法
1.3.1艾纳香挥发油的制备 称取艾纳香叶50 g,粉碎,过40目筛,放入1000 mL 圆底烧瓶中,加入10 倍的纯水,浸泡1.5 h,然后根据文献[6]和《中国药典》2015 年版一部附录XD 挥发油测定方法操作[7],安装挥发油提取器,采用蒸馏法工艺加热提取5 h,再用无水硫酸钠干燥即可。
1.3.2艾纳香挥发油包合研究
1.3.2.1 正交试验设计 通过前期查阅大量文[8-10]和反复预实验,初步确定影响艾纳香挥发油包合的主要因素有:艾纳香挥发油与HP-β-CD 之间的投料比、包合时间、包合温度等,采用L9( 34)正交试验,以包合物油利用率、包合物含油率以及包合物产率为指标,对这3个因素进行考察,因素水平见表1。

表1 因素水平表Tab.1 orthogonal factor level table
1.3.2.2 艾纳香挥发油-HP-β-CD包合工艺 采用饱和水溶液法[11],取适量HP-β-CD于圆底烧瓶中, 根据其溶解度加入一定量的水,使其溶解制备为HP-β-CD饱和水溶液,加入转子后将其置于恒温搅拌器上的水浴锅中保持包合温度恒定,再用胶头滴管吸取少量艾纳香油-乙醇溶液[50%(v/v)],缓慢加入到圆底烧瓶中,分次缓慢加入。为了防止艾纳香油挥发,在圆底烧瓶上安装一个冷凝回流装置,开始计时并将溶液在恒温条件下搅拌一定时间,冷却至室温后置于冰箱中静置24 h,滤过,再用石油醚洗涤(洗涤3次,每次10 ml), 室温放置并自然挥干约30 min,使其残留的有机溶剂挥发后,置于冷冻干燥机中干燥,即得艾纳香挥发油-HP-β-CD包合物。
1.3.2.3 挥发油空白回收试验 根据2015年版《中华人民共和国药典》(四部)附录ⅩD 项下挥发油测定法[7],选取甲法测定,精密量取艾纳香油一定量,置于500 mL的圆底烧瓶中,加水300~500 ml与沸石数粒,振摇混合后,按图所示装置连接好,加热微沸5 h,至测定器中油量不再增加,停止加热,放置片刻,读取挥发油量,并计算供试品中挥发油的含量(%)。
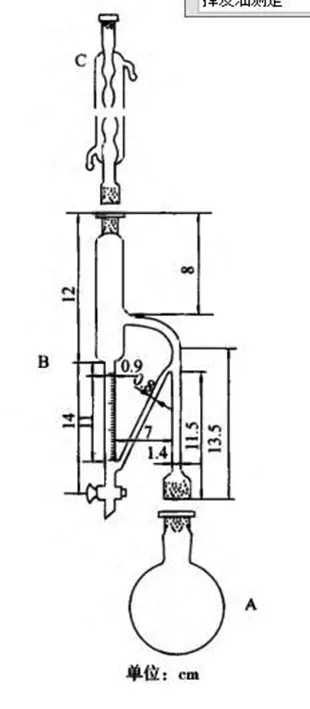
图1 挥发油检测装置Fig.1 Blumea balsamifera volatile Oil
1.3.2.4 包合物挥发油利用率、含油率及包合物产率的测定 取干燥包合物精密称质量,置圆底烧瓶中,加蒸馏水300 mL,连接挥发油测定器,微沸并保持4.5 h,至油量不再增加时停止加热,放置0.5 h,至挥发油呈淡黄色时读数,得到挥发油体积。按下列公式计算包合物油利用率、包合物含油率以及包合物产率。为了便于结果的分析比较,将包合物油利用率、包合物含油率以及包合物产率合并为综合评分,正交试验结果见表3。最后对实验结果进行统计分析,评价各因素对综合评分的影响,最终确定最佳工艺条件。
包合物油利用率(%)即包合率 =[包合物中艾纳香油的量(mL)/(艾纳香油投料量(mL)×空白回收率)]×100%
包合物含油率(%)=[(包合物含油量(mL)×艾纳香油密度(g/ml))/包合物重量(g)]×100%
包合物产率(%)=[干燥后包合物重量(mL)/(HP-β-CD投料量(g)+艾纳香油投料量(mL))]×100%
综合评分=包合物产率×0.3+包合物油利用率×0.5+包合物含油率×0.2
1.3.2.5 验证实验 根据上述正交实验结果,选取最佳包合工艺,取挥发油适量进行验证,经6 次平行实验验证重复性。
1.3.3包合物的质量鉴定
1.3.3.1 薄层色谱法(TCL) 采用TLC法对艾纳香挥发油包合前后的化学性质进行验证[12-13]。分别制备下列供试品溶液。供试品1:称取HP-β-CD 0.1 g,加入蒸馏水1 mL,震荡混匀即可;供试品2:取100 μL艾纳香挥发油与HP-β-CD1 mg混合,再加入无水乙醇1 mL,震荡混匀后再用0.22 μm的滤芯过滤;供试品3:取适量的艾纳香挥发油-HP-β-CD包合物溶液;供试品4:取100 μL的艾纳香挥发油,加入乙酸乙酯1 mL稀释并混匀;供试品5:取适量的艾纳香挥发油-HP-β-CD包合物,装入500 mL放入沸石的圆底烧瓶中,加入300 mL蒸馏水,并连接挥发油提取器,冷凝回流至油量不再增加为止,将提取出的艾纳香挥发油100 μL加入乙酸乙酯1 mL稀释并摇匀;分别将上述供试品溶液用毛细管分别点于同一254 nm薄层荧光板上,以乙酸乙酯 -石油醚(1∶8)为展开剂,将板置于展开槽中展开,挥干溶剂,观察结果。
1.3.3.2 紫外扫描法(UV) 参考文献[13-14]分别取适量1.3.3.1中的供试品1、2、3、4溶液,置于紫外分光光度计中,在 190~400 nm范围内进行紫外扫描,测定吸光度结果。
2 结果与分析
2.1 艾纳香挥发油的提取
参照文献方法可提取到艾纳香油,收油率为3.14%,挥发油为淡黄色透明油状物,具有特殊浓郁香味,如图2所示。

图2 艾纳香油提取物Fig.2 Blumea balsamifera volatile Oil detector
2.2 艾纳香挥发油包合研究
2.2.1艾纳香油空白回收试验 取3组空白试验取其平均值,测得艾纳香挥发油空白回收率为86.67%,取样量及馏出量见表2。

表2 艾纳香挥发油取样量及馏出量Tab.2 The solution and distillate of Blumea balsamifera volatile oil
2.2.2最佳工艺条件的筛选 根据极差R的大小,可以判断各因素对试验指标的影响主次。该正交试验极差R计算结果见表3,比较各R值大小,对于包合物产率、艾纳香油的油利用率和综合评分方面来说,RA>RB>RC,而对于包合物制备过程的含油率来说RB>RC>RA,所以因素对试验指标影响的主次顺序为A、B、C, 即艾纳香油与环糊精的比例对包合物的综合影响最大,温度其次,搅拌时间影响最小。经方差分析结果表明,羟丙基-β-环糊精与艾纳香油的投料量比例(即因素A)对油利用率和综合评分有显著影响,而其他因素对包合工艺的实验结果影响不显著。综合以上数据分析,直观分析和方差分析结果,确定最佳工艺条件为A3B2C1,即艾纳香油:HP-β-CD为1∶8,搅拌温度为50℃,搅拌时间3 h。

表3 艾纳香油-HP-β-CD包合工艺正交试验安排Tab.3 Orthogonal experiment L9(34) of Blumea balsamifera volatile oil-HP-β-CD inclusion technology

表4 以综合评分为指标的方差分析表Tab.4 The variance analysis table with the comprehensive score as index
F0.01(2,2)=99 F0.05(2,2)=19
2.2.3最佳工艺的验证实验 按照实验2.2.4计算方法,包合物的平均产率为96.85%,平均油利用率为83.78%,平均含油率为8.32%,综合平均得分为72.61,与正交实验设计表中的各项指标最高值相对较近,表明本实验所选取的工艺条件比较好,并且具有一定的可行性和重复性。

表5 最佳工艺重复验证Tab.5 the best technology repeatable validation

图3 左为原样图,右为主要成分标记图Fig.3 The left is the original ,and the right is the main component
2.3 包合物的质量鉴定
2.3.1薄层色谱法(TCL) 结果如图3所示,供试品1和供试品3不显斑点,而供试品2、供试品4和供试品5显示相同的斑点,相对供试品2和供试品4,供试品5显示斑点较弱,可能是馏出油的含量或成分发生了一些微小变化,综合结果分析表明,艾纳香油已嵌入 HP-β-CD的空穴结构中形成了包合物,因此供试品3不显示斑点,而供试品2、4、5斑点一致说明包合前后艾纳香油的性质并未发生明显改变,主成分也未发生较大变化。达到包合目的。
2.3.2紫外扫描法(UV) 结果如图4所示,HP-β-CD溶液没有艾纳香挥发油的特征吸收,表明HP-β-CD 对测定无干扰,艾纳香挥发油-HP-β-CD 混合物、艾纳香油、艾纳香油-HP-β-CD包合物所形成的波谱图基本一致,说明三种溶液具有相似的紫外吸收图谱,并且HP-β-CD包合艾纳香挥发油并未改变艾纳香挥发挥发油的理化性质。

图4 波长扫描图Fig.4 wavelength scanning chart
3 结论与讨论
当前,环糊精包合技术发展已趋于成熟,历年来也有许多HP-β-CD包合挥发油或其他药物的实例,HP-β-CD作为一种安全无毒害的材料以及分子“内疏水外亲水”的特性,已广泛应用于中药挥发油产品的制备,并且加快了医药美容等行业的开发应用,具有相当可观的发展前景[9]。
由正交试验结果可知,影响艾纳香挥发油包合效果的主要因素为艾纳香挥发油与HP-β-CD的比例与包合温度。为了考察这两个关键因素对包合工艺的影响程度,在前期预实验中,在保持其他条件不变的情况下, 对艾纳香油与HP-β-CD的投料比和包合温度分别做了进一步单因素影响实验。实验结果显示, 当HP-β-CD的投料量超过艾纳香油投料量的10倍,包合时温度超过60℃时 ,包合率不仅不再增加, 甚至会出现下降的趋势。投料比影响包合效果的原因可能为HP-β-CD过多时,其自身内部的分子运动阻碍了其对艾纳香挥发油的包合作用;而当HP-β-CD过少时,因艾纳香挥发油过多,超过了HP-β-CD的空穴结构承受范围,导致一部分艾纳香油不能被包合而裸露在外,造成损失引起包合率的降低。包合温度影响包合效果的原因可能为当温度过高时,使得分子的热运动加快,扩散阻力减小,导致分子向外扩散的速度加快, 包合过程中艾纳香油的挥发损失增多导致包合率下降,而包合时间相对来说影响不大。
本研究对艾纳香挥发油包合物采用了TLC、UV等手段进行表征分析,结果证明艾纳香挥发油与HP-β-CD并非简单的物理混合,可能是艾纳香挥发油包合进入了HP-β-CD分子空穴内,形成了一个新物象,即形成包合物,说明本工艺适合艾纳香挥发油包合物的制备,且此工艺操作简单,条件易于控制。并且,HP-β-CD包合挥发油可应用溶液搅拌法、冷冻或喷雾干燥等工艺,易于产业化应用。其包合挥发油类物质,不但增强了药物的稳定性和溶解度,且能提高挥发油类物质的生物利用度,降低药物毒性[8],本研究中,将艾纳香挥发油包合后,由液体药物固体粉末化,便于制成多种剂型, 如可制成中药片剂、胶囊剂、颗粒剂、袋泡剂和喷雾剂、滴眼剂、软膏剂等多种剂型,这为艾纳香挥发油新制剂的进一步开发提供了实验基础。
参 考 文 献:
[1] 易 琼,王玉坤,王 鲁.艾纳香油药理学作用评价[J].黑龙江畜牧兽医,2016(08下):149-151.
[2] 李 璞,陈宇琼,黄火强.艾纳香化学成分与药理活性研究进展[J].实用中医内科杂志,2012,26(10):3-5.
[3] 王 嵩,赵永恒,周毅生,等.艾纳香的研究进展及其研究价值探讨[J].中国现代中药,2014,16(11):953-956.
[4] 玲 亮,庞玉新,王 丹,等.中国民族特色药材艾纳香研究进展[J].植物遗传资源学报2012, 13( 4) : 695-698.
[5] 胡 璇,陈振夏,王 凯,等.艾纳香油质量标准初步研究[J].热带农业科学,2016,36(9):87-91.
[6] 夏 嬿,李 祥,陈建伟.不同提取方法对艾纳香挥发油化学组成的影响及其体外抗氧化活性[J].中成药,2014,36(10):2221-2224.
[7] 中华人民共和国药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2010∶156-157.
[8] 郝晶晶,李海亮,龚慕辛.挥发油环糊精包合技术的研究进展及存在问题分析[J].中国实验方剂学杂志,2013,19(2):352-356.
[9] 叶卯祥,严雪黎.β环糊精包合技术在中药挥发油制剂中的应用研究[J].医学综述,2010,16(24):3793-3796.
[10] 徐 磊,蒋剑平,金 铭,等.温莪术油羟丙基-β-环糊精包合物的制备与表征[J].中华中医药志,2015,30(4):1043-1046.
[11] 冯希勇, 朱小虎, 邢海燕.川芎挥发油的β- 环糊精包合工艺研究[J].现代中药研究与实践,2008,22(6):65-66.
[12] 艾 莉.董英杰.张乃先.等.莪术油-羟丙基-β-环糊精包合物的制备与表征[J].沈阳药科大学学报,2007,24(9):528-531.
[13] 黄秋艳,熊 磊,汪红梅,等.苍艾挥发油-羟丙基-β-环糊精包合物的制备及其表征[J].云南中医学院学报,2016,39(1):27-42.
[14] 朱 缨,俞迪佳.豆蔻挥发油羟丙基-β-环糊精包合物制备工艺的研究[J].世界科学技术—中医药现代化技术应用研究,2013,15(2):317-321.
