非金属元素对Ti- Fe- Mn合金储氢性能的影响
2018-05-29冷海燕
时 雨 尹 杰 冷海燕
(省部共建高品质特殊钢冶金与制备国家重点实验室、上海市钢铁冶金新技术开发应用重点实验室和上海大学材料科学与工程学院,上海 200072)
自从Reilly和Wiswall[1]报道以来,TiFe合金由于其优异的吸放氢动力学性能、室温下较高的吸氢量以及低廉的价格而被广泛研究。然而,TiFe合金在室温下吸放氢前先需要在高温下进行严格的活化处理限制了其广泛应用[1]。目前研究者们采用了多种方法来解决活化困难的问题,其中最常见的是采用过渡族元素(Zr、Mn、Ni、Co和Cr等)替代TiFe合金中的Ti或Fe元素[2- 4]。也有研究者研究了各种添加剂,如Mg和Zr7Ni10对TiFe合金储氢性能的影响[5- 6]。另外,还有研究者通过高压扭转形成大塑性变形来充分活化TiFe合金[7- 8]。
相比之下,元素替代是提高TiFe合金储氢性能最有效且经济方便的方法之一。例如,当采用少量的Mn替代TiFe合金中的Fe后,样品不需要活化过程,同时还提高了对杂质的抗性[3,9]。但Mn的添加使得合金的平台压降低,平台斜率增大,导致有效可逆储氢量降低。
此外,有研究者探究了非金属元素的添加对储氢合金吸氢性能的影响。Shen等[10]研究了间隙原子B和C对Ti25V35Cr40合金储氢性能的影响,发现间隙位置掺杂的B或C可以降低晶格中氢原子的稳定性,进而导致第二个平台压升高及有效放氢量降低。Morita等[11]发现,在Ti- Mn Laves相合金中添加B可以大幅度提高平台压及平台斜率因子,并认为这可能是由于富锰颗粒的出现所导致的。Yan等[12]发现,在BCC型V30Ti35Cr25Fe10合金中添加Si可以形成Laves相进而提高合金的活化性能。但到目前为止,鲜有非金属元素对Ti- Fe- Mn合金储氢性能影响的报道。此外,考虑到在合金的大规模熔炼过程中,原材料或制备过程中不可避免地含有一些非金属杂质,其中尤以C、Si等最为明显,因此开展这方面的研究对TiFe合金大规模的应用也有积极作用。
本文主要研究了非金属元素B、C和Si的添加对TiFe0.8Mn0.2合金储氢性能及微观组织的影响,并探究了其对合金吸放氢平台及活化性能的影响。
1 试验材料与方法
TiFe0.8Mn0.2Mx(x=0,0.02,0.04,0.06;M=C,B,Si)合金采用氩气保护的磁悬浮熔炼技术制成,各组元的纯度均高于99.9%。为确保铸锭成分均匀,合金翻转重熔3次。所有合金均未进行热处理。采用D/max 2550型X射线衍射仪(Cu- Kα)分析合金的相组成。采用SU- 1510型扫描电子显微镜观察合金的物相形貌,并结合EDX能谱仪分析物相中各元素含量。
采用日本铃木公司的SUZUKI测试平台测定合金的活化性能及压力- 组成- 温度曲线(P- C- isotherm曲线)。活化性能测试在353 K和4 MPa初始氢压下进行。合金完全活化后进行P- C- isotherm曲线测试,测试温度为333 K。
2 试验结果与讨论
2.1 微观组织
图1为TiFe0.8Mn0.2Mx(x=0,0.02,0.04,0.06;M=B,C,Si)合金的XRD图谱。可以看出,TiFe0.8Mn0.2合金主要由TiFe主相以及少量的TiMn1.5Laves相和富Ti相组成,其中富Ti相的XRD主强峰与TiMn1.5Laves相重合,结合SEM及EDX能谱分析可以区分二者。这一结果与Lee等的报道[3]一致。TiFe0.8Mn0.2B0.02合金与TiFe0.8- Mn0.2合金物相组成一致。随着B含量的增加,TiFe0.8Mn0.2B0.04、TiFe0.8Mn0.2B0.06合金中出现了Ti2Fe相。在TiFe0.8Mn0.2Cx(x=0.02,0.04,0.06)合金中除了TiFe主相以及TiMn1.5Laves相和富Ti相外,还生成了TiC相,其含量随着C含量的增加逐渐增加。与B和C不同,Si的掺杂并未使合金的XRD图谱中出现新相,但结合SEM结果(见图3)发现合金中仍存在富Ti相,并且其含量随着Si含量的增加而增加。在TiFe0.8Mn0.2- Mx合金中TiMn1.5Laves相的含量均随着B、C和Si含量的增加而增加,尤其是TiFe0.8Mn0.2Six合金中,TiMn1.5Laves相的含量最多。
对XRD数据进行分析,得出各合金中主相TiFe相的晶格常数随B、C和Si的添加量的变化规律,如图2所示。可以看出,B和C的添加均使得合金中TiFe相的晶格常数减小,而Si的添加对TiFe相的晶格常数影响不大。从化学计量比的角度分析,TiFe0.8Mn0.2合金中形成的TiMn1.5Laves相必然会导致合金中Ti含量富余,这些富余的Ti部分以富Ti相的形式存在,部分置换TiFe相中的Fe,固溶于TiFe相中,因此TiFe0.8Mn0.2合金中TiFe相的晶格常数(2.983 5Å)大于纯TiFe相的晶格常数(2.976 0 Å)。B和C的添加分别使合金中形成了Ti2Fe相和TiC相,从而消耗了合金中的Ti,使得TiFe相中固溶Ti含量随B和C含量的增加而逐渐降低,导致TiFe相的晶格常数亦随之降低。而Si的添加使得合金中富Ti相和TiMn1.5Laves相增多,但这并未降低TiFe相中固溶Ti含量,因此TiFe相的晶格常数变化不大。
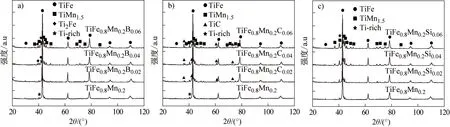
图1 (a)TiFe0.8Mn0.2Bx、(b)TiFe0.8Mn0.2Cx和(c)TiFe0.8Mn0.2Six铸态合金的XRD图谱(x=0,0.02,0.04,0.06)Fig.1 XRD patterns of the as- cast samples of (a) TiFe0.8Mn0.2Bx , (b) TiFe0.8Mn0.2Cx and (c) TiFe0.8Mn0.2Six alloys (x=0, 0.02, 0.04, 0.06)
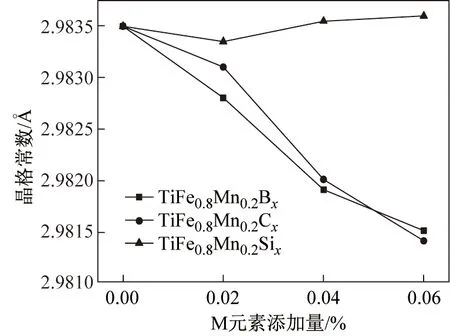
图2 TiFe0.8Mn0.2Mx(M=B,C,Si;x=0,0.02,0.04,0.06)合金中TiFe相的晶格常数与M含量的关系Fig.2 Relationship between the content of M and the lattice parameter of TiFe phase in TiFe0.8Mn0.2Mx(M=B,C,Si; x=0,0.02,0.04,0.06) alloys
图3是铸态TiFe0.8Mn0.2、TiFe0.8Mn0.2B0.06、TiFe0.8Mn0.2C0.06和TiFe0.8Mn0.2Si0.06合金的SEM形貌。可见,TiFe0.8Mn0.2合金由TiFe相、TiMn1.5Laves相和富Ti相组成,其中富Ti相呈颗粒状随机分布在基体TiFe相中,TiMn1.5Laves相不连续地分布在基体上。TiFe0.8Mn0.2B0.06合金由TiFe相、TiMn1.5Laves相和Ti2Fe相组成,其中Ti2Fe相主要呈细小颗粒状分布在晶界上,TiMn1.5Laves相分散地分布在基体中。TiFe0.8Mn0.2C0.06合金主要由TiFe相、TiMn1.5相和TiC相组成,其中TiC相呈较大的球状随机分布在基体中,TiMn1.5Laves相分散地分布在基体中。TiFe0.8Mn0.2Si0.06合金与TiFe0.8Mn0.2合金类似,由TiFe相、TiMn1.5Laves相和富Ti相组成,并且第二相的形态和分布也类似;同时可以看出,相比于TiFe0.8Mn0.2合金,TiFe0.8Mn0.2Si0.06合金中富Ti相和TiMn1.5Laves相的数量有所增加。
2.2 活化性能
图4是TiFe0.8Mn0.2Mx(x=0,0.02,0.04,0.06;M=C,B,Si)合金在4 MPa初始氢压及353 K下的首次吸氢曲线。从图4(a)中可以看出,TiFe0.8Mn0.2B0.02合金的活化性能较TiFe0.8Mn0.2合金差, 这可能是由于B原子占据晶格中的间隙位置从而对氢原子的扩散造成阻碍所致。当xB>0.02时,TiFe0.8Mn0.2B0.04和TiFe0.8Mn0.2B0.06合金的活化性能又得到提升,但仍低于TiFe0.8Mn0.2合金。分析XRD结果可知,在TiFe0.8Mn0.2B0.04和TiFe0.8Mn0.2B0.06合金中出现了Ti2Fe相。有研究认为,Ti2Fe相是在低于1 273 K时通过共晶转变(β- Ti+TiFe→Ti2Fe)而形成的[13]。当温度低于773 K时,在较低冷速下,Ti2Fe相会发生共析转变(Ti2Fe→β- Ti+TiFe)而分解。Polanski等[14]研究发现,在采用激光近净成形技术沉积过程中,由于快速冷却,在有些Ti- Fe合金中仍保留了淬火组织,如Ti2Fe相。但在TiFe0.8Mn0.2合金中并未发现Ti2Fe相,这表明在该合金中Ti2Fe相的形成依赖于B的添加。有研究者证实,氧的存在也会促进亚稳Ti2Fe相的形成[15]。因此,B的存在可能具有类似于氧的作用而使得Ti2Fe相在室温下能够稳定存在。此外,Ti2Fe和TiMn1.5相的含量随着B含量的增加而增加。具有优异活化性能、脆性大的TiMn1.5相的增多可以提高合金的活化性能;但Ti2Fe相的出现会阻碍氢在合金中的扩散[10]。因此TiFe0.8Mn0.2B0.04和TiFe0.8Mn0.2B0.06合金的活化性能优于TiFe0.8Mn0.2B0.02合金,却比TiFe0.8Mn0.2合金差。

图3 (a)TiFe0.8Mn0.2、(b)TiFe0.8Mn0.2B0.06、(c)TiFe0.8Mn0.2C0.06和(d)TiFe0.8Mn0.2Si0.06合金的SEM形貌Fig.3 SEM morphologies of (a) TiFe0.8Mn0.2, (b) TiFe0.8Mn0.2B0.06,(c) TiFe0.8Mn0.2C0.06 and (d) TiFe0.8Mn0.2Si0.06 alloys
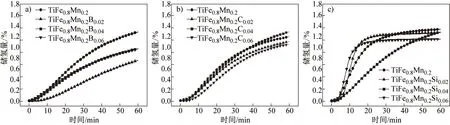
图4 (a)TiFe0.8Mn0.2Bx、(b)TiFe0.8Mn0.2Cx和(c)TiFe0.8Mn0.2Six(x=0,0.02,0.04,0.06)合金在353 K、4 MPa下的首次吸氢曲线Fig.4 Initial hydrogen absorption curves of (a) TiFe0.8Mn0.2Bx, (b) TiFe0.8Mn0.2Cx and (c) TiFe0.8Mn0.2Six alloys(x=0,0.02,0.04,0.06)for the activation at 4 MPa H2 and 353 K
如图4(b)所示,TiFe0.8Mn0.2Cx(x= 0.02, 0.04,0.06)合金的活化性能与TiFe0.8Mn0.2合金相似。通过图1(b)可见,TiC和TiMn1.5相的含量随着C含量的增加而增加,且TiMn1.5相可以提高合金的活化性能,而添加C之后合金的活化性能变化不大,因此TiC相可能会降低合金的活化性能。
Si的添加使得TiFe0.8Mn0.2Six(x= 0.02, 0.04,0.06)合金的活化性能得到了显著提升,由图4(c)可见,随着Si含量的增加,合金完全吸氢的时间逐渐减少。由XRD及SEM分析可知,添加Si的合金中存在TiMn1.5相和富Ti相,同时TiMn1.5相含量随着Si含量的增加显著增加。因此,TiFe0.8Mn0.2Six(x=0.02,0.04,0.06)合金活化性能的提升可能是由于TiMn1.5相的显著增加所导致的。此外,少量富Ti相对活化性能的提升也有一定促进作用。有研究发现[16- 17],β- Ti会优先于TiFe相吸氢形成TiH2,从而导致合金中形成大量的微裂纹和形核位点,进而促进TiFe相的吸氢反应。
2.3 储氢性能
图5为TiFe0.8Mn0.2Bx(x=0,0.02,0.04,0.06)合金在333 K下的P- C- isotherm曲线。由曲线可以看出,TiFe0.8Mn0.2合金具有两个倾斜的吸放氢平台。B的添加使得合金的第一个平台变得平坦,同时平台压略微升高。放氢平台的斜率因子定义为P1/P2,其中P1和P2分别是储氢量(质量分数,下同)为0.3%和0.8%时的分解压。如表1所示,随着B含量的增加,放氢平台的斜率因子由0.384增加至0.602。但是第二个平台的斜率并未发生明显改变,同时平台压也随着B的增加逐渐升高,最终导致最大储氢量的降低。随着B含量的增加,第一个平台压基本不变,第二个平台压升高,合金的最大储氢量降低。其原因可能是:首先,Ti2Fe相几乎不吸氢;其次,部分硼原子占据了晶格中氢原子的位置。例如TiFe0.8Mn0.2B0.02合金的最大储氢量由未添加B时的1.694%降至1.575%,但其放氢平台的斜率因子由0.384提高到了0.595,这使得合金的有效放氢量增加。有效放氢量由式(1)确定:
有效放氢量=W1-W2
(1)
式中:W1和W2分别是放氢压为4和0.2 MPa时的含氢量。因此,TiFe0.8Mn0.2B0.02合金的有效放氢量仅比TiFe0.8Mn0.2合金少了0.022%,远小于最大储氢量的降低值。
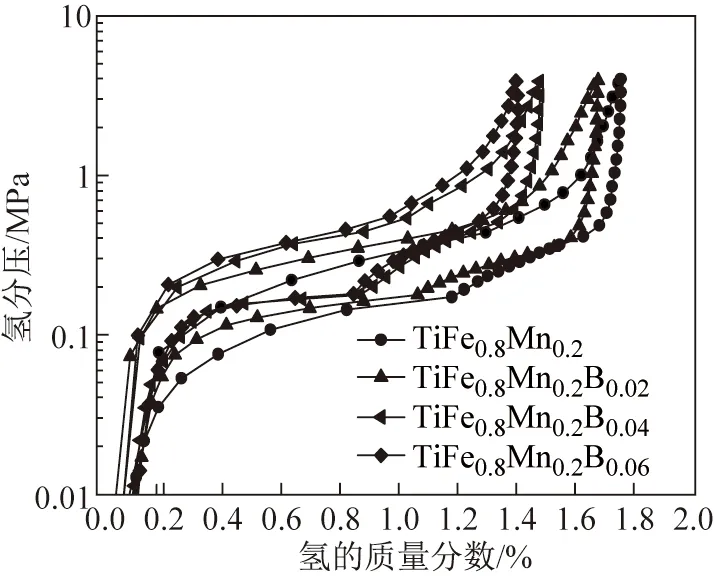
图5 TiFe0.8Mn0.2Bx(x= 0, 0.02, 0.04, 0.06)合金在333 K下的P- C- isotherm曲线Fig.5 P- C- isotherm curves of TiFe0.8Mn0.2Bx(x= 0, 0.02, 0.04, 0.06) alloys at 333 K
图6为TiFe0.8Mn0.2Cx(x=0,0.02,0.04,0.06)合金333 K下的P- C- isotherm曲线。C的添加使得P- C- isotherm曲线的第一个平台压略微升高,同时平台变得更加平坦。如表1所示,随着C含量的增加,放氢平台的斜率因子从0.384提高至0.683。与TiFe0.8Mn0.2合金类似,随着C含量的增加,TiFe0.8Mn0.2Cx合金P- C- isotherm曲线的第二个平台压也升高,导致最大储氢量的降低。TiFe0.8Mn0.2Cx合金中TiC相几乎不吸氢,同时部分碳原子占据了氢原子的间隙位置,因此导致合金的吸氢量降低。同时,随着添加量x由0增加至0.06,合金的有效放氢量从1.393%减少至1.147%。
TiFe0.8Mn0.2Six(x=0,0.02,0.04,0.06)合金在333 K下的P- C- isotherm曲线如图7所示。从图中可以看出,TiFe0.8Mn0.2Six合金的第一个吸放氢平台的平台压及放氢平台的倾斜度均几乎与TiFe0.8Mn0.2合金一致。但是第二个吸氢平台的平台压随着Si含量的增加而升高。合金最大储氢量随着Si掺杂量的增加而降低,这可能是因为随着Si的添加,形成了富Ti相,该相形成稳定的TiH2后在室温不分解放氢,使得储氢量降低;另外,第二个平台压的升高也会导致最大储氢量的降低。随着掺杂量x从0增加至0.06,合金的有效放氢量从1.393%降低至1.000%。
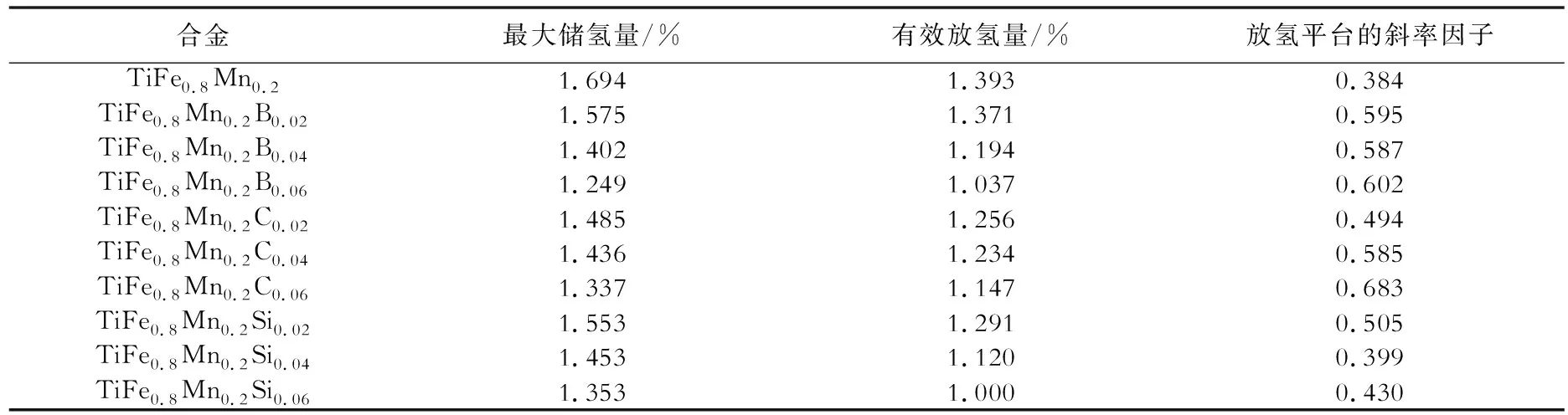
表1 TiFe0.8Mn0.2Mx合金在333 K、4 MPa下的储氢特性Table 1 Hydrogen storing behavior properties of TiFe0.8Mn0.2Mxalloys at 4 MPa H2 and 333 K
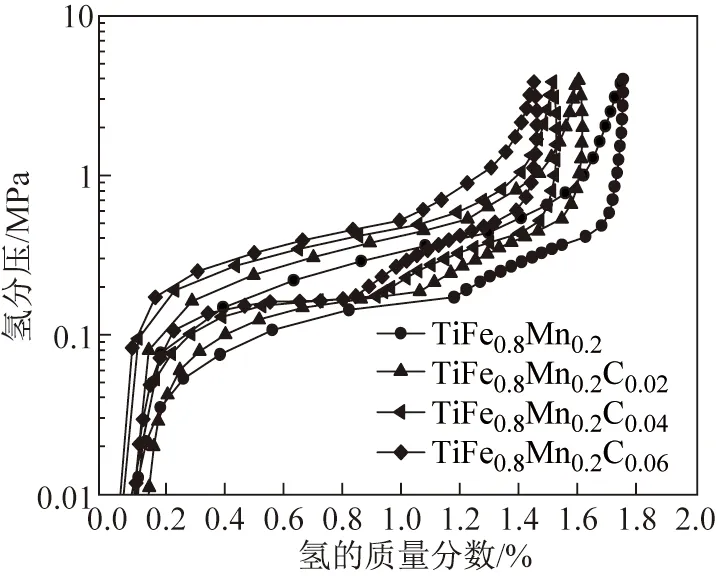
图6 TiFe0.8Mn0.2Cx(x= 0, 0.02, 0.04, 0.06)合金在333 K下的P- C- isotherm曲线Fig.6 P- C- isotherm curves of TiFe0.8Mn0.2Cx(x= 0, 0.02, 0.04, 0.06) alloys at 333 K

图7 TiFe0.8Mn0.2Six(x= 0, 0.02, 0.04, 0.06)合金在333 K下的P- C- isotherm曲线Fig.7 P- C- isotherm curves of TiFe0.8Mn0.2Six(x= 0, 0.02, 0.04, 0.06) alloys at 333 K
对于TiFe0.8Mn0.2合金,当分别掺杂B、C和Si 3种元素后,合金的最大储氢量都随着掺杂元素含量的增加而降低,但是其放氢平台的斜率因子却随着B和C含量的增加而逐渐减小,且Si的掺杂并未使得合金放氢平台的平坦度发生明显变化。如2.1节所述,B和C的添加均使得合金中TiFe相的晶格常数减小,这主要是由于B和C的添加分别使合金中形成了Ti2Fe和TiC相,从而消耗了合金TiFe相中固溶的Ti含量所致。TiFe相中固溶Ti含量的减少使得合金间隙位置的化学势更“均匀、统一”,因此随着B和C含量的增加,TiFe0.8Mn0.2Bx和TiFe0.8Mn0.2Cx合金的第一个放氢平台逐渐变得平坦。而对于TiFe0.8Mn0.2Six合金,Si的添加并未明显改变合金主相TiFe相的晶格常数,说明TiFe相中固溶Ti的含量也未发生变化,因此其PCT曲线具有和TiFe0.8Mn0.2合金类似的放氢平台。
3 结论
(1)Si的添加使得TiFe0.8Mn0.2合金中TiMn1.5相的含量增加,同时形成富Ti相,从而提高了TiFe0.8Mn0.2合金的活化性能。但是Si的掺杂未使得TiFe主相中固溶Ti的含量发生明显变化,因此合金第一个吸放氢平台的斜率变化不大。
(2)B和C的添加分别使合金中生成了Ti2Fe相和TiC相,这两相会阻碍氢的扩散,因此B和C的添加未能提高TiFe0.8Mn0.2合金的活化性能。
(3)Ti2Fe相和TiC相的形成降低了TiFe主相中固溶Ti的含量,而固溶Ti的存在是导致合金吸放氢平台倾斜的主要原因。因此随着B和C含量的增加,合金的第一个吸放氢平台变得更加平坦,这有利于改善合金的有效放氢容量。
(4)3种元素的添加均会导致合金第二个平台压的升高,并生成不吸氢的Ti2Fe相和TiC相,或生成稳定氢化物的富Ti相,因此导致了TiFe0.8Mn0.2合金最大储氢量的降低。
[1] REILLY J J, WISWALLJR R H. Formation and properties of iron titanium hydride[J]. Inorganic Chemistry,1974, 13(1):77- 112.
[2] JANG T H, HAN J I, LEE J Y. Effect of substitution of titanium by zirconium in TiFe on hydrogenation properties[J]. Journal of the Less Common Metals, 1986, 119(2):237- 246.
[3] LEE S M, PERNG T P. Effect of the second phase on the initiation of hydrogenation of TiFe1-xMx(M= Cr, Mn) alloys[J]. International Journal of Hydrogen Energy,1994, 19(3):259- 263.
[4] SINGH B K, SINGH A K, SRIVASTAVA O N. On the synthesis, characterization and hydrogenation behaviour of Fe1-x- Ti1+yNix(x=0.2,y=0.3) hydrogen storage material[J]. International Journal of Hydrogen Energy, 1997, 22(8):805- 808.
[5] MANDAL P, SRIVASTAVA O N. Hydrogenation behaviour of the new composite storage material Mg-x% FeTi[J]. Journal of Alloys and Compounds,1994, 205(1/2):111- 118.
[6] JAIN P, GOSSELIN C, SKRYABINA N, et al. Hydrogenation properties of TiFe with Zr7Ni10alloy as additive[J]. Journal of Alloys and Compounds, 2015, 636:375- 380.
[7] EDALATI K, MATSUDA J, YANAGIDA A, et al. Activation of TiFe for hydrogen storage by plastic deformation using groove rolling and high- pressure torsion: Similarities and differences[J]. International Journal of Hydrogen Energy, 2014, 39(28):15589- 15594.
[8] EDALATI K, MATSUDA J, IWAOKA H, et al. High- pressure torsion of TiFe intermetallics for activation of hydrogen storage at room temperature with heterogeneous nanostructure[J]. International Journal of Hydrogen Energy,2013, 38(11):4622- 4627.
[9] SANDROCK G D, GOODELL P D. Surface poisoning of LaNi5, FeTi and (Fe,Mn)Ti by O2, CO and H2O[J]. Journal of the Less Common Metals,1980, 73(1):161- 168.
[10] SHEN C C, CHOU C P, LI H C, et al. Effect of interstitial boron and carbon on the hydrogenation properties of Ti25V35Cr40alloy[J]. International Journal of Hydrogen Energy,2010, 35(21):11975- 11980.
[11] MORITA Y, GAMO T, KURANAKA S. Effects of nonmetal addition on hydriding properties for Ti- Mn Laves phase alloys[J]. Journal of Alloys and Compounds,1997, 253(6):29- 33.
[12] YAN Y G, CHEN Y G, LIANG H, et al. The effect of Si on V30Ti35Cr25Fe10BCC hydrogen storage alloy[J]. Journal of Alloys and Compounds, 2007, 441(1/2):297- 300.
[13] BATALU D, COSMELEATA G,ALOMAN A. Critical analysis of the Ti- Fe phase diagrams[J]. Upb Scientific Bulletin ,2006,68(4):77- 90.
[14] POLANSKI M, KWIATKOWSKA M, KUNCE I, et al. Combinatorial synthesis of alloy libraries with a progressive composition gradient using laser engineered net shaping (LENS): Hydrogen storage alloys[J]. International Journal of Hydrogen Energy,2013, 38(27):12159- 12171.
[15] LIN Y C, SHTEINBERG A S, MCGINN P J, et al. Kinetics study in Ti- Fe2O3system by electro- thermal explosion method[J]. International Journal of Thermal Sciences,2014, 84(4):369- 378.
[16] LEE S M, PERNG T P. Microstructural correlations with the hydrogenation kinetics of FeTi1+xalloys[J]. Journal of Alloys and Compounds,1991, 177(1):107- 118.
[17] MATSUMOTO T, AMANO M, SASAKI Y. Hydrogenation of FeTi- based alloys containing β- Ti[J]. Journal of the Less Common Metals, 1982, 88(92):443- 449.
