2-吡啶酮肟的合成
2018-03-22牛学丽
牛学丽 ,刘 志 ,杨 华
(1.聊城大学 山东省化学储能与新型电池技术重点实验室,山东 聊城 252059;2.晋城职业技术学院 化工系,山西 晋城 048026)
吡啶酮是一种应用很广泛的化工原料,它可以作为合成利尿药物托拉塞米或其他药物中间体,因此很多吡啶酮及其衍生物被合成[1-2]。由于肟基非常适合与金属参与配位,因此吡啶酮肟引起了化学工作者的极大研究兴趣。吡啶酮肟的衍生物与金属形成了多变的拓扑结构[3-4],以及单分子磁体[5]。
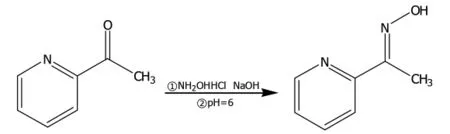
图1:反应方程式Figure 1:The Reaction Equation
1 实验部分
1.1 主要仪器与试剂
Nicolet-460型红外光谱仪(KBr压片,扫描范围 400-4000 cm-1)、Mercurry Plus-400 型核共振波谱仪、X-4数字显示显微熔点测定仪 (未经校正)、ZNCL-GS型油浴电磁搅拌仪、HJ-6型多头磁力搅拌器、Perkin-Elmer2400II型元素分析仪。
2-乙酰吡啶、盐酸羟胺、氢氧化钠、盐酸等试剂和溶剂均为市售分析纯,且使用时未作进一步纯化处理。
1.2 实验步骤
将氢氧化钠和盐酸羟胺按2:1的摩尔比混合,冰浴条件下,用一定量的水溶解。将此溶液缓慢滴加到与盐酸羟胺等摩尔量的2-乙酰吡啶的水溶液中,室温搅拌一段时间,后用稀盐酸酸化,得粉色固体,抽滤,干燥得目标化合物。
2 结果与讨论
2.1 温度对产率的影响
试验了不同温度下反应,产率随温度升高略微有些降低,考虑成本及操作难易程度,笔者选择在室温下反应。而与类似的martin[6]的合成方法相比,笔者只是在溶解过程中使用了冰浴。
2.2 时间对产率的影响
开始反应时,混合溶液为粉色透明溶液。试验了不同反应时间目标产物的产率,发现随时间的推进,产率会不断增加,到6 h后,产率增幅不大,所以把反应时间确定为6 h。而文献[6]中的合成反应需要过夜,时间成本增加。产率随时间变化情况如图2所示。
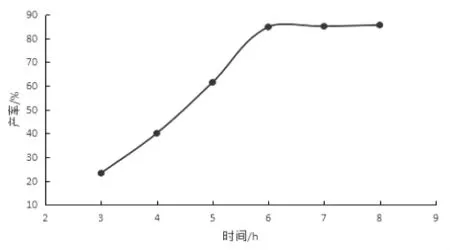
图2:产率对反应时间的变化图Figure 2:The Yield with the Reaction Time
2.3 溶剂对产率的影响
类似的合成中,有水、甲醇和乙醇分别作为反应溶剂的。试验中,用水、甲醇和乙醇作溶剂都可以得到目标产物,而用乙醇作溶剂的产率稍低,水和甲醇为溶剂的反应目标产物的产率相当。综合考虑成本,选用水作溶剂最合适。
2.4 pH值对产率的影响
反应结束后,需要用稀盐酸酸化,以中和反应前加入的氢氧化钠。在pH值为6时,瞬时就会产生大量的沉淀;而pH值大于6时,基本无沉淀,pH值小于6时,沉淀无明显增多。综合以上情况,酸化pH值选择为6。
2.5 2-吡啶酮肟的表征
2.5.1 元素分析结果
C7H8N2O,计算值:C 61.75%,H5.92%,N 20.58%;实验值:C 61.66%,H 5.88%,N 20.63%。
2.5.2 H核磁图谱
对照了标准核磁图谱,高度吻合。在8.64,7.84,7.69和7.28处分别有一个吸收峰,它们是苯环上四个氢的吸收峰;在2.41处有一个吸收峰是羟基上氢的吸收峰;在2.35处的吸收峰是甲基上三个氢的吸收峰,受到肟基的影响向高场移动。
2.5.3 红外图谱
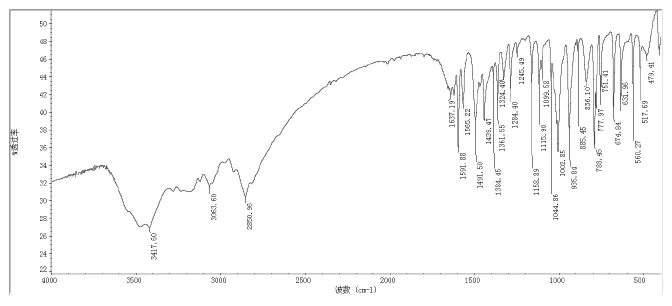
图3:产物的红外吸收图谱Figure 3:The Infrared Absorption Spectra of Products
红外光谱数据 (KBr pellet,cm-1)∶3417(vs),3063(s),2850(s),1637(w),1591(s),1491(m),1439(m),1324(w),1002(s),935(m),836(w),674(m),631(m),560(w),517(w)。
从谱图数据中可以看出,羰基在~1680处的强特征吸收峰消失了,取而代之的是肟基在~1002处的特征吸收峰。
2.5.4 熔点
测定化合物的熔点为:m.p.103℃。
