纳米Fe/Cu双金属的制备及其对水中亚甲基蓝的去除
2018-02-15张文博
张 宏,刘 丹,张文博
(西北民族大学 化工学院 甘肃省高校环境友好复合材料及生物质利用省级重点实验室,甘肃 兰州 730030)
在工业化飞速发展的时代,染料已经成为工业化必不可少的一部分,在印染、纺织、建筑等方面得到广泛的应用[1].染料废水因其色度高、成分复杂,难以进行生物降解,如果长期在水中残留、富集会对水环境产生巨大危害.染料废水被认为是含有大量“三致”毒性的有机污染物[2-4].因此,如何解决染料废水给人类带来的危害已经受到广泛的关注.
纳米零价铁(Fe0)因其比表面积大、还原性高而被认为在水处理领域具有潜在应用前景[5],但在环境中存在易氧化、易聚集等问题,从而限制了其进一步应用.研究表明,在掺杂一种还原电位更高的金属(如Cu、Ag、Pd等)[6-8],可形成双金属体系,能提高体系的反应活性.鉴于Cu是一种廉价、来源广泛,生物毒性较低的金属,因此选用Cu与Fe形成纳米双金属体系,考察其对水中亚甲基蓝的去除性能.
本文采用液相还原法制备纳米Fe/Cu双金属颗粒,运用XRD对其结构进行表征,利用红外光谱对其吸附前后进行表征,研究其去除机理.以亚甲基蓝(MB)为目标污染物,考察了不同pH、不同MB初始浓度,不同停留时间对去除效果的影响,分析去除机理,为纳米双金属在污水处理中的应用提供理论参考.
1 材料
试剂:六水氯化铁(FeCl3·6H2O)、硫酸铜(CuSO4·5H2O)、硼氢化钠(NaBH4)、亚甲基蓝(MB)、无水乙醇,均为分析纯.实验用水为去离子水.
仪器:SHA-BA水浴恒温振荡箱(常州菲普实验仪器厂),81-2磁力搅拌器(上海司乐公司),TGL20M-Ⅱ离心机(湖南凯达公司),UVmini-1280紫外分光光度计(日本岛津公司),DZG-6050型真空干燥箱(上海森信公司),X’PRO型X射线衍射仪(XRD,荷兰PANalytical公司),傅里叶红外光谱分析仪(FTIR,美国热电公司).
2 实验方法
2.1 材料的制备与表征
2.1.1 纳米Fe/Cu双金属的制备
本实验采用液相还原法制备纳米Fe/Cu双金属材料,三口烧瓶提前通N230 min,分别移取0.5 mol·L-1FeCl3·6H2O与0.5 mol·L-1CuSO4·5H2O(Fe、Cu摩尔比为5∶1)于三口烧瓶,加入去离子水和无水乙醇(醇水比为7∶3),磁力搅拌.通过恒压漏斗缓慢滴加0.1 mol·L-1硼氢化钠(NaBH4)溶液.NaBH4的加入量适当过量,以保证Fe3+、Cu2+完全还原.整个过程在N2气中完成.硼氢化钠溶液滴加完毕后,继续磁力搅拌30 min,至反应完全,用去离子水、无水乙醇分别洗涤3次,60 ℃真空干燥12 h,备用.
2.1.2 纳米Fe/Cu材料的表征
材料的结构通过X射线衍射仪进行分析,操作电压40 kV,电流40 mA,扫描范围10°~80°,扫速0.5°/min.
2.2 Fe/Cu双金属对MB去除实验
称取50 mg制备好的Fe/Cu颗粒于50 mL锥形瓶中,准确移入10 mL 125 mg·L-1MB,置于恒温振荡器,温度设为298 K,转速为200 r/min,震荡时间为2 h,吸附完成,离心,取上清液测其吸光度.
2.3 MB定量分析

其中,Qe为MB去除量,mg·g-1;C0为MB的初始浓度,mg·L-1;Ct为t时刻MB的浓度,mg·L-1;V为移取MB溶液的体积,mL;m为Fe/Cu的质量,mg.
3 结果与讨论
3.1 纳米Fe/Cu双金属XRD分析
采用X射线衍射仪对Fe/Cu双金属颗粒进行扫描,扫描范围为10°~80°.从图1可以看出,零价铁的特征峰(44.84°、64.82°)[9]和零价铜的特征峰(43.36°)[10],并无其他明显杂峰.说明Fe/Cu双金属已经成功制备.
3.2 Fe/Cu双金属对水中MB的去除实验
3.2.1 pH对MB溶液去除性能影响
MB初始浓度为125 mg·L-1,用0.1 mol·L-1NaOH和0.1 mol·L-1HCl分别调节pH为1、3、5、7、9、11,反应时间为120 min,考察pH值对MB去除效果,结果如图2.
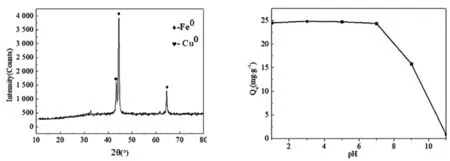
图1纳米Fe/Cu双金属的XRD谱图图2不同pH对MB去除量的影响
由图2可知,在酸性条件下,纳米Fe/Cu双金属对MB的去除效果良好,在pH=3时,去除量达到最大为24. 85 mg/g,去除率可达99.38%.碱性条件下,纳米Fe/Cu对亚甲基蓝的去除性能较差.这可能是由于随着初始pH的增大,溶液中的H+与OH-的含量有关,弱酸环境下更有利于材料对亚甲基蓝的去除.
3.2.2 动力学方程拟合
配制125 mg·L-1MB溶液,调节pH=3,停留时间分别为5 min、30 min、60 min、90 min、120 min、150 min、180 min.取样后立即离心,测上清液吸光度,结果如图3.

图3不同反应时间对MB去除量的影响图4纳米Fe/Cu双金属对MB吸附等温线
由图3可知,在反应开始的30 min内,去除量基本呈线性增加.在45 min时,反应速率平缓,基本达到平衡.出现这种趋势是因为在反应起初,纳米Fe/Cu颗粒可以提供较多的反应活性位点.随着反应的不断进行,材料的活性位点达到饱和,反应逐渐趋于平缓.
为了深入探讨Fe/Cu双金属对MB吸附动力学行为,使用了准一级动力学方程,准二级动力学方程对实验数据进行拟合.
准一级动力学方程:Qt=Qe[1-exp(k1t)].
式中,Qe和Qt分别为平衡吸附量和t时刻吸附量,k1和k2分别为准一级和准二级吸附速率常数.准一级和准二级动力学方程模拟如图3,相关拟合参数见表1.
表1 Fe/Cu对MB吸附动力学方程参数表
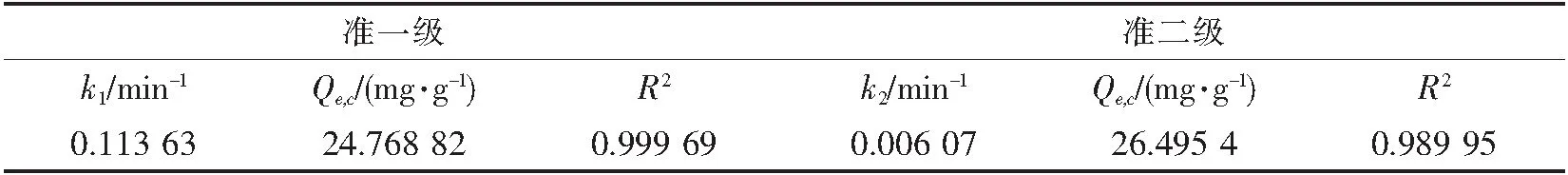
由表1可知,准一级跟准二级均能较好地拟合,准一级动力学方程相关系数R2(>0.99),略高于准二级相关系数R2,且根据准一级动力学方程计算出的理论去除量跟实验值接近,因此准一级动力学方程能更好地模拟纳米Fe/Cu双金属对MB的去除的动力学过程.准一级动力学目前有两种假设[12],分别是以膜扩散为控制因素和以化学、离子交换为控制因素,其机理将在热力学参数中进一步探讨.
3.2.3 等温线拟合
在298 K下,称取数份50 mg 纳米Fe/Cu颗粒,分别对浓度为25 mg·L-1、50 mg·L-1、75 mg·L-1、125 mg·L-1、250 mg·L-1、500 mg·L-1的MB进行去除实验,停留120 min,测其吸光度.对实验数据进行Langmuir和Freundlich等温吸附模型拟合.
式中,Qe和Qm分别是平衡吸附量和最大吸附量;Ce代表平衡浓度;KL是Langmuir吸附平衡常数.
式中,KF和n是Freundlich吸附平衡常数.Langmuir和Freundlich吸附等温方程模拟如图4,相关拟合参数见表2.
表2在298 K下纳米Fe/Cu双金属对MB吸附等温线参数表

由图4可知,纳米Fe/Cu双金属对MB的去除量随着MB初始浓度的升高而不断升高,最后趋于平缓.由表2可知,Langmuir的线性相关系数R2明显高于Freundlich的线性相关系数,表明对MB的去除过程更符合Langmuir吸附等温模型.通过Langmuir吸附等温模型拟合的对MB理论最大吸附量可达65.28mg·g-1.Langmuir吸附等温模型假定材料表面均匀一致且能量分布均匀,是一种描述化学吸附为主要吸附类型的模型,再结合动力学描述中准二级模型拟合中也有较高的相关系数的值(R2=0.989 95).因此整个过程应是以化学吸附为主要控制因素的过程.
3.3 红外谱图分析
采用傅里叶变换红外光谱将纳米材料对亚甲基蓝处理前后进行表征,如图5所示.
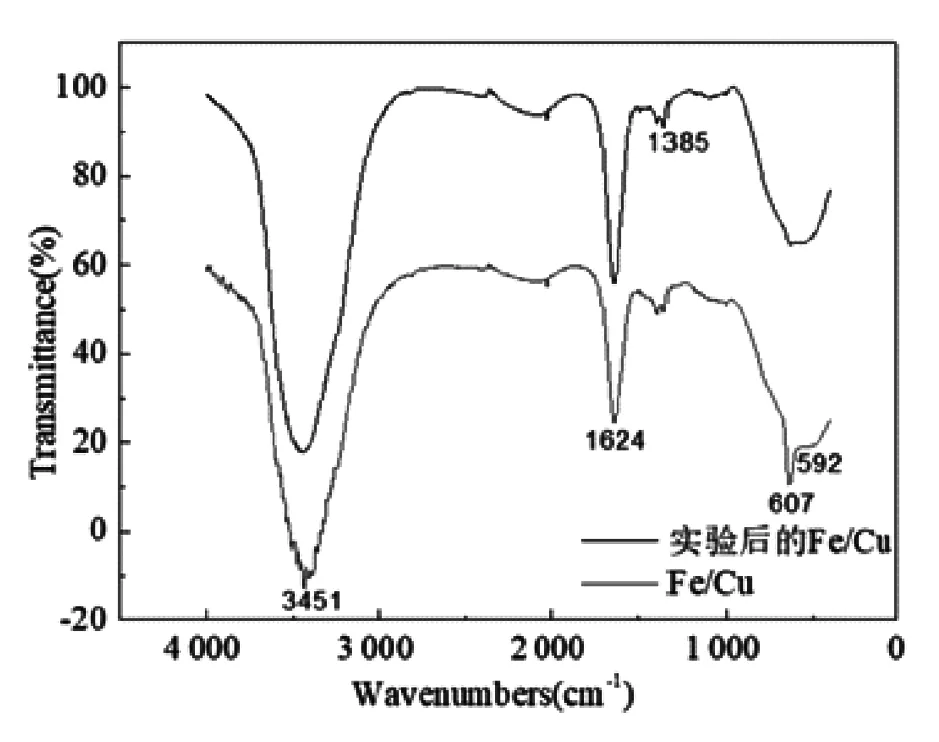
图5 Fe/Cu纳米双金属处理MB前后的红外谱图
根据红外谱图,在红外区出现了Cu-O(607 cm-1)的伸缩振动峰[9],592 cm-1处为Fe-O振动峰.反应后,峰强明显减弱,推测与MB发生化学反应有关.在3 451 cm-1强而宽的吸收峰是-OH的伸缩振动峰,可能是样品表面吸附空气中的水,1 624 cm-1为C=O的伸缩振动吸收峰,1 385 cm-1芳香胺的伸缩振动峰的加强,推测是与MB发生少量的物理吸附所致.
4 结论
1) 在酸性条件下,纳米Fe/Cu双金属颗粒对MB有良好的去除效果,且反应可在较短时间内达到平衡.
2) 准一级动力学方程能较好地拟合Fe/Cu去除MB过程,同时,Langmuir模型能够更好地模拟Fe/Cu对MB的吸附行为.表明MB在Fe/Cu上的吸附过程主要以化学吸附为主.
