家兔Neto2蛋白质的生物信息学分析
2018-02-13赵小峰吴桂梅颜景芝
赵小峰, 吴桂梅, 金 磊, 汪 瑶, 颜景芝
(1.徐州医科大学国家级基础医学实验教学示范中心,江苏徐州 221004;2.江苏省脑病生物信息重点实验室/徐州医科大学生物化学与分子生物学研究中心,江苏徐州 221004)
海人藻酸受体(kainate receptors,简称KARs)是属于离子型谷氨酸受体(ionotropic glutamate receptors,简称iGluRs)的一类受体,通过与谷氨酸结合来介导中枢神经元的快兴奋性传导,参与突触传递、神经调节等神经活动,与脑功能障碍、神经退行性疾病(癫痫、孤独症、精神分裂症等)有密切关系[1]。神经纤毛和特罗德样蛋白质(neuropilin and tolliod-like proteins,简称Neto)是筛选视网膜功能基因时发现的1种Ⅰ型跨膜蛋白质[2],包括Neto1和Neto2 2种类型。研究表明,Neto1和Neto2是海人藻酸受体仅有的2个辅助亚基[3-4],Neto蛋白质在大脑中分布广泛,可通过与KARs的不同亚基结合,调节KARs在突触中的定位和生理特性,进而影响受体通道的脱敏作用及突触转运[1]。但Neto蛋白质调节KARs的结构基础、作用机制还不清楚。本研究利用生物信息学工具对家兔Neto2蛋白质进行预测与研究,旨在为进一步研究家兔Neto2蛋白质在生理和病理条件下的作用及其对KARs功能调控机制提供试验参考。
1 材料与方法
1.1 材料
从GeneBank获得家兔和其他物种Neto2蛋白质的氨基酸序列。在线分析工具为Blast(http://blast.ncbi.nlm.nih.gov/)、BepiPred(http://www.cbs.dtu.dk/services/BepiPred/)、ExPASy(http://ca.expasy.org)、DTU Bioinformatics(http://www.cbs.dtu.dk)。
1.2 方法
利用生物信息学在线工具研究家兔Neto2蛋白质的理化性质(http://web.expasy.org/protparam/)、疏水性(http://web.expasy.org/protscale)、二级结构(http://www.biogem.org/tool/chou-fasman/)、跨膜结构域(http://www.cbs.dtu.dk/services/TMHMM/)、信号肽(http://www.cbs.dtu.dk/services/SignalP/)、亚细胞定位(http://www.genscript.com/psort.html)、三级结构(https://swissmodel.expasy.org/)、功能基序(http://smart.embl-heidelberg.de)、糖基化位点(http://www.cbs.dtu.dk/services/NetOGlyc/)、磷酸化位点(http://www.cbs.dtu.dk/services/NetPhos/),最后使用MEGA6.05软件和String工具研究Neto2蛋白质的分子进化关系、相互作用的蛋白质。
2 结果与分析
2.1 理化性质
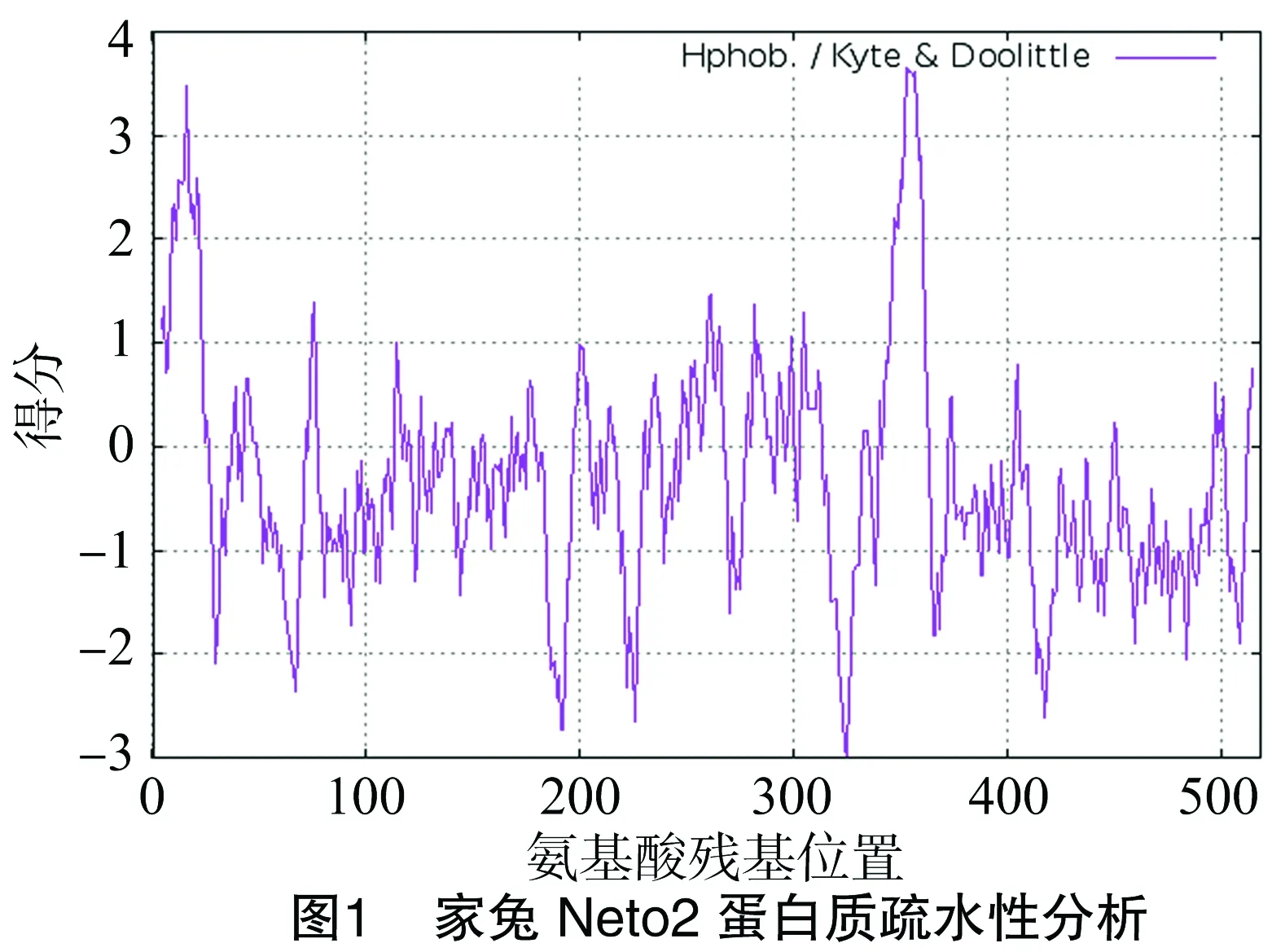
家兔Neto2分子式为C2 608H4 049N703O777S33,含518个氨基酸残基,由20种基本氨基酸组成,氨基酸残基数、含量见表1。家兔Neto2蛋白质分子量为58 742.06 u,等电点为 6.34,含带正电荷的氨基酸残基(赖氨酸+精氨酸)60个,带负电荷的氨基酸残基(谷氨酸+天冬氨酸)64个。在体外,家兔Neto2的半衰期在哺乳动物细胞中为30 h,在酵母 中>20 h,在大肠杆菌中>10 h。蛋白质的不稳定指数为 43.62,根据蛋白质稳定参数在40以下为稳定蛋白质的标准,推测家兔Neto2蛋白质属于不稳定蛋白质[5]。脂溶系数为73.78,总平均亲水系数(grand average of hydropathi city,简称GRAVY)为-0.329,说明该蛋白质为亲水蛋白质[6](正值为疏水性,负值为亲水性,介于-0.5~0.5之间主要为两性蛋白质)。这与ProtScale软件分析的结果(图1)一致,图中显示,大部分氨基酸分值为较低的负值,表明这些氨基酸具有较强的亲水性。
2.2 二级结构分析
进入二级结构在线分析工具,选择参数:窗口参数(windowwidth)为17,相似度(similarity threshold)为8,状态数(number of states)为4,由图2可知,家兔Neto2蛋白质二级结构中α-螺旋占30.69%(159个氨基酸残基),延伸链占19.88%(103个氨基酸残基),β-转角占4.25%(22个氨基酸残基),无规则卷曲占45.17%(234个氨基酸残基)。

表1 家兔Neto2的氨基酸组成
2.3 信号肽和跨膜结构预测
采用SignalP 4.1对家兔Neto2蛋白质进行分析发现,第23位氨基酸的最高原始剪切位点得分是0.490,同时该位点综合剪切分值最高,为0.655,第16个氨基酸信号肽的得分最高,0.942,第1~22个氨基酸信号肽的平均得分为 0.774,趋向于+1,表明家兔Neto2蛋白质存在信号肽(界限值为0.45),最可能的切割位点在22和23氨基酸残基(VEG-IA)之间(图3)。经分析家兔Neto2蛋白质存在跨膜结构,1~338位于膜外,339~361为跨膜区,362~518位于膜内(图4)。

2.4 糖基化和磷酸化位点分析
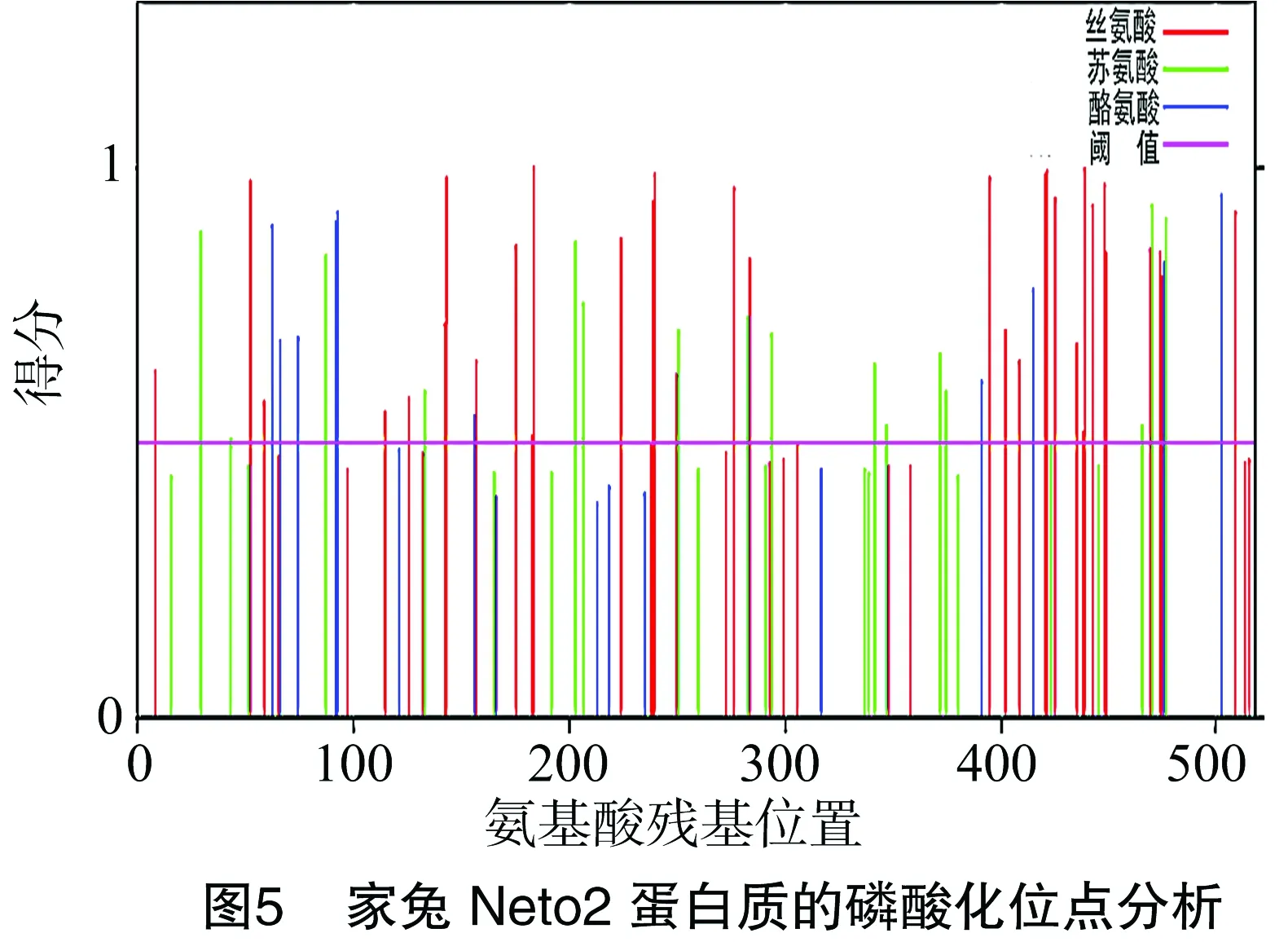
经NetOGlyc 4.0分析,家兔Neto2蛋白质存在糖基化位点,分别是第184、284位的丝氨酸残基和291位的苏氨酸残基,得分依次为0.658 779、0.683 538和0.522 623。对家兔Neto2蛋白质进行磷酸化分析发现,有62个磷酸化位点(得分>0.5)(图5),其中丝氨酸36个,苏氨酸16个,酪氨酸10个。推测不同的位点可被不同的激酶引发磷酸化。

2.5 功能结构分析
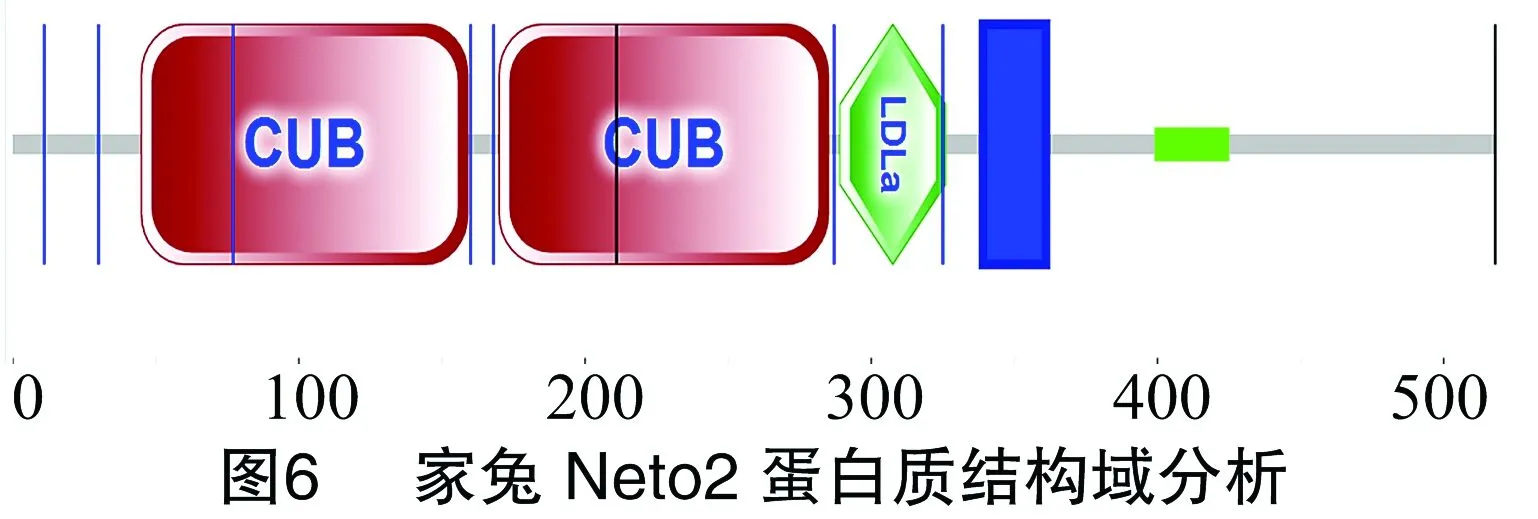
使用GORⅣ、SMART对家兔Neto2蛋白质的功能结构域进行分析,结果(图6)表明,该蛋白质含2个CUB和1个LDLa保守结构域,2个CUB位于45~159、177~292位氨基酸残基处,LDLa位于296~333位氨基酸残基处。C端含有1个复合螺旋区(coiled coil regions,绿色方形区)(404~432位氨基酸残基处),在N端(3~27位氨基酸残基处)还有1个低复杂性区域,此外在346~368位氨基酸残基处为跨膜区域(蓝色方形区)。
2.6 亚细胞定位
亚细胞定位预测结果表明,家兔Neto 2蛋白质主要存在于内质网(44.4%)、线粒体(44.4%)中,细胞核(11.1%)中也有少量分布。Neto2蛋白质在内质网、线粒体中定位较多,说明蛋白质主要发挥受体、运输及结合的作用[7]。
2.7 三级结构及蛋白质相互作用分析
采用同源建模法预测家兔Neto2蛋白质三级结构,第42~237位氨基酸残基参与建模,模板为3kq4.1.B Cubilin。由图7可知,在三级结构中蛋白质无规卷曲、折叠延伸链分布较多,而α-螺旋分布较少,这与二级结构中预测的结构元件分布大致相同。

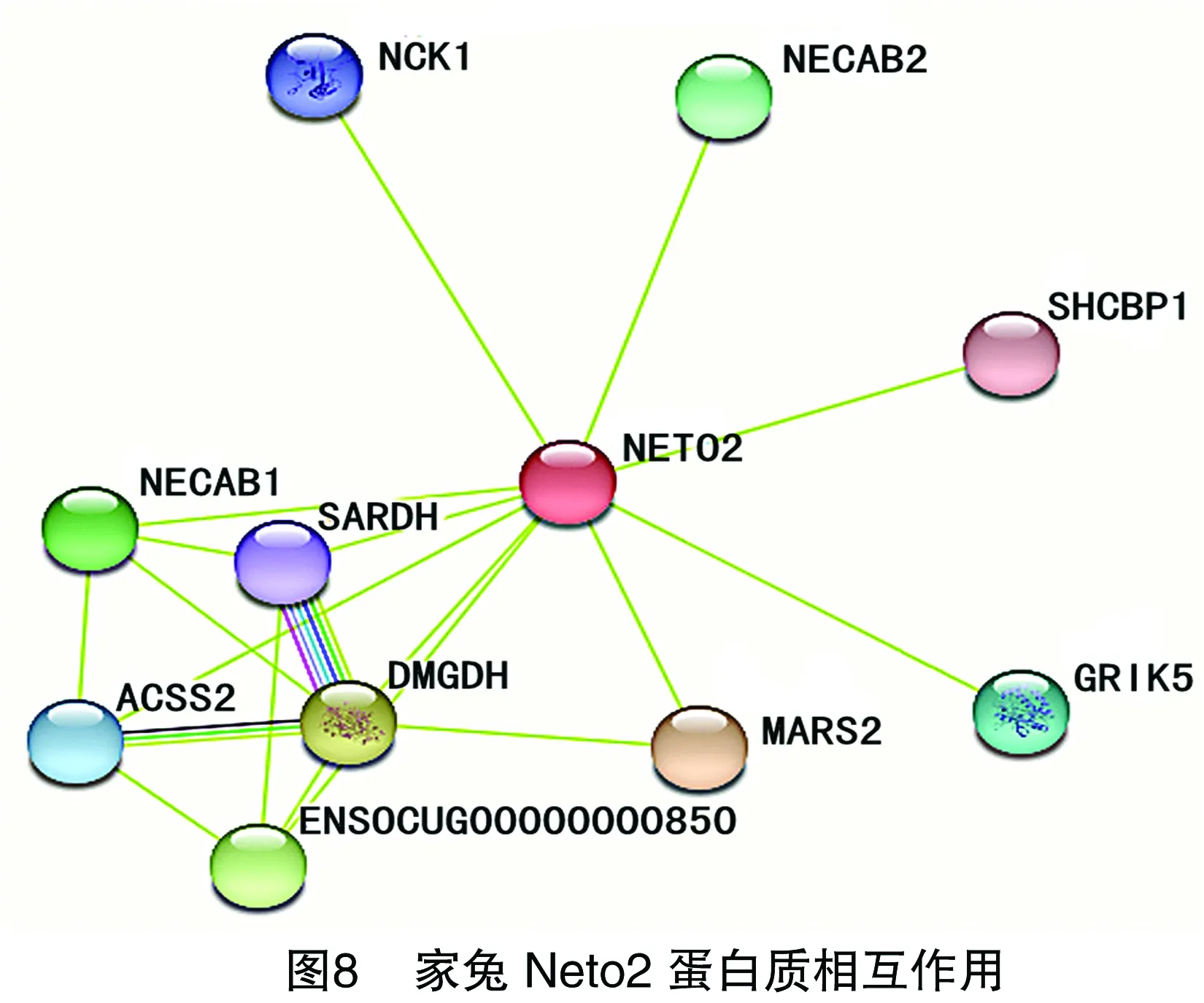
String数据库是搜索已知蛋白质之间及与预测未知蛋白质之间相互作用的在线工具。这种作用包括蛋白质之间直接的物理相互作用及蛋白质之间间接的功能相关性。本研究采用String数据库对家兔Neto2蛋白质进行蛋白质相互作用(protein-protein interaction,简称PPI)分析,若关联系数>0.4,则认为相互作用显著[8]。通过String在线搜索发现,一些与家兔Neto2相互作用的蛋白质,这些蛋白质包括氨基末端钙结合蛋白质1(n-terminal EF-hand calcium binding protein 1,简称Necab1)、氨基末端钙结合蛋白质2(Necab2)、与酪氨酸磷酸化生长因子相关的衔接蛋白质NCK1、SH2结构域连接蛋白质1(SHC binding and spindle associated 1,简称SHCBP1)、谷氨酸盐受体海人藻酸5(glutamate receptor ionotropic kainate 5,简称Grik5)、甲硫氨酰-tRNA合成酶2(methionyl-tRNA synthetase 2,简称MARS2)、二甲基甘氨酸脱氢酶前体(dimethylglycine dehydrogenase precursor,简称Dmgdh)、肌氨酸脱氢酶(sarcosine dehydrogenase,简称SARDH)、乙酰辅酶A合成酶(acetyl-CoA synthetase 2,简称ACSS2)等,由图8可知,家兔Neto2蛋白质参与调节谷氨酸受体活性、β-淀粉样蛋白质(Aβ)生成及神经细胞的记忆调节等活动。
2.8 蛋白质系统进化分析
采用MEGA6.05软件构建系统进化树,由图9可知,啮齿目的小家鼠、褐家鼠、黄金仓鼠聚为一类,再与兔形目的家兔相聚类。灵长目的东非狒狒、人、猕猴和黑猩猩聚为1类;食肉目的雪貂和灵长目聚为1类,之后又与食肉目家犬聚为1类;偶蹄目的绵羊、山羊、家牛聚为1类;奇蹄目的家马和驴聚为1类,再与偶蹄目、食肉目及灵长目相聚类。在Neto2基因遗传进化上,家兔与啮齿目亲缘关系最近,与偶蹄目、奇蹄目、食肉目及灵长目亲缘关系较远,与鸟纲、两栖纲、鱼纲之间亲缘关系更远。
3 讨论
KARs是脊椎动物中枢神经系统中谷氨酸盐离子通道蛋白质,广泛分布于中枢和外周神经系统。KARs由5种亚基(GluK1-5)[9]组成,在突触传递、神经元兴奋、树突生长、神经发育等生命活动中发挥重要作用[10-12]。Neto2蛋白质是新发现的KARs辅助亚基,通过调节KARs的通道特性来影响其功能。Neto2与KARs的GluK2亚型结合,可增加GluK2受体开放概率和脉冲时间,加速脱敏恢复,从而提高KARs稳态电流[13]。Sheng等发现,Neto2通过与GluK1氨基末端区(ATDs)结合协助GluK1进行突触转运[14]。Tang等研究发现,Neto2的C-末端盘状同源区域(PDZ)结合结构域可以与谷氨酸受体相互作用蛋白(glutamate receptor-interacting protein,简称GRIP)相互作用,同时GRIP可以与GluK2的PDZ结合结构域结合,过表达Neto2可增强GRIP与GluK2的结合,从而增加KARs在突触后膜的稳定性[15]。Vernon等研究发现,Neto2蛋白质高表达于新生背根神经,在坐骨神经损伤或者敲除基因Neto2后,活化的丝裂原活化蛋白激酶/胞外信号调节激酶(MEK/ERK)上调Neto2的表达,进而调节轴突的再生及KARs在感觉神经元中的作用[16]。现有研究表明,Neto2蛋白质对KARs的调节具有多样性,深入研究Neto2调控KARs的机制,将有可能为进一步研究癫痫、阿尔兹海默症、疼痛及中风等疾病的治疗方法提供试验基础和理论依据。

本研究通过对家兔Neto2蛋白质的分子特征进行分析发现,家兔Neto2蛋白质由518个氨基酸残基组成,其中大部分氨基酸具有较强的亲水性,说明该蛋白质易溶于水。家兔Neto2蛋白质含有信号肽,主要定位于内质网、线粒体等细胞器内。信号肽不仅决定蛋白质是否为分泌蛋白质,也和蛋白质在细胞内的定位有关[17]。说明该蛋白质为分泌蛋白质,在内质网中合成,能通过囊泡运输至相应细胞区域,具有运输和结合作用。
蛋白质磷酸化是调节和控制蛋白质活力和功能最基本、最普遍、最重要的机制,在细胞信号转导的过程中起重要作用。糖基化可以改变蛋白质的构象,增加蛋白质的稳定性,从而调节蛋白质众多生物学功能[18]。分析结果表明,家兔Neto2蛋白质中存在62个磷酸化位点,3个糖基化位点,且推测家兔Neto2蛋白质为不稳定蛋白质。因此,磷酸化和糖基化可使家兔Neto2变得稳定,在细胞发育、细胞间信号传递和神经细胞功能调节等活动中受蛋白质激酶的调节。据此,笔者推测蛋白质的磷酸化、糖基化修饰对家兔Neto2蛋白质的生物学功能具有重要的调节作用。
分子进化即微观进化,依赖于核酸和蛋白质的序列信息,是阐明物种间相互关系的分子基础[19-20]。通过系统进化树分析发现,家兔Neto2蛋白质与小家鼠、褐家鼠、黄金鼠之间的关系最近,表明Neto2蛋白质在家兔和小家鼠、褐家鼠、黄金鼠中相对保守。家兔Neto2蛋白质二级结构中无规卷曲、α-螺旋含量较高,三级结构中长链卷曲分布较多。家兔Neto2蛋白质可以和Necab1、Necab2、NCK1、SHCBP1、Grik5等蛋白质发生相互作用,说明家兔Neto2蛋白质具有磷酸化活性,在生长发育、跨膜运输、突触传递、KARs信号转导及β-淀粉样蛋白质生成等过程中可能发挥重要作用。本研究对家兔Neto2蛋白质的理化性质、结构特征、进化关系等进行初步分析,为进一步研究家兔Neto2蛋白质的表达和生物活性奠定了工作基础。
