CT图像纹理分析鉴别诊断磨玻璃密度肺腺癌的浸润性
2017-12-22张立娜
罗 婷,张 峥,李 昕,郭 妍,张立娜*,徐 克*
(1.中国医科大学附属第一医院放射科,辽宁 沈阳 110000;2.GE医疗,上海 200000)
CT图像纹理分析鉴别诊断磨玻璃密度肺腺癌的浸润性
罗 婷1,张 峥1,李 昕2,郭 妍2,张立娜1*,徐 克1*
(1.中国医科大学附属第一医院放射科,辽宁 沈阳 110000;2.GE医疗,上海 200000)
目的探讨CT图像纹理分析鉴别诊断表现为磨玻璃密度结节的肺腺癌浸润性的价值。方法收集在我院接受肺部CT检查且手术病理证实为肺腺癌患者100例(浸润性腺癌56例,非浸润性腺癌44例)。随机选择69例为训练组,31例为验证组。使用A.K.(Analysis-Kinetics)分析软件进行影像特征提取;Kruskal-Wallis非参数检验和Spearman相关性分析进行特征降维;使用R语言软件包“GLM”函数,建立Logistic回归模型;以交叉验证方法对回归模型进行检验。采用ROC曲线评价独立预测因素的诊断效能。结果影像特征提取得到396个影像组学特征,经降维最终得到与鉴别肺非浸润腺癌与浸润腺癌最相关的参数3个,建模后验证Logistic回归模型示其诊断准确率为83.30%,敏感度及特异度分别为77.80%、91.70%。结论CT图像纹理分析可有效鉴别表现为磨玻璃密度结节肺腺癌的浸润性。
体层摄影术,X线计算机;肺肿瘤;纹理分析;影像组学
肺内恶性磨玻璃密度结节在病理上对应为原位癌(adenocarcinomas in situ, AIS)、微浸润性腺癌(minimally invasive adenocarcinoma, MIA)或浸润性腺癌(invasive pulmonary adenocarcinomas, IPA)。2011年肺腺癌国际多学科分类标准指出,浸润前病变即原位癌和微浸润性腺癌接受肺段切除后的5年无病生存率接近100%,而浸润性腺癌仍以肺叶切除为主,且术后5年无病生存率<90%[1-2]。因此,术前准确鉴别肺浸润性病变对手术方式的选择以及患者预后的评估有指导作用。术前肺穿刺活检因取材受限常无法准确反应整体病灶的浸润性。传统CT图像难以准确鉴别以磨玻璃密度结节为主要表现的AIS、MIA和IPA。纹理分析方法可对影像图像进行分割,定量提取内部大量特征信息,并对所获得的特征数据进行挖掘、分析,有效地鉴别肿瘤性质,对肿瘤进行病理分型,预测预后,规划治疗方案等[3]。本研究旨在使用CT图像纹理分析方法鉴别肺磨玻璃密度结节的浸润性,并评价其诊断效能。
1 资料与方法
1.1 一般资料 收集2014年2月—2016年11月于我院增强CT检出肺磨玻璃密度结节且直径<30 mm的患者100例,男26例,女74例,年龄35~78岁,平均(56.5±8.6)岁。所有患者CT检查前均未接受活检、放疗、化疗等操作或治疗,且均于CT检查后2周内接受手术治疗,最终病理证实为肺腺癌。
1.2 仪器与方法 采用Siemens Somatom Definition FLash双源CT机。患者取仰卧位,双臂上举,于吸气末进行全肺扫描。参数:管电压100 kV 或140 kV,管电流Care Dose 4D,扫描层厚2 mm,重建层厚2 mm,重建层间距2 mm,矩阵512×512,FOV 350 mm×350 mm。增强扫描采用双筒高压注射器于肘静脉注射70~90 ml非离子型对比剂碘普罗胺,注射速度2.5~3.0 ml/s,注射30~40 s后获得动脉期图像。
1.3 纹理特征提取 将所有患者薄层增强CT图像(肺窗)导入A.K.分析软件(Analysis-Kinetics,GE),由1名从事胸部影像诊断12年的影像医师在不知晓病理结果的情况下对病灶逐层勾画ROI,ROI的大小取决于病变大小且尽量与病灶边缘保持一致。软件自动计算得到图像形态、亮度等相关特征参数以及基于灰度共生矩阵和步长矩阵等的高阶纹理特征参数。
1.4 建立预测模型 按照7∶3的比例,经计算机任意选取69例患者作为训练组(非浸润腺癌32例、浸润腺癌37例),31例作为验证组(非浸润腺癌12例、浸润腺癌19例)。将获得的纹理特征参数全部导入R语言软件包,剔除结果为nan或Inf的特征参数,得到剩余特征;再经特征预处理和降维得特征纹理参数,利用R语言软件包中的“GLM”函数建立线性回归(Logistic linear regression, LLR)模型。以交叉验证方法(10折,重复10次)对LLR模型进行检验,并绘制ROC曲线,计算其鉴别磨玻璃密度肺腺癌的浸润性的敏感度和特异度。
1.5 统计学分析 使用R语言软件(R Studio Version 1.0.143-©2009-2016 R Studio, Inc.)进行统计学分析。以病理结果为金标准,采用Kruskal-Wallis非参数检验统计肺非浸润腺癌与浸润腺癌有统计学差异的影像学特征;Spearman相关性分析进行特征去冗余,剔除自相关性系数高于0.9(|r|>0.9)的纹理参数,得到最终特征参数。ROC曲线下面积(area under curve, AUC)为0.5~0.7时其诊断价值较低,>0.7~0.9时诊断价值中等,>0.9时诊断价值较高。P<0.05为差异有统计学意义。
2 结果
100例患者中,非浸润性肺癌44例,病灶平均最大直径(1.44±0.69)cm,浸润性肺癌56例,病灶平均最大直径(1.89±0.62)cm(图1)。
将图像导入R语言软件包,得到基于病灶大小、边缘形态、位置信息、灰度共生矩阵、灰度步长矩阵算法等的影像组学特征共396个,剔除肺非浸润腺癌与浸润腺癌间差异无统计学意义的参数,剩余14个特征;再进行特征去冗余,剔除自相关性高的参数,剩余3个特征,分别为熵总值、聚类萌、球面不对成性。影像组学得分计算公式如下:影像组学得分=-24.946 20+聚类萌×0.000 007 864 712+熵总值×20.567 46+球面不对成性×5.676 74利用Logistic回归分析方法对3个特征纹理参数建立预测模型并进行交叉验证。训练组非浸润腺癌与浸润腺癌影像组学得分分别为-0.54(-1.39~0.10)、1.04(0.33~2.59),差异有统计学意义(P=0.04)。ROC曲线分析示验证组AUC为83.30%[95%CI(60.60%,90.72%)],其鉴别诊断非浸润腺癌与浸润腺癌的敏感度、特异度及准确率分别为77.80%、91.70%、83.30%(图2)。
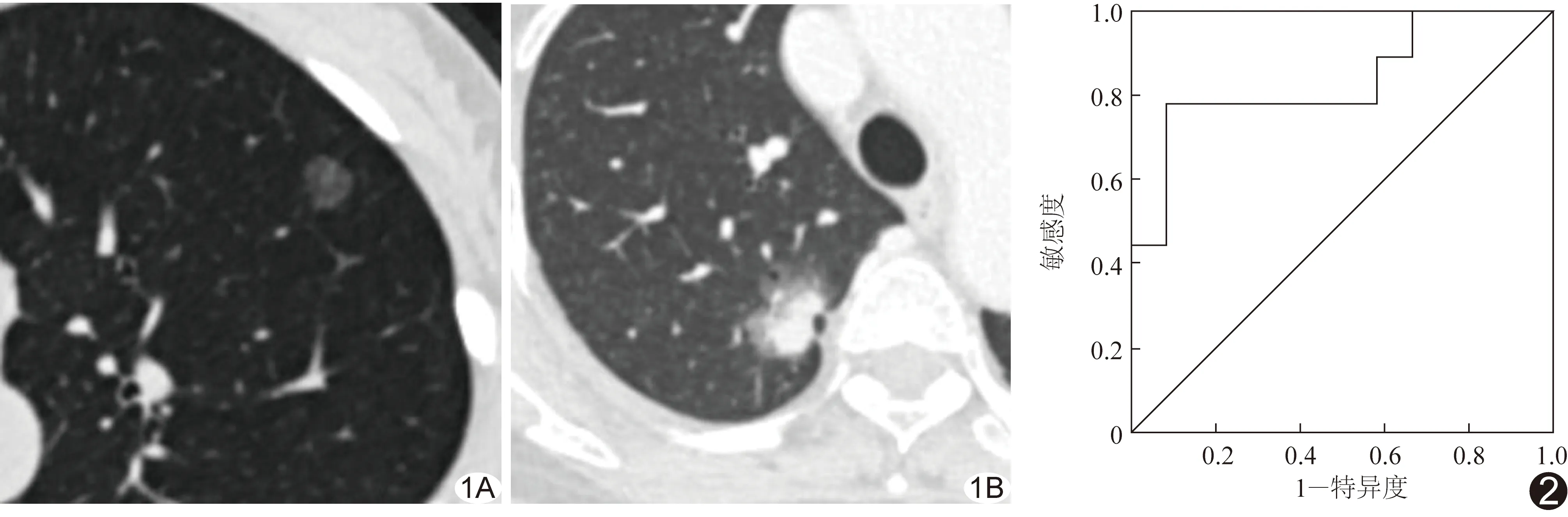
图1 磨玻璃密度肺腺癌 A.左肺上叶纯磨玻璃密度结节,病理显示为原位癌伴局部微浸润; B.右肺上叶以磨玻璃密度为主的混合磨玻璃密度结节,病理显示为腺癌样生长 图2 验证组ROC曲线鉴别磨玻璃密度肺腺癌的诊断效能
3 讨论
传统采用术前穿刺活检或高年资影像医师CT图像判读法判断表现为磨玻璃密度结节肺腺癌的浸润性。但由于穿刺活检取材受限,穿刺病理结果常难以准确判断整体病灶的侵袭性,且为有创检查,存在着一定的操作风险和结果的不确定性[3]。传统CT图像判读多依据病变大小、实性成分大小及占比、形态、边缘、内部特征(空泡征、增粗小血管等)、周边特征(胸膜牵拉、血管聚集等)判断病灶的侵袭性。研究[4-5]表明,混合磨玻璃结节中实性成分占比越高,说明其更具恶性侵袭性。病灶病理恶性等级越高,出现胸膜牵拉征的比例越高[6]。Lee等[7]发现胸膜牵拉、实性成分大小以及实性成分占比3个因素均为鉴别浸润性肺腺癌的独立危险因素。实际临床应用中,不同级别和资历的医师对上述影像特征的理解和认识存在着一定差异,判别能力也各不相同,且传统图像特征分析存在操作复杂、人为因素影响大、影像特征特异性不足等问题,影响临床图像判读的准确性。
影像组学利用数学算法提取影像图像高维复杂特征,并通过对影像数据深度挖掘来定量分析肿瘤异质性,目前已被证实可有效提高诊断准确率[3]。肺CT纹理分析基于定量分析的优势,已被逐渐应用于肺结节的行为预测,为早期诊断和个体化治疗提供临床依据[8-9]。本研究使用基于CT图像的纹理分析方法提取磨玻璃密度结节的影像特征,并经降维得到3个特征纹理参数,利用Logistic回归分析方法建立基于特征纹理参数的预测模型,用以鉴别以磨玻璃结节为影像学特征的肺腺癌的浸润性,并在验证组中得到了较好的结果。本研究经交叉验证检验,基于CT图像纹理特征的预测模型对鉴别磨玻璃密度结节肺腺癌浸润性的准确率为83.30%。Ma等[10]从127例肺结节图像中提取了大量影像组学纹理特征,并分析得出纹理特征鉴别诊断良恶性结节的准确率为82.70%,与本研究结果类似。纹理特征表明异质性越高,包括熵和一致性,反映病灶的恶性程度越高[11]。Lee等[12]单独运用临床和CT图像特征分析,其鉴别诊断亚实性结节的准确率为79.00%,但前者结合纹理分析之后,鉴别准确率高达92.90%。说明纹理分析可在一定程度上帮助放射科医师提高阅片的准确率,为精准的临床诊断提供可靠依据。
本研究存在一定局限性:①本研究为回顾性单中心研究,样本存在偏倚;②3D ROI的勾画采用二维手动勾画,而自动或半自动的ROI选择会节省更多人力,ROI的变异性也会较小;③预测模型仅建立在纹理分析参数基础之上,未考虑相关临床影响因素。
综上所述,基于CT图像纹理分析的预测模型可较好区分以磨玻璃密度结节为主要影像学表现的肺腺癌是否为浸润性病变,可为患者术前手术方式选择和术后预后评估提供重要参考。
[1] Travis WD, Brambilla E, Noguchi M, et al. International association for the study of lung cancer/American thoracic society/European respiratory society international multidisciplinary classification of lung adenocarcinoma. J Thorac Oncol, 2011,6(2):244-285.
[2] Van Schil PE, Asamura H, Rusch VW, et al. Surgical implications of the new IASLC/ATS/ERS adenocarcinoma classification. Eur Respir J, 2012,39(2):478-486.
[3] Lambin P, Rios-Velazquez E, Leijenaar R, et al. Radiomics: Extracting more information from medical images using advanced feature analysis. Eur J Cancer, 2012,48(4):441-446.
[4] Matsuguma H, Oki I, Nakahara R, et al. Comparison of three measurements on computed tomography for the prediction of less invasiveness in patients with clinical stage I non-small cell lung cancer. Ann Thorac Surg, 2013,95(6):1878-1884.
[5] Ohde Y, Nagai K, Yoshida J, et al. The proportion of consolidation to ground-glass opacity on high resolution CT is a good predictor for distinguishing the population of non-invasive peripheral adenocarcinoma. Lung Cancer, 2003,42(3):303-310.
[6] Takashima S, Maruyama Y, Hasegawa M, et al. CT findings and progression of small peripheral lung neoplasms having a replacement growth pattern. AJR Am J Roentgenol, 2003,180(3):817-826.
[7] Lee SM, Park CM, Goo JM, et al. Invasive pulmonary adenocarcinomas versus preinvasive lesions appearing as ground-glass nodules: Differentiation by using CT features. Radiology, 2013,268(1):265-273.
[8] Wilson R, Devaraj A. Radiomics of pulmonary nodules and lung cancer. Transl Lung Cancer Res, 2017,6(1):86-91.
[9] Gillies RJ, Kinahan PE, Hricak H, et al. Radiomics: Images are more than pictures, they are data. Radiology, 2016,278(2):563-577.
[10] Ma J, Wang Q, Ren Y, et al. Automatic lung nodule classification with radiomics approach//Medical Imaging 2016: PACS and Imaging Informatics: Next Generation and Innovations, 2016:978906.
[11] Son JY, Lee HY, Lee KS, et al. Quantitative CT analysis of pulmonary ground-glass opacity nodules for the distinction of invasive adenocarcinoma from pre-invasive or minimally invasive adenocarcinoma. PloS One, 2014,9(8):e104066.
[12] Lee SH, Lee SM, Goo JM, et al. Usefulness of texture analysis in differentiating transient from persistent partsolid nodules(PSNs): A retrospective study. PLoS One, 2014,9(1):e85167.
CTtexturefeaturesindifferentialdiagnosisofinvasionofgroundpulmonaryadenocarcinomamanifestingglassdensitynodule
LUOTing1,ZHANGZheng1,LIXin2,GUOYan2,ZHANGLina1*,XUKe1*
(1.DepartmentofRadiology,theFirstHospitalofChinaMedicalUniversity,Shenyang110000,China;2.GEHealth,Shanghai200000,China)
ObjectiveTo explore the value of CT texture analysis in differential diagnosing invasion of pulmonary adenocarcinoma manifesting ground glass density nodule.MethodsTotally 100 patients with pulmonary adenocarcinoma manifesting ground glass density nodule (56 invasive adenocarcinomas and 44 non-invasive adenocarcinomas) confirmed by pathology underwent CT scanning. Patients were randomly divided into training group (n=69) and validation group (n=31). Image features were extracted using A.K. (Analysis-Kinetics) analysis software, and feature dimensionality reduction was conducted withKruskal-WallisandSpearmananalysis. TheLogisticmodel was established with R language package "GLM" function, then regression model was tested with cross-validation method. ROC curve analysis was performed to evaluate the differentiating value of identified variables.ResultsTotally 396 texture parameters were obtained from imaging features, and of which 3 features had the relationship with differential diagnosis of invasion of pulmonary adenocarcinoma manifesting ground glass density nodule. ROC curve showed that area under the curve of theLogisticmodel in validation group was 83.30%, and the sensitivity and specificity were 77.80% and 91.70%, respectively.ConclusionTexture analysis has the potential to improve the differentiation of invasion of pulmonary adenocarcinoma manifesting ground glass density nodule.
Tomography, X-ray computed; Lung neoplasms; Texture analysis; Radiomics
R734.2; R814.42
A
1003-3289(2017)12-1788-04
公益性行业科研专项(201402013)、国家自然科学基金青年科学基金(81301222)、辽宁省科技厅项目(2012020073-302)。
罗婷(1994—),女,安徽马鞍山人,在读硕士。研究方向:胸部影像诊断。E-mail: luotingemma56@163.com
张立娜,中国医科大学附属第一医院放射科,110000。E-mail: zhanglnda@163.com
徐克,中国医科大学附属第一医院放射科,110000。E-mail: kexu@vip.sina.com
2017-09-30
2017-11-09
10.13929/j.1003-3289.201709175
