螺旋CT评价原发性颌面部成釉细胞瘤的价值
2017-11-28田涛王韶颖石慧敏
田涛, 王韶颖,石慧敏
·头颈部影像学·
螺旋CT评价原发性颌面部成釉细胞瘤的价值
田涛, 王韶颖,石慧敏
目的评估64排螺旋CT对原发性颌面部成釉细胞瘤的诊断价值。方法对112例经手术病理证实的原发性颌面部成釉细胞瘤的术前CT图像进行回顾性分析。病理类型包括实体/多囊型70例、单囊型35例、促结缔组织增生型6例和骨外/外周型1例。测量肿瘤增强前后兴趣区(ROI)的CT值,研究该肿瘤的螺旋CT强化特征。结果本组原发性颌面部成釉细胞瘤中囊性、囊实性、实性者分别为50、52、10例,分别占44.64%,46.43%,8.93%。多房状75例(66.96%)。增强后囊壁、间隔和实性部分强化,可见壁结节样强化,其中28例(84.85%)肿瘤强化程度达50%以上。111例骨内肿瘤中97例边缘有硬化线(87.39%),105例有明显骨质膨隆(94.59%),104例骨皮质变薄或破坏、中断(93.69%)。105例肿瘤与邻牙有密切关系(93.75%)。结论螺旋CT可清晰显示原发性颌面部成釉细胞瘤的影像学特征,为指导临床治疗提供更多信息。
成釉细胞瘤; 体层摄影术,X线计算机; 病理学
颌面部成釉细胞瘤是常见的良性牙源性上皮性肿瘤,具有局部侵袭性,如果处理不当会导致较高的复发率[1-2]。该肿瘤有四种大体病理类型:实体/多囊型、单囊型、促结缔组织增生型和骨外/外周型[3]。对于低复发率的单囊型成釉细胞瘤一般采用刮治术,对于复发率高的实体/多囊型多采用切除术[4]。因此,术前全面观察肿瘤内部结构、准确判断肿瘤类型对临床治疗方法的选择十分重要。传统颌面部成釉细胞瘤影像学诊断主要依赖X线全景片,但X线全景片密度分辨力差、有图像重叠,无法达到临床治疗前判断肿瘤的要求。本文将原发性颌面部成釉细胞瘤的螺旋CT表现与病理进行对照分析,为临床治疗方法的选择提供更为精确的影像学资料。
材料与方法
1.研究对象
搜集本院自2013年1月-2015年1月拟诊为原发性颌面部成釉细胞瘤的病例共112例,其中男64例、女48例,年龄10~86岁,平均34.98岁。肿瘤最大6.4 cm×9.5 cm×5.5 cm,最小0.7 cm×1.3 cm×1.2 cm,所有病例均经手术病理证实。所有病例均为初次发病的原发病例。病理类型包括实体/多囊型70例、单囊型35例、促结缔组织增生型6例和骨外/外周型1例。
2.检查方法
采用Philips Brilliance 64排螺旋CT扫描仪。62例行CT平扫,50例行增强扫描。扫描范围从颈根部至颅底水平。增强扫描前对患者行碘过敏实验,阴性者方可以进行检查。扫描参数:管电压140 kV,管电流490 mAs,探测器准直64×0.625,螺距0.609,球管转速0.75 s/r,扫描视野22 cm×22 cm~25 cm×25 cm,层厚5 mm,间距5 mm,应用标准算法重建,重建层厚1 mm,重建间隔1 mm,重建矩阵512×512。增强扫描采用高压注射器注射经肘静脉注入非离子型碘对比剂欧乃派克(350 mg I/mL),注射剂量100 mL,注射流率3~3.5 mL/s,对比剂注入后延迟45 s进行增强扫描。
3.图像处理
所有原始数据均传入Philips Extended Brilliance Workspace工作站,由一名经验丰富的放射科医生应用工作站自带软件进行多平面重组(multiplanar reformation,MPR)和容积再现(volume rendering,VR)的图像后处理。MPR后处理包括冠状面和与下颌骨走行一致的斜矢状面,间隔1 mm。测量CT值时选取病灶最大层面(若病灶为囊实性的,则分别选取囊性成分的最大层面和实性成分的最大层面),勾画兴趣区ROI测得CT值。ROI取样时尽量避开肉眼可见的出血、骨性间隔等,ROI均为椭圆形,取样范围以不小于瘤灶面积的80%为佳。测量3次CT值后取平均值。
由两名不知病理结果的高年资放射科医生以骨窗(窗宽1500 HU,窗位400 HU)和软组织窗(窗宽250 HU,窗位35 HU)阅读所有CT原始图像,并阅读MPR和VR后处理图像,对各影像学特征性表现做出判定,意见不一致时经协商达成一致。
4.统计学分析
所有数据均采用SPSS 19.0软件包进行处理和统计分析。平均CT值用表示。
结果
1.肿瘤类型和位置
随着智能船舶系统的功能日趋多样化、复杂化,船舶数据呈现出海量、高维的特点,使得传统的船舶数据网络管理平台已不能满足现代船舶的应用需求。此外,网络化、精细化和智能化的管理已成为海上运输业赖以生存和发展的必备条件,而这种发展趋势的基础和关键是对船舶数据的合理管理与运用,进而推动船舶数据管理模式的不断发展创新。本文提出一种适用于智能船舶的分布式数据网络管理平台,结合智能船舶系统固有的特点和船舶应用需求的多样性,为船舶数据获取、处理和分析建立良好的平台,大大提高船舶数据的管理效率。
112例原发性颌面部成釉细胞瘤中,囊性肿块50例(图1),实性10例,囊实性52例(图2)。囊性肿块内有时可见到上层囊液、下层血液的液-液平(图1)。
112例原发性颌面部成釉细胞瘤均通过CT准确定位,其中,发生在颌骨内111例,包括下颌骨98例和上颌骨13例,发生在骨外软组织内1例。下颌骨的肿瘤单侧90例(左侧42例,右侧48例),双侧8例。下颌骨病变范围涉及体部、角部、升支、颏部、髁突及冠突,以下颌后牙区为中心者多(69例)、前牙区为中心者少(29例)。
2.CT值
10例实性肿瘤及52例囊实性肿瘤实性部分的CT值平扫为26~79 HU,平均CT值为(45.056±11.434) HU。增强后囊壁、内部间隔和实性部分强化,强化往往不均匀,部分囊壁强化呈结节状(图2)。10例实性肿瘤及52例囊实性肿瘤中,完成增强CT检查的共33例(包括实性肿瘤3例和囊实性肿瘤30例),增强后CT值增加了21~94 HU,平均CT值增加(44.970±20.062) HU,计算增强程度:增强程度=(增强后CT值-增强前CT值)/增强前CT值×100%。通过以上公式计算,增强程度为30.38%~313.33%,平均(102.29±58.06)%,其中增强程度达50%以上的28例(84.85%,28/33),增强程度为30%~50%的5例。增强程度代表了增强后CT值的增加程度。
3.瘤灶特征
观察瘤灶的7个方面:形态、内部结构、骨质膨隆、边缘、周围骨皮质改变、灶内是否含牙及与邻牙关系(表1)。多房状病灶分房大小可一致或不一致。本组75例多房状病灶中,分房大小不一致者69例,分房大小一致的“蜂窝状”改变者病例6例,包括蜂窝状实性病灶3例和蜂窝状囊实性病灶3例。
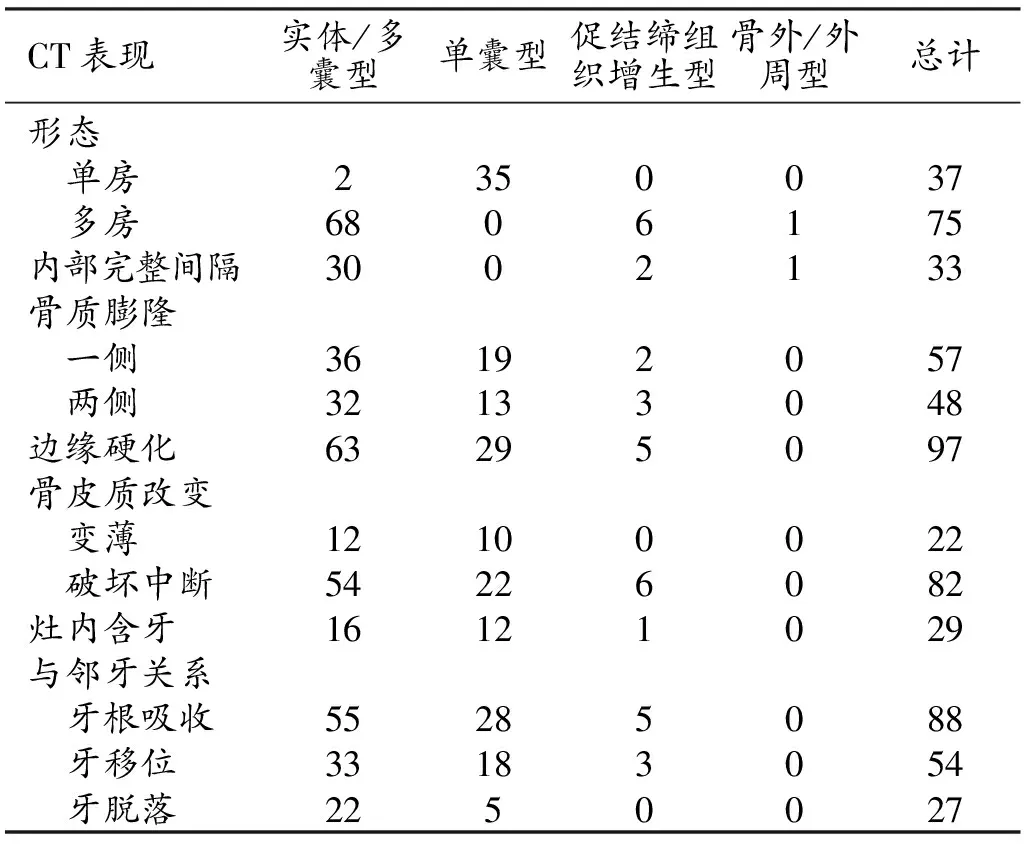
表1 各病理类型颌面部成釉细胞瘤CT特征
病灶内部间隔可表现为骨样高密度影、软组织密度影、或部分骨样部分软组织密度影,后两者于增强后可见不同程度的强化。
明显的骨质膨隆包括向一侧膨隆和两侧膨隆。一侧膨隆中向唇侧和/或颊侧44例以及向舌侧13例(图2),两侧膨隆为向唇侧颊侧和/或舌侧腭侧(图1)。骨内病灶边缘可见弧线状硬化。所有病灶周围骨髓腔内均未见明显增生硬化或破坏。 骨膜反应仅有1例,表现为层状骨膜反应。
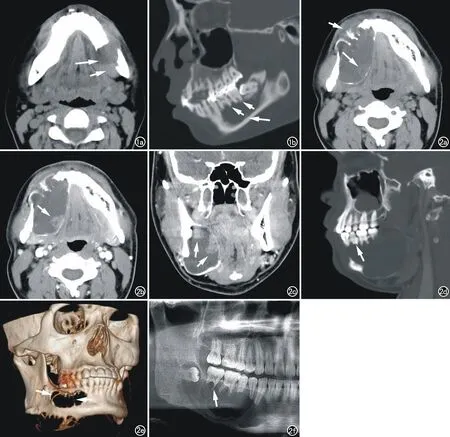
轴面软组织窗示右侧下颌骨颏部、体部多房囊实性灶,边界清楚,囊性部分CT值19HU,实性部分为囊壁上结节状突起(长箭),CT值42HU,病灶处骨质膨隆明显,向舌侧突出且,周围骨皮质变薄、颊侧局部不连续且部分突入颊侧软组织(短箭);b)CT增强横轴面软组织窗示增强后囊壁结节状强化(箭),增强后CT值85HU;c)CT增强冠状面重组软组织窗示增强后囊壁结节状强化(箭);d)CT矢状面重建骨窗示邻近牙根吸收(箭);e)VR示病灶内多个骨性间隔(箭);f)X线全景片显示骨质改变、邻牙牙根吸收(箭)及部分灶内骨性间隔。
图1 女,32岁,左下颌骨单囊型成釉细胞瘤。a) CT平扫横轴面软组织窗示下颌骨体部、角部单房状囊性灶,上层CT值15HU左右的囊液(长箭),下层为CT值60HU左右的血液(短箭),可见液-液平,病灶处骨质膨隆明显,向颊舌侧突出,周围骨皮质变薄、局部不连续; b) CT矢状面重组骨窗示病灶为单房状,内部见局部隆起的骨嵴(长箭),邻近牙根吸收(短箭)。图2 男,24岁,右下颌骨实体/多囊型成釉细胞瘤。a) CT平扫横
105例病灶与邻牙有关,表现为牙根吸收、牙移位和牙脱落。
4.周围软组织情况
本组中50例病灶突入周围软组织且与其分界不清(图2),2例周围软组织增厚,3例在周围软组织内形成肿块。9例表现为增强后周围软组织不同程度强化。
讨论
1.流行病学
颌面部成釉细胞瘤的发病具有明显的地域性特征,在非洲、中国和印度,它是最常见的良性牙源性肿瘤[5]。该肿瘤的好发年龄为30~60岁,平均发病年龄37.4岁,20岁以下者少见[6]。本组病例的发病年龄为10~86岁,平均34.98岁,略小于文献报道。
颌面部的成釉细胞瘤好发于颌骨,以下颌骨多见,下颌骨的成釉细胞瘤中80%发生于下颌磨牙区及下颌升支[6]。本组病例中,除1例外均位于颌骨内,位于上颌骨(13例)明显少于下颌骨(98例),而下颌骨中,又以前牙区为中心者明显少于以后牙区为中心者。以上结果与文献报道所述一致。本组病例中,下颌骨的成釉细胞瘤中,发生于单侧者(90例)明显多于双侧(8例),而发生于单侧的病例中,左、右侧的病例数相近(左侧42例,右侧48例)。
2.CT表现特征
颌骨内的病灶以分房大小不一的多房状为多,本组中占66.96%,分房大小一致的“蜂窝状”者较少,而两种分房形态同时存在者罕见(本组中仅1例)。多房状病灶内部可有或无完整间隔。间隔可为骨性或软组织密度的纤维性间隔,因后者于增强后可强化,故增强后显示纤维性间隔较平扫时清晰。
本组病例中,以囊性、囊实性肿块为多,而实性者较少,三者所占比例分别为44.64%,46.43%,8.93%。实性部分平均CT值为(45.056±11.434) HU,稍高于文献报道[7]。有学者报道[8],在继发感染时,成釉细胞瘤内部的CT值可达到100 HU或以上。这可能是本研究中成釉细胞瘤内部CT值偏高的原因之一。对照病理后发现,另一个内部CT值偏高的原因可能是肿瘤内的出血。Crusoé-Rebello等[7]认为实性成釉细胞瘤中央部分的CT值较低,在本研究病例中无类似发现。
Hayashi等[9]在组织学上证实了成釉细胞瘤是血供丰富的肿瘤;Tozaki等[10]通过对16例成釉细胞瘤动态CT观察后发现,对比剂注射30 s后成釉细胞瘤CT值明显提高。本研究中,肿瘤强化程度达50%以上的占84.85%(即以明显强化为主),这个结果与上述文献报道相符。
本组病例表现为肿瘤实性部分、囊壁和内部间隔的强化,囊壁上有时可见壁结节样强化。分析原因,囊壁强化及有时出现的壁结节状强化,主要是成釉细胞瘤上皮局限于囊壁表面或向进一步向囊腔内侵入形成壁结节而导致的[11]。而肿瘤内部间隔强化主要是由于成釉细胞瘤上皮侵犯腔内纤维囊而形成的[11]。
本研究中的肿瘤边界常较清楚,87.39%(97/111)骨内病灶有边缘硬化。颌骨内的肿瘤大多引起病灶处骨质的明显膨隆(94.59%,105/111),一侧明显膨隆者以向唇和/或颊侧膨隆明显者居多(77.19%, 44/57),此特征与文献报道的一致[12]。病灶周围骨皮质常见变薄或破坏中断(93.69%,104/111),尤以破坏中断居多(73.87%,82/111),骨皮质的上述改变可能与成釉细胞瘤的侵袭性有关[13]。
肿瘤邻近骨髓腔内通常无明显改变,骨膜反应亦少见(本组病例中仅发现1例有层状骨膜反应者,手术病理提示为实体/多囊型成釉细胞瘤伴不典型增生)。
肿瘤内含牙者较少,而与邻牙有关者极其多见(93.75%,105例,105/112),表现为牙根吸收截断、牙移位或者牙脱落,其中以邻牙牙根吸收者最多(83.81%,88例,88/105)。该肿瘤的这种侵蚀牙体及牙槽组织的现象,也是其具有侵袭性特征的体现[6]。
此外,本研究发现,原发性颌面部成釉细胞瘤的另一个侵袭性征象是其对周围软组织的侵犯,表现为突入周围软组织并与其分界不清以及周围软组织增厚或于周围软组织内形成肿块,部分病例增强后周围软组织有强化。44.64%(50/112)的病例于CT上观察到上述改变。
3.鉴别诊断
由于颌面部成釉细胞瘤为牙源性上皮肿瘤,发生部位有一定特征性,与周围牙一般都有关系,据此较易与骨源性良性肿瘤鉴别。
颌面部肿瘤中,与原发性成釉细胞瘤表现相似的最常见的肿瘤是牙源性角化囊性瘤。但后者通常骨质膨胀不明显;以单囊形态为主,多囊者分房大小基本一致;CT增强后内部多无强化表现;可有邻牙移位,但邻牙脱落和牙根吸收很少见,亦无牙槽骨、颌骨骨皮质破坏等侵袭性表现[6]。基于以上特点,通过仔细审阅螺旋CT图像,两者不难鉴别。
对于单囊型成釉细胞瘤,需与单纯性骨囊肿、含牙囊肿鉴别。单纯性骨囊肿多与牙体牙周组织无关,不会出现牙根破坏吸收现象[6]。含牙囊肿常位于所含牙的牙釉质-牙本质的交界处,所含牙常为恒牙,且多仅有牙根无牙冠,邻牙少有牙根吸收[6]。
4.比较影像学
X线:颌面部成釉细胞瘤的影像学诊断以前主要依靠X线全景片,但X线全景片的缺点是密度分辨率低、图像有重叠,这些缺点使其对该肿瘤的内部结构、周围软组织情况难以做出判断。
CT:螺旋CT具有明显高于X线全景片的密度分辨力的优势以及断层扫描的特点。付建国[14]认为, CT的高分辨力增加了空间信息的利用,对于诊断颌骨肿瘤性病变,CT能提供更多信息。应用MPR后处理技术,可从任意断面对肿瘤进行细致观察,对肿瘤内部结构尤其是纤维间隔的判断上更为精确,对周围软组织改变的显示更为清晰,因而弥补了X线全景片的不足。VR技术的应用,更为直观地显示了颌骨内成釉细胞瘤的骨质膨隆破坏。同时,VR图像能完整显示肿瘤内部骨性间隔以及肿瘤灶内含牙和邻牙情况。特别是对于邻牙牙根吸收的直观的三维的显示,其优势是非常明显的。这些不仅对于颌面部成釉细胞瘤的循证定性非常重要,更是临床医生制定治疗方案前希望得到的信息。CT检查的软组织分辨力较MRI低,对于密度相近的组织成分难以确定,CT平扫易漏诊或误判,只有通过增强才能辨别,但对于碘过敏的患者又无法行增强检查,这是CT检查的主要缺点。此外,CT还有射线量大、费用昂贵等缺点。
MRI:MRI具有软组织分辨力高、多参数、多平面成像、无电离损伤、不受碘过敏影响的优点。但其缺点是检查时间长、费用更昂贵。更重要的是,MRI对骨改变及骨性成分的判断不如CT,对牙的显示不敏感。因此,在对颌面部成釉细胞瘤的定位和定性上,MRI和CT孰优孰劣仍需进一步探讨。
综上所述,颌面部成釉细胞瘤的CT特征为骨质膨隆明显,肿瘤多为多房状、囊实性,边界清楚,增强后囊壁、间隔和实性部分明显不均匀强化,有侵袭征即骨皮质变薄或破坏中断、周围软组织改变、邻近牙根吸收截断、牙移位或牙脱落。
螺旋CT可从显示颌面部成釉细胞瘤内部结构及周围软硬组织的改变,可对肿瘤准确定位和定性,为指导临床治疗提供更有价值的帮助。
[1] McClary AC,West RB,Pollack JR,et al.Ameloblastoma:a clinical review and trends in management[J].Eur Arch Otorhinolaryngol,2016,273(7):1649-1661.
[2] Scholl RJ,Kellett HM,Neumann DP,et al.Cysts and cystic lesions of the mandible:clinical and radiologic-histopathologic review[J].Radiographics,1999,19(5):1107-1124.
[3] Barnes L,Eveson JW,Reichart P,et al.World Health Organization classification of tumours:pathology amp; genetics head and neck tumours[M].Lyon:International Agency for Research on Cancer,2005:298-302.
[4] Infante-Cossio P,Prats-Golczer V,Gonzalez-Perez LM,et al.Treatment of recurrent mandibular ameloblastoma[J].Exp Ther Med,2013,6(2):579-583.
[5] Mullapudi SV,Putcha UK,Boindala S.Odontogenic tumors and giant cell lesions of jaws-a nine year study[J].World J Surg Oncol,2011,9(1):68.
[6] 余强,王平仲.颌面颈部肿瘤影像诊断学[M].上海:世界图书出版公司,2009:41-47,53-56.
[7] Crusoé-Rebello I,Oliveira C,Campos PS,et al.Assessment of computerized tomography density patterns of ameloblastomas and keratocystic odontogenic tumors[J].Oral Surg Oral Med Oral Pathol Oral Radiol Endod,2009,108(4):604-608.
[8] Ariji Y,Morita M,Katsumata A,et al.Imaging features contributing to the diagnosis of ameloblastomas and keratocystic odontogenic tumours:logistic regression analysis[J].Dentomaxillofac Radiol,2011,40(3):133-140.
[9] Hayashi K,Tozaki M,Sugisaki M,et al.Dynamic multislice helical CT of ameloblastoma and odontogenic keratocyst: correlation between contrast enhancement and angiogenesis[J].J Comput Assist Tomogr,2002,26(6):922-926.
[10] Tozaki M,Hayashi K,Fukuda K.Dynamic multislice helical CT of maxillimandibular lesions:distinction of ameloblastomas from other cystic lesions[J].Radiat Med,2001,19(5):225-230.
[11] Slootweg PJ.Odontogenic tumours-an update[J].Curr Diagn Pathol,2006,12(1):54-65.
[12] 管帅,郝大鹏,刘吉华,等.颌骨成釉细胞瘤的影像学诊断[J].实用放射学杂志,2014,30(5):747-750.
[13] Scholl RJ,Kellett HM,Neumann DP,et al.Cysts and cystic lesions of the mandible:clinical and radiologic-histopathologic review[J].Radiographics,1999,19(5):1107-1124.
[14] 付建国.颌骨肿瘤性病变的CT诊断[J].放射学实践,2006,21(9):951-952.
ValueofspiralCTintheevaluationofprimarymaxillofacialameloblastoma
TIAN Tao,WANG Shao-ying,SHI Hui-min.
Department of Radiology,Shanghai Ninth People's Hospital,Shanghai Jiaotong University School of Medicine,Shanghai 200011,China
Objective:To assess the value of 64-slice spiral CT in the diagnosis of primary maxillofacial ameloblastoma.MethodsThe preoperative CT images of 112 patients with surgery and pathology proven primary maxillofacial ameloblastoma were analyzed retrospectively.Tumor pathology included 70 solid/multicystic type (n=70),unicystic type (n=35),desmoplastic type (n=6) and extraosseous/peripheral type (n=1).CT values of region of interest (ROI) in tumor before and after contrast administration were measured and the enhancement characteristics were analyzed.ResultsOf the 112 cases with primary maxillofacial ameloblastomas,there were cystic type (50 cases,44.64%),cystic-solid type (52 cases,46.43%) and solid tumor (10 cases,8.93%).75 tumors (66.96%) were multilocular.Contrast enhancement could be assessed in cystic wall,septa and solid regions.Mural nodular enhancement could be seen.The degree of enhancement was more than 50% in 28 cases (85%).Of the 111 cases with intra-osseous lesions,97 (87.39%) lesions had marginal scleroses,105 (94.59%) lesions had obvious osseous expansion,104 (93.69%) lesions had cortical thinning,destruction or interruption.105 (93.75%) tumors had close relationship with adjacent tooth.ConclusionImaging characteristics of primary maxillofacial ameloblastomas could be shown clearly on spiral CT,which can provide useful information for the guidance of clinical treatment.
Ameloblastoma; Tomography,X-ray computed; Pathology
200011 上海,上海交通大学医学院附属第九人民医院放射科
田涛(1975-),女,上海人,硕士,主治医师,主要从事头颈部影像学诊断工作。
王韶颖,E-mail:syw330@sina.com;石慧敏,E-mail:2240542827@qq.com
R814.42;
A
1000-0313(2017)11-1126-05
10.13609/j.cnki.1000-0313.2017.11.006
2017-03-05)
