豌豆种子吸附等温线与热力学性质研究
2017-11-16陶志超
杨 昭 李 想 陶志超
(天津大学机械工程学院,天津 300072)
豌豆种子吸附等温线与热力学性质研究
杨 昭 李 想 陶志超
(天津大学机械工程学院,天津 300072)
采用静态称量法测量30、40、50℃时豌豆种子的吸附等温线,对实验数据进行非线性拟合,并通过对净等量吸附热、微分熵、焓熵补偿、扩张压力、净积分焓和净积分熵等热力学性质参数的研究,分析种子吸附特性和进一步揭示吸附机理,为选择和优化种子干燥和贮藏条件提供理论依据。实验结果表明,温度恒定时,平衡含水率随水分活度升高而升高,吸附等温线属于类型Ⅱ且GAB模型拟合效果最佳(R2=0.998 9,误差平方和为4.52×10-5);净等量吸附热和微分熵随着平衡含水率升高而降低的规律符合焓熵补偿理论,该理论反映出吸附过程是非自发反应,属于焓驱动,而当干基含水率达到25%时,净等量吸附热值接近纯水的汽化潜热(43.30 kJ/mol);种子吸附过程的扩张压力随水分活度升高而升高,随温度升高而降低,当扩张压力一定时,净积分焓和净积分熵随着平衡含水率升高而降低,净积分熵达到最小值后逐渐升高,此最小值在30、40、50℃温度条件下分别为-137.79、-140.29、-137.74 J/(mol·K),对应的水分活度和平衡含水率分别为0.017、0.045、0.062和2.7%、2.5%、2.4%,这些条件可作为豌豆种子贮藏的最稳定条件。
豌豆种子; 脱附; 吸附; GAB模型; 热力学性质
引言
豌豆作为重要的蛋白质资源,具有较高的营养价值[1]。2014年我国豌豆总产量1 071万t,占世界产量的61.5%[2]。采后种子含水率较高,其生理活性和酶活性强,养分消耗速率快,以致运输和贮藏期间种子品质下降或发生腐烂。因此,有必要寻求最佳干燥和贮藏条件。
水分活度aw是含水食品质量评估的重要指标,而平衡含水率Me既能表明物料的物理、化学和微生物稳定性,又是食品干燥动力学、干燥特性曲线和传热传质等研究的重要基础数据。aw与Me的关系曲线,即吸附等温线,能够反映不同含水食品的吸湿性质,预测干燥过程水分变化,同时又是产品保质稳定性评估、包装方式设计、干燥设备设计以及采后干燥、贮藏条件优化的重要工具[3-4]。数学模型可预测物料不同条件下吸附等温线的变化,并有助于深入研究吸附过程的热力学性质。对其中涉及的热特性参数的研究有助于揭示吸附机理,分析干燥过程能量需求和优化物料贮藏的最稳定条件,为干燥过程和贮藏策略的高质量优化提供重要信息[5]。
目前,许多食品的水分吸附特性已有大量研究报道[3-9],MAJD等[10]发现Peleg模型描述葡萄种子吸附过程最佳。OUERTANI等[11]通过研究木材脱水过程的能量需求、焓熵关系以及扩张压力等参数的变化来优化其干燥工艺。然而这些报道对食品吸附的热力学性质研究只局限于净等量吸附热和微分熵等微分变化量,缺乏对食品整体能量变化和整体稳定性的考虑,如对积分焓和积分熵的了解有利于控制和预测贮藏期间水分与物料结合能的变化和食品发生腐烂的可能性,指导生产实践,对农产品的贮藏具有重要的价值。本文以豌豆为例研究种子吸附特性,预测模型及其热力学性质,在揭示脱水机理的同时,分析各热力学参数之间内在关系,为豌豆种子干燥、贮藏条件的选择和优化提供理论基础。
1 材料与方法
1.1 材料与仪器
新疆绿色中号豌豆,采购于天津市某农贸市场,初始含水率为14%(干基,下同)。吸附实验样品于45℃下干燥至含水率4%;脱附实验样品通过人工加湿至含水率35%。样品于4℃条件下密封保存。
1.2 平衡含水率测定
采用静态称量法测量样品含水率。将(5±0.1) g样品放入分别装有10种饱和盐溶液的密封瓶中(水分活度0.11~0.92),于30、40、50℃的恒温箱中保存。定期称量,当3次质量变化小于0.002 g时实验结束。初始含水率由干燥箱法测定[11],3次重复测量取平均。
1.3 等温线模型
表1中的4种模型用于拟合实验数据。本文采用误差平方和(SSE)和决定系数(R2)来评估模型拟合优劣。R2值越大,SSE越小,表明拟合度越高。表中n、A、B表示3个不同常量。
GAB模型的3个参数(Mm、C和K)都是温度的函数。Mm为单层含水率,C和K分别与单层吸附热和多层吸附热有关。温度对GAB模型参数的影响可表示为[12]
Mm=Mm0exp(ΔH/(RT))
(1)
C=C0exp((HM-HN)/(RT))
(2)
K=K0exp((HL-HN)/(RT))
(3)
式中HL——平均蒸气冷凝热,取43.30 kJ/mol
ΔH——阿罗尼乌斯能级因子,kJ/mol
HM、HN——单层、多层水吸附热,kJ/mol
R——通用气体常数,取8.314 J/(mol·K)
T——绝对温度,K
Mm0、C0、K0——常数
固体吸附表面积是指与被吸附水分直接接触的全部表面积,在确定食品的水结合性质中起着重要的作用,可由Mm确定[9],公式为
Sa=MmAmNA/MH2O=3.53×103Mm
(4)
式中Sa——固体吸附表面积,m2/g
NA——阿伏伽德罗常数,取6.022×1023mol-1
MH2O——水的摩尔质量,取18 g/mol
Am——水分子面积,取1.06×10-19m2
1.4 净等量吸附热与微分熵
净等量吸附热表示一定温度和水分活度条件下,物料中的水分蒸发热超出纯水汽化潜热的部分,是设计脱水设备的基础参数。在含水率一定时公式为[13]
(5)
式中qst——净等量吸附热,kJ/mol
若不考虑温度的影响,公式为
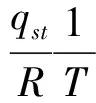
(6)
式中b——常数
微分熵指水分子与物料成分的吸引力或排斥力,是食品加工过程中能量分析的重要工具,其大小与特定能级下可获得水吸附位数量成正比。微分熵ΔS与aw和1/T的关系函数为
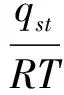
(7)
qst与Me之间的关系[4]为
qst=q0exp(-Me/M0)
(8)
式中q0——单层水分子净等量吸附热,kJ/mol
M0——初始含水率,%
1.5 焓熵补偿理论
焓熵补偿是指吸附过程中焓与熵的变化具有线性关系,该理论可用于研究许多食物系统中的物理化学现象,如蛋白质降解和抗坏血酸含量降低等[14],线性关系式[4]为
qst=TlΔS+ΔG
(9)
式中Tl——等速温度,即反应速率相同时温度,K
ΔG——温度为Tl时的吉布斯自由能,用于确定自发反应(ΔG<0)或非自发反应(ΔG>0),kJ/mol
参数Tl与ΔG由式(9)线性拟合计算得到。为了验证补偿理论,常将Tl与调和平均温度Thm作比较[11],公式为
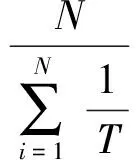
(10)
式中N——等温线总数
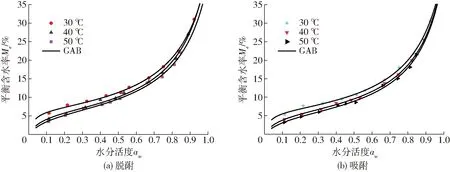
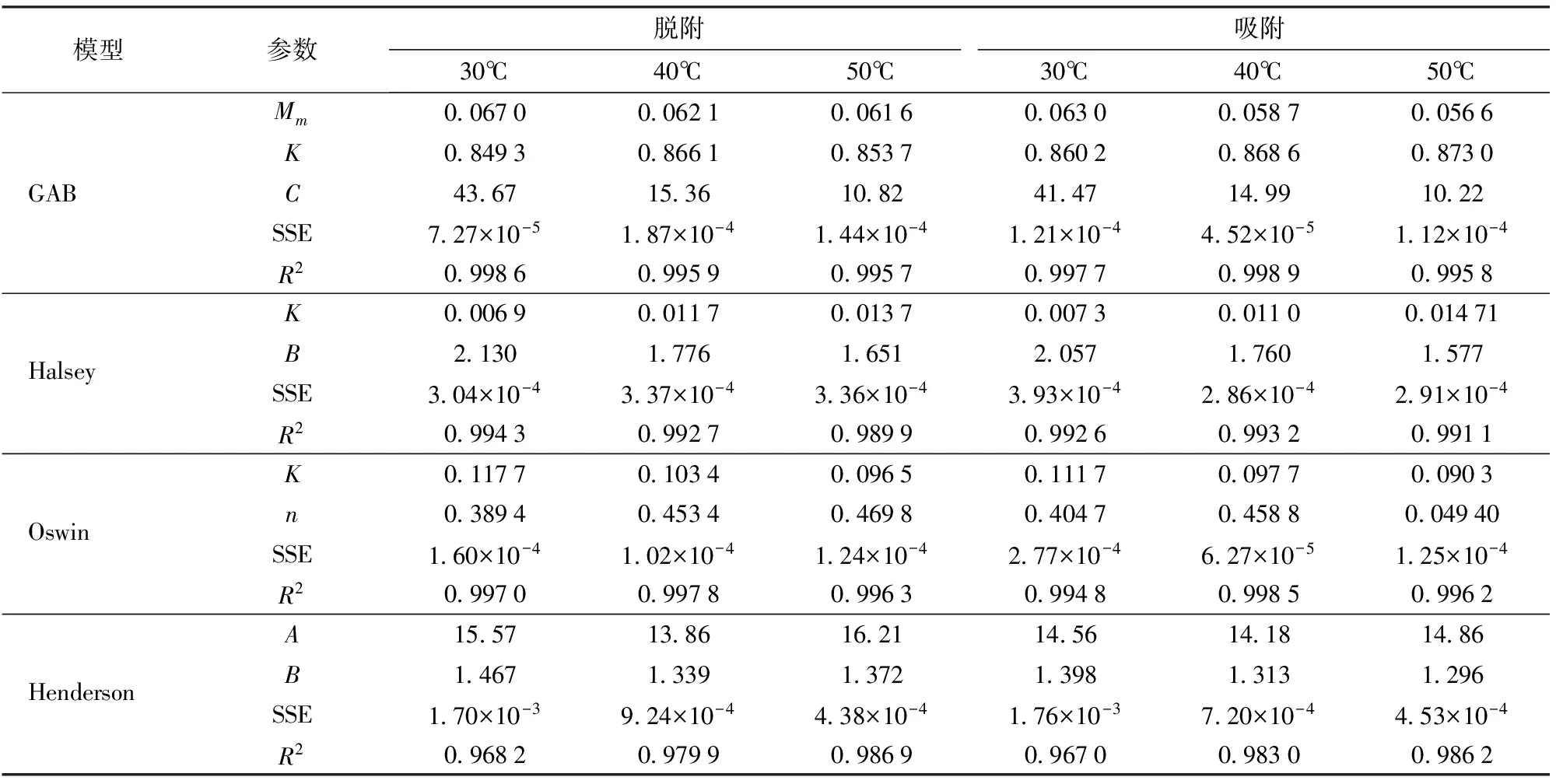
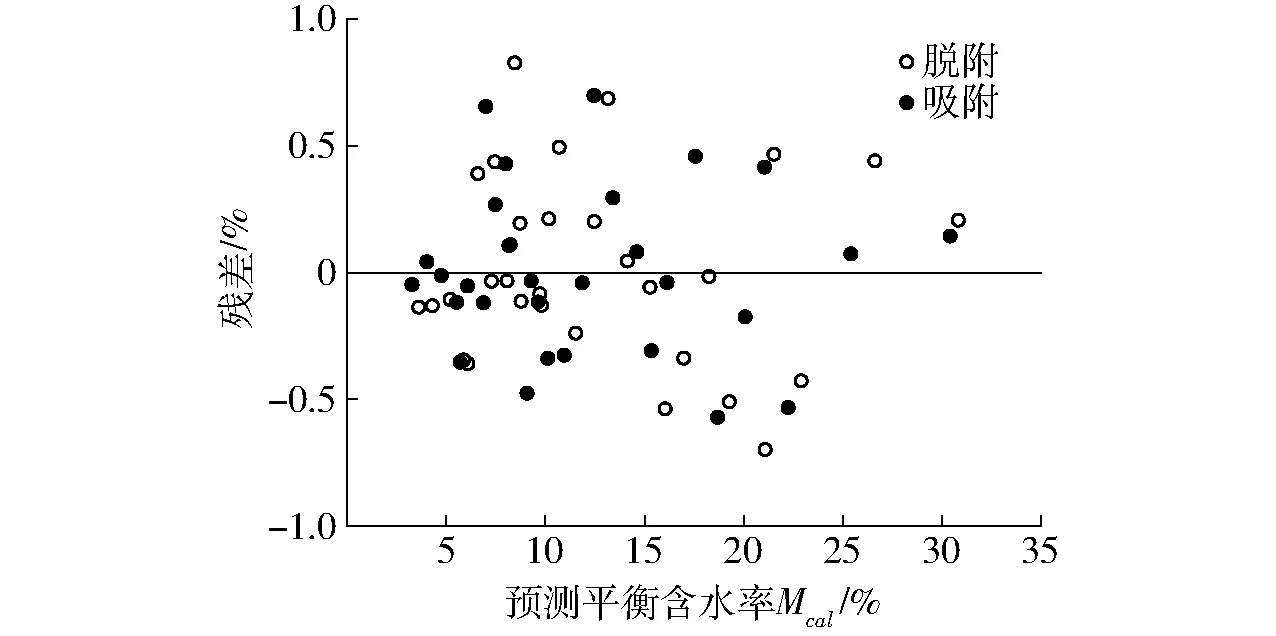
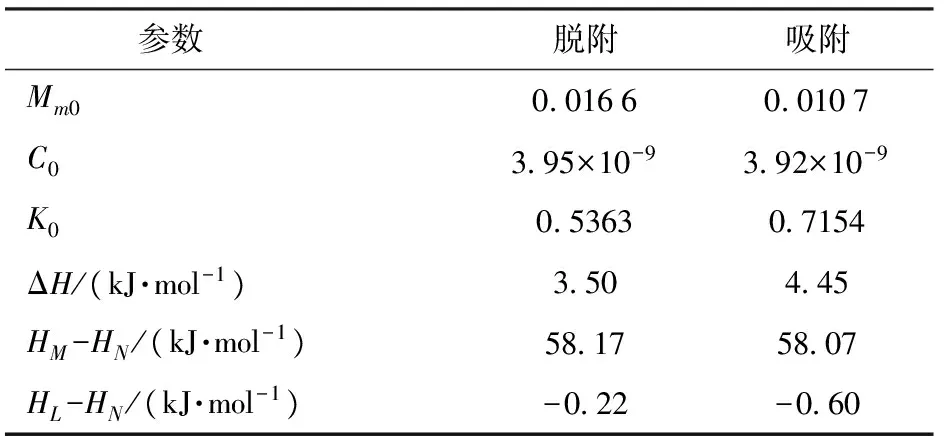
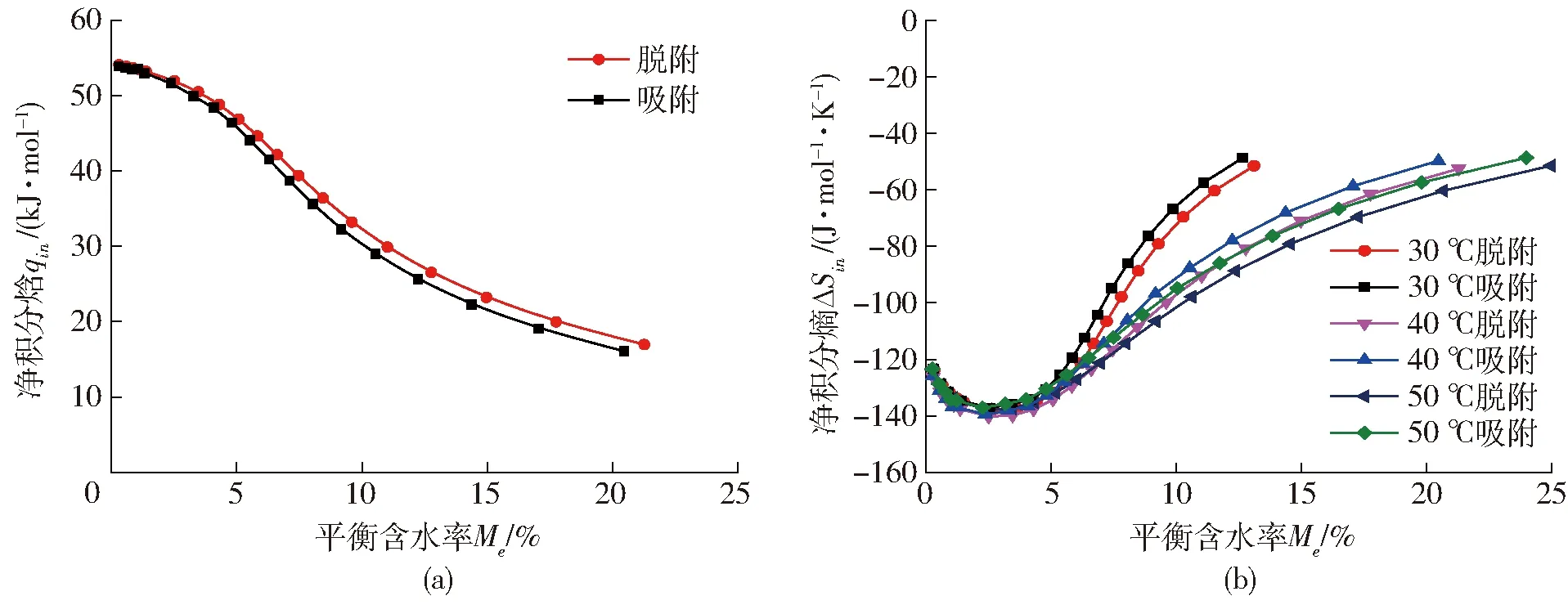
当Tl和Thm之间存在较大差异时,补偿理论才会成立。Tl>Thm时,吸附过程由吸(放)热控制,为焓驱动;Tl (11) 由于qst与Me有关,式(11)可变换得到 (12) 其中 ΨT=(1/Tl-1/T)-1 式中ΨT——温度校正系数 K1、K2——常数 ΨTlnaw与Me的关系可用于确定一定温度和水分活度下物料的含水率。若种子在不同温度下的数据可用式(12)表示,则说明ΨT适用,该经验式的有效性已被学者验证[4,11]。 1.6 扩张压力 扩张压力是为防止表面扩张而垂直作用在表面任意单位长度上的力,代表表面过剩的自由能,可反映多孔介质水分扩散的驱动力。其参数由GAB模型得到,计算式为[15] (13) 式中π——扩张压力,J/mol KB——玻尔兹曼常数,取1.38×10-23J/K 1.7 净积分焓与净积分熵 净积分焓qin代表全部可用能,能反映水分子与固体的结合强度。扩张压力π一定时,qin满足公式[15] (14) 净积分熵ΔSin表示水分子运动的无序性和随机性,量化了被吸附水分子的流动性,其计算公式为[15] (15) 2.1 吸附等温线 图1为豌豆种子在30~50℃时的脱附和吸附等温线。温度恒定时,Me随aw升高而升高。所有等温线呈S型,属于类型Ⅱ。在aw恒定时,Me随着温度的升高而降低,其原因在于水分子在高温下处于激发态,很容易脱离吸附位点,在微观上表现为吸附力下降,在宏观上表现为种子吸湿能力下降。因此,在保证种子活力的前提下,可适当提高贮藏温度和降低贮藏空气湿度来维持低水平的含水率,减小种子腐烂率。 2.2 等温线拟合模型 表2为4种等温线的模型拟合参数和检验结果。GAB模型对实验数据的拟合效果最佳,具有最高决定系数(R2=0.998 9)和最低残差平方和(SSE为4.52×10-5),可用于预测豌豆种子等温线,分析热力学性质。图2为GAB模型的残差分析,散点随机分布且平衡含水率预测值与实验值的残差很小,可忽略不计。 表3为GAB模型参数拟合结果。HM-HN为 图1 豌豆种子的脱附、吸附等温线Fig.1 Desorption and adsorption isotherms of pea seed 表2 豌豆种子脱附、吸附等温线模型参数及精度Tab.2 Model parameters and accuracy of desorption and adsorption isotherms for pea seed 图2 GAB模型拟合残差图Fig.2 Residual plots for GAB model 正值是由于水蒸气在主要的吸附位点发生强烈的放热反应,表明单层水分子吸附热高于多层水分子吸附热,这也解释了物料干燥后期由于内部单层水分子难以脱离固体表面,使得物料内部水分扩散速率低于表面蒸发速率而导致干燥速度下降。HL-HN为负值表明水汽凝结热低于多层水分子吸附热。脱附和吸附过程的焓值变化表明食品的水分吸附特性有一定程度的不可逆性[16]。表4为在30~50℃范围内与被吸附水分直接接触的种子固体表面积。可以看出,温度的变化对固体吸附面积有显著影响。随着温度的升高,水分子更容易脱离吸附位点,从而引起了单层含水率Mm的下降,因此Sa下降。多数食品的Sa都在100~250 m2/g范围内[17],而豌豆种子的Sa值接近250,较高的Sa值是因为内部较多微孔结构的存在。 表3 GAB模型特征参数Tab.3 Characteristic parameters of GAB model 表4 豌豆种子的固体吸附表面积Tab.4 Solid surface area of pea seed m2/g 2.3 净等量吸附热和微分熵 由表2中GAB模型计算得到qst与Me的关系曲线,如图3a所示。脱附和吸附时qst在低Me处均具有较高的数值(53.47 kJ/mol和52.39 kJ/mol),并随着Me升高而快速下降;Me达到25%后,qst逐渐趋于0,表明此时的蒸发热与纯水汽化潜热相同。这是因为在低含水率时,水分子在活跃的极性位点被吸附并形成单分子层,而将该层水分移除所需的能量较高。随着水分吸附形成多分子层,水分子与固体结合强度降低,导致qst降低。该现象表明干燥过程中单位水分移除所需的能量在不断变化,而物料干燥后期,应在保证物料品质的情况下适当提高能量(如温度)来维持单位水分的干燥速率。Me恒定时,脱附时qst高于吸附时,说明脱附过程热量的变化要比吸附过程大。由式(8)进行非线性拟合得到的qst与Me的经验关系式如下: 脱附 qstde=173.5exp(-Me/0.035 9) (R2=0.988 0) 吸附 qstad=183.7exp(-Me/0.033 5) (R2=0.992 3) 图3b为微分熵ΔS与Me的变化曲线。可以看出,ΔS随Me的升高而降低,在平衡含水率21%以后趋于稳定。脱附过程和吸附过程微分熵ΔS的变化范围分别为2.47~147.95 J/(mol·K)和1.06~146.56 J/(mol·K)。ΔS的变化说明可用吸附位数量在低Me时较多,并随着被吸附的水分子数量增加而减少。脱附时ΔS高于吸附时,说明脱附过程具有较多的吸附位数量。ΔS与Me的经验关系式如下: 脱附 ΔSde=522exp(-Me/0.033 4) 吸附 ΔSad=559exp(-Me/0.031 9) 图3 豌豆种子净等量吸附热与微分熵随含水率的变化关系Fig.3 Relationship of net isosteric heat and differential entropy of pea seed with equilibrium moisture content 2.4 焓熵补偿理论 图4表示qst与ΔS呈较高的线性关系,公式如下: 脱附 qstde=347.3ΔS+0.694 吸附 qstad=346.3ΔS+0.675 由拟合结果可知,Tl(347.3 K和346.3 K)与Thm(312.9 K)差异显著,焓熵补偿理论成立。Tl>Thm,表明过程由焓驱动。吉布斯自由能是提高吸附位点活性的必要因素[5],脱附过程ΔG(694 J/mol)和吸附过程ΔG(675 J/mol)表明2个非自发反应过程,需要能量供应,而控制贮藏环境的能量强度可减少物料的各类恶化反应,从而保证加工质量。 图4 豌豆种子吸附过程净等量吸附热与微分熵的关系Fig.4 Relationship of enthalpy and entropy for sorption processes in pea seed 图5 30~50℃时平衡含水率与温度校正系数的关系Fig.5 Equilibrium moisture at temperature range of 30~50℃ 图6 不同温度条件下的扩张压力等温线Fig.6 Spreading pressure isotherms at different temperatures 补偿理论可用于研究温度对水分平衡性质的影响,并确定温度、水分活度和含水率三者的关系。如图5所示,ΨT与Me在温度条件下二者表现为线性关系,即证明了温度校正系数ΨT适用于式(12)。由图可知,温度对水分平衡的影响遵循一次幂率,表明温度变化相同时,Me的变化也近似相同。通过线性回归得到脱附参数值(K1=10 732.16 K,K2=1.19×10-6)和吸附参数值(K1=10 467.18 K,K2=9.7×10-7)。 2.5 扩张压力 不同温度下π与aw的关系如图6所示。π随aw的升高而升高,aw恒定时,π随温度升高而降低。脱附过程与吸附过程具有相似的趋势。这表明其他条件不变时,aw的升高或温度的下降都会提高豌豆种子表面过剩自由能,并降低吸附位点活性,使水分子与吸附位点的亲和力减弱。木材和豆类也有类似的结果[11,15]。由此可得,干燥过程中,高扩张压力有利于维持高的干燥速率,而贮藏过程中,低扩张压力有利于抑制水分参与化学反应,维持物料的品质。 2.6 净积分焓与净积分熵 特定扩张压力下,净积分焓qin与Me的关系如图7a所示。qin随Me升高而降低。该变化与IGLESIAS等[18]的研究结果相似。IGLESIAS等[18]认为已被吸附的多层水使物料结构产生变化,水分子与固体表面吸附位点由于发生了相对位移而分离,造成固体与水分子的总结合能下降。净积分焓除了用于估测总干燥能量需求外,还与物料干燥速率相关。在干燥过程中,水分由多层逐渐转为单层,物料结构收缩,吸附位点彼此靠近,使剩余水分子被紧紧束缚,而总结合能的提高表现为干燥速率的下降。图中,脱附qin在Me为0.3%~21.3%范围内变化为16.94~54.08 kJ/mol, 吸附qin在Me为0.3%~20.3%范围内的变化为16.06~53.88 kJ/mol。可以看出,脱附qin高于吸附qin,可能是由吸附过程的不可逆膨胀导致的。 图7 豌豆种子净积分焓与净积分熵随平衡含水率的变化关系Fig.7 Relationship of net integral enthalpy and net integral entropy of pea seed with equilibrium moisture content 不同温度条件下的净积分熵ΔSin与Me的变化关系如图7b所示。低Me下,ΔSin随Me升高而降低。Me一定时,脱附ΔSin低于吸附ΔSin。随着种子吸附水分,脱附ΔSin在含水率2.4%、2.5%、2.7%处达到最低点,分别为-137.74、-140.29、-137.79 J/(mol·K),然后逐渐升高。上述净积分熵值代表最高的稳定性条件,与TORRES等[15]、KAYA等[19]的研究现象相似。最初的降低说明已有的吸附位点正趋于饱和,在单分子层处,最强吸附位点的吸附阻碍了水分子移动。随着水分吸附出现多层水分子,临界含水率以外的吸附水提高了ΔSin。此外,ΔSin为负值,可能是因为吸附剂本身结构的变化[19],而30℃时ΔSin快速升高并保持负值,说明低温能够减弱这种结构变化。在最小ΔSin处水分被强烈吸附,难以进行与种子腐烂相关的化学反应, 因此其对应的含水率优于GAB模型得到的单层含水率。30~50℃条件下,豌豆种子脱附过程达到最小ΔSin时对应的最稳定条件如表5所示,水分活度随温度升高而升高,该条件可为豌豆种子的贮藏提供有价值的参考。 表5 豌豆种子最稳定条件Tab.5 Maximum stability conditions of pea seed (1)豌豆种子的平衡含水率随水分活度降低和温度升高而降低,高温会降低种子的吸湿能力。为维持种子的贮藏品质,可适当提高贮藏温度和降低空气湿度。豌豆种子吸附特性属于类型Ⅱ等温线,描述该等温线的最适模型为GAB模型。 (2)净等量吸附热和微分熵与平衡含水率的变化关系表明在干燥过程中,随着水分蒸发,物料脱去单位质量水分所需的能量逐渐升高,移除水分将更加困难。因此,在保证物料品质前提下,应逐渐予以更高的能量来移除水分。 (3)调和平均温度与等速温度的不同验证了焓熵补偿理论,并得出吸附过程为非自发反应,由焓驱动;温度对食品吸附特性的影响遵循一次幂率,且此关系可用于预测30~50℃内物料的含水率。 (4)干燥过程中,适当提高温度使水分被快速移除,水分子与物料的亲和力会提高,即扩张压力降低;干后贮藏过程中,低空气湿度条件使物料表面维持较低的扩张压力,从而提高水分子与物料的亲和力,使水分难以参与化学反应。 (5)净积分焓随平衡含水率的降低表明水与固体结合强度的降低。30、40、50℃时的净积分熵分别在2.7%、2.5%、2.4%平衡含水率处存在最小值,说明上述温度、平衡含水率和对应的水分活度能使豌豆种子处于最稳定状态,有利于种子的贮藏。 1 DAHL W J, FOSTER L M, TYLER R T.Review of the health benefits of peas (PisumsativumL.)[J].British Journal of Nutrition, 2012, 108(Supp.1):S3. 2 FAO.Production crop[EB/OL].[2017-01-06].http:∥www.fao.org/faostat/en/#data/QC. 3 SAMAPUNDO S, DEVLIEGHERE F, BDE M, et al.Sorption isotherms and isosteric heats of sorption of whole yellow dent corn[J].Journal of Food Engineering, 2007, 79(1):168-175. 4 HASSINI L, BETTAIEB E, DESMORIEUX H, et al.Desorption isotherms and thermodynamic properties of prickly pear seeds[J].Industrial Crops & Products, 2015, 67:457-465. 5 FREITAS M L F, POLACHINI T C, SOUZA A C, et al.Sorption isotherms and thermodynamic properties of grated Parmesan cheese[J].International Journal of Food Science & Technology, 2016, 51(1): 250-259. 6 石启龙,赵亚,马占强.雪莲果吸附等温线及热力学性质研究[J/OL].农业机械学报,2014,45(1):214-221.http:∥www.j-csam.org/jcsam/ch/reader/view_abstract.aspx?file_no=20140134&flag=1.DOI:10.6041/j.issn.1000-1298.2014.01.034. SHI Qilong,ZHAO Ya,MA Zhanqiang.Moisture sorption isotherm and thermodynamic properties of yacon[J/OL].Transactions of the Chinese Society for Agricultural Machinery,2014,45(1):214-221.(in Chinese) 7 AGHA M K K, LEE W S, BUCKLIN R A, et al.Sorption isotherms for triticale seed[J].Transactions of the ASABE, 2014, 57(3):901-904. 8 SOLEIMANI M, TABIL L, SHAHEDI M, et al.Sorption isotherm of hybrid seed corn[C]∥CSBE/SCGAB 2006 Annual Conference, 2006: Paper No.06-215. 9 GABRIELAS R, MARIANAA M, LUIZAA P.Moisture sorption properties of chitosan[J].LWT—Food Science and Technology, 2010, 43(3):415-420. 10 MAJD K M, KARPARVARFARD S H, FARAHNAKY A, et al.Thermodynamic properties of water sorption isotherms of grape seed[J].International Agrophysics, 2014, 28(1): 63-71. 11 OUERTANI S, AZZOUZ S, HASSINI L, et al.Moisture sorption isotherms and thermodynamic properties of Jack pine and palm wood: comparative study[J].Industrial Crops and Products, 2014, 56: 200-210. 12 SANNI L O, ATERE C, KUYE A.Moisture sorption isotherms of fufu and tapioca at different temperatures[J].Journal of Food Engineering, 1997, 34(2): 203-212. 13 SIMAL S, FEMENIA A, CASTELL-PALOU, et al.Water desorption thermodynamic properties of pineapple[J].Journal of Food Engineering, 2007, 80(4): 1293-1301. 14 LABUZA T P.Enthalpy/entropy compensation in food reactions[J].Food Technology, 1980,34(2):67-77. 15 TORRES M D, MOREIRA R, CHENLO F, et al.Water adsorption isotherms of carboxymethyl cellulose, guar, locust bean, tragacanth and xanthan gums[J].Carbohydrate Polymers, 2012, 89(2): 592-598. 16 MCMINN W A M, MAGEE T R A.Studies on the effect of temperature on the moisture sorption characteristics of potatoes[J].Journal of Food Process Engineering, 1999, 22(2): 113-128. 17 CASSINI A S, MARCZAK L D F, NOREA C P Z.Water adsorption isotherms of texturized soy protein[J].Journal of Food Engineering, 2006, 77(1): 194-199. 18 IGLESIAS H A, CHIRIFE J, VIOLLAZ P.Thermodynamics of water vapour sorption by sugar beet root[J].International Journal of Food Science & Technology, 1976, 11(1): 91-101. 19 KAYA S, KAHYAOGLU T.Moisture sorption and thermodynamic properties of safflower petals and tarragon[J].Journal of Food Engineering, 2007, 78(2): 413-421. SorptionIsothermsandThermodynamicPropertiesofPeaSeed YANG Zhao LI Xiang TAO Zhichao (SchoolofMechanicalEngineering,TianjinUniversity,Tianjin300072,China) Sorption isotherms of pea seed were determined experimentally by using a static gravimetric at temperature of 30℃, 40℃ and 50℃ and within the water activity (aw) range of 0.11~0.92.Four mathematical models were determined by using non-linear regression method.The results showed that equilibrium moisture content (EMC) was decreased as the increase of temperature, and the GAB model fitted well the isotherms data of pea seeds and was considered as the best model for predicting seed moisture.The thermodynamic properties involving in net isosteric heat, differential entropy, enthalpy-entropy compensation, spreading pressure, net integral enthalpy and net integral entropy were analyzed systematically for further understanding of water sorption mechanism.The net isosteric heat and differential entropy were obviously decreased with the increase of EMC, which satisfied the compensation theory.The data indicated that moisture sorption of pea seed was non-spontaneous and enthalpy-controlled processes.And the net isosteric heat approached to the latent heat of pure water around 25% (dry basis).The expansion pressure of seed sorption process was decreased with the increase of temperature at givenawand increased with the increase ofawat a given temperature.When expansion pressure was at fixed level, the net integral enthalpy was decreased with the increase of EMC, while the net integral entropy was decreased with the increase of EMC to a minimum value of -137.79 J/(mol·K), -140.29 J/(mol·K) and -137.74 J/(mol·K) at 30℃, 40℃ and 50℃, respectively, and then tended to increasing trends.Theaw(0.017, 0.045 and 0.062) and EMC (2.7%, 2.5% and 2.4%), which resulted in the minimum net integral entropy values at the temperatures of 30℃, 35℃ and 40℃, respectively, can be considered as the maximum stability storage conditions of pea seed. pea seed; desorption; adsorption; GAB model; thermodynamic properties 10.6041/j.issn.1000-1298.2017.10.041 S375 A 1000-1298(2017)10-0323-07 2017-01-09 2017-04-17 天津市自然科学基金重点项目(16JCZDJC33900) 杨昭(1960—),女,教授,博士,主要从事制冷与热泵干燥研究,E-mail: zhaoyang@tju.edu.cn
2 结果与讨论
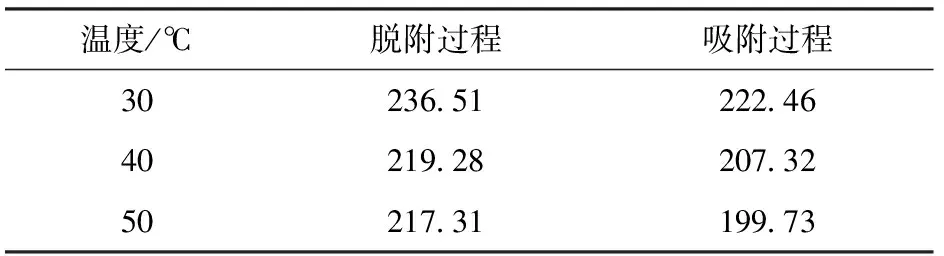
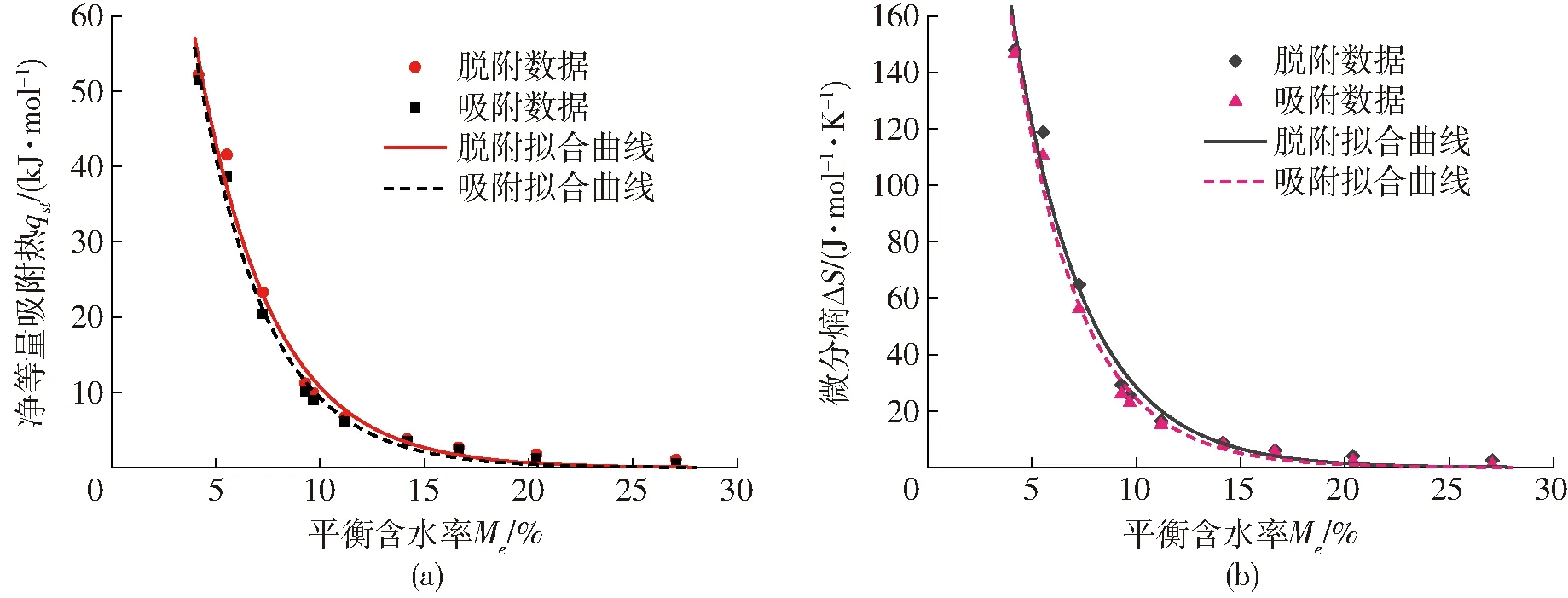
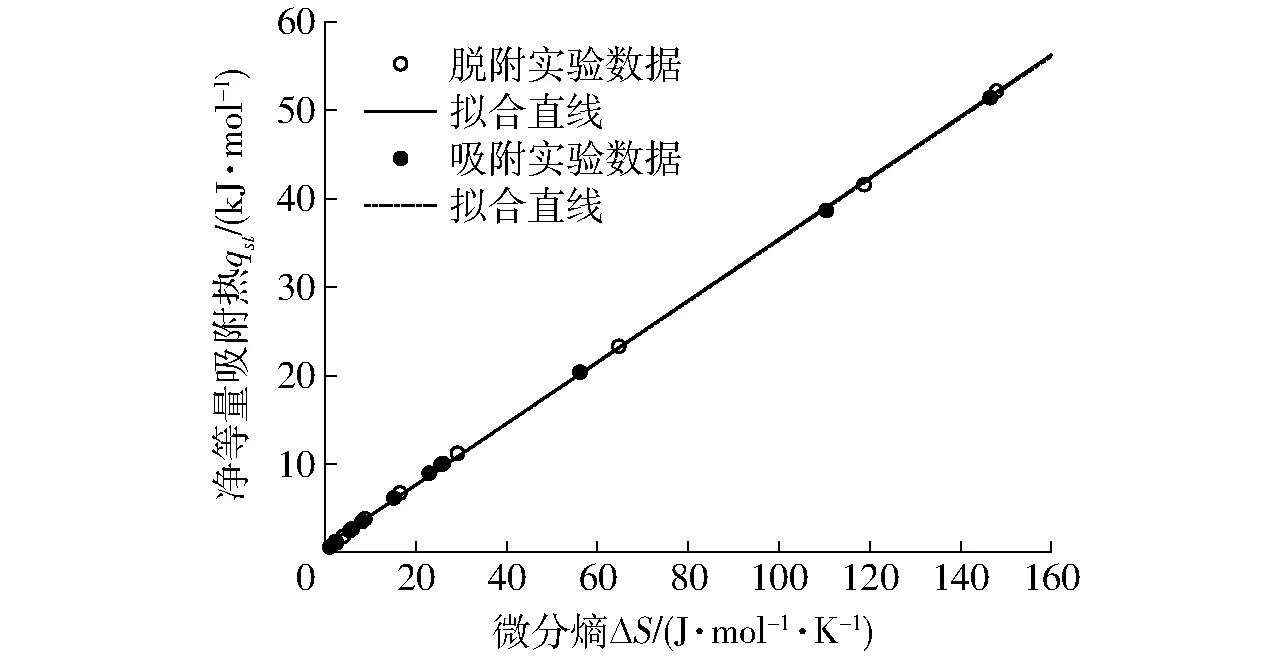
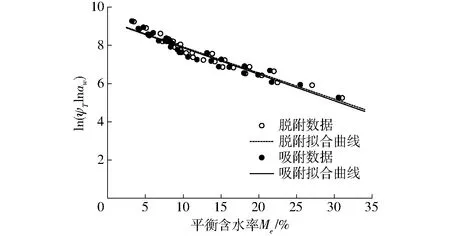


3 结论
