丁姜和胃膏贴剂体外透皮释药研究
2017-10-12张伟曹嘉王慧曹云飞王玮
张伟,曹嘉,王慧,曹云飞,王玮*
(1. 青岛市海慈医疗集团,山东 青岛 266033;2. 山东中医药大学,山东 济南 250355)
丁姜和胃膏贴剂体外透皮释药研究
张伟1,曹嘉1,王慧1,曹云飞2,王玮1*
(1. 青岛市海慈医疗集团,山东 青岛 266033;2. 山东中医药大学,山东 济南 250355)
采用体外透皮扩散池法,以离体大鼠腹部皮肤为屏障,对丁姜和胃膏贴剂透皮释药液中的丁香酚含量测定方法和不同时间段单位面积透皮累积释药量进行实验研究。结果表明,采用Agilent Zorbax SB-C18(150 mm×4.6 mm,5μm)色谱柱,甲醇-水(65∶35,V/V)为流动相,检测波长280 nm的色谱条件,丁香酚含量测定的重复性相对标准偏差为0.932%,24 h内样品溶液稳定性相对标准偏差为1.843%,平均加样回收率为97.419 2%,相对标准偏差为1.426%。透皮释药呈现一种先快后慢趋势,10 h以内累积释药总量占20 h内累积释药总量的76.71%,10~20 h内累积释药总量仅占23.29%。
丁姜和胃膏贴剂;体外透皮扩散池法;离体大鼠皮肤屏障;丁香酚含量测定;单位面积累积渗透量
Abstract∶The in vitro transdermal diffusion cell method was applied, the abdominal skin of rats in vitro was taken as the barrier, and the content determination of eugenol in transdermal solution of Dingjiang Hewei plaster and the cumulative release amount of transdermal drug per unit area in different time periods were researched. Experimental results showed the chromatographic conditions were as followed: Agilent Zorbax SB-C18column (150 mm×4.6 mm, 5 μm), methanol-water(65∶35,V/V) as mobile phase, detection wavelength was 280 nm, the RSD of the repeatability of eugenol content was 0.932%, the RSD of sample solution stability within 24 h was 1.843%, the average recovery was 97.4192%,and its RSD was 1.426%. Eugenol transdermal drug release showed a trend of first fast, then slow. The total cumulative drug release within the first 10 h accounted for 76.71% of the total cumulative drug release within 20 h, while the accumulative release total amount within 10~20 h was only 23.29%.
Key words∶Dingjiang Hewei plaster; in vitro transdermal diffusion cell method;isolated rat skin as barrier;the content determination of eugenol;cumulative transdermal amount per unit area
丁姜和胃贴膏为青岛市中医医院外用中药制剂,具有疏通经络、扶正祛邪、降逆止呕、行气安胎之功效[1-2],丁香酚作为丁香的主要活性成分[3-4],是该贴膏剂中主要生物活性成分之一。本实验以丁香酚为指标,进行丁姜和胃膏贴剂离体透皮释药液中的丁香酚成分含量测定方法以及膏贴剂的离体透皮药效学研究,为临床合理选择用药方法提供参考依据。
1 仪器与材料
RYJ-6B型药物透皮扩散实验仪(上海黄海药检仪器有限公司);Agilent1100型高效液相色谱仪(美国安捷伦公司);HHW-4 型双显恒温水浴锅( 金坛市双捷实验仪器厂)。
丁香酚对照品(批号:110725-201414,纯度99.8 %,中国食品药品鉴定研究院);甲醇(色谱纯,天津市凯信化学工业有限公司);其他试剂均为分析纯。
实验用丁姜和胃膏贴剂(批号150615),由青岛市中医医院中药制剂实验室按制备工艺制成。
实验动物健康大鼠(动物批号SCXK(鲁)2014-0007),由山东中医药大学实验动物中心提供。
2 实验方法与结果
2.1体外透皮释药实验
2.1.1 离体鼠皮制备
将健康大鼠腹部用电动剃毛机剃毛,再用8%的硫化钠脱毛,颈椎脱臼处死后,立即小心剥离腹部皮肤,除去皮下脂肪组织及粘连物,用生理盐水清净[5-6],置生理盐水中于-20 ℃低温冷冻保存备用[7]。每次用前自然解冻,选取无破损的完整鼠皮应用。
2.1.2 经皮渗透释药实验
将自然解冻后的鼠皮表面用滤纸吸干水分,鼠皮外表面与揭去防粘保护膜的丁姜和胃膏贴剂紧密贴敷,剪成与接受室口径大小一致的圆形贴片(2.8 cm2),鼠皮内侧面(真皮层)面向接受室,贴上膏贴剂的鼠皮外表面面向扩散室,再上夹固定于两室之间。自侧口向接受室中注满37 ℃保温的30%乙醇生理盐水液(释药接收液),排净空气,使鼠皮真皮层面与接受液充分接触[8-9];采用循环水浴保温,开动磁力搅拌子以150 r/min的恒速搅拌,维持接受室的动态环境,开始计时。
本实验使用的药物透皮扩散实验仪共有6套独立的渗透扩散装置,可以同时进行6组独立的经皮渗透释药实验。为方便实验操作,将同一批次样品膏贴剂分别安装到6套装置上,间隔30 min进行6组独立的平行实验。
2.1.3 待测经皮释药液制备
每组实验分别于开始计时后0.5、1、2、4、6、10、15、20 h 8个时间段从接受室侧口全部取出释药接收液,同时自侧口立即注满37 ℃预温的30%乙醇生理盐水,排净接受室气泡后继续实验[10-11]。将取出的释药接收液(约6.15 mL)用三氯甲烷提取3次,每次0.5 mL,提取液用三氯甲烷定容至2.0 mL,作为待测释药液。6套渗透扩散装置上的6组经皮渗透释药实验在设定的8个时间段,分别制得6组(每组8份)待测释药液,备用。
2.2丁香酚含量测定
2.2.1 色谱条件

2.2.2 对照品溶液制备
精密吸取丁香酚标准品适量,用一定量甲醇溶解后制成浓度为7.984 μg·mL-1的丁香酚对照品储备液10.0 mL。微孔滤膜(直径0.45 μm)滤过,取续滤液适量,加甲醇稀释制成浓度分别为0.7984、1.996、3.992、5.988、7.984 μg·mL-15个浓度梯度对照品溶液,备用。
2.2.3 供试品溶液制备
将2.1.2项下方法制得的第一套渗透扩散装置释药组4 h的待测释药液作为供试品溶液,备用。
2.2.4 HPLC图谱制备
将2.2.2项下浓度为5.988 μg·mL-1对照品溶液和2.2.3项下制得的供试品溶液,按2.2.1项下色谱条件进样测定,HPLC色图谱见图1。
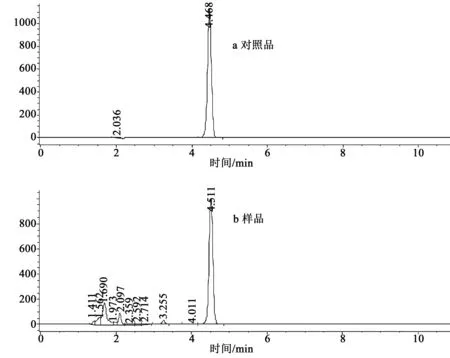
图1 高效液相色谱图 Fig.1 The chromatogram of HPLC
2.2.5 对照品线性关系
将2.2.2项下浓度分别为0.798 4、1.996、3.992、5.988 、7.984 μg·mL-15个浓度梯度对照品溶液,按2.2.1项下色谱条件进样、测定,记录峰面积。以丁香酚浓度(X) 为横坐标,峰面积(Y) 为纵坐标,进行线性回归,得到回归方程为:Y=1 273.9X+17.853,r=0.998 7。结果表明,丁香酚浓度在0.798 4 ~7.984 μg·mL-1范围内其峰面积呈良好的线性关系。
2.2.6 精密度实验
精密吸取浓度为5.988 μg·mL-1丁香酚对照品溶液10 μL,按2.2.1项下色谱条件重复进样6次,测得丁香酚的峰面积积分值分别为8 167.1、890.2、8 101.5、8 304.2、8 253.5、8 283.4,相对标准偏差为0.941 % (n=6)。表明该方法精密度良好。
2.2.7 重复性实验
精密吸取2.2.3项下制成的同一批供试品溶液6份,重复进样测定6次。丁香酚的峰面积积分值分别为7 103.5、7 145.6、7 185.9、7 148.2、7 202.7、7 018.2,结果相对标准偏差为0.932 %,表明样品重复性较好。
2.2.8 稳定性实验
取2.2.3项下制成的同一批供试品溶液适量,分别室温放置0、2、4、8、10、12、24 h后进样测定,丁香酚峰面积积分值分别为7 103.5、7 115.6、7 185.9、7 285.2、7 380.7、7 415.2。计算相对标准偏差为1.843 %,表明样品溶液在24 h内稳定。
2.2.9 加样回收实验
取已知丁香酚含量为5.562 2 μg·mL-1的透皮释药液5份,每份1.0 mL,分别精密加入浓度为7.984 μg·mL-1的丁香酚对照品溶液0.2、0.4、0.6L、0.8、1.0 mL,用甲醇定容至2.0 mL,分别制成理论值为3.579 7、4.377 9、5.026 2、5.974 7、6.773 1 μg·mL-1的5份加样样品液;按2.2.1 项下色谱条件分别进样、测定。5份样品重复进样测定5次,计算各份样品平均回收率和总平均回收率。结果丁香酚的总平均回收率为97.419 2%,相对标准偏差为1.426%。符合含量测定要求。实验结果见表1。
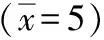
表1 丁香酚加样回收率结果
2.3丁香酚累积释药量测定
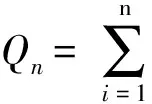

表2 丁香酚累积透皮释药实验结果(x±s,n =6)
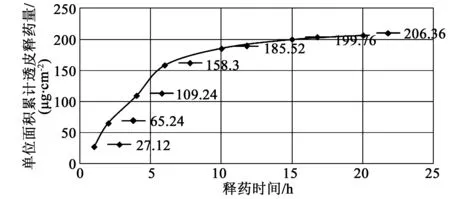
图2 丁香酚累积透皮释药曲线图Fig.2 Curve of the eugenol cumulative transdermal release (=6)
2.4实验结果及分析
不同时间段单位面积累积透皮释药曲线结果显示,丁姜和胃膏贴剂中丁香酚透皮释药呈现一种先快后慢趋势,10 h以内是快速透皮释药阶段,在此时间段的累积释药总量占20 h内累积释药总量的76.71%,10 h以后进入缓慢阶段,此时间段的累积释药总量仅占20 h内累积释药总量的23.29%。提示起效时间主要在10 h以内。这为临床合理用药提供了参考依据。
3 讨论
丁香酚是丁姜和胃膏贴剂主要生物活性成分之一,选择测定丁香酚单位面积离体鼠皮累积释药量,可在一定程度上体现该膏贴剂透皮药效情况。释药接收液的选择,既要充分考虑透皮成分的溶解性能,使其在持续释放出来后快速溶解,减少接受液对指标成分透皮释放的影响,还要考虑其他成分对指标成分含量测定的干扰。选择实验中,分别对生理盐水、不同浓度乙醇生理盐水接受液进行比较。结果显示,30%乙醇生理盐水杂峰少、丁香酚峰峰型好且与杂峰分离度高。因此,选择30%乙醇生理盐水作为最佳释药接受液体系。
外用药药物成分经皮渗透量一般较低。在接受液处理方法实验中,采用一次性全部取出接受液,并对其中的指标成分丁香酚采用三氯甲烷少量多次萃取,以增加相对浓度的处理方法。结果表明全部接受液提取3次,每次0.5 mL,能够完全提取接受液中丁香酚成分,释药成分测定结果精确度高。
丁香酚含量测定研究中,参考有关资料[12-19],实验比较了不同比例的甲醇-水、甲醇-醋酸水、甲醇-磷酸水和乙腈-磷酸水等流动相洗脱系统对丁香酚成分分离效果的影响,结果发现甲醇-水系统洗脱时间适中,其中甲醇-水(65∶35,V/V)丁香酚色谱峰与其相邻峰分离度最好,故选择此系统为HPLC法测定丁香酚含量的流动相。
以选定的色谱条件和实验方法,对丁姜和胃膏贴剂透皮释药液中丁香酚含量测定进行重复性、稳定性和加样回收率测定实验。结果显示,样品溶液丁香酚含量测定的重复性相对标准偏差为0.932%,24 h内样品溶液的稳定性相对标准偏差为1.843%,平均加样回收率为97.419 2%,相对标准偏差为1.426%,表明该方法能满足含量测定要求。
[1]李红彩, 于源源, 苏利英. 中药丁姜和胃膏神阙穴贴敷治疗妊娠恶阻疗效及对胃电图的影响[J]. 中华中医药学刊, 2014,32(3)﹕614-615.
[2]李红彩, 于源源. 中药丁姜和胃膏神阙穴贴敷治疗妊娠恶阻临床疗效观察[J]. 世界中医药, 2013, 8(8)﹕921-923.
[3]付振喜,王建清,金政伟,等.丁香挥发油的提取工艺及化学成分分析[J]. 安徽农业科学,2010,38(11)﹕5628-5630.
[4] 臧亚茹.丁香及其有效成分药理作用的实验研究[J].承德医学院学报,2007,24(1)﹕71-73.
[5]马永功,杨全伟,肖柳.消痤凝胶中丹酚酸 B 离体大鼠透皮率测定[J].湖北民族学院学报(医学版),2015 ,32(4)﹕64-66.
[6]何群,韩军涛,陈光宇,等.四妙君逸软膏与散剂离体透皮特性的比较研究[J].中成药,2012,34(6)﹕1052-1056.
[7]杨晓宁,禹玉洪,郝东方,等.丁桂儿脐贴体外透皮特性考察[J].中国实验方剂学杂志,2014,20(9)﹕9-11 .
[8]张伟, 唐明, 于爽,等.川芎超微细粉和普通细粉在通窍活血巴布剂中透皮释药的对比研究[J].世界中西医结合杂志,2012,7(10)﹕854-856.
[9]张伟,高文勇,张云丽,等.六白白疕巴布剂经皮吸收研究[J].齐鲁药事,2010,29(12)﹕710-711.
[10]张伟,唐明,张莉,等.通窍活血巴布剂体外透皮释药研究[J].中医外治杂志,2011,21(3)﹕5-6.
[11]吴和珍,付聪,杨艳芳,等.天杏咳喘贴中盐酸麻黄碱和盐酸伪麻黄碱的大鼠离体透皮试验[J].中国实验方剂学杂志,2013,19(18)﹕58-61.
[12]王友凤,曹云飞,张伟. 丁姜和胃贴膏组方药物超临界 CO2提取工艺研究[J]. 山东中医杂志,2016,35(12)﹕1067-1070.
[13]赵红革.HPLC法测定舒更胶囊中丁香酚的含量[J].山西中医学院学报,2013,14(1)﹕33-35.
[14]张锐,卢金清,江汉美,等.高效液相色谱法测定不同产地丁香中丁香酚含量研究[J].亚太传统医药,2015,11(12)﹕36-38.
[15]孙绪丁,李怀平,孙跃宁,等.HPLC法测定固本明目颗粒中丁香酚含量[J].亚太传统医药,2016,12(24)﹕39-41 .
[16]余小平.高效液相色谱法测定丁香中丁香酚的含量[J].药物分析杂志2008,28(6)﹕975-977.
[17]黎迎,陆洋,杜守颖,等.对《中国药典》2010 年版丁香药材中丁香酚含量测定方法的探讨[J].中药新药与临床药理, 2012,23(5)﹕579-582.
[18]乌珠木.HPLC 法测定蒙药安神补心六味丸中丁香酚的含量[J].中国民族医药杂志,2013,19(1)﹕49-51.
[19]王森,陈爱华,刘红宁,等.HPLC测定狗皮膏中桂皮醛和丁香酚的含量[J].中国实验方剂学杂志,2013,19(15):73-75.
Study on in vitro transdermal drug release of Dingjiang Hewei plaster
ZHANG Wei1,CAO Jia1,WANG Hui1,CAO Yun-fei2,WANG Wei1*
(1. Qingdao Hiser Medical Group,Qingdao 266033, China;2.Shandong University of Traditional Chinese Medicine,Jinan 250355, China)
R284.1
A
1002-4026(2017)05-0032-05
10.3976/j.issn.1002-4026.2017.05.006
2017-03-17
青岛市2014年度医药科研指导计划(2014-WJZD 058)
张伟(1962—),男,主任药师,研究方向为中药外用制剂剂型研究、中药制剂质量控制研究。E-mail:hczjsys@126.com
*通信作者,王玮(1972— ),男,主管中药师,研究方向为中药外用药剂型研究。E-mail: haicizw@126.com
