试论“发展学生核心素养”的基本路径
2017-09-16李志华
李志华
(南京师范大学苏州实验学校江苏苏州215133)
试论“发展学生核心素养”的基本路径
李志华
(南京师范大学苏州实验学校江苏苏州215133)
“核心素养”被誉为课程发展与设计的关键DNA。在教学实践基础上,结合名师教学课例研讨,提出“发展学生核心素养”的基本路径,即提升学生的“核心素养”必须从提升教师的核心素养开始;“发展学生核心素养”的教育教学改革必须从转变教育教学理念开始;“发展学生核心素养”必须从立足课堂、研究教学开始。
化学;核心素养;发展路径;课例
核心素养是“核心的”素养,不仅是“共同的”素养,更是关键的、必要的、重要的素养,是经过社会贤达精心挑选,而且是可学习、可教学、可评量的关键必要素养。关注“发展学生核心素养”的教学过程不仅可以提升教师课程设计与教学实施的效能及学生学习的效能,更可以发挥国民教育的学校功能,进而彰显个人发展与社会发展的协调功能。因此,“核心素养”被誉为课程发展与设计的关键DNA。
为加强名师引领,提高教学效益,探索“发展学生化学核心素养”的基本路径,苏州市教育科学研究院于2017年5月16日开展高中化学名师教学课例研讨活动。田长明(江苏省教学名师)和金茹(江苏省青年教师“高中化学”基本功比赛一等奖获得者)两位教师在江苏省苏州实验中学借班上课。教学课题为高中化学选修课程《化学反应原理》中的“酸碱中和滴定”。笔者有幸观摩此次活动,并就发展学生核心素养的基本路径,结合这两节课做出如下思考。
一、“发展学生核心素养”必须实现改变传统课堂
张华教授认为,阻碍核心素养发展的学习方式有:接受式学习、储蓄式学习、输入式学习等,其实这都是当下多数课堂教学中的主流。笔者以为“改课”的瓶颈不在学生,而在教师。老师们的口头禅是“教都教不会,还能自己学会呀?”,这种疑问式的感叹正是症结所在。多年的改革实践表明,课程改革的成败很大程度上决定于课程改革的意识和理念能否在课堂中生根发芽。现实中的课堂常常成为“教案剧”的演出舞台,教师是主角,接受能力强的学生是配角,多数学生是“路人甲”甚至是“听众或观众”。在这样的课堂教学里,主角和配角如果能成功地演绎预先设定的教案,教学就是成功的。这是传统课堂教学评价里属于具有正常样态的课堂,显然这种正常是“不正常”的,更是与“发展学生核心素养”背道而驰的。
事实上,儿童是天生就具备学习能力的。正如杭州特级教师刘松的观点:学习是与生俱来的,人天生就爱学习且会学习;学习是学生内部生成的过程;教师存在的专业意义完全就是让儿童发生更好的学习。因此,必须让自主学习、小组合作、充分展示(学习中的输出)等教学组织方式,以及质疑、纠偏、比较、完善、归纳、演绎等深度学习行为成为课堂的“核心要素”。
1.少教多学
传统课堂的最大问题是教师包办、学生依赖,学生没有成为学习的主体。瑞士教育心理学家皮亚杰认为:“一切真知都应由学生自己获得,或由他重新发现,至少由他重新建构,而不是草率地传递给他”。学生处于被动学习的地位,异化为知识的容器,无法体验知识形成的完整过程,更无法体验主动学习所带来的成就感。学习理论认为:“学习产生于经验,例如实践、对他人的观察等”。这一概念强调学习的主体性体验,这种体验让学习进入生命领域,因为有了体验,学习不再仅仅属于认知、理性范畴,同时也是身心发展和人格健全的过程,学习表现为学生主体性参与以及由此产生的自我建构。
金老师的教学案设计中出现了大量的“留白”,留给学生充足的学习空间,整个课堂“教”的时间不足15分钟。田老师的课堂以问题为线索展开学习,将问题抛出以后老师就“退居二线”,将充足的时间和空间让给学生。两位名师的研究课例均能积极探索“少教多学”的教学模式,即教师越来越少地教授知识,学生越来越多地主动学习。简而言之就是教师的“教”在时间和空间上做减法,学生的“学”在时间和空间上做加法,凸显学生学习的主体地位。让化学教学实现从以教师的教为中心到以学生的学为中心,从以课堂教学为中心到课堂教学与学生课内外自学相结合,从以传授知识为中心到传授知识与培养智能、提高核心素养并重的切实转变。
2.小组合作
小组合作学习中,教师的部分角色逐步由小组成员担纲,通过“兵教兵”的过程,让小组同学切身感受到“闭关自守”所无法领略的学习视界。优秀学生充分享受“教会别人、提升自己”的双重喜悦,建立起强烈的学习成就感。由于是学生之间的平等交流,课堂上交换意见、切磋思想、争论方法成为学习“新常态”,成绩暂时滞后的学生更能从小组合作中收获到传统课堂“师讲生听”所无法达到的学习成果,使核心素养提升成为可能。
这两节课均能积极倡导小组合作学习,调动小组每位成员的学习积极性。金老师在“酸碱中和滴定”操作阶段,安排同桌两人组成学习小组,分担准备、操作、观察、记录等工作。在“误差讨论”环节就出现的争议问题“滴定前俯视,滴定后仰视”组织小组讨论。田老师在进行“指示剂选择及变色情况”的教学中,让班级组成若干四人小组,分别研究酚酞、甲基橙、石蕊是否适合作为酸碱中和滴定的指示剂?如果用作指示剂,滴定前后的变色情况如何?
3.充分展示
传统教学的最大苦恼是学生不易看到自己的学习成果,难以回答“学习发生的程度及效果”。化学教学中学生展示的内容主要包括:再现学习知识、描述相应情境、呈现知识体系、解决实际问题、完成相应操作、交流学习心得、产生新的问题等。学生展示的组织形式主要包括异组同质展示、团队成果展示、个体优先展示、正误对比展示等。学生展示的行为方式主要有口头表达、实物展示、角色扮演、媒体演示、实验操作、模型搭建、板演、展板、墙报、表演、演讲、论文、辩论等。学生展示不仅是学习成果的展示,更是一次次通过高效学习,“核心素养”不断提升和强化的过程;学生展示不仅能满足学习知识的教学需要,更能达成学生“自我实现”的价值需求。学生展示强调思维外化,这为明确“学习是否发生”与衡量“学习是否有效”提供了可能。通过展示中的讨论形成师生、生生之间的“教学交往”、“协作活动”,将一次次“一知半解”升格为“全知全解”,使“核心素养”得以顺利发展。
如:田老师让学生完成计算“在20mL0.1000mol·L-1的盐酸溶液中,分别滴加0.1000mol·L-1的氢氧化钠溶液19.98mL和20.02mL,计算反应后溶液的pH值”以后,小组代表上台展示计算结果以及结果所带来的启示。金老师要求学习小组向全班展示滴定操作过程,其他同学及时指出滴定操作中的“不规范”问题并加以改正。
二、学科“核心素养”必须根植教师头脑之中
“化学核心素养”包含“宏观辨识与微观探析”、“变化观念与平衡思想”、“证据推理与模型认识”、“实验探究与创新意识”、“科学精神和社会责任”等五个要素。教师的首要工作是准确理解化学核心素养的内涵,并进一步把握化学核心素养的内容属性、内涵特点及内在联系等。
只有在完整地理解核心素养各要素的内涵和发展要求的基础上,教师才能在课堂教学设计中从教学内容、教学情境创设、教学方式选择、学习方式指导等方面系统化落实核心素养发展的各项目标。
1.理解核心素养内涵
在上课之后的说课阶段,两位名师分别就“发展学生化学核心素养”这一主题发表各自见解。从可操作的教学层面而言,化学核心素养包括“宏微结合的表征方法”、“变化可控的反应规律”、“服务社会的绿色价值”、“同类相似的物质性质”、“实验探究的实现途径”等。这些有别于传统教学所关注的知识、技能,将学科教学的目标指向“高阶思维和能力发展”,其实这才是“发展学生核心素养”的关键。
教师在发展学生化学学科核心素养时,要将学生学习兴趣的激发,结构化的化学基础知识的学习,科学探究和调查等关键能力的培养,化学基本观念、化学研究方法和思维方式的形成,化学学科价值的理解和价值观的建立融合等方面统一起来,其中既包含体现化学学科特点的学科素养,也包括跨学科的素养要素。
2.把握核心素养要素
教师在通晓学科核心素养的基础上,进一步确定出中学生应该具备的化学学科核心素养的发展要素。例如:物质的客观性和可认知性的观念与认知能力;科学精神、科学探究意识和探究能力;物质变化和能量转化的规律意识与理性思维习惯;宏观视野、微观分析和符号表征能力;交流合作意识、科学伦理意识和社会责任感等等。
通过化学课程的学习,使学生初步具备科学精神,具有社会责任感,养成合作意识,具备和他人交流、沟通的习惯和能力;初步形成化学学科的基本观念,能运用化学知识解释、预测物质结构、性质和变化,了解如何控制化学过程;初步具备科学探究能力,知道获取物质及其变化的信息、基于证据进行推理判断,具有批判性评估的能力,能运用化学知识参与社会问题的讨论,提出建设性意见等。沿着这样的路径,帮助学生发展核心素养的方向才不会跑偏。
3.优化教学单元设计
学科素养的形成,需要依托结构化的学科知识和技能,需要具备认识、理解自然和社会的学科观念和思维模式,还要了解学科学习和研究方法,在学习过程中孕育正确的世界观、价值观和人生观。
基于核心素养的教学单元设计,强调用结构化的思想,着眼于发展学生的学科素养,解读教学内容,整体安排教学设计。如果教师对教学内容在发展学生核心素养的功能心中无数,就无法通过化学知识的教学,有意识地发展学生的学科素养。其结果必然是把分散在教材不同章节里的教学内容,变成彼此之间互不相连的知识碎片,只抓知识点,而丢掉单元教学内容中蕴含的核心素养培养要求。
三、“核心素养”必须在日常课堂中生根发芽
化学核心素养的培养,要求通过课堂、依托课堂在发展学生适应社会和个人发展的必备品质和关键能力的培养上下工夫。教师应从基于有利于教师教的知识点单元设计转向基于有益于发展学生核心素养的单元设计。依据结构化的教学单元设计组织课堂教学,努力提高教师基于核心素养的课堂设计能力。积极探索基于问题解决的课堂教学设计,以问题及其解决作为教学的主线。在教师的策划、指导和支持下,学生积极主动地参与问题的发现、提出与解决,整理展示学习成果,在探索问题解决的过程中推进核心素养的有效发展。课堂教学还要紧紧围绕立德树人的方针要求,将人文素养、科学精神和伦理教育有机融合,全面发展学生的核心素养。
如:围绕“酸碱中和滴定”学习主题,确定基于核心素养的教学设计,两位名师分别采取不同的教学策略,将“发展核心素养”的中心任务落实在课堂教学之中。
1.突出反应原理的教学
化学反应原理旨在探究化学反应的规律及其应用。反应原理的教学让学生不仅“知其然”更能“知其所以然”,同时为有志于从事化学及其相关专业的学生提供较为完整和系统的化学反应原理相关知识,为将来进一步学习化学打下坚实的基础。两位名师都将“理解中和滴定的基本原理”作为重要的学习目标。
通过课前预习,学生已初步建立起“酸碱中和滴定是用已知物质的量浓度的酸(或碱)来滴定一定体积未知物质的量浓度的碱(或酸),通过测定反应完全时消耗已知浓度的酸(或碱)的体积,从而推算出未知浓度的碱(或酸)的物质的量浓度的方法”。
田老师在教学中的处理十分“老道”,课堂上通过问题链的形式引导学生深入思考。
问题1:现有一瓶未知物质的量浓度的稀盐酸,请设计方案测定它的浓度。
师生共同分析:
x元酸和y元碱反应完全时,应满足什么关系式?
xc(酸)V(酸)=yc(碱)V(碱)
我们把已知浓度的酸(或碱)称为标准液,未知浓度的碱(或酸)称为待测液,关系式又如何?
xc(标准)V(标准)=yc(待测)V(待测)
从而推出:
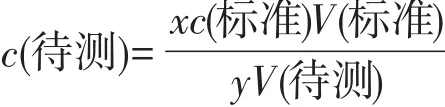
继而,田老师要求学生完成“练一练”:

图1 滴定过程中溶液pH的变化
用0.1032mol·L-1的盐酸溶液滴定25.00mL未知浓度的氢氧化钠溶液,至两者恰好完全反应时,用去盐酸溶液27.84mL,则氢氧化钠溶液的物质的量浓度为多少?
通过问题1的讨论,学生进一步加深了对酸碱中和滴定基本原理的理解。
问题2:现用一定浓度的稀盐酸标准液,滴定某浓度一定体积的氢氧化钠溶液,恰好完全反应时,溶液的pH为多少?我们如何判断反应已经完全?
给出“常见指示剂的变色范围”

引导学生思考:在0.1mol·L-1的盐酸溶液中,滴加0.1mol·L-1的氢氧化钠溶液,某同学认为滴加过程中溶液的pH变化情况如下图所示,你认为该同学的看法是否正确?
通过预先设置的“练一练”:在20mL0.1000mol·L-1的盐酸溶液中,分别滴加0.1000mol·L-1的氢氧化钠溶液19.98mL和20.02mL,计算反应后溶液的pH(lg5=0.7)。

图2 滴定过程中溶液pH的突变
学生通过计算发现,多滴0.04mL氢氧化钠溶液(不足一滴,补充告之胶头滴管的一滴液体约为0.05mL),溶液的pH值由4.3突变到9.7(如上图)。
要求学生完成“算一算”:现有某瓶氢氧化钠溶液(其真实浓度为0.1000mol·L-1),现用两种方法测定其浓度。
方法一:在20mL0.1000mol·L-1的盐酸溶液中,滴加2-3滴甲基橙做指示剂,然后滴加该氢氧化钠溶液19.98mL时,反应达到终点,计算该氢氧化钠溶液的物质的量浓度。
方法二:在20mL0.1000mol·L-1的盐酸溶液中,滴加2-3滴酚酞做指示剂,然后滴加该氢氧化钠溶液20.02mL时,反应达到终点,计算该氢氧化钠溶液的物质的量浓度。
学生通过计算得知,方法一所得浓度为0.1001mol·L-1,方法二所得浓度为0.0999mol·L-1。
由此学生得出“选用指示剂判断反应是否完全,肯定会存在误差,但选用合适的指示剂,会使误差很小,在许可的范围内,可以忽略不计”的结论。
2.重视实验操作的训练
化学是一门以实验为基础的自然科学,化学教学决不能离开化学实验。通过化学教学让学生掌握基本的化学实验方法和技能,了解化学实验在研究物质的组成、结构和性质中的应用。了解化学实验研究的一般过程,初步形成运用化学实验解决问题的能力。
金茹老师将课堂中的一大部分时间(约20分钟)“用心”于“如何进行酸碱中和滴定”的实验操作之中。
首先介绍滴定实验中涉及的仪器(酸式滴定管、碱式滴定管、锥形瓶、带蝴蝶夹的铁架台)及试剂(已知浓度的标准溶液、未知浓度的待测溶液)。
继而重点突破“如何进行酸碱中和滴定”这一重点问题。教学中,按实验步骤展开操作训练教学:
(1)滴定准备阶段
①查漏:首先检查滴定管是否漏水。
②洗涤:用蒸馏水将滴定管、锥形瓶洗净。
③润洗:分别用标准液和待测液润洗相应的滴定管。
④注液:向滴定管中注入相应的标准液和待测液,使液面位于滴定管0刻度以上2-3cm处。
⑤赶气泡:将滴定管尖嘴部分的气泡赶尽使之充满溶液。
⑥调节液面:将滴定管内液面调至0刻度或0刻度以下某一刻度,记录下初始刻度V0。
⑦加液:向锥形瓶中加入一定体积的待测液,然后滴加2至3滴指示剂。
(2)滴定
左手控制滴定管的开关,右手旋摇锥形瓶,边滴边振荡,眼睛注视锥形瓶内颜色的变化,滴定先快后慢,当接近终点时,应一滴一摇动,最后一滴刚好使指示剂的颜色发生明显的变化,且半分钟内溶液的颜色不变。
(3)读数
达终点后,眼睛平视刻度线,记下终了刻度V1消耗溶液V1-V0。
(4)复滴
重复上述操作2-3次。
(5)计算
根据滴定所用标准液体积,取几次操作的平均值,代入公式计算出待测液的浓度。
在“如何确定酸碱恰好完全反应”这一问题上金茹老师利用pH传感器(如左下图)并用计算机辅助绘图(如右下图)帮助学生成功突破这一教学难点。

图3 pH传感器应用于酸碱中和滴定
3.设置真实问题的情景
“问题情境教学”之父马赫穆托夫认为,“问题情境教学”的心理学依据是问题性思维理论。创设问题情境的实质是引起主体内心的认知冲突,动摇主体已有的认知结构平衡状态,以激起学生急于获取新知识的愿望和探究新事物的兴趣。发展学生学科素养,要求学科教学要在与现实生活紧密关联的、真实性的问题情境中展开,要采用基于问题的、基于项目的活动方式,基于体验、合作和探究的建构式学习。需要选择或创设合理的学习情境,通过恰当的学习活动以促进学习的发生,在学习者和情境的持续互动中,不断尝试问题解决的过程中形成学科观念、学科思维模式和探究技能等关键性素养。
“在实际问题情境的思考中解决问题”,两位名师都将此作为重要的教学原则和教学策略,分别体现在多处教学设计之中。
金老师在“数据处理”阶段,给出真实的三组实验数据引导学生分析思考。

表1 实验数据
同时与学生共同设计表格(如下图)帮助学生更好地进行数据分析,为以后的化学以及其他学科的试验数据分析提供良好的科学范例。这种不仅提出问题,更能和同学一起探究得出问题解决范例的做法,在现实教学中应不断加强。

表2 中和滴定(NaOH—→——HCl)数据处理表格
在“误差分析”部分,以0.1000mol/L的NaOH滴定20.00mL未知浓度的盐酸溶液为例:c(HCl)=c(NaOH)V(NaOH)/c(HCl)(如表3)。
田长明老师在“指示剂的选择”中让学生思考:用作酸碱中和滴定的指示剂(常见酸碱指示剂的种类及变色范围见下图)有没有具体的要求?

表3 误差分析

学生分析发现,酸碱中和滴定一般不选用石蕊做指示剂:其一是其变色范围大,其二是变色不明显。
继而通过研究得出,滴定终点时指示剂颜色的变化:

在“实验操作”中,引导同学思考:
如何量取20mL的盐酸溶液?
如何准确量取20.00mL的盐酸溶液?
如何准确量取20.00mL的氢氧化钠溶液?
通过这一问题将“粗略测量”与“精确测量”选用仪器的区别,以及“酸式滴定管”、“碱式滴定管”盛放试剂的要求基本解决。
“问题驱动”作为科学探究的基本方法和重要路径,这是“发展学生核心素养”的基本策略。
“核心素养”已成当下教育界的一大热词,以“发展学生核心素养”为导向的新一轮课程改革已拉开帷幕。苏州市教科院开展与组织的“发展学生化学核心素养”研究极具时代价值和深远意义。实践表明,提升学生的“核心素养”必须从提升教师的核心素养开始;“发展学生核心素养”的教育教学改革必须从转变教师的教育教学理念开始;教育教学改革的推进必须扎扎实实地从立足课堂、研究教学开始。
[1]闫桂琴,梁永平.中学化学教学论[M].北京:北京师范大学出版社,2010:23-33
[2]江苏省教育科学研究院课程教材研究中心,江苏省中小学教学研究室.普通高中课程标准教学要求[M].南京:江苏教育出版社,2007:56-59
[3]冯卫东.情境教学全操作手册[M].南京:江苏教育出版社,2010:61-63
[4]黄光雄,蔡清田.核心素养:课程发展与设计新论[M].上海:华东师范大学出版社,2017:4-10
[5]王云生.课堂转型与学科核心素养培养[M].上海:上海教育出版社,2016:3-50
[6]杨梓生.对高中化学学科核心素养的认识[J].中学化学教学参考,2016(8):1-2
[7]王有智.学习心理学[M].北京:中国社会科学出版社,2010:260-280
[8][美]戴尔·H.申克.学习理论(第六版)[M].南京:江苏教育出版社,2012:340-350
[9]姜正川.大脑是如何高效学习的[M].南京:南京大学出版社,2014:23-30
[10]丁芳.高中化学学科思想建构与能力培养的探索与实践[M].重庆:西南师范大学出版社,2016:96-98
[11]黄光雄,蔡清田.核心素养:课程发展与设计新论[M].上海:华东师范大学出版社,2017:3-6
1008-0546(2017)09-0013-05
G632.41
B
10.3969/j.issn.1008-0546.2017.09.004
