中药0期临床药效学试验探索*
2017-08-31梁丽喆李国信于雪峰
梁丽喆,李国信,于雪峰
中药0期临床药效学试验探索*
梁丽喆,李国信**,于雪峰**
(辽宁中医药大学附属第二医院沈阳110034)
目的:以舒血宁注射液为研究对象,探索中药开展0期临床药效学试验的可行性。方法:确立适合中药0期(早期)临床评价的关键技术标准。按照所建立的研究方法,进行健康受试者低剂量舒血宁注射液体内给药,收集给药前和给药后血清,进行人主动脉内皮细胞模型损伤的体外实验,并以临床给药剂量的血液样本为对照,验证低剂量用药与临床剂量用药的药效学趋势一致性。结果:在过氧化氢诱导的内皮细胞损伤实验中,低剂量舒血宁注射液含药血清能够影响细胞增殖,保护细胞形态,减少细胞损伤所导致的离子释放以及细胞上清分泌,转录组差异表达具有药效学趋势。结论:与临床给药组相比,低剂量给药具有大致相同的药理活性趋势,中药0期临床药效学试验具有可行性。
中药0期临床试验药效学舒血宁注射液
中药作为天然药物,具有多组分、多途径、多靶点等的特点,组分与靶点间的关系相互交叉,故在单味中药甚至方剂配伍的疗效研究中,探寻明确的作用机制相对困难[1-3]。随着中药现代化进程的推进,中药新药研发偏重于提取有效组分并且剂型西化,而组分中药能否替代单味中药或者处方所具备的疗效,成为中医界亟需解释和解决的问题。西药0期临床试验,以小样本、小剂量、短时间的方式在人体进行临床前试验,中药若能借鉴其“探索”思路,在新药研发初期,从微观角度进行人体的药效机制评价,将会拓宽中药新药优选途径,节约时间、经费和人力[4,5]。本研究与西药0期临床试验设计进行类比,拟定适合中药的0期(早期)临床评价方法,并以舒血宁注射液的示范性临床试验,对所建立方法进行验证。
1 方法学建立
1.1 药物选择
西药0期临床试验多数应用于肿瘤等没有治疗药物或治疗方案不合理的疾病,药物具备治疗窗宽、靶点明确、生物标记确证等特性[6];中药吸收代谢过程复杂,明确的药效机制探讨仅见于个别成分,选择符合中药开展0期(早期)临床试验的药物特点如下:①代谢途径相对简单:以静脉给药的中药注射剂为宜,作为代谢途径相对单一的中药成药,其直接入血,现代药理研究相对简单;②成分种类相对分明:选择成分种类分明(如黄酮、内酯类、生物碱)的药物进行试验,按每种成分的主要药效作用分别进行机制探讨;③生物标记相对确切:采用对其主要成分有足够研究基础的药物,从文献中获得用于该药物药效学检测的常用生物标记物、药物作用靶点以及相应检测方法,既可以对试验设计的科学性进行支撑,也能为临床验证提供便利。
1.2 试验设计
西药0期临床试验是在药物开发早期,于较短时间内在少量目标患者(不超过30人)进行结构类似化合物的临床研究,为从众多类似物中挑选出最佳候选药物提供理想平台[7]。针对中药成分在体内代谢复杂的状况,本研究将西药0期临床试验设计与中药特有的血清药理学方法相结合,进行健康受试者体内给药后的体外诱导损伤试验,模拟药物在患者体内代谢情况。通过检测给药前后含药血清作用下的细胞生物标记物变化,进行药效机制探讨,既避免了患者不能耐受小剂量给药,及健康受试者不能体现药物疗效的尴尬局面,又在一定程度上减轻伦理压力,在动物血清药理学实验的基础上更进一步。
1.3 指标选择
西药0期临床药效试验根据药物成分及作用特点,对起效靶点及能够反应疗效的生物标记物,采用芯片、放射元素跟踪等方式进行作用机制通路内的敏感指标检测[8,9]。中药药效作用相互交叉,故本研究采取复杂问题简单化的处理方式,将中药按照其效应成分的主要功能分类进行体外损伤诱导,再利用损伤后的血液样本及靶向细胞,进行较为公认的体外药效指标检测和全序列转录组基因测序,以此完成对多组分、多靶点的中药疗效的微观的、全面的探讨。
2 示范性试验
舒血宁注射液是从银杏叶中提取并制备的灭菌水溶液包括内酯类(银杏内酯A,B,C,白果内酯)和黄酮类成分,具有较为明确的抗氧化、抗血小板聚集等作用,临床常用于缺血性心脑血管疾病[10,11]。本文以低剂量舒血宁注射液的健康受试者含药血清干预H2O2诱导损伤的人主动脉内皮细胞,并与临床给药剂量组对照,比较其疗效趋势,探索中药开展早期临床药效学评价的可行性[12]。
2.1 材料与方法
2.1.1 试验受试者与细胞
8名健康志愿者,男女各半,年龄20-45岁,体重指数19-24(BMI=体重kg/身高cm2);心电图、血尿常规、凝血、肝肾功能等检查指标均在正常范围;无烟、酒嗜好;获取知情同意并志愿受试。人主动脉血管内皮细胞株(HAEC)由中国医科大学提供。
2.1.2 主要仪器与试药
JEM-1200EX透射电镜(日本电子株式会社);激光共聚焦扫描显微镜(德国Leica公司)。
舒血宁注射液(黑龙江珍宝岛药业股份有限公司,5 mL/17.5 mg,批号:B20140907);1640培养基、PAN胎牛血清、胰蛋白酶、青链霉素双抗(美国Hyclone公司);细胞毒性检测试剂盒、异硫氰酸荧光素标记的鬼笔环肽、Fluo-3/AM(美国Sigma公司);酶联免疫双抗体夹心法试剂盒(瑞士罗氏公司)。
2.2 含药血清制备
8名受试者分为低剂量试验组和临床剂量对照组,每组4人。分别将临床给药剂量的1/6.25(11.2 mg)和临床给药剂量(70 mg)的舒血宁注射液添加至250 mL葡萄糖注射液中,每天早晨用药前1 h统一进食,随后按一定滴速静脉滴注,2 h静点完毕,每天1次,连续给药7天。末次给药结束时从肘静脉取血10 mL,置于促凝试管中,离心得血清,56℃水浴灭活,微孔滤膜过滤除菌后,装冻存管-80℃冰箱保存。
2.3 细胞培养及分组
人主动脉血管内皮细胞株(Human Aorta Endothe⁃lial Cells,HAEC)常规复苏,90%贴壁时进行1:2传代。实验设空白组(细胞+空白血清)、模型组(细胞+空白血清+H2O2)、低剂量试验组(细胞+低剂量含药血清+H2O2)、临床剂量试验组(细胞+临床剂量含药血清+H2O2)。以0%、2%、5%、10%、15%、20%、25%、30%、50%的血清体积分数考察最佳空白血清添加量,每组设6个复孔。
2.4 过氧化氢诱导的内皮细胞损伤模型的建立
取对数生长期的HAEC细胞,2×108/L的密度100 μL接种于96孔板内,细胞培养箱中培养24 h,不同的96孔板分别加入浓度为100、200、300、400、500、600 μmol·L-1的H2O2共同培养24 h。终止培养后,每孔加入MTT溶液10 μL,避光继续培养4 h后弃液加DMSO 100 μL,避光摇床10 min,于酶标仪上测定各孔A492处的OD值。
2.5 细胞实验样本处理
以2×108/L的密度种板,细胞培养箱中培养24 h后弃去培养基,以含相应浓度的空白及含药血清的条件培养基预处理2 h,加入相应浓度H2O2,再次孵育24 h,按照检测试剂要求,对细胞及细胞上清液进行收样。
2.6 增殖能力测定
终止培养后,每孔加入MTT溶液10 μL,避光继续培养4 h后弃液加DMSO 100 μL,避光摇床10 min,于酶标仪上测定各孔A492处的OD值。
2.7 细胞凋亡流式检测
6孔板培养细胞,终止后胰酶消化收集,离心后PBS清洗,100 μL 1×binding buffer避光染色15 min(含Annexin V和PI各5 μL),作单染和空白对照,加入400 μL 1×bindingbuffer,过滤网转移至流失管中待测。
2.8 吖啶橙染色
96孔板培养细胞,终止后PBS清洗,将AO和EB溶液按1∶1混合制备工作液,2%比例PBS稀释后,每孔加入100 μL,5 min后镜下观察染色情况。
2.9 钙离子浓度测定
终止培养后HBSS溶液3次清洗,每孔加入稀释的Fluo 3-AM工作液以覆盖细胞为度;细胞培养箱孵育30 min,去液并用HBSS溶液清洗以充分去除工作液。每孔加入HBSS溶液以覆盖细胞,培养箱孵育约20 min后,用激光共聚焦或荧光显微镜检测细胞,激发波长480-500 nm,发射波长525-530 nm。
2.10 细胞骨架鬼笔环肽染色
96孔板培养细胞,终止后PBS清洗,每孔加入100 μL 4%多聚甲醛覆盖,室温固定30 min;PBS洗3遍,加入100 μL打孔液5 min;荧光洗液清洗、封闭;1∶1 000稀释Alexa Fluor 546 phalloidin染色,清洗4次;1∶600稀释DAPI染色剂,清洗4次;弃液,加入50 μL防荧光猝灭封片剂,封口膜封好,4℃保存待测。
2.11 透射电镜检测
6孔板培养细胞,终止后胰酶消化收集,加2.5%戊二醛固定。经漂洗,脱水,浸透,包埋,聚合,超薄切片,醋酸铀柠檬酸铅染色,于透射电镜下观察摄片。
2.12 细胞分泌功能测定
终止培养后,采用酶联免疫吸附双抗体夹心法(ELISA)对各组细胞培养液上清中NO、SOD和MDA含量进行检测,采用放射免疫法检测ET。ELISA过程严格按照试剂盒中说明书步骤进行。
2.13 全转录组RNA测序
对于低剂量试验组的空白血清和含药血清进行6孔板培养细胞,终止后胰酶消化收集,加入裂解液后冻存待测
2.14 统计学分析
应用SPSS 17.0进行统计描述和分析,计量资料用(xˉ±s)表示,多组间差异性比较采用ANOVA,两两比较采用LSD,P<0.05为差异有统计学意义。
3 结果
3.1 不同添加量空白血清对内皮细胞活力的影响
结果显示:15%的血清浓度对内皮细胞的增殖无明显抑制或促进作用,最接近常规培养,为理想条件(图1)。
3.2 不同浓度过氧化氢诱导内皮细胞模型建立的结果
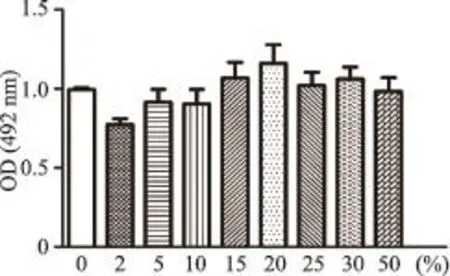
图1 不同添加量血清对内皮细胞毒性损伤OD值变化
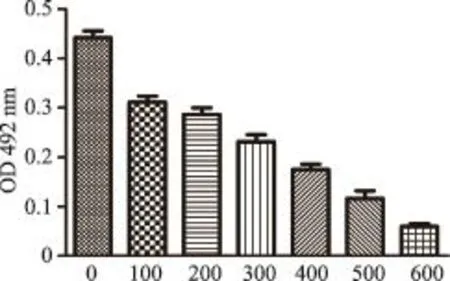
图2 不同浓度过氧化氢对内皮细胞毒性损伤OD值变化
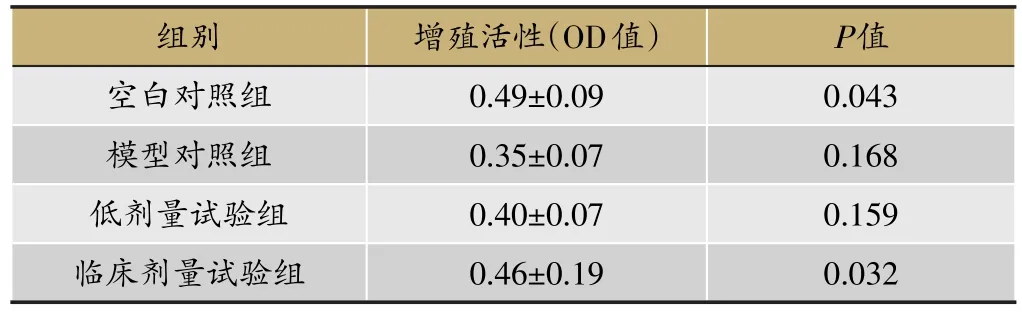
表1 各组血清对细胞增殖活性OD值的影响
由图2可见,细胞活力随H2O2浓度的升高而受到抑制,当H2O2浓度为300 μmol/l,作用24 h时,细胞损伤率接近50%,考虑为理想造模条件。
3.3 舒血宁注射液含药血清对细胞增殖活性的影响
由表1结果显示:与模型对照组相比,含药血清组均能改善细胞的增殖能力,且随药物剂量的增加,呈递增趋势。空白对照组与临床剂量给药组P<0.05,有统计学意义。
3.4 细胞凋亡流式检测
图3显示,模型组HAEC发生显著凋亡,14.7%早凋,66.6%晚凋,凋亡发生率81.3%;低剂量试验组血清干预后,晚凋下降至27.9%;临床剂量试验组早凋和晚凋均显著减少,试验组凋亡发生率分别为54.4%和23.2%。
3.5 吖啶橙染色
由图4可见,模型组出现明显凋亡,其中绿色荧光聚集和染色增强,提示早凋发生,个别细胞核有橘红色荧光,提示晚凋;在给予低剂量血清预先处理后,晚凋细胞明显减少;临床剂量试验组进一步缓解了凋亡情况,表现为细胞核染色较浅,细胞间染色均匀。
3.6 钙离子浓度测定
由图5结果所示:与空白组比较,模型组钙离子荧光强度明显增强,舒血宁注射液含药血清的干预,可以使钙离子荧光强度降低,具有药物浓度依赖性。
3.7 细胞骨架鬼笔环肽染色
由图6结果所示:空白组细胞骨架呈丝网状排列,清晰有序;模型组细胞形态皱缩排列紊乱,微丝减少或缺失;含药血清干预后,细胞形态趋于规则,随血清中药物含量增加,细胞骨架呈丝网状排列清晰可见。
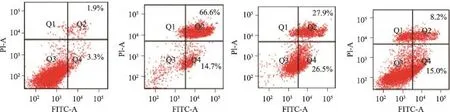
图3 细胞凋亡的流式检测
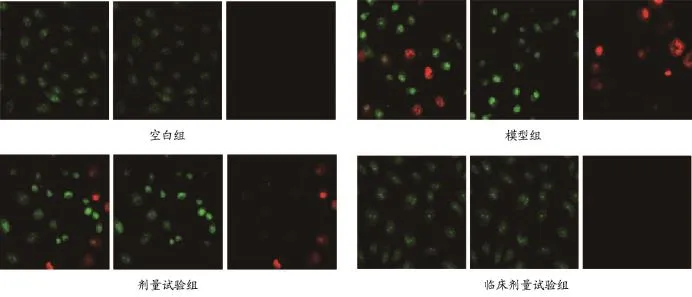
图4 吖啶橙染色
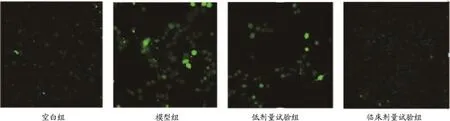
图5 各组细胞钙离子浓度测定(×400)
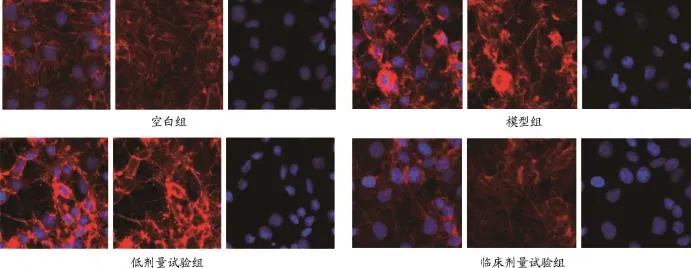
图6 各组细胞鬼笔环肽染色(×400)

图7 各组内皮细胞的超微结构(×15 000)

图8 各组内皮细胞的超微结构(×30 000)
3.8 电镜检测
由图7和图8结果所示:空白组细胞核呈椭圆形,核膜核仁清楚,染色质分布均匀,胞质内见溶酶体、线粒体、核糖体、高尔基复合体、粗面内质网及脂滴等细胞器。模型组细胞核形状不规则,核膜模糊,核内染色质凝聚,胞质小面积溶解,胞质内细胞器减少。舒血宁注射液含药血清干预后,细胞微观结构改善,随着血清含药量升高,细胞核逐渐清晰,胞质内细胞器逐渐增多。
3.9 细胞分泌功能测定
由表2可见,与模型组相比,试验组均能不同程度降低细胞内ET和MDA含量,提高NO和SOD活性,且随血清浓度的增加呈递进趋势。
3.10 全转录组RNA测序
由表3、表4可见,低剂量试验组含药血清干预前后(较模型组而言),基因表达和基因表达趋势均出现差异,与本药物已有文献对照,该差异符合药物已知功能。
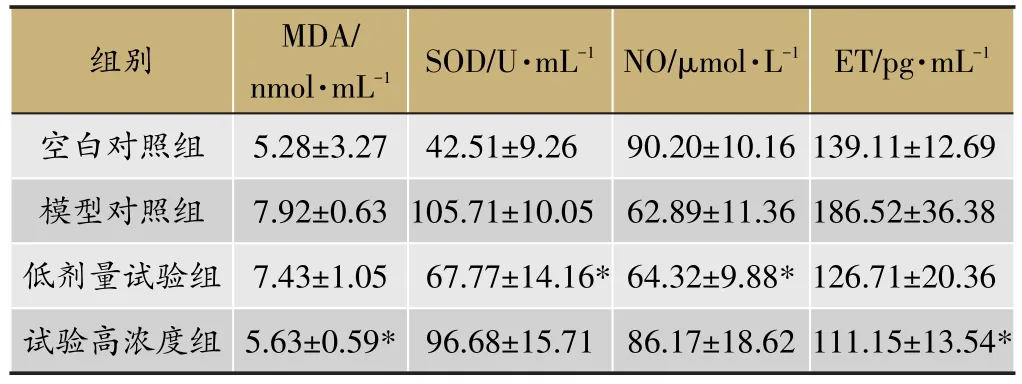
表2 不同组别血清作用下细胞MDA、SOD、NO、ET水平释放
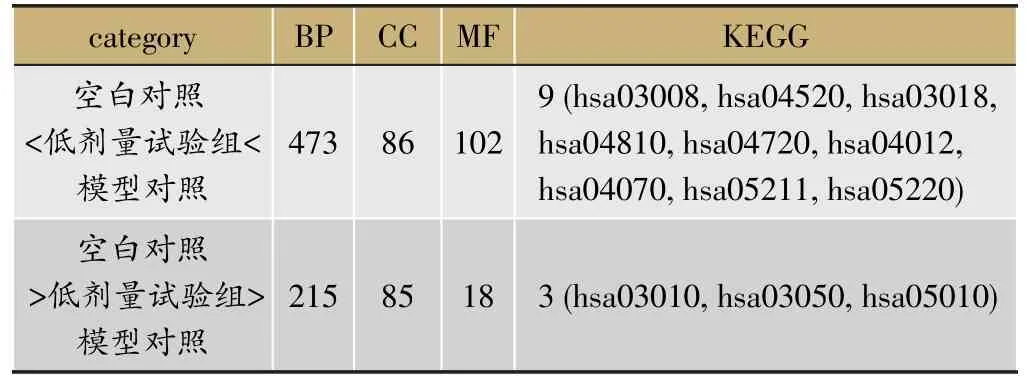
表3 试验组给药前后转录组基因表达差异(Enrichment_Analysis)
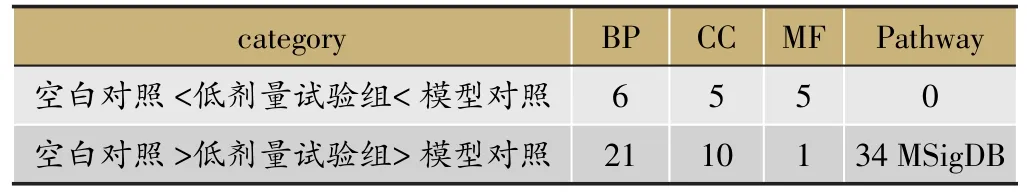
表4 试验组给药前后转录组基因表达差异趋势(GREAT_Analysis)
4 讨论
中药在长期的临床应用中,已经具备了明确的功效分类,大量的现代药理研究也为中药作用机制进行了有力补充[13,14]。在中药提取物的新药研发过程中,利用基因、蛋白组学对差异性测序结果进行解析,以及不为组分与靶点间错杂的对应关系所牵制,选择现代文献中该味或类似中药相关起效靶点作为检测指标,是中药早期临床评价中对于药效机制判定的两种候选方法[15,16]。
考虑到开展中药早期临床评价伦理审批的特殊性和疗效评价指标的敏感性,本研究以上市中药舒血宁注射液为示范,将健康受试者的含药血清作用于受损靶细胞,模拟疾病人群用药后的细胞状态,在前期的药代动力学探索基础上,确定药效试验的给药剂量和采血时间,对药物主要的效应成分(黄酮类)的主要功能(抗氧化作用)进行相应的体外诱导(H2O2损伤),结合透射电镜、放射免疫法、转录组测序等高敏感性检测方法,对低剂量中药的药效学进行综合评价,同时,两个剂量组大致相同的药效学趋势表明,中药早期临床评价具有可行性。
1金少华.中药西药化与西药中药化探讨.中国实用医药,2008,3(26): 173-174.
2李野,杨悦.中药研发的路径选择.中国药房,2005,16(11):815-816.
3叶峥嵘,吴琳.对“西药中药化”的思考.中华中医药杂志,2012,27 (10):2616-2617.
4U S Department of Health and Human Services Food and Drug Adminis⁃tration Center for Drug Evaluation and Research(CDER).Guidance for industry,investigators,and reviewers exploratory IND studies,2006.
5Kinders R,Parchment R E,Ji J,et al,Phase 0 clinical trials in cancer drug development:from FDA guidance toclinical practice.Mol Interv, 2007,7(6):325-334.
6FDA.Exploratory IND studies.http://www.fda.gov/Drugs/default.htm.
7EMEA.Concept paper on the development of a CHMP guideline on the non-clinical requirements to support early phase I clinical trials with pharmaceutical compounds.
8EMEA.Position paper on non-clinical safety studies to support clinical trials with a single microdose.2014.
9ICH M3(R2).Guidance on non-clinical safety studies for the conduct of human.clinical trials and marketing authorization for pharmaceuticals (step 5).2014.
10任艳萍.中药矮地茶质量控制与体内代谢及舒血宁注射液的多组分测定与药动学研究.石家庄:河北医科大学硕士学位论文, 2013.
11王世伟,张小慧.中药注射剂的不良反应现状及注意事项.中国医药导报,2011,8(4):118-120.
12林圆圆,杜武勋,张少强等.基于血清药理学的中药复方时效关系研究.中医杂志,2013,54(14):1175-1178.
13麦景标,冯俭,孙川,等.中药新药研发的新模式.湖北中医杂志, 2011,33(5):73-74.
14李朋收,时晓娟,刘洋洋,等.中药复方效应物质基础研究及展望.辽宁中医药大学学报,2014,16(9):108-113.
15金磊.中药研究开发的现状及对未来发展的思考.中国医药科学, 2011,1(18):32-33.
16周娜.中西医的碰撞.亚太传统医药,2015,11(17):1-2.
Abstract:Shu-Xue-Ning(SXN)injection was used as study subject in order to explore the feasibility of pharmacodynamics experiment of Phase 0 clinical trial in Chinese materia medica(CMM).This paper tried to establish key-technique standards which fit to the evaluation on CMM phase 0(early)clinical evaluations.According to the established research methods,this research selected volunteers and assured low dose SXN injection inside their body.And then,serum before and after medication were collected for the HAEC in vitro experiment.Blood sample of the clinical dosage was used as control to verify the tendency consistency of pharmacodynamics in low dose and clinical dose.The results showed that in the H2O2inducing HAEC damage experiment,low dose SXN injection can affect the cell proliferation,protect the shape of cells,reduce the release of ion owing to cell damages and influence the secretion in cells.Complete-sequence RNA gave differential multiterm expression before and after the low dose.It was concluded that compared with the clinical group,low dose medication had similar metabolic tendency.The pharmacodynamics experiment of phase 0 CMM clinical trial is feasible.
Exploratory on Phase 0 Clinical Pharmacodynamics Trial in Chinese Materia Medica
Liang Lizhe,Li Guoxin,Yu Xuefeng
(The Second Affiliated Hospital to Liaoning University of Traditional Chinese Medicine,Shenyang 110034,China)
Chinese materia medica,phase 0 clinical trial,pharmacodynamics Shu-Xue-Ning injection
10.11842/wst.2017.05.024
R969
A
(责任编辑:陈宁,责任译审:王晶)
2017-05-12
修回日期:2017-05-20
*科学技术部国家“十二五”重大新药创制项目(2012ZX09303-017):中药新药临床评价研究技术平台,负责人:李国信;辽宁省科学技术计划项目(2015225015):肺系重大疾病中医转化医学规范化研究,负责人:李国信。
**通讯作者:李国信,博士,主任医师,主要从事中药新药研究;于雪峰,硕士,主任医师,主要从事肺病中药研究。
