胸腹腔镜联合食管癌根治术后肺部并发症的危险因素分析
2017-08-12杨立新梁伟于婵娟吕红博权荣喜
杨立新 梁伟 于婵娟 吕红博 权荣喜
·论著·
胸腹腔镜联合食管癌根治术后肺部并发症的危险因素分析
杨立新 梁伟 于婵娟 吕红博 权荣喜
目的 分析胸腹腔镜联合食管癌根治术后肺部并发症的危险因素,探讨肺保护性通气策略对肺部并发症的影响。方法 行胸腹腔镜联合食管癌根治术患者348例,采用单因素和多因素分析方法探讨胸腹腔镜联合食管癌根治术后肺部并发症的独立危险因素。结果 348例患者肺部并发症的发生率为24.42%。多因素分析显示,高龄[优势比(OR)=3.934,95%可信区间(95%CI):1.431~9.478]、吸烟(OR=3.256,95%CI:1.204~8.863),术前合并糖尿病(OR=4.835,95%CI:1.454~11.562),术前合并慢性阻塞性肺疾病(OR=6.714,95%CI:1.528~13.762),肿瘤位于胸上段(OR=4.346,95%CI:1.447~10.382),术前合并低蛋白血症(OR=3.977,95%CI:1.344~9.896)是胸腹腔镜联合食管癌根治术后肺部并发症的危险因素,术中采取肺保护性通气策略(OR=0.273,95%CI:0.194~0.875)是胸腹腔镜联合食管癌根治术后肺部并发症的保护因素。结论 通过分析食管癌术后肺部并发症发生的相关危险因素,发现肺保护性通气策略是胸腹腔镜联合食管癌根治术后肺部并发症发生的保护因素。
胸腹腔镜联合食管癌根治术; 肺保护性通气策略; 危险因素; 保护性因素
肺部并发症(pulmonary complications,PCs)是食管癌术后最常见的并发症,其发生率达20.0%~40.0%,主要包括肺部感染、急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)、肺不张、肺栓塞、乳糜胸和胸腔积液等[1-4]。肺部并发症可导致食管癌手术患者的住院时间延长,并增加其住院死亡率[5-7]。自2000年首次报道胸腹腔镜联合食管癌根治术以来,胸腹腔镜联合食管癌根治术已被广泛地应用于治疗食管癌[8-9],与传统开放手术比较,可显著降低术后肺部并发症的发生率[9],尤其适用于年老或肺功能不良患者[10]。我们对胸腹腔镜联合食管癌根治术后肺部并发症的危险因素进行分析,重点探讨肺保护性通气策略对肺部并发症的影响。
对象与方法
一、对象
2015年1月~2016年12月,我院接受胸腹腔镜联合食管癌根治术的患者348例。纳入标准:(1)食管癌初治患者;(2)行全麻下胸腹腔镜联合食管癌根治术的患者;(3)术前美国麻醉医师协会(American society of anesthesiologists,ASA)分级为Ⅰ~Ⅱ级;(4)麻醉方式均采取单腔气管插管持续CO2吹入(人工气胸)法;(5)糖尿病和高血压等慢性疾病控制良好;(6)患者临床资料完整。
排除标准:(1)年龄>80岁或<18岁;(2)术前接受过放化疗;(3)合并严重心肺功能疾患及免疫疾病;(4)合并严重肝肾功能损害;(5)合并有其他肿瘤;(6)外科手术操作不当改为开胸手术者;(7)因胸膜粘连严重改为开胸手术者。本研究经新疆医科大学附属肿瘤医院伦理委员会批准(批准号:W2015102)。
二、方法
1.分组:回顾性分析术后10天内患者的体温、咳嗽、咳痰、胸片、血常规、痰细菌培养和动脉血气分析等临床资料,获取研究对象术后肺部感染、肺不张、肺水肿、支气管痉挛、低氧血症;吸空气氧的情况下患者动脉血氧饱和度(SaO2%≤91%)、持续30秒,同时动脉血氧分压(PaO2<60 mmHg),并排除同时并发其它肺部并发症]、ARDS的发生情况[11-13]。根据有无肺部并发症发生,将研究对象分为病例组(85例)和对照组(263例)。

表1 病例组和对照组基本情况和既往病史的单因素分析结果
注:与对照组比较,aP<0.05;BMI:体重指数;COPD:慢性阻塞性肺疾病
2.观察指标:收集以下变量作为研究因素:(1)基本情况及既往病史,包括年龄、性别、民族、居住地、文化程度、体重指数(body mass index,BMI)、吸烟史、饮酒史、高血压病史、糖尿病病史、慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)病史和冠心病病史。(2)临床病理特点:包括肿瘤部位、病理类型、TNM分期、术前肺功能第一秒用力呼气量/用力肺活量(FEV1/FVC)、术前C-反应蛋白(CRP)、术前血红蛋白、术前血小板计数、术中通气策略、手术时间和术中出血量。
三、统计学处理
结 果
1.基本情况:348例患者肺部并发症的发生率为24.42%(85/348),其中肺部感染49例,肺不张47例,低氧血症64例,气胸4例,ARDS 5例。病例组和对照组的基本情况和既往病史见表1。单因素分析显示,两组患者性别、民族、居住地、文化程度、BMI、饮酒史、高血压病史和冠心病病史比较,差异无统计学意义(P>0.05),年龄、吸烟史、糖尿病病史和COPD病史比较,差异有统计学意义(P<0.05)。
2.临床特点:病例组和对照组的临床特点见表2。单因素分析显示,两组患者病理类型、TNM分期、术前CRP、术前血小板计数和术中出血量比较,差异无统计学意义(P>0.05),肿瘤部位、术前肺功能、术前血红蛋白、术中通气策略和手术时间比较,差异有统计学意义(P<0.05)。
3.多因素分析:将年龄、吸烟史、糖尿病病史、慢性阻塞性肺疾病病史、肿瘤部位、术前肺功能、术前血红蛋白、术中通气策略和手术时间纳入多因素分析,结果显示,高龄、吸烟、术前合并糖尿病、术前合并慢性阻塞性肺疾病、肿瘤位于胸上段、术前合并低蛋白血症是胸腹腔镜联合食管癌根治术后发生肺部并发症的危险因素,而术中采取保护性通气策略是胸腹腔镜联合食管癌根治术后发生肺部并发症的保护因素。
讨 论
食管癌手术会挤压、摩擦肺泡,加之通气和非通气侧肺萎陷、通气侧肺内分流过度,引起气道压力和肺不张的面积增大,导致术后并发肺部并发症。食管癌术后肺部感染的发病机制包括肺防御机制削弱、肺组织顺应性降低和肺泡萎陷等,并与通气不良有密切相关性[14]。传统通气策略采取大潮气量(tidal volume,VT)通气方式,通过充分膨胀肺组织来避免潮气量过小引起的低氧血症、二氧化碳储留和肺不张等[15]。保护性通气策略以小VT通气为基础,辅以呼气末正压通气(positive end-expiratory pressure,PEEP)和肺复张(recruitment maneuvers,RM)[16],可降低肺泡过度膨胀产生的气道压和剪切力,减少肺泡表面活性物质的丧失,减少肺上皮细胞因机械刺激产生的炎性因子的释放,从而降低肺部乃至全身炎症反应[17-18]。本研究中保护性通气策略为VT(6 ml/kg)+ PEEP;5 cmH2O(1 cmH2O=0.098 kPa)]+Pplat≤30 cmH2O+RM。常规通气策略为VT(9 ml/kg)。两种策略的吸入氧浓度(FiO2)均为100%,术中维持呼气末二氧化碳分压(PetCO2)在35~45 cmH2O,并及时调整呼吸频率,以减轻二氧化碳储留。术毕停人工气胸后,保护性策略采用控制性肺膨胀方法:PC(40 cmH2O)+PEEP(0 cmH2O)+FiO2100%,持续40 s;传统策略采用传统手控膨肺5~10次。多因素分析显示,胸腹腔镜食管癌根治术中采取肺保护性通气策略是肺部并发症的保护因素,其优势比为0.273。

表2 病例组和对照组临床特点的单因素分析
注:aFEV1/FVC:第一秒用力呼气量/用力肺活量
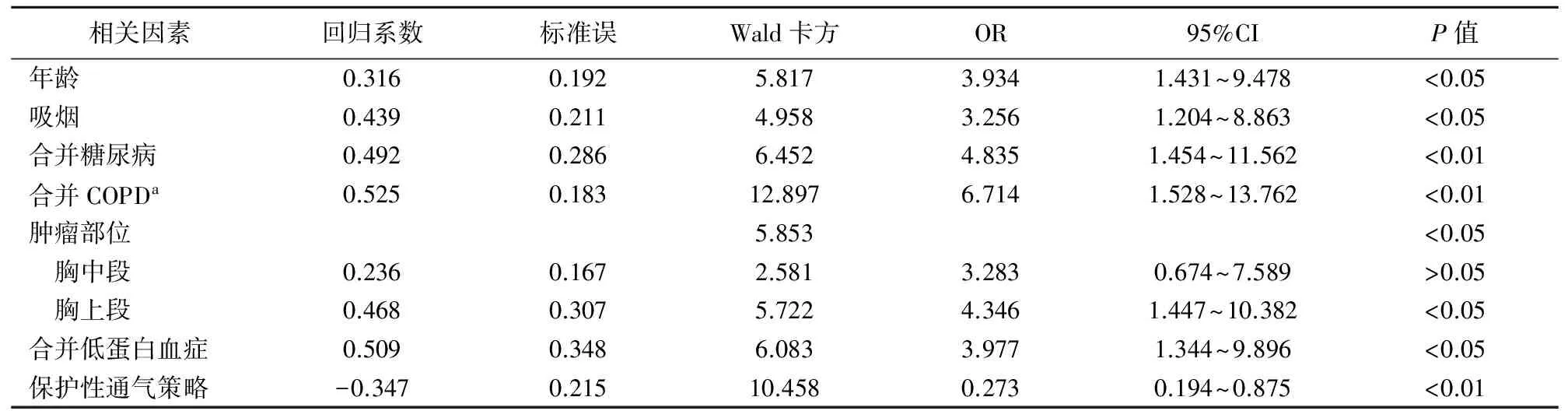
表3 胸腹腔镜联合食管癌根治术后发生肺部并发症的危险因素和保护因素
注:a慢性阻塞性肺疾病
肿瘤部位不同可导致手术对肺造成的损害程度也不相同,胸上段的吻合操作对肺挫伤程度更严重,更容易损伤支气管支、迷走神经肺支和喉返神经,喉返神经受损可引起声门闭合不良和吞咽功能障碍,患者不能有效咯痰,肺部感染和误吸发生率增高,故较高部位的吻合操作可导致肺部感染的风险增大[19];低蛋白血症可导致患者免疫功能降低,肺部感染的发生率显著上升[20-21],此类患者术后易出现肺分流增加、换气功能降低和肺间质水肿,可导致低氧血症;糖尿病患者长期高血糖状态可降低免疫功能,还可使血浆渗透压升高,白细胞的吞噬作用和趋化作用也会减弱[22]。此外,糖尿病患者的糖化血红蛋白上升,氧饱和度增加,血红蛋白不易释放出氧,易导致低氧血症;COPD患者气道的纤毛和上皮细胞,易并发术后肺部感染[23];高龄患者肺组织的顺应性、弹性回缩力和通气功能降低,支气管纤毛输送系统的功能降低,且常合并COPD,这些均可增加术后肺部感染的风险,加之高龄患者体质虚弱、免疫功能差,由此而导致的痰液淤滞和抵抗力降低更易并发肺部感染[24];烟草中的有害物质可损害肺和气管的生理功能,进而降低呼吸道的防御能力,且其损害程度与烟龄呈正比[25]。本研究发现高龄、吸烟、合并糖尿病、合并COPD、肿瘤位于胸上段、合并低蛋白血症是胸腹腔镜联合食管癌根治术后肺部并发症的危险因素,与之前的研究基本一致[2-3,11,19,21-24,26]。
总之,本研究通过调整食管癌术后肺部并发症的相关危险因素,发现肺保护性通气策略是胸腹腔镜联合食管癌根治术后肺部并发症的保护因素,具有临床推广的价值。
[1] Shirinzadeh A,Talebi Y.Pulmonary complications due to esophagectomy[J].J Cardiovasc Thorac Res,2011,3(3):93-96.
[2] 田学涛,黄吉利,田文涛.食管癌术后肺部感染的多因素Logistic回归分析[J].临床肺科杂志,2016,21(11):2080-2083.
[3] 马良赟,廖泽飞,王耿杰.食管癌术后肺部并发症危险因素的多因素Logistic回归分析[J].中国危重病急救医学,2011,23(10):625-628.
[4] D'journo XB,Michelet P,Avaro JP,et al.Respiratory complications after oesophagectomy for cancer[J].Rev Mal Respir,2008,25(6):683-694.
[5] Atkins BZ,Shah AS,Hutcheson KA.Reducing hospital morbidity and mortality following esophagectomy[J].Ann Thorac Surg,2004,78(4):1170-1176.
[6] Law S,Wong KH,Kwok KF,et al.Predictive factors for postoperative pulmonary complications and mortality after esophagectomy for cancer[J].Ann Surg,2004,240(5):791-800.
[7] Ferguson MK,Celauro AD,Prachand V.Prediction of major pulmonary complications after esophagectomy[J].Ann Thoracic Surg,2011,91(5):1494-1500;discussion 1500-1501.
[8] Lazzarino AI,Nagpal K,Bottle A,et al.Open versus minimally invasive esophagectomy:trends of utilization and associated outcomes in England[J].Ann Surg,2010,252(2):292-298.
[9] Zhang Y,Zhang GJ,Wu QF,et al.Combined thoracoscopic and laparoscopic esophagectomy:experience,technique and cautions[J].J Thorac Dis,2013,5(6):902-905.
[10]Zeng F,He B,Wang Y,et al.Combined thoracoscopic and laparoscopic minimally invasive esophagectomy[J].J Thorac Dis,2014,6(2):152-155.
[11]刘建民,张新叶.食管癌术后并发肺部感染临床分析与防治策略[J].河南大学学报:医学版,2013,32(2):147.
[12]黄春,汪斌,向小勇,等.胸外科高龄患者应用大剂量盐酸氨溴索的临床效果[J].中华胸心血管外科杂志,2012,28(3):171-173.
[13]Ferguson ND,Fan E,Camporota L,et al.The Berlin definition of ARDS:an expanded rationale,justification,and supplementary material[J].Intensive Care Medicine,2012,38(10):1573-1582.
[14]Wright CD,Kucharczuk JC,OBrien SM,et al.Predictors of major morbidity and mortality after esophagectomy for esophageal cancer:a Society of Thoracic Surgeons General Thoracic Surgery Database risk adjustment model[J].J Thorac Cardiovasc Surg,2009,137(3):587-595.
[15]Bendixen HH,Hedley-Whyte J,Laver MB.Impaired oxygenation in surgical patients during general anesthesia with controlled ventilation.A concept of atelectasis[J].N Engl J Med,1963,269:991-996.
[16]Ferrando C,Mugarra A,Gutierrez A,et al.Setting individualized positive end-expiratory pressure level with a positive end-expiratory pressure decrement trial after a recruitment maneuver improves oxygenation and lung mechanics during one lung ventilation[J].Anesth Analg,2014,118(3):657-665.
[17]Lipes J,Bojmehrani A,Lellouche F.Low Tidal Volume Ventilation in Patients without Acute Respiratory Distress Syndrome:A paradigm shift in Mechanical Ventilation[J].Crit care Res Pract,2012,2012:416864.
[18]Tusman G,Bohm SH,Warner DO,et al.Atelectasis and perioperative pulmonary complications in high-risk patients[J].Curr Opin Anaesthesiol,2012,25(1):1-10.
[19]刘树,汪道峰,方翼,等.食管癌三野淋巴结清扫术后肺部感染的危险因素分析[J].中华医院感染学杂志,2013,23(11):2604-2606.
[20]Gupta SC,Reuter S,Phromnoi K,et al.Nimbolide sensitizes human colon cancer cells to TRAIL through reactive oxygen species- and ERK-dependent up-regulation of death receptors,p53,and Bax[J].J Biol Chem,2016,291(32):16925.
[21]马春平,陆亚东,丁浩,等.食管癌患者术后肺部感染影响因素分析[J].山东医药,2013,53(44):62-64.
[22]陈晓珍,张怀忠,方韬,等.食管癌术后并发症危险因素的Logistic分析及护理干预[J].中国药物与临床,2014,14(3):300-302.
[23]石平,熊小敏,曾茄,等.食管癌术后肺部感染危险因素的评估[J].四川医学,2010,31(8):1117-1118.
[24]谭何易,赖应龙.食管癌术后并发肺部感染的相关因素[J].中华实验和临床感染病杂志(电子版),2016,10(4):467-472.
[25]杨薇,贺蓓.吸烟患者肺间质异常对肺总量及肺气肿的影响[J].中华医学杂志,2011,91(31):2231.
[26]张晓勤,雷雨,丛伟.食管癌术后肺部感染患者临床特点及危险因素分析[J].肿瘤预防与治疗,2015,28(4):187-189,208.
(本文编辑:杨泽平)
读者·作者·编者
《临床外科杂志》已开通微信平台,微信号码:lcwkzz。可通过扫描杂志中文目录右上的二维码,或直接搜索《临床外科杂志》来关注本刊微信平台。
我刊将通过微信平台与官方网站同步发布杂志最新动态,如每期目录、临床外科领域最新进展等。您可通过该平台与《临床外科杂志》编辑部进行互动,提出您的宝贵意见和建议。
Risk factors analysis for pulmonary complications after thoracoscopic combined with laparoscopic esophagectomy
YANGLixin,LIANGWei,YUChanjuan,etal.
(DepartmentofICU,UnionHospital,TumorHospitalofXinjiangMedicalUniversity,Urumqi830011,China)
Objective To identify risk factors for pulmonary complications after thoracoscopic combined with laparoscopic esophagectomy and explore the effect of a lung protective ventilation strategy(LPVS)on pulmonary complications.Methods The clinical data were retrospectively collected for 348 patients undergoing thoracoscopic combined with laparoscopic esophagectomy,and independent risk factors for pulmonary complications after thoracoscopic combined with laparoscopic esophagectomy were identified with univariate and multivariate analysis.Results The incidence of pulmonary complications was 24.42%.According to the results of multivariate analysis,advanced age;Odds ratio(OR)= 3.934,95% confidence interval(CI):1.431~9.478],smoking(OR=3.256,95%CI:1.204~8.863),perioperatively complicated with diabetes mellitus(OR=4.835,95%CI:1.454~11.562),perioperatively complicated with chronic obstructive pulmonary disease(OR=6.714,95%CI:1.528~13.762),upper thoracic esophageal cancer(OR=4.346,95%CI:1.447~10.382)and perioperatively complicated with hypoproteinemia(OR=3.977,95%CI:1.344~9.896)were independent risk factors for pulmonary complications after thoracoscopic combined with laparoscopic esophagectomy,and an intraoperative LPVS(OR=0.273,95%CI:0.194~0.875)was a protective factor.Conclusion An intraoperative LPVS was a protective factor for pulmonary complications after thoracoscopic combined with laparoscopic esophagectomy.
thoracoscopic combined with laparoscopic esophagectomy; lung protective ventilation strategy; risk factors; protective factor
10.3969/j.issn.1005-6483.2017.07.011
新疆维吾尔自治区自然科学基金资助项目(2015211C128)
830011 乌鲁木齐,新疆医科大学附属肿瘤医院重症医学科(杨立新、梁伟、 权荣喜),麻醉科(于婵娟),胸外科(吕红博)
权荣喜,Email:2214178173@qq.com
2017-02-28)
