基于张量法的阿尔兹海默症脑图像分类*
2017-06-10杨宁徐盼盼刘佩嘉李淑龙
杨宁,徐盼盼,刘佩嘉,李淑龙
(1. 南方医科大学生物医学工程学院//广东省医学图像处理重点实验室,广东 广州 510515; 2. 华南理工大学数学学院,广东 广州 510641)
基于张量法的阿尔兹海默症脑图像分类*
杨宁1,徐盼盼1,刘佩嘉2,李淑龙1
(1. 南方医科大学生物医学工程学院//广东省医学图像处理重点实验室,广东 广州 510515; 2. 华南理工大学数学学院,广东 广州 510641)
为了识别阿尔兹海默症(Alzheimer’s Disease,AD)与轻度认知障碍(Mild Cognitive Impairment,MCI)患者,提出了一种基于三阶张量方法的以MRI图像脑灰质灰度为特征的分类方法。采集了70例AD患者,112例MCI患者(包含在随访中转化为AD的,MCI-C:MCI Converters与未转化为AD的,MCI-NC:MCI Non-converters各56例),以及70例正常人(NC)的MRI脑图像,提取脑灰质各体素的灰度,获得三阶灰度张量。采用基于张量的独立成分分析,以取得三阶灰度张量的独立成分;为了降低特征维数,利用支持张量机,将张量特征转化为向量特征,再利用递归特征消除法获取有效的主要特征。最后,对四组人群进行分类:AD-NC, MCI-NC, AD-MCI, MCI-C-MCI-NC,此分类模型采用7折交叉验证的方法进行训练测试。此外,还结合样本的基本信息与认知分数进行分类,证明了基本信息、认知分数和脑灰质灰度提供了互补的信息,有助于提升分类效果。结果表明,该方法拥有优良的分类性能,有助于对AD与MCI的诊断治疗。
阿尔兹海默症;轻度认知障碍;张量;认知分数;独立成分分析;支持张量机;递归特征消除
阿尔兹海默症(AD)是一种起病隐匿的进行性发展的神经系统退行性疾病,其多发于65岁以上的人群。2015年,全球痴呆患者人数已达4680万人,其中50%-75%为阿尔兹海默症患者。目前在中国,阿尔兹海默症患者人数已居世界第一,同时也是全球增速最快的国家之一。然而,阿尔兹海默症的诊疗率却与发病情况呈强烈反差,全球阿尔兹海默症及其它类型痴呆患者中,仅有22%接受过诊断。在中国这个比例更低,有49%的病例被误认为是自然老化,仅21%的患者得到了规范诊断,仅19.6%接受了药物治疗。因此,正确诊断阿尔兹海默症,尤其是正确诊断其早期阶段的轻度认知障碍(MCI),对阿尔兹海默症的早期发现与治疗至关重要。
Fisher 判别分析(FDA)、改进的线性判别分析(MLDA)、支持向量机,K-近邻法(KNN)等智能分类方法均可用于阿尔兹海默症的分类。Dai等[1]运用了改进的线性判别分类的方法,解决了在小样本大特征维数空间中类内散度矩阵奇异的问题,其AD-NC分类准确率达89.47%。支持向量机是目前比较常用的分类方法,其基本思想为结构风险最小化准则,旨在寻找一个超平面,使得离超平面最近的样本点有更大的间距。黄文强等[2]建立了一种变量可分离的支持向量分类模型,其算法优于传统的支持向量机。Liu等[3]提出了基于高阶图形匹配特征选择的阿尔兹海默症的识别,采用支持向量机作分类器,其AD-NC分类准确率达92.17%。Willette等[4]结合多种数据,利用判别分类分析对独立成分特征进行分类,其AD-NC分类准确率达94.8%。陈振洲等[5]提出了基于SVM的特征加权K-近邻算法,其利用支持向量机来确定特征的权重,以分析特征对分类的相关性的强弱,大大提升了分类的准确率。
然而,目前有关基于脑图像的阿尔兹海默症的分类研究常用的方法是把高阶数据直接向量化,这会破坏高阶数据本身的空间结构信息与内在相关性;此外,长度极大的向量会导致小样本事件与维数灾难,从而降低机器学习方法的性能。所以,本文提出了基于三阶张量方法的阿尔兹海默症诊断方法,直接以MRI脑图像的灰质灰度构建三阶张量,以此三阶张量为特征,利用张量的运算方法进行研究分析。这不但能更好地保持高阶数据的空间结构信息与内在相关性,也能更好地避免小样本事件与维数灾难。
根据磁共振成像原理,体素的灰度会受到周围体素的影响而不能真实反映该体素真正的灰度值,我们采用独立成分分析法,提取出每个体素的独立成分(灰度值)形成新的三阶灰度张量。考虑到,三阶灰度张量特征信息会有冗余,并且每一模的维度较高,会影响学习效率,我们采用递归特征消除法并结合支持张量机对新三阶张量每一模进行特征选择并向量化。最后我们采用支持向量机进行分类。
此外,本文还结合样本的基本信息与认知分数进行分类,证明了基本信息、认知分数与MRI脑灰质图像的三阶灰度张量特征具有很好的互补作用,其对于诊断阿尔兹海默症或轻度认知障碍有着非常好的效果。
1 材料与图像预处理
本文所用数据来自于阿尔兹海默症神经图像组织(ADNI)数据库www.adni.loni.usc.edu。ADNI由美国国立卫生研究院衰老研究所(NIA),美国国家生物医学成像与生物工程研究所(NIBIB),美国食品药物监督管理局(FDA)等机构在2003年发起,其旨在采集分析AD、MCI、NC人群各类脑图像,研究AD、MCI等疾病,以便有效地防止或延迟AD的发生。
1.1 样本数据
所有研究对象的年龄介于55~90岁之间,有良好的视力与听力完成神经心理学的测试;一般健康状况良好;有六等级教育经历或良好的工作经历(排除智力低下);缺血指数量表评分小于或等于4;老年抑郁量表小于6。
对于正常人群(NC),其满足的条件与标准有:韦氏记忆量表(Wechsler Memory Scale)评分正常;简易精神状态检查表(Mini-Mental State Exam, MMSE)分数介于24~30之间;临床痴呆评定量表(Clinical Dementia Rating, CDR)分数为0;记忆评分(Memory Box score)为0;认知正常,没有认知功能或日常生活的障碍。
对于轻度认知障碍人群(MCI),其满足的条件与标准有:韦氏记忆量表(Wechsler Memory Scale)评分不正常;简易精神状态检查表(Mini-Mental State Exam, MMSE)分数介于24~30之间;临床痴呆评定量表(Clinical Dementia Rating, CDR)分数为0.5;记忆评分(Memory Box score)大于或等于0.5;一般的认知功能表现正常,以至于医生不能将其确诊为阿尔兹海默症;没有痴呆表现;保留日常生活的能力。
对于阿尔兹海默症人群(AD),其满足的条件与标准有:韦氏记忆量表(Wechsler Memory Scale)评分不正常;简易精神状态检查表(Mini-Mental State Exam, MMSE)分数介于20~26之间;临床痴呆评定量表(Clinical Dementia Rating, CDR)分数为0.5或1.0;认知不正常,符合阿尔兹海默症的评定标准。
本文所使用的数据为MRI脑图像及相应的基本信息、认知分数,其中包括AD,NC人群各70例,MCI人群112例(MCI-C与MCI-NC各56例),总共252例样本数据,所有样本对象均知情同意。其详细的样本信息见表1。
1.2 预处理
本文所用的T1加权MRI脑图像由ADNI数据库提供,全部图像为研究对象首次采集的基准图像,且都经过了特定的图像预处理:图像几何失真校正与图像强度非均匀性校正。采用SPM8(www.fil.ion.ucl.ac.uk/spm/software/spm8)软件中的VBM8工具箱[6],将预处理过的图像分割为灰质、白质与脑脊液,提取分割后脑灰质各体素的灰度值,形成三阶灰度张量特征数据。
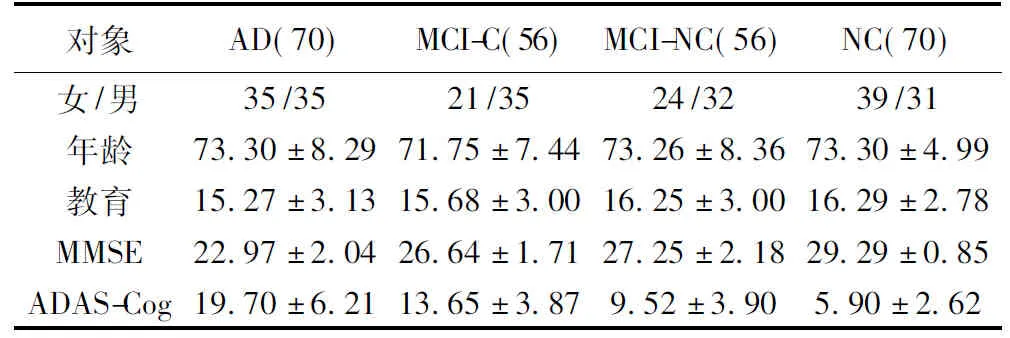
表1 研究对象信息Table 1 The information of research subjects
2 方法与实验
首先,我们通过SPM8软件分割MRI脑图像,提取分割后脑灰质各体素的灰度值,形成三阶张量并以此张量为特征。其次,对三阶的灰度张量特征采用基于张量的独立成分分析提取其独立成分,形成新的三阶张量特征。接着,利用递归特征消除法并结合支持张量机对新三阶张量特征进行特征选择并向量化,形成降维了的向量特征。最后,采用支持向量机进行分类。
2.1 张量概念与运算
2.1.1 张量概念 张量是向量与矩阵的高阶推广,一阶张量是向量,二阶张量是矩阵,三阶或三阶以上的张量就是高阶张量。一个N阶张量,可以把它记为X∈RL1×L2×…×LN,其中Li≥1,张量中的元素可以记为:xl1,l2,…,lN,1≤li≤Li,1≤i≤N。
2.1.2 张量的模-n纤 张量的模-n纤定义为仅仅改变第n模索引值而固定其它模索引值的过程。对于三阶张量,其有行纤(模-1纤)、列纤(模-2纤)和管纤(模-3纤)(图1),分别表示为x:jk,xi:k,xij:,如图1所示。
2.1.3 张量的模-n展开 张量的模-n展开是把张量排成模-n纤,再把各个纤按照顺序排成矩阵的列,从而形成矩阵的过程。如果一个N阶张量,经过模-n展开,其在(l1,l2,…,ln,…,lN)上的元
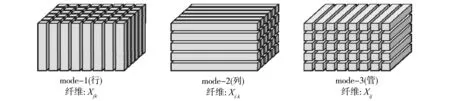
图1 三阶张量的模-1纤,模-2纤,模-3纤Fig.1 The third-order tensor of the mode -1 fiber, mode -2 fiber, mode -3 fiber
素对应于展开后的矩阵的(ln,l)位置上,其中[7],
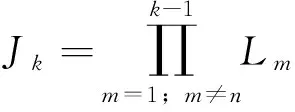
(1)
例如,三阶张量X=(xl1l2l3)L1×L2×L3∈RL1×L2×L3按模-2展开成矩阵Y=(yl2l)L2×L1L3∈RL2×L1L3,其中
l=(l3-1)L1+l1
(2)
2.1.4 张量n-模乘法 一个n阶张量X∈RL1×L2×…×LN,与一个矩阵Y∈RJ×Ln的n-模乘法,其所得张量为:
Z∈L1×L2×…×Ln-1×J×Ln+1×…×LN
其中,Z中的元素表示为:
(3)
特别地,一个n阶张量X∈RL1×L2×…×LN,与一个向量y∈R1×Ln的n-模乘法,其所得张量为Z∈L1×L2×…×Ln-1×1×Ln+1×…×LN,张量从n阶降至n-1阶。
2.2 基于张量的独立成分分析
独立成分分析(Independent Component Analysis, ICA)是一种提取数据中相互独立成分的方法。该方法的目的是将观察到的数据进行某种线性分解,使其分解成统计独立的成分。
独立成分分析可矩阵表示为X=AS,其中A是一个混合方阵。ICA算法根据X找到W,从而求得独立成分S=WX。根据中心极限定理,独立随机变量的和在一定条件下趋近于高斯分布。即独立随机变量的和比原独立随机变量更接近高斯分布。所以,可以认为越具有高斯性,其独立性越差,反之,非高斯性越强,独立性越强。本文采用最大化负熵的方法,寻找样本数据非高斯性最大的成分。当非高斯性度量达到最大时,则表明已完成各独立成分的分离。
(4)
再把S1按模-1合成n1×n2×n3的三阶张量,仍然记为S1。接着对S1按模-2展开成矩阵Y2∈Rn2×n1n3,重复以上的步骤求得W2∈Rn2×n2,使得
S2=S1×2W2=W2Y2∈Rn2×n1n3
(5)
再把S2按模-2合成n1×n2×n3的三阶张量,仍然记为S2。最后对S2按模-3展开成矩阵Y3∈Rn3×n1n2,重复以上的步骤求得W3∈Rn3×n3,使得
S3=S2×3W3=W3Y3∈Rn3×n1n2
(6)
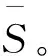
(7)
而对于任意一个样本X(包括训练样本和测试样本),其提取独立成分后的结果为
S=X×1W1×2W2×3W3
(8)
2.3 支持张量机
支持张量机(SupportTensorMachine,STM)是支持向量机的高阶推广,其保留了支持向量机结构风险最小化准则的基本思想,同样,旨在寻找一个超平面,使得离超平面最近的高阶张量样本点有更大的间距。
对于任意一个样本张量X∈Rn1×n2×n3,可得其独立成分的三阶样本张量S∈Rn1×n2×n3,所构造的分类函数为:
(9)
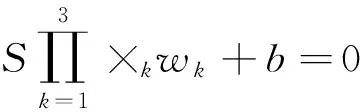
i=1,2,…,n,ζi≥0
(10)
为了使结构风险(误分次数)达到最小,并允许少数离群点存在,得到如下优化问题:
ζi≥0,i=1,2,…,n
(11)
对于优化问题(11),我们通过迭代法求解,其步骤为:
步骤1:初始化w1,w2,w3为全为1的向量。
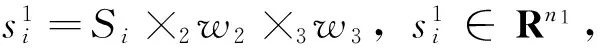
ζi≥0,i=1,2,…,n
(12)
这就转化为支持向量机的分类模型,运用拉格朗日对偶的方法即可求解出新的w1,b,并更新w1。
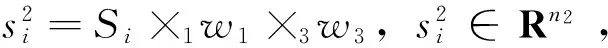
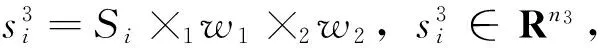
步骤5:重复步骤2-4直至w1,w2,w3,b变化很小。
从上面的迭代步骤可以看出支持张量机实际上是3个支持向量机的迭代过程,其直接将三阶张量数据作为分类模型的输入,从而保持了三阶张量原来的结构信息与内在相关性[8]。
2.4 递归特征消除法
递归特征消除(Recursivefeatureelimination,RFE)是一种逐步消除对分类不起作用或作用很小的特征的特征降维(特征选择)方法[9]。类似于陈振洲等[5]的方法,RFE的主要思想是利用支持向量机来确定特征的权重,以选择出对分类相关性强的特征。基于三阶张量的MRI脑图像数据,其中含有对分类效果作用不显著的或者两类中比较相似的特征,剔除这些冗余的或者不相关的特征,能提高分类模型的精确度,也能减少分类算法运行的时间。
对上述独立成分分析提取的各训练样本张量的独立成分三阶张量Si(i=1,2,…,n)及支持张量机训练出的三阶张量各模的特征权重向量wk,k=1,2,3,按以下步骤进行特征消除:
步骤1:令
(13)
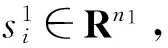
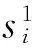
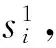
步骤5:根据步骤4得到的特征索引序列,在样本(包括训练样本与测试样本)中选定不同维度的特征子集。为了能找到分类效果最好的特征子集,我们利用支持向量机分别对含有不同特征子集的样本进行训练测试,训练测试效果最好所对应的特征子集为最优特征子集(维数降低),从而得到模-1所对应的最优特征子集及其最优分类指标。这里也可以考虑加入基本信息或认知分数特征进行特征选择。
步骤6:对于模-2,令
(14)
然后类似步骤1-5,可以得到模-2所对应的最优特征子集及其最优分类指标。
步骤7:对于模-3,令
(15)
然后类似步骤1-5,可以得到模-3所对应的最优特征子集及其最优分类指标。
步骤8:平均步骤5、 6、 7得到的各分类评价指标作为总评价指标。
上述算法就是递归特征消除的过程,此方法采用支持张量机将张量转化为向量进行分析,分别提取了模-1、模-2、模-3对应的主要特征,这可更好地保持三维图像原来的结构信息与内在相关性,也避免了直接采用向量化特征所带来的维数灾难。
整个实验过程采用7折交叉验证的方法,总分类效果为7折交叉验证的平均。总流程图如图2所示。
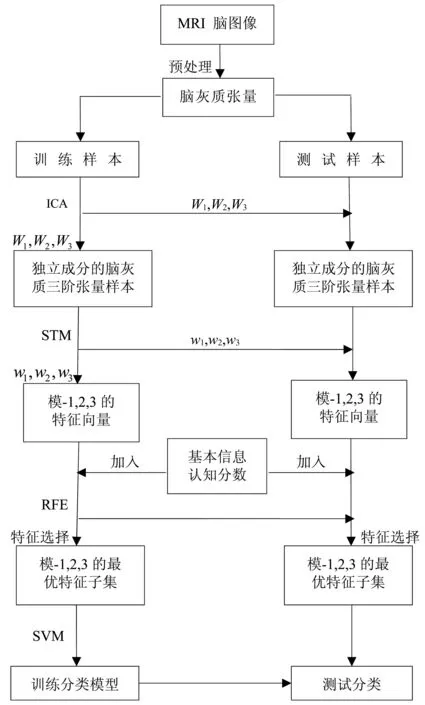
图2 算法总流程图Fig.2 The general flow chart of our algorithm
3 结 果
本文提出了基于张量方法的以MRI脑图像数据为主要特征,并结合认知分数及基本信息数据特征的识别方法。考虑到在MR成像过程中,邻近体素会相互影响,因此每个体素点的灰度值不能真实地反映该体素的灰度值。采用基于张量的独立成分分析进行特征提取,获取每个体素的独立成分,从而得到新的灰度张量特征。实验表明,对比于没有采用独立成分分析作特征提取而直接利用支持张量机进行分类的情况(STM),采用独立成分分析获取独立成分的灰度张量特征(ICA+STM)有助于提高识别性能,如图3所示。由此证明了特征提取的有效性。此外,并不是灰质的每个体素都与阿尔兹海默症有关,或者灰质的不同体素在对阿尔兹海默症的诊断中具有相似的作用,因此整个灰质的灰度张量作为识别特征时,会有信息冗余。剔除这些不相关的特征或冗余信息能提高诊断性能。本文采用基于支持张量机的递归特征消除对独立成分的灰度张量数据进行特征选择(ICA+RFE+STM)。对比没有采用递归特征消除(ICA+STM)的情况,ICA+RFE+STM方法大大提高了分类精确度,如图3所示。由此证明了特征选择的重要性。
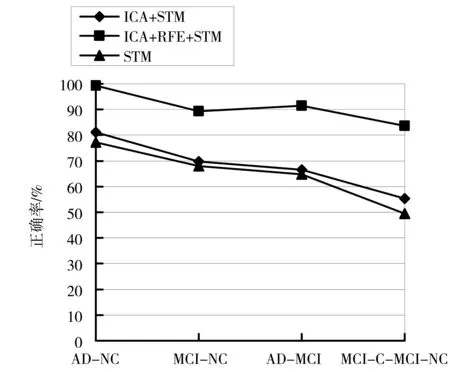
图3 特征提取ICA与特征选择RFE的优势Fig.3 The advantages of feature extraction ICA and feature selection RFE
本文在MRI脑图像的基础上,结合认知分数(Alzheimer’s Disease Assessment Scale-Cognitive subscale, ADAS-Cog分数与Mini-Mental State Exam, MMSE分数)和样本的基本信息(年龄、性别、教育程度)作为特征,结果如表2-5所示。
表2 AD与NC的分类结果
Table 2 The classification result of AD-NC %
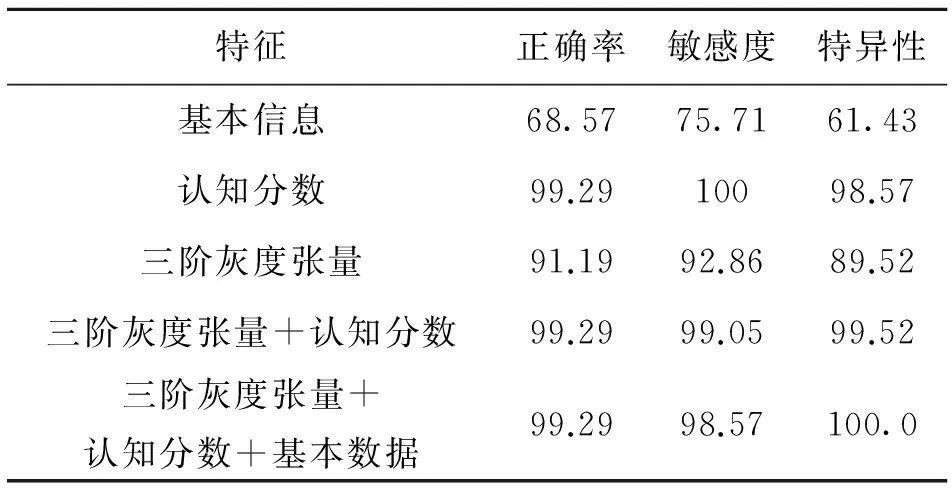
特征正确率敏感度特异性基本信息68.5775.7161.43认知分数99.2910098.57三阶灰度张量91.1992.8689.52三阶灰度张量+认知分数99.2999.0599.52三阶灰度张量+认知分数+基本数据99.2998.57100.0
表3 AD与MCI的分类结果
Table 3 The classification result of AD-MCI %
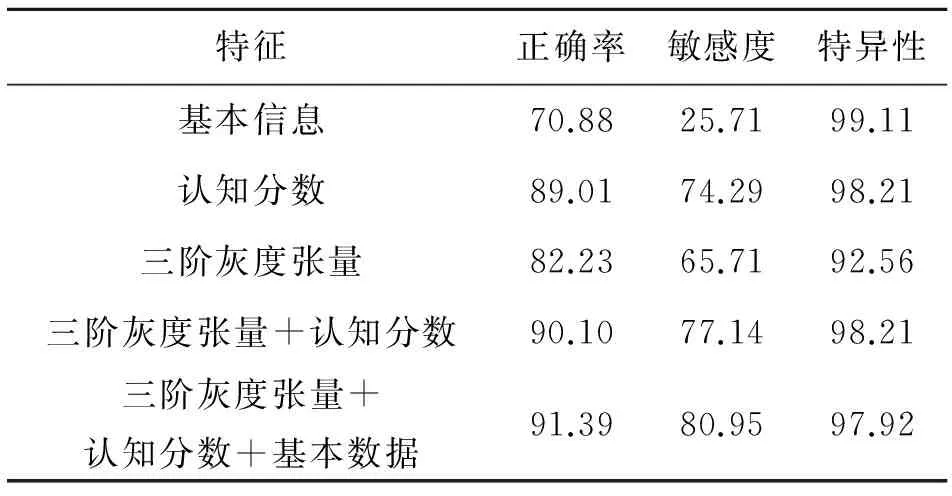
特征正确率敏感度特异性基本信息70.8825.7199.11认知分数89.0174.2998.21三阶灰度张量82.2365.7192.56三阶灰度张量+认知分数90.1077.1498.21三阶灰度张量+认知分数+基本数据91.3980.9597.92
表4 MCI与NC的分类结果
Table 4 The classification result of MCI-NC %
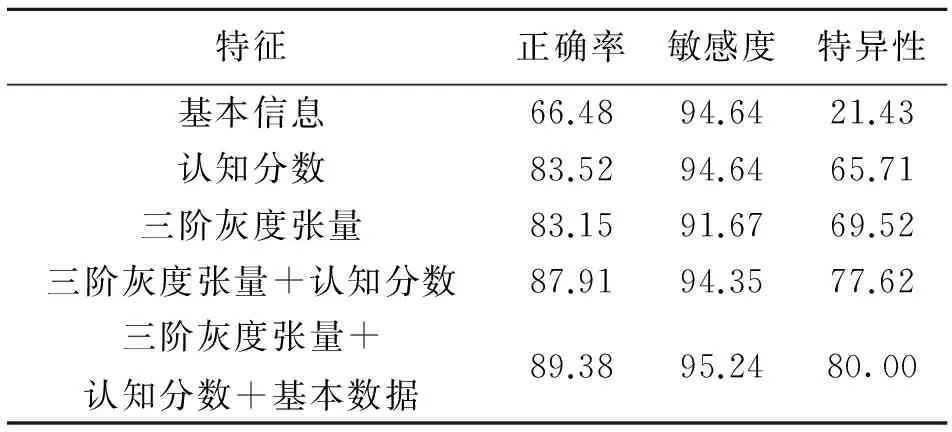
特征正确率敏感度特异性基本信息66.4894.6421.43认知分数83.5294.6465.71三阶灰度张量83.1591.6769.52三阶灰度张量+认知分数87.9194.3577.62三阶灰度张量+认知分数+基本数据89.3895.2480.00
表5 MCI-C与MCI-NC分类结果
Table 5 The classification result of MCI-C-MCI-NC %
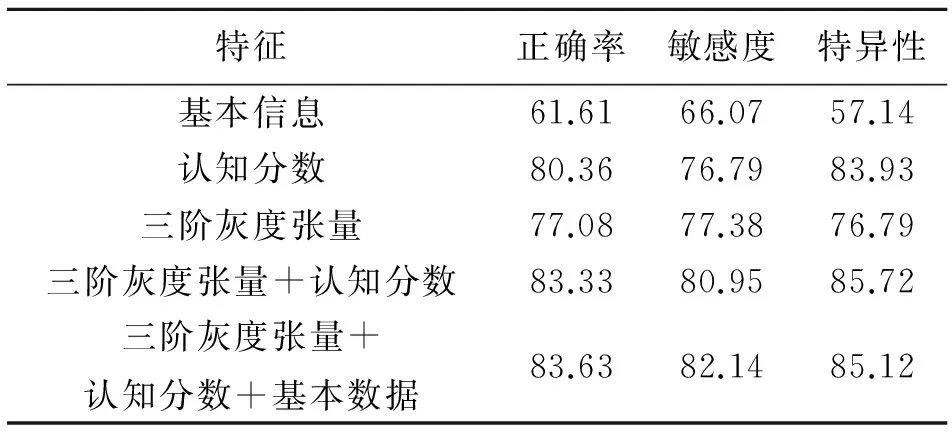
特征正确率敏感度特异性基本信息61.6166.0757.14认知分数80.3676.7983.93三阶灰度张量77.0877.3876.79三阶灰度张量+认知分数83.3380.9585.72三阶灰度张量+认知分数+基本数据83.6382.1485.12
由表2-5可以看出,特征模态越多,分类性能越好。认知分数或三阶灰度张量作特征进行分类能达到良好的效果,而二者结合能大大提升分类性能,并且提升幅度在MCI-NC和MCI-C-MCI-NC的识别中更有优势。即使再结合基本信息数据,分类性能也有所提升,但效果没那么明显,而且仅用基本信息(年龄、性别、教育程度)作特征进行分类效果相对较差。这说明了认知分数和灰质灰度在阿尔兹海默症的诊断中起了主要作用,而基本信息数据与阿尔兹海默症的相关性比较低,但其也包含着有效的信息,这些不同类型数据提供着互补的信息,结合不同模态的数据作特征进行分类,有助于对阿尔兹海默症或轻度认知障碍的诊断治疗。
Shen等[10]提出了基于相似矩阵的损失函数的阿尔兹海默症识别方法,他们把MRI、PET脑图像数据分割成若干个感兴趣区域,并结合脑脊液数据形成特征向量,利用相似矩阵法选取主要特征,然后用支持向量机进行分类。对于AD-NC, MCI-NC, MCI-C-MCI-NC这三种人群的分类,Shen-MPC(结合MRI,PET与CSF数据)分类正确率比Shen-M(只用MRI数据)高。不同模态的数据提供了互补的信息,有助于提升分类性能,但也要求每个人患者都得做MRI、PET检查及脑脊液检测才能达到有效的诊断,不但检查费用高,也会增加患者的心理负担及身体负面影响,在临床上较难实现。本文提出的基于张量的以MRI脑图像为特征的方法(Proposed-M),与Shen的方法相比,除了AD-NC分类正确率比较低之外(但也有90%以上的正确率),其它两种分类的效果皆比Shen的好。而当本文方法结合MRI脑图像数据、认知分数(Cognition)及基本信息数据(Basic Information)(Proposed-MCB),其分类正确率明显优于Shen的结果(如图4所示)。本文方法只需要用到MRI脑图像及基本信息、认知分数信息,意味着患者只需做磁共振检查,及认知分数测试。相对于Shen的方法,这不但可以降低患者的检查项目从而降低就医成本,也可降低做身体检查给患者心理及生理带来的负面影响,在临床上更容易实现。
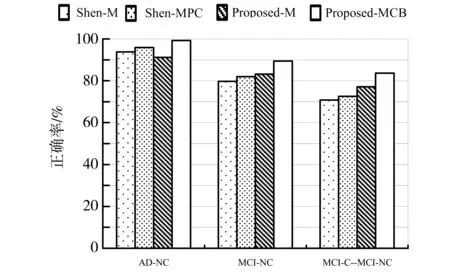
图4 本文所提出方法与Shen方法的分类性能比较Fig.4 Comparison of classification performances of our proposed method and Shen’s method
Willette等[4]提出了基于独立成分分析的阿尔兹海默症识别方法,其采用独立成分分析对MRI脑图像数据进行特征提取,提取出30个主要的特征,再依次结合基本信息、认知分数(Cognition)、CSF(脑脊液)、ApoE4(载脂蛋白E4)等不同模态的数据,得出了AD与NC的识别率最高可达94.8%、MCI与NC识别率最高可达84.7%、AD与MCI识别率最高可达83.1%、MCI-C与MCI-NC识别率最高可达80.3%。本文提出的方法,只需结合MRI脑图像数据、认知(Cognition)分数与样本的基本信息(Basic information)作为特征(Proposed-MCB),就能达到比上述方法更优越的效果:AD-NC,MCI-NC ,AD-MCI, MCI-C--MCI-NC正确率分别可达99.3%,89.4%,91.4%,83.6%,如图5所示。这也证明了本文所提出的方法的优越性。
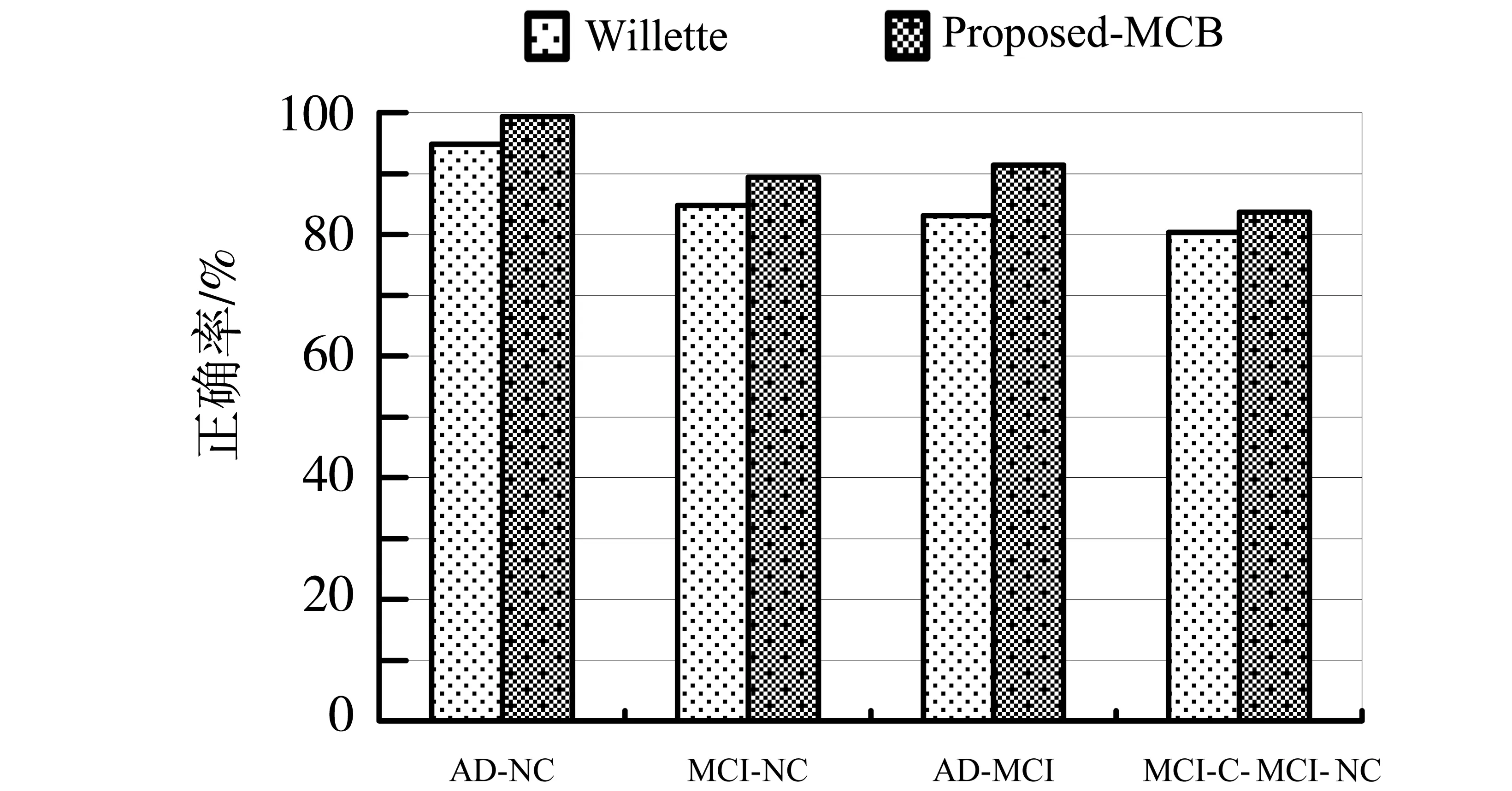
图5 本文所提出方法与Willette方法的分类性能比较Fig.5 Comparison of classification performances of our proposed method and Willette’s method
4 结 论
本文提出了基于张量的以MRI脑图像灰质为主要特征结合认知分数特征的阿尔兹海默症识别方法。我们采用基于张量的独立成分分析提取MRI脑灰质图像的灰度张量特征;然后,利用支持张量机将灰度张量特征转化为各个模的向量特征;接着,采用递归特征消除法,对向量化的各模向量特征进行特征选择,得到最优特征子集;最后,采用支持向量机对特征最优选择后的4组人群(AD-NC,MCI-NC ,AD-MCI,MCI-C--MCI-NC)进行识别分类,得其分类性能参数。与前人的研究相比,我们所提出的方法明显更加优异:认知分数或三阶灰度张量作特征进行分类能达到良好的效果,而二者结合能大大提升分类性能,其提升幅度在MCI-NC和MCI-C--MCI-NC的识别中更有优势。即使再结合基本信息数据,分类性能也有所提升,但效果没那么明显,而且仅用基本信息(年龄、性别、教育程度)作特征进行分类效果相对较差。这说明了认知分数和灰质灰度在阿尔兹海默症的诊断中起了主要作用,而基本信息数据与阿尔兹海默症的相关性比较低,但其也包含着有效的信息,这些不同类型数据提供着互补的信息,结合不同模态的数据作特征进行分类,有助于对阿尔兹海默症或轻度认知障碍的诊断治疗。由于阿尔兹海默症是一种不可逆的疾病,所以对其发病前(轻度认知障碍阶段)的诊断干预是非常有必要的。而本文在轻度认知障碍的研究中,MCI-NC 与MCI-C--MCI-NC的这两组分类,其正确率高达89.38%(敏感性95.24%,特异性80%)与83.63%(敏感性82.14%,特异性85.12%),这可为阿尔兹海默症发病前的干预治疗提供非常重要的依据,从而有利于延迟甚至防止阿尔兹海默症的发生。研究结果表明,本文所提出的方法能有效地识别出阿尔兹海默症患者或轻度认知障碍患者,可为阿尔兹海默症临床的诊断、预防与治疗提供非常重要的帮助。
[1] DAI Z J, YAN C G, WANG Z Q, et al. Discriminative analysis of early Alzheimer’s disease using multi-modal imaging and multi-level characterization with multi-classifier(M3) [J]. NeuroImage, 2012, 59(3): 2187-2195.
[2] 黄文强, 黄榕波, 朱思铭. 一类变量可分离支持向量分类机的研究与应用[J]. 中山大学学报(自然科学版),2006, 45(3): 9-12. HUANG W Q, HUANG R B, ZHU S M. Application research on a kind of support vector classsification machine with seperable variables [J]. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2006, 45(3): 9-12.
[3] LIU F, SUK H, SHEN D G, et al. High-order graph matching based feature selection for Alzheimer’s disease identification [J]. Medical Image Computing & Computer-assist Intervention, 2013, 16(2): 311-318.
[4] WILLETTE A A, CALHOUN V D, EGAN J M, et al. Prognostic classification of mild cognitive impairment and Alzheimer’s disease: MRI independent component analysis [J]. Psychiatry Research Neuroimaging, 2014, 224(2): 81-88.
[5] 陈振洲, 李磊, 姚正安. 基于SVM的特征加权KNN算法[J]. 中山大学学报(自然科学版), 2005, 44(1): 17-20. CHEN Z Z, LI L, YAO Z A.Feature-weighted k-nearest neighbor algorithm with SVM [J]. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2005, 44(1): 17-20.
[6] EGGERT L D, SOMMER J, JANSEN A, et al. Accuracy and reliability of automated gray matter segmentation pathways on real and simulated structural magnetic resonance images of the human brain [J]. PLoS One, 2012, 7(9): e45081. [doi: 10.1371/journal.pone.0045081]
[7] 孙明芳. 基于张量的图像识别方法的研究[D]. 长春:吉林大学, 2012. SUN M F. The research of image recognition method based on tensor [D]. Changchun: Jilin University, 2012.
[8] 李林军. 基于支持张量机的三维荧光光谱分析方法及在真菌毒素检测中的应用[D]. 杭州:浙江大学, 2013. LI L J. The three-dimensional fluorescence spectrometry analysis methods based on support tensor machine and its application to mycotoxins detection [D]. Hangzhou: Zhejiang University, 2013.
[9] GUYON I, WESTON J, VAPNIK V, et al. Gene selection for cancer classification using support vector machines [J]. Machine Learning, 2002, 46(1/2/3): 389-422.
[10] ZHU X F, SUK H, SHEN D G, et al. A novel matrix-loss function for joint regression and classification in AD diagnosis [J]. NeuroImage, 2014, 100: 91-105.
Prognostic classification of Alzheimer’s disease brain image based on tensor method
YANGNing1,XUPanpan1,LIUPeijia2,LIShulong1
(1. School of Biomedical Engineering, Southern Medical University//Guangdong Provincial Key Laboratory of Medical Image Processing,Guangzhou 510515, China; 2. School of Mathematics, South China University of Technology, Guangzhou 510641, China)
A classification method based on the third-order tensors of brain structural magnetic resonance images is proposed to automatically identify Alzheimer’s disease and mild cognitive impairment. Brain structural magnetic resonance images from 70 AD patients, 112 MCI patients (included patients were converted to AD during follow-up, MCI-C: MCI Converters and patients were not converted to AD during follow-up, MCI-NC: MCI Non-converters) and 70 NCs (normal controls) are collected. The third-order tensors are obtained by extracting image intensity of each voxel of gray matter. In order to obtain the independent components of the third-order tensors, independent component analysis (ICA) is applied. Then, support tensor machine (STM) and recursive feature elimination (RFE) are used to reduce features dimensions and determine dominate features for classification. Finally, the classification of four groups, such as AD-NC, MCI-NC, AD-MCI, MCI-C--MCI-NC, is implemented by using 7-fold cross-validation method. In addition, basic information and cognitive scores are combined with the third-order tensor for classification. It is proved that basic information, cognitive scores and image intensity of brain gray matter provide complementary information, which is helpful to improve the classification effect. The experiment results show that this method can achieve excellent classification effect, which contributes to the diagnosis and treatment of Alzheimer’s disease and mild cognitive impairment.
AD; MCI; tensor; cognitive scores; independent component analysis; support tensor machine; recursive feature elimination
10.13471/j.cnki.acta.snus.2017.02.007
2016-08-05 基金项目:国家自然科学基金 (11201219);广东省医学图像处理重点实验室项目(2014B030301042)
杨宁(1990年生), 男;研究方向:影像组学,医学图像分析;E-mail:1157663200@qq.com
李淑龙(1981年生), 女;研究方向:影像组学,医学图像分析;E-mail:shulong@smu.edu.cn
R742;R445.2
A
0529-6579(2017)02-0040-08
