磁共振扩散峰度成像鉴别不同腮腺疾病及诊断腮腺腺淋巴瘤的应用
2017-06-05石清磊苏家威库雷志郑雪萍
俞 顺,石清磊,苏家威,包 强,库雷志,郑雪萍
(1.福建医科大学省立临床学院 福建省立医院放射科,福建 福州 350001;2.西门子中国有限公司医学诊断产品事业部,北京 100102)
头颈部影像学
磁共振扩散峰度成像鉴别不同腮腺疾病及诊断腮腺腺淋巴瘤的应用
俞 顺1*,石清磊2,苏家威1,包 强1,库雷志1,郑雪萍1
(1.福建医科大学省立临床学院 福建省立医院放射科,福建 福州 350001;2.西门子中国有限公司医学诊断产品事业部,北京 100102)
目的 探讨磁共振扩散峰度成像(DKI)鉴别不同类型腮腺疾病及诊断腮腺腺淋巴瘤(PAL)的价值。方法 回顾性分析57例腮腺疾病患者的DKI及DWI资料,分为感染性病变组(n=10)、混合瘤组(n=19)、PAL组(n=14)、其他良性肿瘤组(n=4)、恶性肿瘤组(n=10)。并将其中19例单侧腮腺病变患者的对侧正常腮腺作为正常对照组。比较各组病灶DKI扩散峰度系数(Kmean、Krad、Kax)、扩散系数(Dmean、Drad、Dax)、FA值及传统ADC值的差异。采用二分类Logistic回归筛选在PAL的诊断中具有统计学意义的指标,建立Logistic回归方程。绘制ROC曲线对筛选后的指标及二分类Logistic回归模型的诊断效能进行分析。结果 各组间Kmean、Krad、Kax、Dmean、Drad、Dax、FA及ADC值的差别均有统计学意义(P均<0.05)。ROC曲线分析显示,FA联合Kax值诊断PLA的曲线下面积(AUC)为0.88±0.06(0.79~0.94),高于单纯Kax[0.80±0.07(0.70~0.88)]和FA的AUC[0.63±0.10(0.52~0.73)],差异均有统计学意义(P均<0.05);其敏感度、特异度、准确率、阳性预测值、阴性预测值分别为71.43%、95.78%、91.77%、76.92%、94.44%。结论 DKI可用于鉴别不同类型腮腺疾病,联合应用FA及Kax值有利于提高对PAL的诊断能力。
腮腺疾病;腺淋巴瘤;诊断,鉴别;磁共振成像
腮腺腺淋巴瘤(parotid adenolymphoma, PAL)是临床较为常见的头颈部疾病,术前影像学检查有助于腮腺疾病的定性诊断,且术前合理的定性诊断有助于临床选择合适的手术方式。常规MRI已成为目前腮腺疾病的主要影像学诊断方法之一,但其以病灶的部位、形态和信号强度特点为主要评价指标来判断病变的性质,诊断敏感度及特异度较低,且存在多征象重叠等缺点[1-6]。DWI在腮腺疾病的诊疗中表现出较大潜力,但传统DWI模型是建立在组织内的水分子符合正态分布的假设基础之上,而实际组织内水分子的运动是非正态分布的,因此其应用价值受到一定限制。基于非正态分布的扩散峰度成像(diffusion kurtosis imaging, DKI)模型有望在腮腺疾病的诊疗中提供更有价值的信息[7-10]。本研究主要探讨DKI在鉴别诊断不同类型腮腺疾病及诊断PAL的应用价值。
1 资料与方法
1.1 一般资料 回顾性分析2014年5月—2015年6月于我院接受DKI及DWI检查的57例腮腺疾病患者资料,男37例,女20例,年龄21~86岁,中位年龄52岁。PAL患者共14例(PAL组)。非PAL患者共43例,包括感染性病变10例(感染性病变组;木村病2例、炎症性淋巴结肿大2例、感染性蜂窝织炎3例、第1腮裂瘘合并感染1例、干燥综合征累及腮腺2例),混合瘤19例(混合瘤组),其他良性肿瘤4例(其他良性肿瘤组;基底细胞腺瘤2例、血管瘤1例、神经鞘瘤1例),恶性肿瘤10例(恶性肿瘤组;黏液表皮样癌3例、腺体泡细胞癌2例、鳞状细胞癌2例、嗜酸性细胞癌1例、黏膜相关组织边缘区B细胞淋巴瘤1例、原始神经外胚层瘤1例)。并对其中19例单侧发病患者,取对侧正常腮腺作为对照(正常腮腺组)。47例腮腺肿瘤均经手术切除术后病理证实;10例感染性病变中,炎症性淋巴结肿大、木村病及第1腮裂瘘合并感染为术后病理结合临床诊断,感染性蜂窝织炎和干燥综合征累及腮腺均经临床治疗和随诊后确诊。
1.2 仪器与方法 采用Siemens Aera 1.5T MR扫描仪器,20通道头颈联合线圈。头颈部常规MR检查(T2WI、T1WI、脂肪抑制T2WI)后,行轴位DWI及DKI。DWI扫描参数:TR 6 800 ms,TE 82 ms,层厚 4 mm,层间距0,矩阵192×153,FOV 220 mm×213 mm,b值取0、1 000 s/mm2,NEX 1,采集时间1 min 57 s。DKI扫描参数:TR 4 000 ms,TE 93 ms,层厚 4 mm,层间距0,矩阵128×128,230 mm×230 mm,NEX 1,b值取0、1 000、2 000 s/mm2,扩散敏感梯度方向30,iPAT因子2,采集时间4 min 46 s。
1.3
图像后处理 DKI源图像通过DKE软件处理,结合常规T2WI轴位图像,观察并获得病灶ROI的扩散峰度系数及扩散系数。扩散峰度系数包括:平均峰度(mean kurtosis, Kmean)、轴向峰度(axial kurtosis, Kax)、径向峰度(radial kurtosis, Krad);扩散系数包括:平均扩散系数(mean diffusivity, Dmean)、轴向扩散系数(axial diffusivity, Dax)、径向扩散系数(radial diffusivity, Drad)及FA值。通过MMWP工作站对DWI图像进行分析,测量病灶的ADC值。
1.4 统计学分析 采用SPSS 22.0统计分析软件,首先对数据以Komogorov-Smirnov法进行正态分布检验,以Leneve法进行方差齐性检验。多组间的比较采用单因素方差分析,因数据方差不齐,因此采用Tamhane'sT2检验进行组间两两比较。而后采用二分类Logistic回归筛选在PAL与非PAL疾病诊断中有意义的参数值,并建立回归方程,分析该模型对PAL与非PAL的鉴别诊断效能,Y=log(p/1-p),其中p表示该疾病为PAL的概率。最后采用MedCac 13.0软件,绘制ROC曲线,分析筛选后的参数及二分类Logistic回归方程对PAL的诊断价值。以P<0.05为差异有统计学意义。
2 结果
2.1 不同类型腮腺疾病鉴别诊断 各组DKI指标及传统ADC值见表1。不同类型腮腺疾病各组间DKI指标及传统ADC差异均有统计学意义(P均<0.001)。扩散峰度系数(Kmean、Krad、Kax)在PAL组最高,在混合瘤组和其他良性肿瘤组较低,差异有统计学意义(P均<0.001);而扩散系数(Dmean、Drad、Dax)在PAL组最低,在混合瘤组和其他良性肿瘤组较高,差异有统计学意义(P均<0.05)。组间两两比较结果见表2。
2.2 DKI指标诊断PAL 采用二分类Logistic回归对诊断PAL的DKI指标进行筛选结果显示,Kax(P<0.001)和FA(P=0.003)对PAL具有较高的诊断效能。建立Logistic回归方程为:Y=-6.68-41.34×FA+11.09×Kax,由回归方程获得诊断PAL的阈值为-0.75,高于该值提示为PAL。ROC曲线分析显示,FA联合Kax诊断PLA的AUC为[0.88±0.06(0.79~0.94)]高于单纯Kax[0.80±0.07(0.70~0.88)]和FA[0.63±0.10(0.52~0.73)],差异均有统计学意义(Z=1.836,P=0.0464;Z=2.406,P=0.016 1;图1),FA联合Kax诊断PAL的敏感度、特异度、准确率、阳性预测值及阴性预测值分别为71.43%、95.78%、91.77%、76.92%及94.44%。
3 讨论
3.1 DKI的基本原理 生物组织中水分子的扩散运动受细胞屏障、细胞器及细胞内外间隔等多种因素影响,导致水分子的扩散呈非正态分布。DKI基于组织内水分子非正态分布的假设,可反映组织内的水分子非正态分布的扩散大小及程度,并通过峰度对模型内水分子的扩散运动进行校正[11-14],该模型更符合人体组织内水分子的实际扩散运动情况。DKI的主要指标包括扩散峰度系数(Kmean、Krad、Kax)、扩散系数(Dmean、Drad、Dax)和FA值。Kmean指所有梯度方向的扩散峰度平均值,组织结构越复杂,水分子扩散受限越明显,Kmean值越大。Krad指所有垂直于主本征向量方向的扩散峰度平均值。Kax指主本征向量方向的扩散峰度值;组织结构越疏松,Kax值越小,趋向同性扩散;组织结构越紧密规则,Kax值越大,趋向异性扩散。Dmean表示在DKI成像模型中利用K值校正之后多个方向扩散系数的平均值。Dax表示在校正之后模型中多个方向扩散系数中最大的扩散值,即径向扩散本征值。Drad为除Dax外多个方向扩散系数的平均值。DKI模型的FA值与传统DTI的FA值不同,该FA值为利用DKI模型校正之后的扩散值计算所得到的FA值。
3.2 DKI鉴别诊断不同类型腮腺疾病 DKI指标中的扩散峰度系数(Kmean、Krad、Kax)和扩散系数(Dmean、Drad、Dax)在不同类型腮腺病变中具有不同的变化趋势,这是由于两者所反映的信息不同所致,扩散峰度系数(Kmean、Krad、Kax)主要反映组织结构相关特性[15],而扩散系数(Dmean、Drad、Dax)主要反映水分子弥散情况。本研究对不同类型腮腺疾病各组进行两两分析,发现扩散峰度系数(Kmean、Krad、Kax)在各组间表现出统计学差异共22次(P均<0.05),而扩散系数(Dmean、Drad、Dax)为15次(P均<0.05),见表2;与既往国内外学者[12-15]研究发现DKI峰度相关参数具有更高的敏感度的结果相符。本研究中,扩散峰度系数(Kmean、Krad、Kax)在PAL组最高,分析原因为PAL的组织病理学特点所致,PAL是由上皮组织和淋巴组织组成的良性肿瘤,上皮组织形成不规则的大腺管及微囊腔,增生的淋巴组织形成淋巴滤泡,肿瘤细胞间质内微血管丰富,且瘤体内细胞分布密集,细胞外间隙较少。此外,本研究显示扩散峰度系数(Kmean、Krad、Kax)在混合瘤组和其他良性肿瘤组较低,这可能是由于混合瘤组织结构紧密度,组织结构空间复杂程度、组织内细胞核的异型性及间质中血管增生程度均较低所致。
表1 各组DKI参数值及传统ADC值比较(±s)
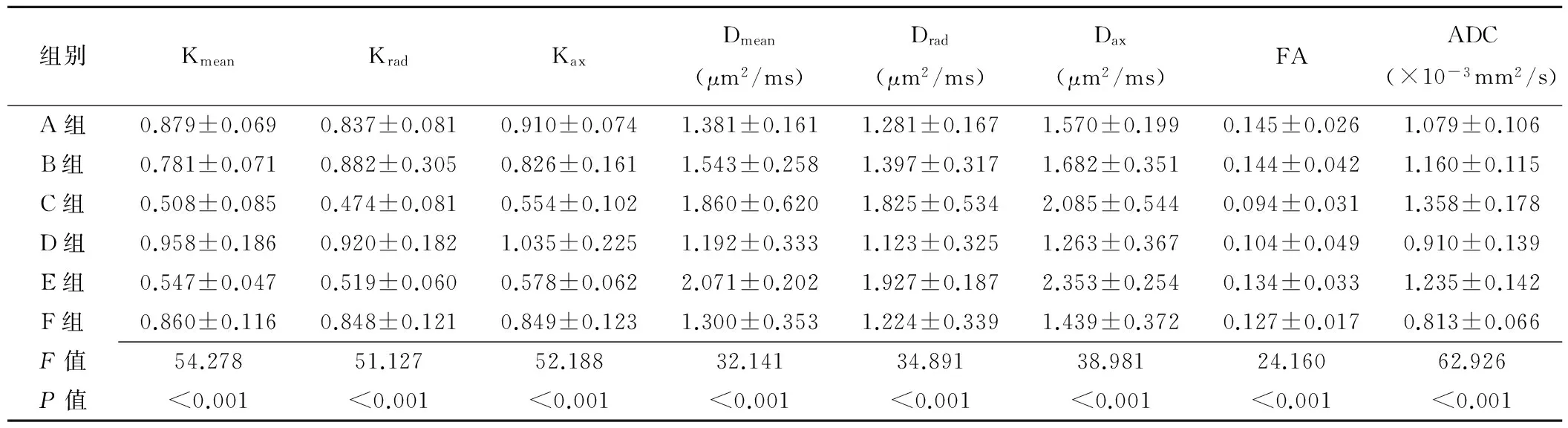
表1 各组DKI参数值及传统ADC值比较(±s)
组别KmeanKradKaxDmean(μm2/ms)Drad(μm2/ms)Dax(μm2/ms)FAADC(×10-3mm2/s)A组0.879±0.0690.837±0.0810.910±0.0741.381±0.1611.281±0.1671.570±0.1990.145±0.0261.079±0.106B组0.781±0.0710.882±0.3050.826±0.1611.543±0.2581.397±0.3171.682±0.3510.144±0.0421.160±0.115C组0.508±0.0850.474±0.0810.554±0.1021.860±0.6201.825±0.5342.085±0.5440.094±0.0311.358±0.178D组0.958±0.1860.920±0.1821.035±0.2251.192±0.3331.123±0.3251.263±0.3670.104±0.0490.910±0.139E组0.547±0.0470.519±0.0600.578±0.0622.071±0.2021.927±0.1872.353±0.2540.134±0.0331.235±0.142F组0.860±0.1160.848±0.1210.849±0.1231.300±0.3531.224±0.3391.439±0.3720.127±0.0170.813±0.066F值54.27851.12752.18832.14134.89138.98124.16062.926P值<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001
注:A组:正常腮腺组;B组:感染性病变组;C组:混合瘤组;D组:PAL组;E组:其他良性肿瘤组;F组:恶性肿瘤组
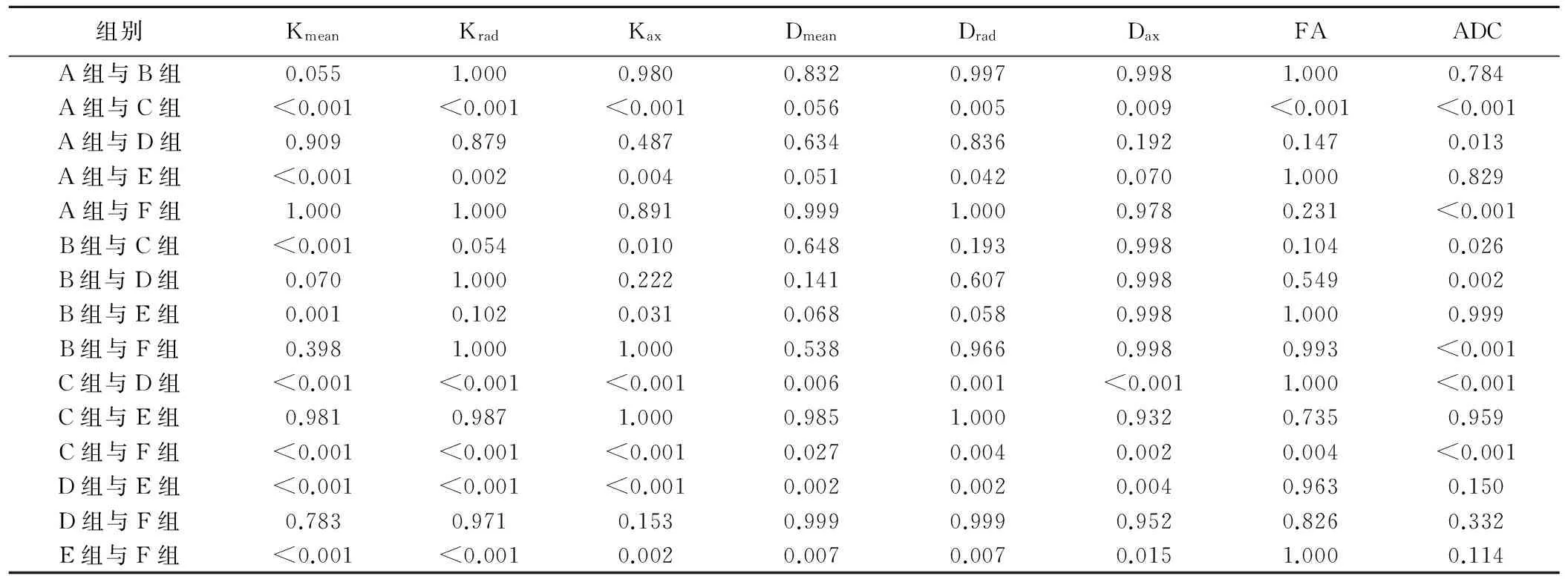
表2 各组间DKI参数及传统ADC值两两比较(P值)
注:A组:正常腮腺组;B组:感染性病变组;C组:混合瘤组;D组:PAL组;E组:其他良性肿瘤组;F组:恶性肿瘤组
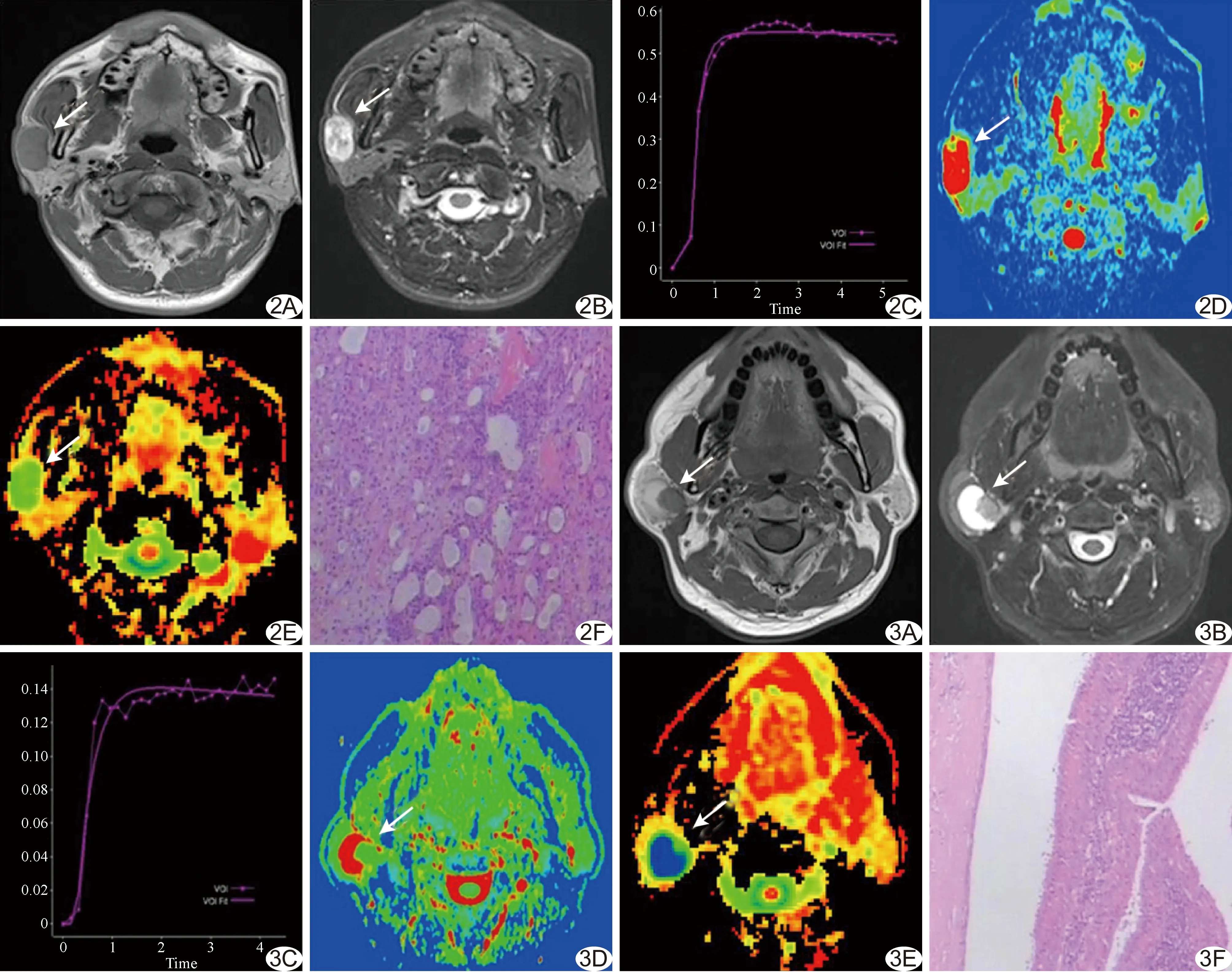
图2 患者男,39岁,PAL
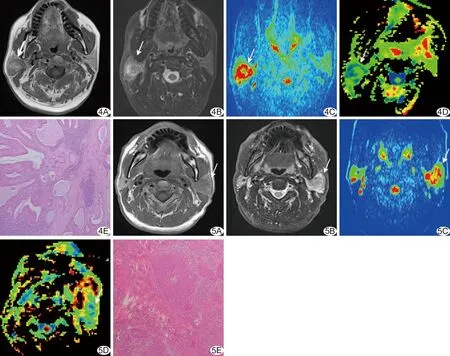
图4 患者男,68岁,PAL
A、B.T1WI及T2WI示右侧腮腺病灶信号不均,累及深、浅叶,呈浸润性,表现为恶性肿瘤征象; C.病灶DWI呈高信号,ADC=0.717×10-3mm2/s; D.Kax伪彩图,Kmean=1.029、Krad=1.091、Kax=1.266、FA=0.128;E.病理图(HE, ×40) (箭示病灶)
图5 患者男,53岁,腮腺鳞状细胞癌
A、B.T1WI及T2WI示病灶位于左侧腮腺,信号不均,累及深、浅叶、浸润性,表现恶性肿瘤征象; C.病灶DWI呈高信号,ADC=0.784×10-3mm2/s; D.Kax伪彩图,Kmean=0.710、Krad=0.674、Kax=0.738、FA=0.152; E.病理图(HE,×40) (箭示病灶)
3.3 DKI对PAL的诊断效能 本研究单独对PAL采用二分类Logistic模型进行分析,一方面是由于PAL的特殊病理特点,依靠传统DWI技术鉴别PAL与其他腮腺肿瘤在影像学表现方面存在较大程度的重叠;另一方面由于应用DKI对腮腺疾病进行两两分析表明,DKI指标对PAL显示出较高的诊断能力,例如DKI模型对PAL与形态学表现相似、TIC曲线类型一致的腮腺良性肿瘤之间(图2、3),及形态学表现恶性的PAL与其他腮腺恶性肿瘤之间(图4、5)具有较高的鉴别诊断能力。本研究结果显示,DKI诊断PAL的敏感度和特异度均较高。
本研究的局限性:①研究时间较短,收集的样本量有限,在对PAL的鉴别诊断中各组病例数量差别较大,易导致统计效能偏低;②由于DKI原始图像分辨率较低,导致在测量时存在一定的误差。
总之,DKI对于不同类型腮腺疾病具有较高的鉴别诊断能力,联合应用FA及Kax值有助于对PAL的诊断。
[1] 郑少燕,曾向廷,吴先衡,等. 3.0T MR动态增强扫描半定量分析对腮腺肿块鉴别诊断的价值.临床放射学杂志,2015,34(3):346-350.
[2] 杨功鑫,王平仲,朱文静,等.腮腺肿瘤的磁共振弥散加权成像评价.中国医学计算机成像杂志,2013,19(6):489-493.
[3] 王新宇. 3.0T磁共振弥散加权成像在鉴别腮腺多形性腺瘤和腺淋巴瘤的诊断价值.中国临床医学影像杂志,2014,25(9):662-664.
[4] 张赞霞,程敬亮,张勇.DWI联合动态增强MRI鉴别诊断腮腺肿瘤良恶性.中国医学影像技术,2014,30(7):1015-1018.
[5] Yerli H, Aydin E, Haberal N, et al. Diagnosing common parotid tumours with magnetic resonance imaging including diffusion-weighted imaging vs fine-needle aspiration cytology: A comparative study. Dentomaxillofac Radiol, 2010,39(6):349-355.
[6] Wang P, Yang J, Yu Q, et al. Evaluation of solid lesions affecting masticator space with diffusion-weighted MR imaging. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 2010,109(6):900-907.
[7] Van Cauter S, Veraart J, Sijbers J, et al. Gliomas: Diffusion kurtosis MR imaging in grading. Radiology, 2012,263(2):492-501.
[8] Shimoji K, Uka T, Tamura Y, et al. Diffusional kurtosis imaging analysis in patients with hypertension. Jpn J Radiol, 2014,32(2):98-104.
[9] Kamagata K, Tomiyama H, Hatano T, et al. A preliminary diffusional kurtosis imaging study of Parkinson disease: Comparison with conventional diffusion tensor imaging. Neuroradiology, 2014,56(3):251-258.
[10] Yoshida M, Hori M, Yokoyama K, et al. Diffusional kurtosis imaging of normal-appearing white matter in multiple sclerosis: Preliminary clinical experience. Jpn J Radiol, 2013,31(1):50-55.
[11] Jensen JH, Helpern JA. MRI quantification of non-Gaussian water diffusion by kurtosis analysis. NMR Biomed, 2010,23(7):698-710.
[12] Wu EX, Cheung MM. MR diffusion kurtosis imaging for neural tissue characterization. NMR Biomed, 2010,23(7):836-848.
[13] De Santis S, Gabrielli A, Palombo M, et al. Non-Gaussian diffusion imaging: A brief practical review. Magn Reson Imaging, 2011,29(10):1410-1416.
[14] 单艺,卢洁,李坤成.扩散峰度成像在缺血性脑卒中的研究进展.中国医学影像技术,2013,29(12):2046-2048.
[15] Jensen JH, Helpern JA, Ramani A, et al. Diffusional kurtosis imaging: The quantification of non-gaussian water diffusion by means of magnetic resonance imaging. Magn Reson Med, 2005,53(6):1432-1440.
Application of diffusion kurtosis imaging in differential diagnosis of parotid gland disease and diagnosis of parotid adenolymphoma
YUShun1*,SHIQinglei2,SUJiawei1,BAOQiang1,KULeizhi1,ZHENGXueping1
(1.DepartmentofRadiology,FujianProvincialHospital,ClinicalSchoolofFujianMedicalUniversity,Fuzhou350001,China; 2.DiagnosticImaging,SiemensLtd.,Beijing100102,China)
Objective To investigate the value of diffusion kurtosis imaging (DKI) in differential diagnosis of parotid gland disease and diagnosis of parotid adenolymphoma (PAL). Methods DKI and DWI data of 57 patients with parotid gland disease were etrospectively analyzed. Totally 57 cases were divided into infectious lesions group (n=10), pleomorphic adenoma group (n=19), PAL group (n=14), other benign parotid tumor group (n=4) and malignant parotid tumor group (n=10). Contralateral normal parotid glands in 19 patients with unilateral parotid gland lesions were treated as control group. The quantitative parameters including kurtosis concerning parameters (Kmean, Krad, Kax), diffusivity concerning parameters (Dmean, Drad, Dax), fractional anisotropy (FA) and conventional apparent diffusion coefficient (ADC) values were retrospectively reviewed. The binaryLogisticregression method was used to confirm parameters with significant difference in diagnosing PAL. AndLogisticregression equation was constructed to diagnose PAL. ROC analysis was conducted to evaluate the diagnostic value of the confirmed parameters and theLogisticregression equation. Results Significant difference of the parameters including Kmean, Krad, Kax, Dmean, Drad, Dax, FA and ADC values were found among different groups (allP<0.05). ROC analysis demonstrated a higher area under the curve (AUC) for FA+Kax[0.88±0.06 (0.79—0.94)] than Kax[0.80±0.07 (0.70—0.88)] and FA [0.63±0.10 (0.52—0.73)], respectively (bothP<0.05). The sensitivity, specificity, accuracy, positive predictive value and negative predictive value was 71.43%, 95.78%, 91.77%, 76.92% and 94.44%. Conclusion DKI showed high diagnostic capacity in differential diagnosis of parotid gland disease. The combination of FA and Kaxcan improve the diagnostic accuracy in diagnosis of PAL.
Parotid diseases; Adenolymphoma; Diagnosis, differential; Magnetic resonance imaging
福建省卫生厅青年科研课题资助计划(2013-1-3)。
俞顺(1983—),男,福建福清人,硕士,主治医师。研究方向:主要从事磁共振检查及诊断。
俞顺,福建医科大学省立临床学院 福建省立医院放射科,350001。E-mail: 76429310@qq.com
2016-06-09
2016-12-19
10.13929/j.1003-3289.201606045
R739.8; R445.2
A
1003-3289(2017)04-0523-06
