硫酸亚铁溶液离子平衡研究
2017-04-11李怡璞王丹英上海一品颜料有限公司上海201814
李怡璞,王丹英 (上海一品颜料有限公司,上海 201814)
知识窗
硫酸亚铁溶液离子平衡研究
李怡璞,王丹英 (上海一品颜料有限公司,上海 201814)
铁皮法制备的硫酸亚铁溶液中含有多种重金属杂质离子,加入沉淀剂后,存在电离、水解、沉淀平衡。根据已有的热力学数据,通过化学平衡的方法对硫酸亚铁溶液中几种常见的重金属离子的沉淀原理进行理论分析。
化学平衡;重金属离子;硫酸亚铁溶液
0 引言
铁与稀硫酸反应,可以制备硫酸亚铁,硫酸亚铁是生产氧化铁颜料的一个重要原材料[1]。由于铁资源的多样性,铁皮法制备的硫酸亚铁溶液中含有Fe2+、SO42-、H+、OH-,以及杂质离子Cu2+、Pb2+、Zn2+、Hg2+、Co2+、Ni2+等,加入沉淀剂后会进一步引入HS-、S2-等。本研究通过化学平衡法对硫酸亚铁溶液中几种常见重金属离子的沉淀原理进行理论分析。
硫酸亚铁溶液中存在电离平衡、水解平衡和沉淀的溶解平衡,有许多平衡常数,如水的离子积Kw、弱酸弱碱的电离常数(KaKb)、溶度积(Ksp)、水解平衡常数(Kh)等[2],以上各种平衡常数与化学平衡常数有着明显的共性,都是渗透化学平衡常数的应用,因此都可借助于平衡方程式来加以分析。
1 硫酸亚铁溶液中加入沉淀剂后重金属离子行为
硫酸亚铁溶液中加入沉淀剂后,体系中很快产生黑色沉淀,即相关离子形成了相应的沉淀物,体系中发生如下的化学反应[3]:

由于溶液中的[S2-]与溶液中的[H+]有关,再加上氢硫酸是二元弱酸,存在如下电离平衡:
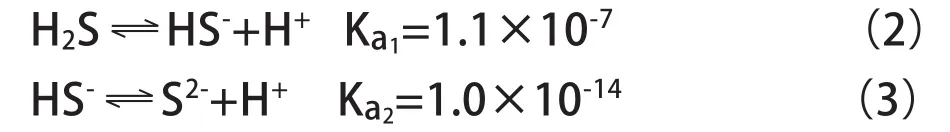
所以,由(1)+(2)+(3),溶液中的反应可以写为:
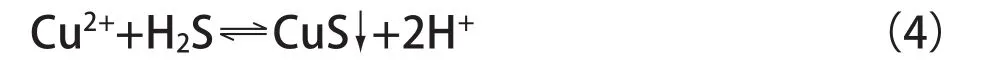
则,反应的平衡常数为:
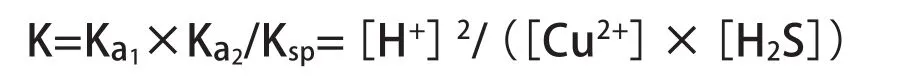
由于溶液中H2S分子的溶解度随温度和压力而变化,常温常压下,H2S饱和溶液的浓度为0.10 mol/L。按H2S的离解常数计算,当pH为9时,约99%的H2S以HS-形式存在;当pH为7时,HS-与H2S各占1/2;当pH为5时,则有99%的硫化氢以H2S的形式存在。以沉淀剂加量为0.005 mol/L计,整理得:
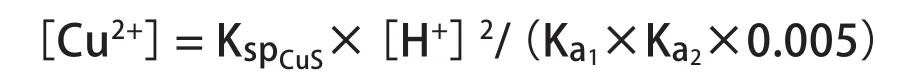
两边取负对数,得:

同理可得:

由计算过程可看出,沉淀的生成受pH和生成沉淀所需离子的共同影响,离子浓度影响了式中的常数,所以上述一系列式子仅在[H2S]=0.005 mol/L时适用。
溶液中的离子浓度越小,对应离子的负对数越大,越易于生成沉淀。从计算结果可以看出:Hg2+、Cu2+、Pb2+、Zn2+极易生成硫化物沉淀,且生成的沉淀不溶于酸,随着pH增大,离子的负对数增大,溶液中离子浓度变小,沉淀更完全。
对于Co2+而言,α-型CoS沉淀在低pH时会分解,而转化成β-型CoS沉淀后,则变得非常稳定,不再溶于酸。这与Co含量小试的试验结果一致:(1)当pH=1时,无法生成α-型CoS沉淀,当pH>2时,能生成CoS沉淀,且随着pH的增加,Co含量降低明显。(2)延长沉淀时间,α-型CoS沉淀会转化成不溶于酸的β-型CoS沉淀。此外,Ni2+的变化规律与Co2+相同,可以确定α-型NiS沉淀在低pH时溶于酸,延长沉淀时间,α-型NiS沉淀最终转化成溶解度常数更小的γ-型NiS沉淀。理论计算结果与试验结果一致,证明了理论方法适用于本研究体系。
对于Fe2+而言,当pH大于3时,多余的沉淀剂会与Fe2+反应生成黑色沉淀。在实际生产中,可根据生产需要选择合适的沉淀剂加量,并分散均匀,从而充分发挥沉淀剂的沉淀效果。
2 结语
控制一定的条件,将硫酸亚铁溶液中的Hg2+、Cu2+、Pb2+、Zn2+较彻底地转化为沉淀物在热力学上是完全可能的。对于Co2+、Ni2+而言,溶液的pH是影响除杂效果的关键因素,在适宜的pH条件下,延长沉淀时间,有利于生成更稳定的沉淀物,达到更好的除杂效果。此外,添加沉淀剂去除重金属的程度随沉淀剂用量的增加而加大,但当沉淀剂用量增加到一定程度后,进一步增加其用量,对沉淀的促进作用并不明显,所以可按照实际生产需要调整沉淀剂的用量。
1 朱骥良,吴申年.颜料工艺学[M]. 2版.北京:化学工业出版社,2002.
2 傅献彩.物理化学[M]. 5版.北京:高等教育出版社,2015.
3 David R. Lide. Handbook of Chemistry and Physics[M]. 78th Edition,1997-1998.
Study on the Ion Equilibrium of Ferrous Sulfate Solution
Li Yipu,Wang Danying (Shanghai Yipin Pigment Co.,Ltd.,Shanghai,201814,China)
Ferrous sulfate solution prepared with scrap process contains a variety of heavy metal impurity ions. After adding precipitation agent,the solution existed ionization balance,hydrolysis balance and precipitation balance. Based on the available thermodynamic data,the precipitation principle of usual heavy metal ions in ferrous sulfate solution was analyzed by the method of chemical equilibrium.
chemical equilibrium;heavy metal ion;ferrous sulfate solution
TQ 622.1+5;TQ 111.17
A
1009-1696(2017)01-0054-02
2016-11-10
李怡璞,女,华东理工大学材料科学与工程专业硕士研究生,现就职于上海一品颜料有限公司着色事业部,负责安全性颜料的技术研究工作。
