可用于白光照明的单一基质荧光粉(Sr0.95Mg0.05)3(PO4)2:Eu2+的发光特性
2017-01-12马玉涛李晨霞邓德刚华有杰
马玉涛,李晨霞,邓德刚,华有杰
(中国计量大学 光学与电子科技学院,浙江 杭州 310018)
可用于白光照明的单一基质荧光粉(Sr0.95Mg0.05)3(PO4)2:Eu2+的发光特性
马玉涛,李晨霞,邓德刚,华有杰
(中国计量大学 光学与电子科技学院,浙江 杭州 310018)
采用高温固相法合成系列Eu2+掺杂的单一基质的白光荧光粉(Sr0.95Mg0.05)3(PO4)2.该荧光粉可有效被270~390 nm的紫外光激发,激发波长范围与紫外LED芯片相匹配.在激发波长为350 nm时,发射光谱中有两个发射峰,峰值分别位于410 nm和570 nm,对应于Eu2+的4f65d1→4f7跃迁,是Eu2+占据了基质中Sr2+的十配位和六配位的两种不同的格位后,形成的两个发光中心.当Eu2+的掺杂浓度为1mol%时,具有最大的发光强度,继续增加Eu2+的浓度后,会出现浓度猝灭现象.通过将Eu2+的掺杂浓度从0到0.01,可以使该荧光粉的CIE色坐标从(0.259 5,0.198 7)的蓝光区域逐渐移动到(0.324 5,0313 3)的白光区域.基于实验结果和理论分析计算表明,这种荧光粉是一种潜在的用近紫外光激发产生白光LED的荧光粉.
单一基质;荧光粉(Sr0.95Mg0.05)3(PO4)2:Eu2+;白光LED
白光二极管由于其节能、环保、发光效率高、使用寿命长等优点被视为是白炽灯和荧光灯的潜在替代品而受到广泛的关注[1].目前获得白光使用最广泛的方法是用GaN蓝光芯片包覆着Y3Al5O12:Ce3+(YAG:Ce3+)黄色荧光粉[2].但是这种白光LED还有一些缺点,比如经过长时间工作后,由于芯片和荧光粉的衰退速率不一样,导致这种LED灯的显色性变差[3-5].为了克服以上提到的缺陷,用紫外芯片(UV-LED)激发的单一基质发白光的荧光粉是一种可行的途径.对于单一基质的荧光粉而言,不存在颜色重吸收和配比调控问题,因此具有更好的发光效率和显色性[6].所以在单一基质发白光的荧光粉上人们进行了大量的探索研究,并取得一定的成果.
目前,由于Eu2+离子极好的发光特性,所以人们对Eu2+离子掺杂的荧光粉进行了广泛的研究.Eu2+作为在荧光粉中使用最多的激活离子,是因为它的激发光谱可以覆盖NUV芯片的发射光谱范围,同时它的发射光谱范围可以从蓝光区域到红光区域,这些优异的发光特性归因于它的4f-5d能级的跃迁.对于单一基质通过掺杂Eu2+离子来实现发白光有一些的要求,基质中必须有多个阳离子晶格格位.当基质中的阳离子晶格格位被Eu2+离子取代后,就会形成多个发光中心,因此在可见光谱范围内就会出现多个发射峰,这样就会复合产生白光.磷酸盐由于其物理化学性质稳定,结构丰富,制备温度低,良好的热稳定性以及廉价的原料和高亮度等优点而被作为发光材料并广泛应用[7].Eu2+离子掺杂的磷酸盐荧光粉最近被作为新的应用于白光LED中的发光材料而被广泛研究,例如Eu2+掺杂的Ba3Y(PO4)3荧光粉能够被近紫外光有效的激发从而实现黄光的发射,Eu2+掺杂的Sr5(PO4)3Cl荧光粉能够被近紫外光激发而实现蓝光的发射,Eu2+掺杂的Ca4(PO4)2O荧光粉能够被蓝光激发,产生强烈的红光[8,9].然而据我们所知,目前还没有关于Eu2+掺杂的(Sr0.95Mg0.05)3(PO4)2单一基质作为一种潜在的实现白光照明的荧光粉的报告.因此,我们研究分析了(Sr0.95Mg0.05)3(PO4)2:Eu2+荧光粉的发光特性及其在白光LED中的潜在应用价值.
1 实验部分
1.1 原料与和合成
以SrCO3(分析纯)、MgCO3(分析纯)、NH4H2PO4(分析纯)和Eu2O3(99.99%)为原料,在还原气氛下采用传统的高温固相法制备了一系列的(Sr0.95Mg0.05)3(PO4)2:xEu2+(x=0~0.05)荧光粉.按照合适的化学计量比称量原料,然后将原料放入玛瑙研钵中研磨至均匀,再放到马弗炉中600 ℃保温2 h.待冷却后取出再将样品研磨成粉末状.之后将预烧过的样品放到氧化铝坩埚中,在N2-H2(95%/5%)的还原气氛下1 200 ℃,保温3 h.自然冷却至室温,取出样品研磨,即可得到(Sr0.95Mg0.05)3(PO4)2:xEu2+系列白光荧光粉.
1.2 样品表征
采用德国Bruker Axs D2 PHASER型X射线衍射仪器,辐射源铜靶Kα线(λ=0.154 06 nm),步长为0.02°,扫面范围为10°~70°,工作电压为30 kV,工作电流为10 mA,来测定样品的衍射图.采用美国的PL3-211-P光谱仪(HORIBA JOBIN YVON,America),用450 W的氙灯作为激发光源去探测样品的激发和发射光谱图.样品的发光寿命是在这台仪器测量,增加了370 nm的脉冲光谱然后在多通道扩展模式下测出来的.漫反射光谱是用日本的UV-3600 UV-Vis(Shimadzu, Japan)测量,以白色粉体BaSO4作为参考标准.温度对光谱发光特性的影响是用荧光粉光谱和热淬灭分析仪测量的(Everfine, China).
2 结果与讨论
2.1 物相分析
图1是采用高温固相x法在1 200 ℃下合成的(Sr0.95Mg0.05)3(PO4)2:xEu2+(x=0~0.05)系列样品的X射线衍射光谱与标准卡片的对比图.从图中可以看出掺杂Eu2+后的样品的衍射峰与(Sr0.95Mg0.05)3(PO4)2标准的卡片(JCPDS #14-0491)的衍射峰匹配得很好,没有出现杂峰.对比不同掺杂浓度的样品发现Eu2+的加入没有使基质的结构发生明显的变化.所得样品的(Sr0.95Mg0.05)3(PO4)2:Eu2+是空间群为R-3m的斜方六面体,其中基质(Sr0.95Mg0.05)3(PO4)2与Sr3(PO4)2是相同的结构,Sr3(PO4)2是空间群为R-3m的三方晶系,晶格参数为a=b=5.390 1 Å,c=19.785 0 Å,V=497.81 Å,Z=3.由于Sr2+的离子半径较大于Mg2+的离子半径,所以当少量的Mg2+取代Sr2+时会使基质的晶格参数减小.在基质(Sr0.95Mg0.05)3(PO4)2中Sr2+有两种不同的配位环境[9],Sr/Mg1为六配位,Sr/Mg2为十配位的.因为在基质中Sr2+的数量远大于Mg2+,所以我们用Sr(1)代替Sr/Mg1,用Sr(2)代替Sr/Mg2.考虑到离子半径和价态,Eu2+会随机取代基质中的Sr2+的位置.
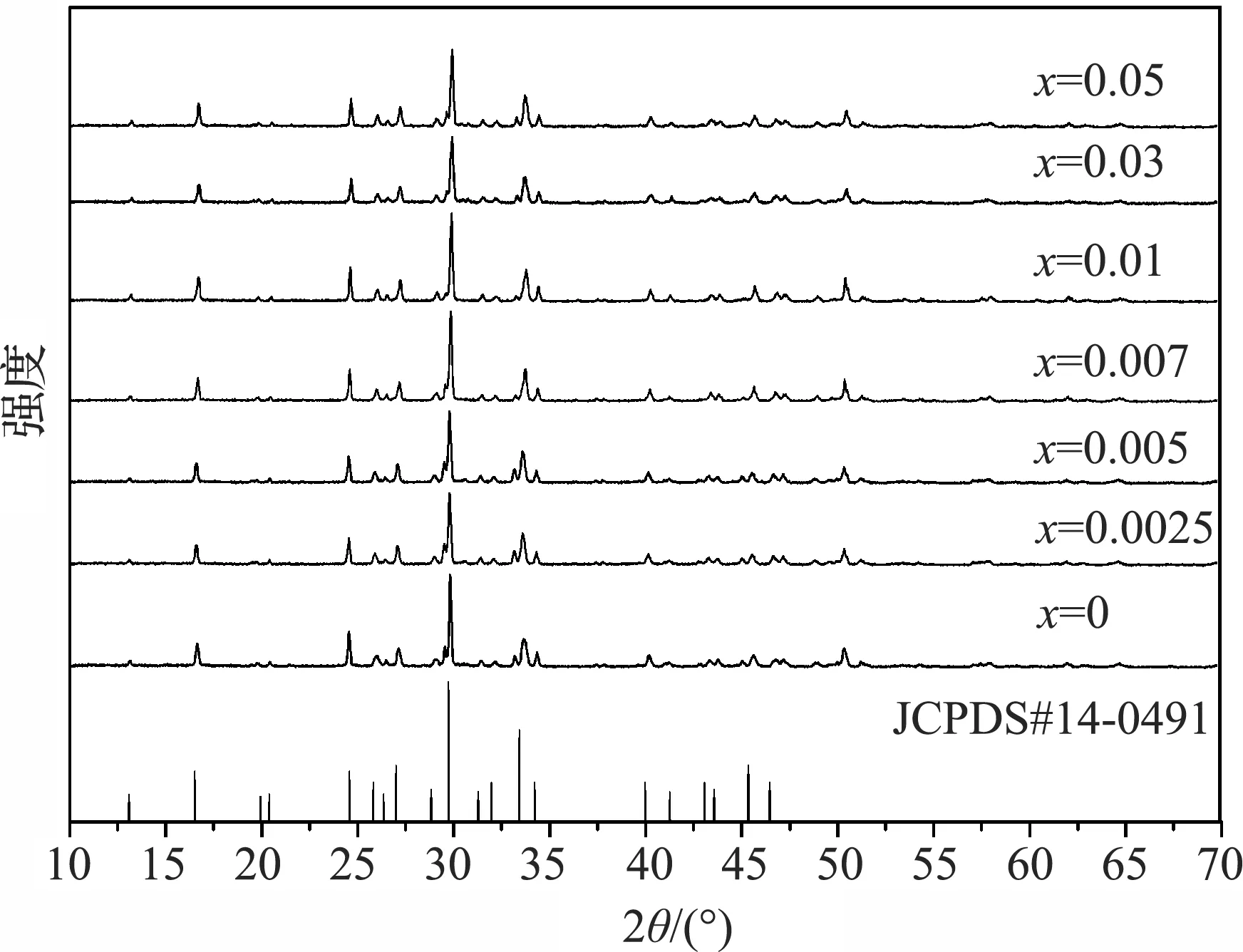
图1 荧光粉(Sr0.95Mg0.05)3(PO4)2:xEu2+与标准卡片对比图Figure 1 XRD patterns of (Sr0.95Mg0.05)3(PO4)2: xEu2+ phosphor and the standard data card as a reference
2.2 漫反射特性
图2(a)所示的是Eu2+掺杂与不掺杂的样品
的漫反射光谱图.由图可以看出基质(Sr0.95Mg0.05)3(PO4)2在300~800 nm的范围内表现出很高的反射特性,在200~300 nm范围内又表现出很强的吸收特性,这是因为价带和导带之间的传递.相比于不掺杂Eu2+的样品,掺杂Eu2+的样品在250~400 nm表现出很强的吸收特性,这是对应于Eu2+的4f7→4f65d1能级跃迁.可以在图2(a)中看出两个吸收带分别位于220~310 nm和310~400 nm.这种现象同样也证实了Sr2+在基质中存在着两种不同的配位环境.当这两种不同的配位环境下的Sr2+被Eu2+随机取代后就会表现出两种不同的吸收带的出现.随着Eu2+掺杂浓度的增加,两处的吸收带也逐渐增强,同时吸收带的边缘也逐渐向长波方向移动.这种吸收带边缘随着Eu2+浓度增加而出现红移的现象是由于Eu2+的5d晶体场的分裂和斯托克斯位移导致的.基质(Sr0.95Mg0.05)3(PO4)2的带隙可有方程1估算出
[F(R∞)hv]n=A(hv-Eg).
(1)
式(1)中,hv为光子能量,A为比例常数,Eg是带隙的值,n=1/2表示直接传递,n=2表示间接传递.F(R∞)为Kubelka-Munk函数.基质(Sr0.95Mg0.05)3(PO4)2的吸收光谱由Kubelka-Munk函数计算得知[10]
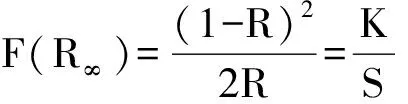
(2)
式中的R,K和S分别表示反射、吸收和散射系数.图2(b)所示的是基质(Sr0.95Mg0.05)3(PO4)2的吸收光谱,由Kubelka-Munk函数计算得出的.由K/S=0推断并计算出Eg的值约为5.28eV.
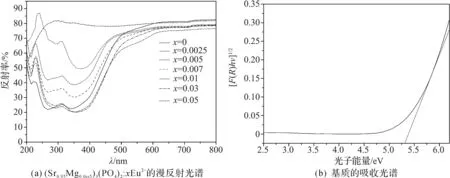
图2 漫反射光谱与基质的吸收光谱Figure 2 Diffuse reflection spectra of (Sr0.95Mg0.05)3(PO4)2:xEu2+ and absorption spectra of matrix
2.3 光谱特性
图3所示的是(Sr0.95Mg0.05)3(PO4)2:0.01Eu2+的激发与发射光谱.样品(Sr0.95Mg0.05)3(PO4)2:Eu2+在570 nm波长监测下的激发波长在230 nm到390 nm表现出宽的激发带,源于Eu2+中的4f7→4f65d1电偶传递,激发光谱与近紫外LED芯片相匹配.黄光发射宽谱对应于Eu2+中的4f65d1→4f7能级跃迁辐射,这是由于在大多数晶体中,Eu2+的4f65d1能级高于4f7,所以Eu2+通常会产生d→f的宽带跃迁发射[11-14].
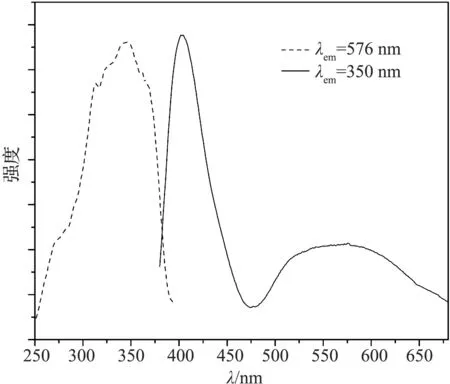
图3 (Sr0.95Mg0.05)3(PO4)2:0.01Eu2+的激发和发射光谱Figure 3 Photoluminescence and photoluminescence excitation spectra of (Sr0.95Mg0.05)3(PO4)2: 0.01Eu2+excited at 350 nm
(Sr0.95Mg0.05)3(PO4)2:Eu2+荧光粉有两个宽的发射带峰值分别位于410nm和570nm处.光谱中没有明显的尖锐的f-f传递线性峰值,说明在还原气氛下Eu3+完全被还原为Eu2+.从下图4中可以看出(Sr0.95Mg0.05)3(PO4)2:Eu2+荧光粉的发射光谱光谱中有两个发射峰.考虑到在基质中Sr2+有两种配位环境,Sr1为六配位的,Sr2为十配位的,同时十配位的数量是六配位的数量的两倍还多.这两种不同的配位环境都可以被Eu2+取代,根据文献知,410 nm的发射峰是Eu2+取代Sr2产生的,570 nm的发射峰是Eu2+取代Sr1产生的[15].因为Sr2数量多于Sr1的,所以Eu2+取代Sr2的数量会更多,所以在410 nm处的光强会强于570 nm处的光强.

图4 在350 nm激发下的不同Eu2+浓度的 (Sr0.95Mg0.05)3(PO4)2:Eu2+的发射光谱Figure 4 Emission spectra of (Sr0.95Mg0.05)3(PO4)2: Eu2+ phosphor with varying Eu2+ concentration under UV excitation at 350 nm
激活剂的浓度对发光强度有很大的影响,为了得到最佳发光强度的荧光粉,我们研究了不同离子浓度的系列荧光粉(Sr0.95Mg0.05)3(PO4)2:xEu2+.从图4中可以看出随着Eu2+浓度的增加,发射强度也逐渐增加,直到Eu2+浓度为1 mol%,再继续增加,发射光谱开始减弱,主要是由于Eu2+浓度猝灭引起的.在Eu2+浓度较小的时候发光强度较低.随着Eu2+浓度的增加,会使发光中心之间的平均距离减小,同时基质的吸收激发光能力增强,能量传递加快,当Eu2+掺杂浓度达到1 mol%后,发光强度达到最大值.继续增加Eu2+浓度,Eu2+→Eu2+之间的相互作用增强,然后产生大量的无辐射跃迁,导致Eu2+浓度猝灭,导致发光强度减弱.以上可知样品的激活离子的最佳浓度为0.01.
Eu2+在(Sr0.95Mg0.05)3(PO4)2:xEu2+荧光粉的发光机制可以由以下的方程拟建每激活离子的发光强度可由以下方程式求得[16-17]
I/x=K[1+β(x)Q/3].
(3)
I为发光强度,x为激活离子的浓度,K和β在一给定的激发和晶体结构中时常数.Q=3为离子之间交换耦合相互作用,另外Q=6,8和10时分别代表电偶极子-电偶极子,电偶极子-电四极子,电四极子-电四极子相互作用.为了计算出准确的Q值,log(xEu2+)对log(I/xEu2+)的关系如下图5所示.可以得出线性斜率分别为-1.22和-1.65,因此两处发射峰的Q值分别为3.64和4.97.结果表明在410nm处的浓度猝灭机制是离子之间的交换耦合相互作用导致,在570nm处的浓度猝灭机制是电偶极子-电四极子相互作用导致.
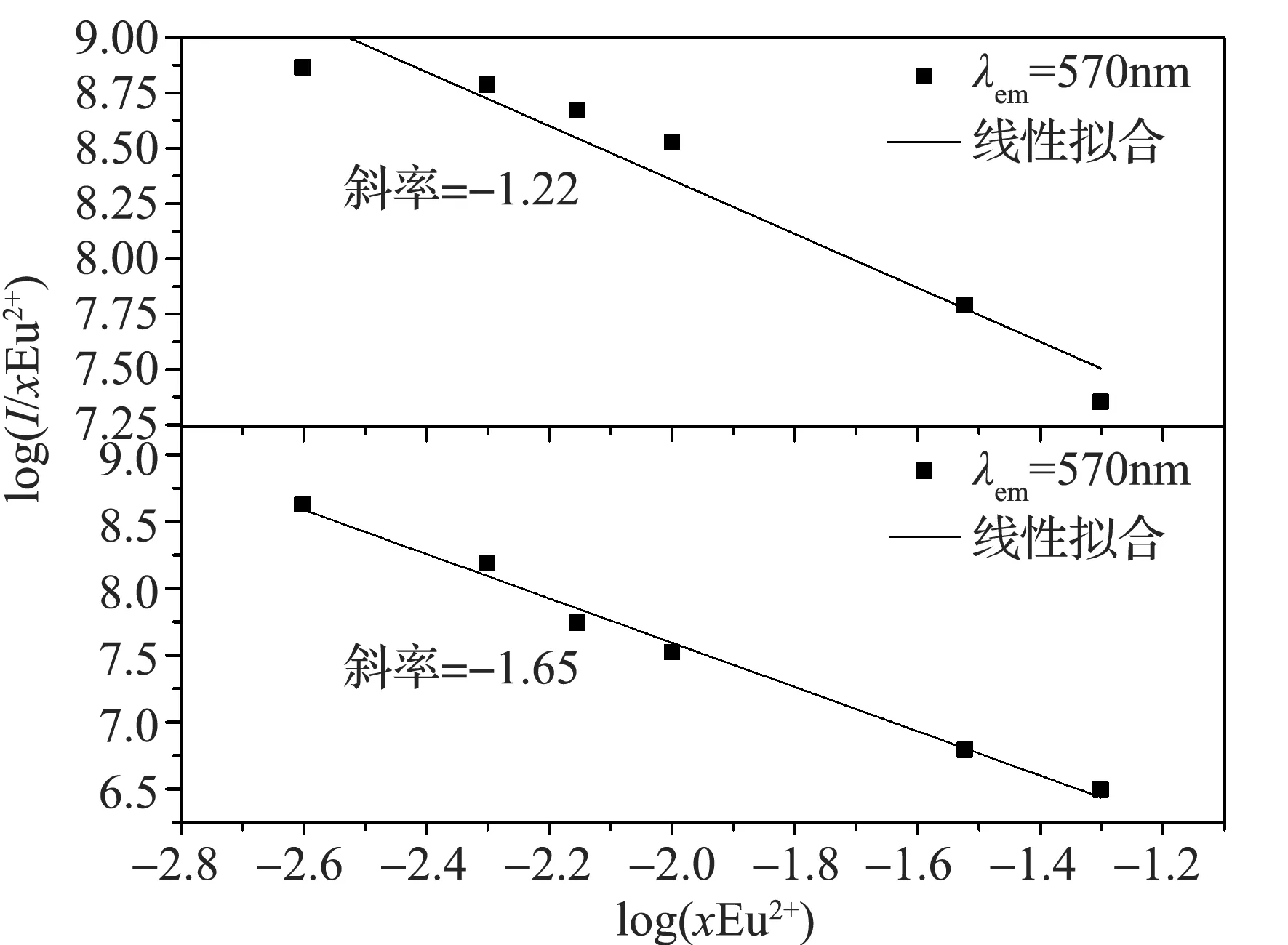
图5 在350 nm激发下的log(xEu2+)和 log(I/xEu2+)关系图Figure 5 Relationship between log(xEu2+) versus log(I/xEu2+) under the excitation of 350 nm
图6是(Sr0.95Mg0.05)3(PO4)2:0.01Eu2+荧光粉在室温下的荧光寿命曲线,分别是在峰值为408 nm和570 nm处的监测下测得的.一般来说,随着激活离子浓度增加,激活离子之间的距离减小,彼此之间发生能量传递.因此不同激活离子浓度的荧光寿命曲线不一样[17,18].考虑到该荧光粉中存在两个发光中心,寿命曲线可由双指数方程拟合[19]
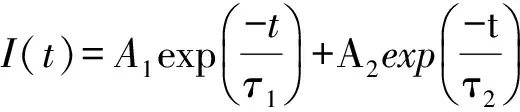
(4)
I为发光强度,A1和A2为常数,t为时间,τ1和τ2为指数部位的衰减时间.平均寿命时间(τ)可由下方程式计算得[19]
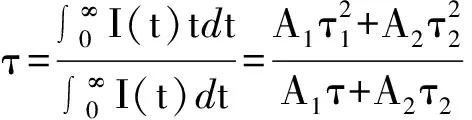
(5)
I(t)为在时间t时的发光强度,Eu2+的在峰值为408nm和570nm处的平均寿命计算为0.35和0.21μs.实验结果表明在基质(Sr0.95Mg0.05)3(PO4)2中Eu2+随机取代基质中的两种不同配位环境的Sr2+而成为发光中心.
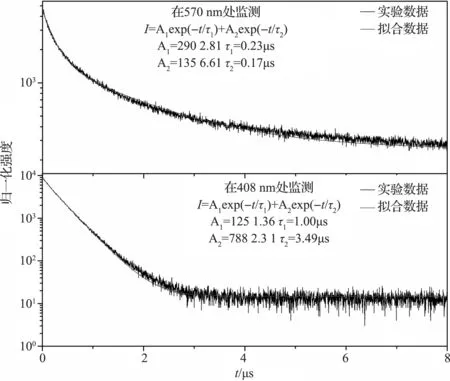
图6 在408 nm和570 nm处监测得的寿命图Figure 6 Decay profiles of (Sr0.95Mg0.05)3(PO4)2: 0.01Eu2+ phosphor monitored at 408 nm, 570 nm
荧光粉的热稳定性是衡量发光材料的重要参数之一.由于温度猝灭的影响,大部分发光材料的发光强度随着温度升高逐渐减弱.导致温度猝灭的主要机制是无辐射能量传递导致.图7所示的是样品(Sr0.95Mg0.05)3(PO4)2:0.01 Eu2+在350 nm波长激发下的发射光谱的两个峰值随温度变化(30~200 ℃)的曲线,从图中可以看出发射光强都随着温度的升高逐渐减弱.当温度达到100 ℃时,峰值为410 nm处的光强减弱为原来的95.3%,峰值为570 nm处的光强减弱为原来的49.4%.因此格位Eu1和Eu2上的温度衰减速率不一样,原因是在高能量中心和低能量中心之间存在着能量传递,导致低能量的衰减速率减慢.这种现象也证实了荧光粉(Sr0.95Mg0.05)3(PO4)2: Eu2+存在着两个不同的发光中心.
图8是在350 nm波长激发下样品(Sr0.95Mg0.05)3(PO4)2:xEu2+的CIE色坐标以及样品实图.从图中可以看出随着Eu2+浓度增加,色坐标从(0.259 5,0.198 7)逐渐移动到(0.324 5, 0.313 3).根据浓度猝灭可知,当Eu2+掺杂浓度超过0.01时,双峰的强度均会减弱,但是黄色部分的减少速率更大,所以色坐标又回到蓝光部分(0.250 7,0.199 9).这种现象表明可以通过控制Eu2+的浓度来实现发射光谱从蓝光区域到白光区域的变化.因此,以上实验结果表明Eu2+掺杂的(Sr0.95Mg0.05)3(PO4)2是一种潜在的应用于白光LED中的单一基质实现发白光发射的荧光粉.
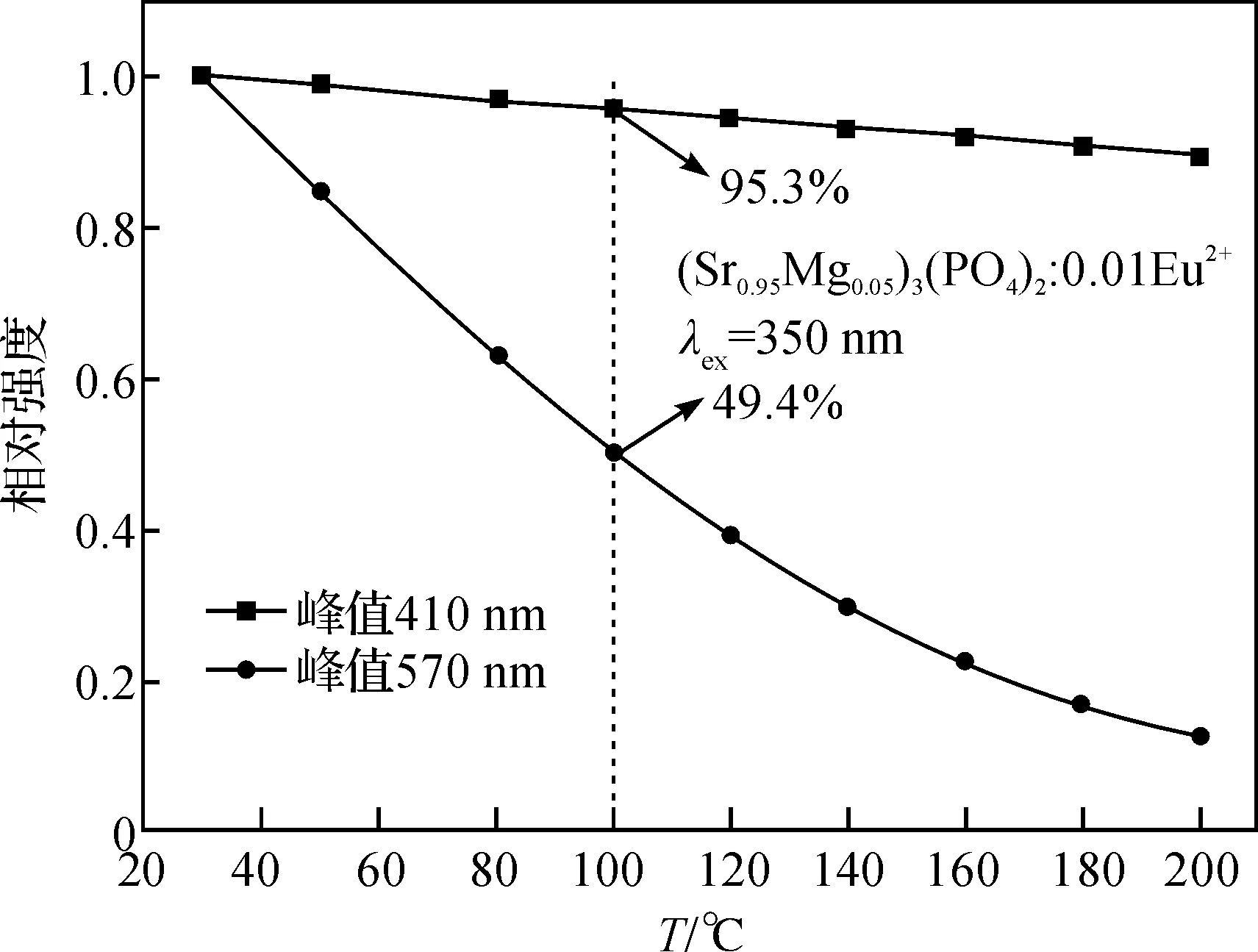
图7 双峰强度随温度变化的归一化值Figure 7 Normalized emission intensity of the two peaks as a function of temperature
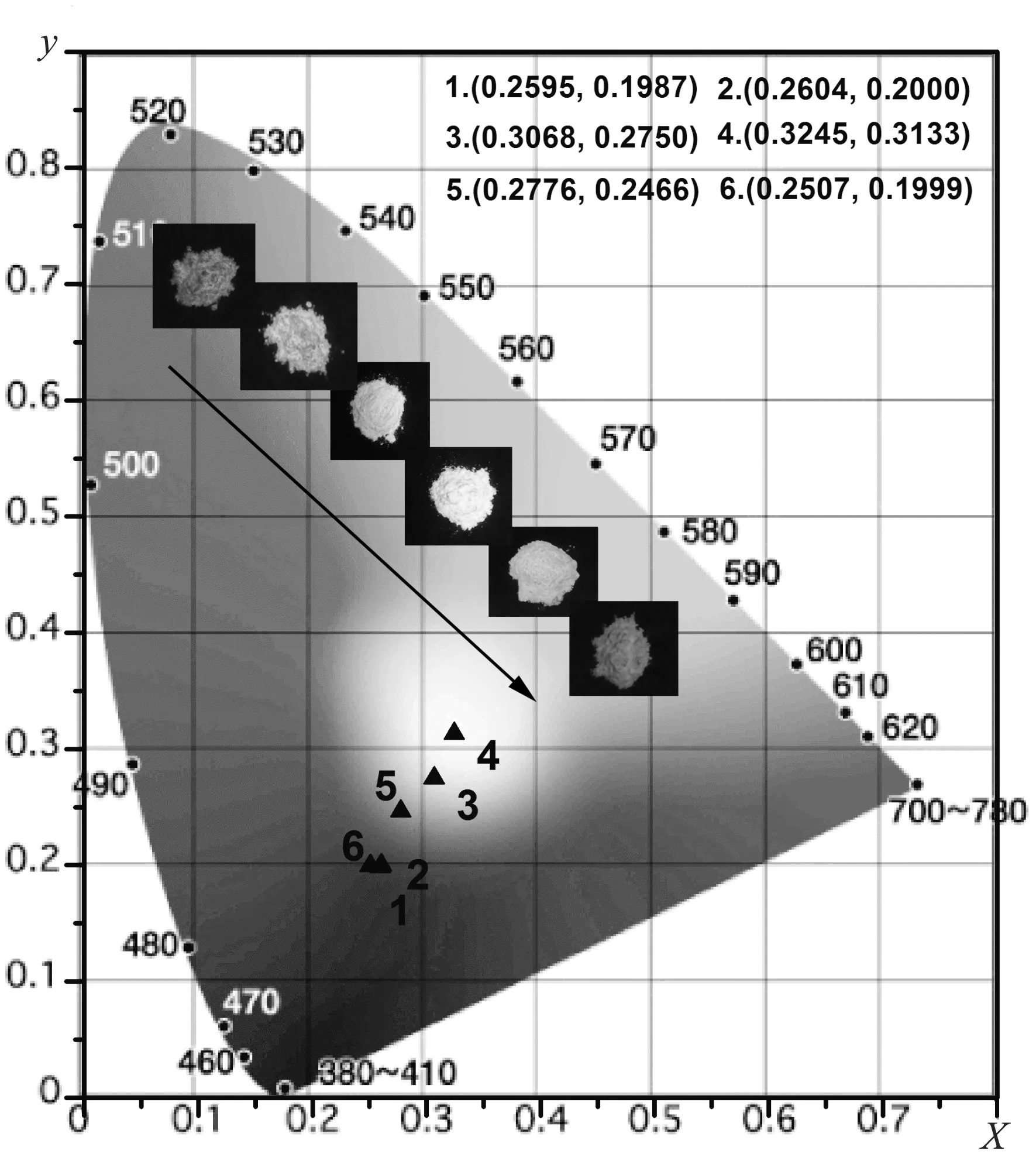
图8 在350 nm激发下的(Sr0.95Mg0.05)3(PO4)2: xEu2+(x=0.002 5, 0.005, 0.007, 0.01, 0.03, 0.05)的CIE色度坐标图,插图为样品在360 nm 激发下的实图Figure 8 CIE chromaticity diagram of (Sr0.95Mg0.05)3(PO4)2: xEu2+ phosphors excited at 350 nm (x=0.002 5, 0.005, 0.007, 0.01, 0.03, 0.05). The inset shows the phosphors together with their photos taken under 360 nm excitation
3 结 语
采用高温固相法合成了一系列新型双峰发射的(Sr0.95Mg0.05)3(PO4)2:xEu2+荧光粉,并研究了Eu2+对(Sr0.95Mg0.05)3(PO4)2的晶体结构,发光特性以及发光寿命的影响,也研究了激活离子浓度的淬灭机制.这种荧光粉在近紫外区域有较强的吸收特性,当激发波长为350 nm时,发射光谱会有两个较强的发射峰,峰值分别位于410 nm和570 nm,这是由于Eu2+进入基质晶格后随机取代两个不同配位环境的Sr2+而形成两种不同的发光中心产生的.实验得知Eu2+的最佳掺杂浓度为0.01.经过理论计算,在410 nm处的浓度猝灭机制是由离子之间的交换耦合相互作用引起的,在570 nm处的浓度猝灭机制是电偶极子-电四极子相互作用引起的.随着掺杂Eu2+浓度从0到0.01逐渐变化,荧光粉的CIE色坐标也逐渐从蓝光区域逐渐移动到白光区域.以上实验结果表明,(Sr0.95Mg0.05)3(PO4)2: Eu2+是一种潜在的可用于白光LED照明中的单一基质荧光粉.
[1] KIM J S, JEON P E, CHOI J C, et al. Warm-white-light emitting diode utilizing a single-phase full-color Ba3MgSi2O8:Eu2+, Mn2+Phosphor[J]. Applied Physics Letters,2004, 84(15):2931-2933.
[2] MUTHU S, SCHUURMANS F J P, PASHLEY M D. Red, green, and blue LEDs for white light illumination[J]. IEEE Journal on Selected Topics in Quantum Electronics,2002,8(2):333-338.
[3] HUANG C H, CHEN T M. A novel single-composition trichromatic white-light Ca3Y(GaO)3(BO3)4:Ce3+. Mn2+. Tb3+phosphor for UV-light emitting diodes[J]. Journal of Physical Chemistry C,2011,115(5):2349-2355.
[4] SETLUR A A, HEWARD W J, GAO Y, et al. Crystal chemistry and luminescence of Ce3+-doped Lu2CaMg2(Si.Ge)3O12and its use in LED based lighting[J]. Chemistry of Materials,2006,18(14):3314-3322.
[5] XIA Z, MA C, MOLOKEEV M S, LIU Q, et al. Chemical unit cosubstitution and tuning of photoluminescence in the Ca2(Al1-xMgx)(Al1-xSi1+x)O7:Eu2+phosphor[J]. Journal of the American Chemical Society,2015,137(39):12494-12497.
[6] JANG H S, WON Y H, JEON D Y. Improvement of electroluminescent property of blue LED coated with highly luminescent yellow-emitting phosphors[J]. Applied Physics B: Lasers Optical,2009,95(4):715-720.
[7] TANG Y, HU S, LIN C, et al. Thermally stable luminescence of KSrPO4:Eu2+phosphor for white light UV light-emitting diodes[J]. Applied Physics Letters,2007,90(15):151108-151111.
[8] ZHENG J, CHENG Q, WU S, et al. An efficient blue-emitting Sr5(PO4)3Cl:Eu2+phosphor for application in near-UV white light-emitting diodes[J]. Journal of Materials Chemistry C,2015,42(3):11219-11227.
[9] WU Z C, SHI J X, WANG J, et al. A novel blue-emitting phosphor LiSrPO4:Eu2+for white LEDs[J]. Journal of Solid State Chemistry,2006,179(8):2356-2360.
[10] DENG D, YU H, LI Y, et al. Ca4(PO4)2O:Eu2+red-emitting phosphor for solid-state lighting: structure, luminescent properties and white light emitting diode application[J]. Journal of Materials Chemistry C,2013,19(1):3194-3199.
[11] DORENBOS P. Energy of the first 4f7→4f65d transition of Eu2+in inorganic compounds[J]. Journal of Luminescence,2003,104(4):239-260.
[12] XIE R J, HIROSAKI N, MITOMO M, et al. Optical properties of Eu2+in α-SiAlON[J]. Journal of Physical Chemistry B,2004,108(32):12027-12031.
[13] HARANATH D, SHANKER V, CHANDER H, et al. Tuning of emission colours in strontium aluminate long
persisting phosphor[J]. Journal of Physics D: Applied Physics,2003,36(18):2244-2248.
[14] LIU H, ZHANG Y, LIA L, et al. Synthesis, broad-band absorption and luminescence properties of blue-emitting phosphor Sr8La2(PO4)6O2:Eu2+for n-UV white-light-emitting diodes[J]. Ceramics International,2014,40(8):13709-13713.
[15] CHEN F, YUAN X, ZHANG F, et al. Photoluminescence properties of Sr3(PO4)2: Eu2+, Dy3+double-emitting blue phosphor for white LEDs[J]. Optical Materials,2014,37: 65-69.
[16] LI K, GENG D, SHANG M, et al. Color-tunable luminescence and energy transfer properties of Ca9Mg(PO4)6F2:Eu2+, Mn2+phosphors for UV-LEDs[J]. Journal of Physical Chemistry C,2014,118(20):11026-11034.
[17] LI H, ZHAO R, JIA Y, et al. Sr1.7Zn0.3CeO4:Eu3+novel red-emitting phosphors: synthesis and photoluminescence properties[J]. ACS Applied Materials & Interfaces,2014,6(5):3163-3169.
[18] SOHN K S, CHION Y Y, PARK H D. Photoluminescence behavior of Tb3+-Activated YBO3phosphors[J]. Journal of the Electrochemical Society,2000,147(5):1988-1992.
[19] YU H, DENG D, CHEN L, et al. Luminescent properties of novel Ca2.89Mg0.11(PO4)2:Eu2+single-phase white light-emitting phosphor for white LEDs[J]. Ceramics International,2015,41(3):3800-3805.
Luminescence properties of a novel single-phase phosphor (Sr0.95Mg0.05)3(PO4)2:Eu2+for white light emitting diodes
MA Yutao, LI Chenxia, DENG Degang, HUA Youjie
(College of Optical and Electronic Technology, China Jiliang University, Hangzhou 310018, China)
A series of single-phase white-light-emitting, Eu2+-doped (Sr0.95Mg0.05)3(PO4)2phosphors were synthesized by the traditional solid-state reaction method. This phosphor could be effectively excited by UV light in the range of 270 to 390 nm, which matched well with that of ultraviolet LEDs. Under the excitation of 350 nm, this phosphor exhibited two broad emission bands, with peaks of 410 nm and 570 nm, which originated from two luminescence centers, related to 4f65d1→4f7transition of Eu2+occupying the ten-coordination Sr sites and six-coordination Sr sites, respectively. The emission intensity increased gradually with increasing Eu2+ions content up to a maximumxvalue of 1mol%, after which it decreased because of the concentration quenching. The CIE chromaticity coordinates of the prepared double-emitting (Sr0.95Mg0.05)3(PO4)2:Eu2+phosphor could shift from blue (0.259 5, 0.198 7) to white area (0.324 5, 0.313 3) by changing the Eu2+doping concentration from 0 to 0.01. Based on experimental results and theoretical calculation, the luminescence characteristics indicate that this phosphor has great potential to serve as an attractive candidate in the application of n-UV excited white LEDs.
single-phase; phosphors (Sr0.95Mg0.05)3(PO4)2: Eu2+; white LEDs
2096-2835(2016)04-0458-07
10.3969/j.issn.2096-2835.2016.04.018
2016-10-13 《中国计量大学学报》网址:zgjl.cbpt.cnki.net
国家自然科学基金资助项目(No.51272243, 61405185, 61370049, 51402077, 61575182),浙江省自然科学基金资助项目(No.LR14A040002, LQ13E020003,LY16F050004).

TH744
A
