亚稳态MInS2(M=Ag,Cu)花状微米球的热分解法合成及其生长机理
2016-12-20王跃邹晓川王存石永芳
王跃 邹晓川 王存 石永芳
(1重庆第二师范学院生物与化学工程系,重庆400067)
(2中国科学院福建物质结构研究所光电材料化学与物理重点实验室,福州350002)
亚稳态MInS2(M=Ag,Cu)花状微米球的热分解法合成及其生长机理
王跃*,1邹晓川1王存1石永芳*,2
(1重庆第二师范学院生物与化学工程系,重庆400067)
(2中国科学院福建物质结构研究所光电材料化学与物理重点实验室,福州350002)
采用热分解法制备了三维的亚稳态正交相AgInS2和六方相CuInS2花状微米球。通过X射线衍射(XRD),场发射扫描电子显微镜(FESEM)等对样品进行表征,对AgInS2的光催化性能进行了评估,并借助于热重-差热分析(TG-DTA)等手段研究了亚稳态正交相AgInS2和六方相CuInS2花状微米球的生长机理。实验结果表明,反应温度和反应物中金属离子的投料比对生成纯相的MInS2均有影响,而AgInS2花状微米球能在可见光下较好地催化降解亚甲基蓝。
亚稳态MInS2;花状微米球;热分解法;生长机理
三元金属硫化物MInS2(M=Ag,Cu),作为两种重要的Ⅰ-Ⅲ-Ⅵ族半导体材料,因其具有独特的光电和催化性能,在发光二极管、非线性光学器件、太阳能电池、光催化、生物标记等领域具有潜在的应用前景,近几年越来越受到人们的关注,渐渐成为研究的热点[1-8]。目前,人们已经运用水热法、溶剂热法、热注入法和微波法等成功制备出了多种形貌的纳米MInS2(M=Ag,Cu),如零维的纳米颗粒[9]、一维的纳米纤维[10]、二维的纳米片[11]等。到目前为止,有关三维MInS2(M=Ag,Cu)花状微米球结构的报道不多[12-13]。在本文中,我们借助于热分解法,通过改进原来二元硫化物前驱体的合成路线,成功地制备出三元硫属化合物MInS2(M=Ag,Cu)花状微米球。与纯溶剂法相比,热分解法合成的优势在于:(1)前驱体(指金属与有机配体形成的配合物)中的长碳链有机配体可以控制热分解过程中颗粒的成核和生长;(2)吸附在颗粒表面的有机配体能够有效阻止颗粒聚集;(3)反应条件温和,设备简单。因此,在合成过程中,有效避开了溶液法中常用的有机配体十二硫醇和油胺,通过在250~280℃裂解金属有机前驱体,成功地制备了亚稳态正交相AgInS2和六方相CuInS2。同时,我们通过XRD、SEM等手段对所得样品进行了详细地表征,对MInS2(M=Ag,Cu)花状微米球的生成机理也做了探讨。最后,对AgInS2的光催化性能也做了适当的评估。
1 实验部分
1.1试剂
分析纯的硝酸银(AgNO3)、醋酸铜(Cu(CH3COO)2·H2O)、硝酸铟(In(NO3)3·4.5H2O)、二硫化碳(CS2)、氢氧化钾(KOH)、无水乙醇(C2H5OH)、三氯甲烷(CHCl3)、二氯甲烷(CH2Cl2)、丙酮(CH3COCH3)均购自国药集团化学试剂有限公司;二正辛基胺(HN(C8H17)2)购自百灵威试剂公司;氩气(Ar)购自福州华鑫达气体有限公司。以上试剂均直接使用。
1.2MInS2(M=Ag,Cu)花状微米球的制备
1.2.1配体的合成
将0.264 g氢氧化钾(稍过量)溶于25 mL的无水乙醇中,充分溶解后加入1.8 mL二正辛基胺,在冰浴搅拌下缓慢加入0.36 mL二硫化碳(稍过量),继续反应3 h,得到配体溶液。
1.2.2前驱体合成
先将溶于乙醇中的硝酸铟(0.478 g)(依据前期的探索实验,In稍过量有利于生成三元相)加入上述配体溶液中,搅拌均匀,再将溶于乙醇的醋酸铜(0.100 g)或硝酸银(0.170 g)加入其中继续搅拌,然后将反应液体进行旋蒸除去溶剂,将旋蒸后得到的固体溶于三氯甲烷中,过滤,将滤液蒸发,用丙酮洗涤,随后蒸去丙酮,得到粘土状前驱体。
1.2.3目标产物的生成
将制备的适量前驱体转入试管内,再将试管放置于相应的长石英管(6 cm×1 m)中,两端塞好中心带孔的橡胶塞并通入氩气,然后开启管式炉,使之温度维持在250~280℃下3 h,之后自然冷却降温,得到的黑色固体用CH2Cl2和EtOH/H2O反复洗涤4次,自然干燥。
1.3测试与表征
X射线粉末衍射数据在RIGAKU D-MAX-2500或PANalytical X′Pert Pro衍射仪上收集,工作电压40 kV,电流100 mA,Cu Kα1射线(λ=0.154 nm),步长0.05°,收集2θ角度范围为5°~85°,所收集的数据经Jade 6.5软件(标准卡片采用ICDD PDF2-2004版本)分析。所有纳米产物的SEM图像均是通过JSM 6700F场发射扫描电子显微镜(FESEM)观察获得,其工作电压10 kV,电流10μA。紫外-可见吸收光谱在PerkinElmer Lambda35 UV-Vis光谱仪上测得,将少量样品超声分散在相应溶剂中,然后,移取少量溶液于比色皿中,用相应的溶剂作参比进行测试。在氮气气氛下,热分析(热重与差热)数据在NETZSCH STA 449F3热综合分析仪上收集;其过程如下:将5~10 mg样品放入预先处理干净的氧化铝坩埚中,在将空气赶出系统后,利用升温程序,以5℃·min-1的升温速率,将系统从室温加热至目标温度。
1.4光催化性能测试
样品的光催化活性是通过在紫外-可见光照射下降解亚甲基蓝(MB)水溶液进行检测。将100 mg AgInS2纳米粉悬浮于100 mL浓度为0.001%的MB水溶液中。在进行照射前,开启搅动按钮,并把该悬浊溶液放置于黑暗中1 h,以确保吸附-脱附平衡。之后把整套装置暴露于300 W的卤钨灯(整套设备自制)下,整个反应过程不间断搅动与照射。期间,每隔0.5 h,取出4 mL包含光催化剂和MB的悬浊液,并经离心沉降除去AgInS2颗粒。所得清液的MB浓度采用紫外-可见分光光度计进行分析,测量波长668 nm处的吸光度进行表征。
2 结果与讨论
2.1正交相AgInS2与六方相CuInS2的结构和形貌
AgInS2和CuInS2花状微米球的XRD图如图1a、b所示。其中,AgInS2的各峰(图1a)与正交相的AgInS2(PDF#25-1328)一致,且看不到其它杂相的峰。而CuInS2的XRD图(图1b)在现有的数据库中未能找到匹配的图,但通过晶体数据模拟,其图跟六方相纤锌矿型CuInS2粉末衍射图一致,图中26.29°、27.72°、29.79°、38.6°、46.44°、50.35°和54.98°分别对应于六方相CuInS2的(100)、(002)、(101)、(102)、(110)、(103)和(112)晶面,这与文献报道的结构相吻合[14-16]。如图1c所示,正交相AgInS2的晶胞由AgS4和InS4四面体组成,通过共顶点的S原子连接;而六方相CuInS2的晶胞(图1d)则是由混合占据的Cu、In与S组成四面体,通过共顶点的S原子连接。从两者结构可知,一旦M、In原子从有序占据变为混合占据,其正交相也会相应转变为六方相[17]。
文献报道,AgInS2在自然界存在着2种不同晶型:室温下的四方相黄铜矿和高温下的正交相类纤锌矿,两者的转变温度为620℃[18];而CuInS2在自然界存在着3种不同晶型:黄铜矿、闪锌矿和纤锌矿,其中,黄铜矿是热力学稳定的结构[19]。由此可见,我们制备的正交相类纤锌矿型AgInS2和六方相纤锌矿型CuInS2花状微米球均属亚稳相,而传统的常温常压方法不易获得,因此我们的热分解合成方法为制备亚稳相结构提供了一种可行性的思路。
我们采用SEM对所得产物的形貌进行分析。如图2a所示,在280℃下加热3 h制备的AgInS2为花状微米球,尺寸在1~3μm,其中除单分散的球体外,还有部分是几个球粘在一起的聚合体,但内部花瓣的厚度均在25 nm左右。与AgInS2类似,250℃下加热3 h制备的CuInS2也为花状微米球(图2b),其尺寸也在1~3μm之间,内部花瓣的厚度也在25 nm左右,只是形貌的均一性要差些,因为除了大部分的花状微米球外,还带有部分尺寸小于1μm的不规则颗粒。为了能获得形貌更加均一的CuInS2花状微米球,我们尝试了不同的温度和时间,但效果都不够理想,这表明,制备形貌均一的三维CuInS2纳米结构有一定难度,这或许就是目前很少有三维六方相纤锌矿型CuInS2纳米结构报道的原因。

图2 (a)280℃下加热3h制备的AgInS2花状微米球的SEM图;(b)250℃下加热3 h制备的CuInS2花状微米球的SEM图Fig.2(a)SEM image of AgInS2flowerlike microsphere prepared at 280℃for 3 h;(b)SEM image of CuInS2flowerlike microsphere prepared at 250℃for 3 h

图3 (a)AgS2CNR2/In(S2CNR2)3的热重-差热分析(TG-DTA)测试曲线;(b~c)不同温度下加热3 h所得产物的XRD图Fig.3(a)TG-DTA curve of AgS2CNR2/In(S2CNR2)3;(b~c)XRD patterns of products prepared at different temperatures for 3 h
2.2反应温度对产物物相的影响
为了考察反应温度对产物的影响,我们选取了不同的温度进行尝试,并对前驱体进行了热分析(热重与差热)测试。如图3a、4a所示,前驱体AgS2CNR2/ In(S2CNR2)3与Cu(S2CNR2)2/In(S2CNR2)3均在150℃附近出现第一个峰,应该是C-S键断裂造成的,相应生成单斜相Ag2S和正交相Cu2S,这与图3b、4b所对应的XRD图吻合。差热分析的第二个峰均出现在252℃,应该是由于In(S2CNR2)3吸热缓慢释放出In3+,而In3+通过部分取代Ag+、Cu+最终形成AgInS2和CuInS2引起的,这与图3c、4c所对应的XRD图吻合;另外,由于AgInS2在生成过程中涉及单斜相向正交相的转变,故Ag的吸热峰比Cu的强。第三个峰出现在330℃左右,此时,有机副产物已经挥发完全,故在热重分析(TG)线上不再发生任何重量的变化,当然,对于制备AgInS2和CuInS2而言,温度已经偏高,因为两者分别出现了杂相AgIn5S8与四方相CuInS2(图3d、4d)。因此,要想获得纯相的正交类纤锌矿型AgInS2与六方纤锌矿型CuInS2,其合适的温度范围应该在250~280℃。

图4 (a)Cu(S2CNR2)2/In(S2CNR2)3的热重-差热(TG-DTA)测试曲线;(b~c)不同温度下加热3 h所得产物的XRD图Fig.4(a)TG-DTA curve of Cu(S2CNR2)2/In(S2CNR2)3;(b~c)XRD patterns of products prepared at different temperatures for 3 h
2.3生成亚稳相AgInS2与CuInS2花状微米球的可能机理
正交相类纤锌矿型AgInS2与六方相纤锌矿型CuInS2在常温下并非热力学稳定结构,属亚稳相,因此在常温常压下不容易合成。根据文献报道,要想获得动力学稳定的结构,可以通过适当调节反应物的比例以降低同质异构体间的转变势垒[20]来实现;也可以通过提高空间位阻的方式减小金属离子配位数[21]的方法来实现。在我们制备过程中,上述2个因素也确实起了重要的影响。
2.3.1金属离子比例的影响
Ag+(102 pm)、Cu+(77 pm)与In3+(80 pm)的半径都远远小于S2-(184 pm)的半径,且Ag+、Cu+所带的电荷仅为In3+的1/3,故Ag+、Cu+在晶格中的迁移速度大幅高于In3+,在同一裂解温度下会优先生成Ag2S和Cu2S[15]。因此,我们尝试了3个In3+适量或稍微过量的不同比例进行考察,其结果如表1所示。
由表1可知,对Ag而言,只有适当过量的In才能获得纯相的AgInS2,这是因为在正交相AgInS2中,Ag和In并非混合占据,要想形成相应结构,In必须完全且有序地取代相应位置的Ag,而适当过量的In有利于这一过程的进行。但对于Cu而言,只要在确保nCu+nIn≤nS的前提下,In是否过量影响不大,都能获得纯相的CuInS2,这应该与六方纤锌矿型CuInS2结构中Cu、In是混合占据的特性有关。既然Cu与In在结构上是混合占据,表明无论是Cu过量还是In过量,都不会改变晶体的整体结构,只会改变Cu和In在晶体内部各自所占的比例。这一点,在调节nCu:nIn=1.25:1时仍得到纯相的六方纤锌矿型CuInS2上得到了验证。再者,晶体内部Cu和In所占比例的不同,有可能会影响晶体的能隙,这为调控CuInS2的光吸收范围提供了一种潜在的思路。
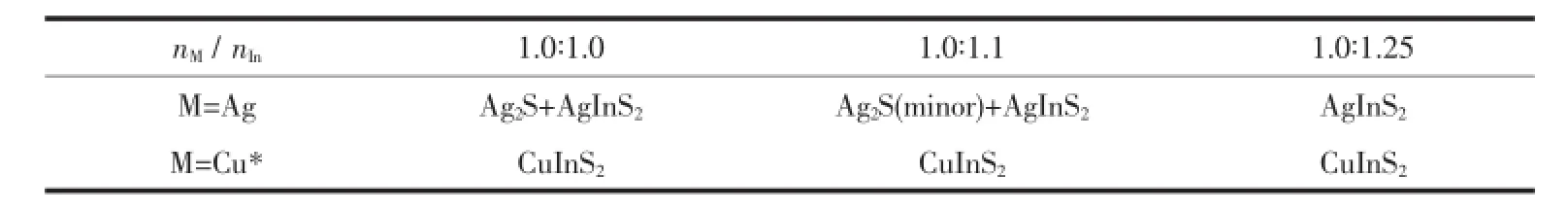
表1 由不同比例金属离子制备的前驱体裂解所得的产物Table 1 Products obtained using precursors pyrolysis synthesized by different feed ratio of metallic ions
2.3.2有机配体的影响
热分解法制备微纳米结构时,很重要的一步就是选择合适的长碳链配体,不仅能与金属离子进行有效地配合形成前驱体,还能控制热分解过程中颗粒的成核和生长,且吸附在颗粒表面从而有效阻止颗粒的聚集。在本次实验中,我们选择二正辛基胺(HNR2,R=-C8H17)来制备相应的配体二正辛基二硫代铵基甲酸钾KS2CNR2(反应式1),所有的合成反应如下所示[22]:

Scheme 1 Reactions to generate MInS2(M=Ag,Cu)
首先,新制备的KS2CNR2与Ag+、Cu2+、In3+配位形成相应的配合物AgS2CNR2(反应式2)、Cu(S2CNR2)2(反应式3)和In(S2CNR2)3(反应式4)。需要强调的是,在减压除去乙醇的过程中,由于这些配合物都是在溶液中形成,并经过充分搅拌,因此在最后的固体形式中,并不是简单的机械混合,而应该是在接近分子水平上的均匀混合,如此能确保In3+在没有溶剂的环境中跟生成的二元硫化物有充分接触的机会,这一点是制备三元硫化物的关键所在。采用类似的方法,我们之前还成功地获得了亚稳态六方相的MIn2S4(M=Mn,Fe,Co)[22b]。此后,随着温度的上升,Cu(S2CNR2)2在剩余二正辛基胺的作用下还原成CuS2CNR2(反应式5)。当温度进一步上升时,AgS2CNR2和CuS2CNR2分解为相应的Ag2S(反应式6)和Cu2S(反应式7),由于Ag+和Cu+在高温条件下具有高的扩散性,能够在晶格的阳离子空穴中自由移动[23],故从In(S2CNR2)3中缓慢释放出来的In3+能部分取代Ag2S和Cu2S晶格中的Ag+和Cu+,从而逐渐形成正交相类纤锌矿型AgInS2和六方相纤锌矿型CuInS2。另一方面,我们前期的工作表明,之所以能够得到三维的花状微米球结构,是制备所用的有机配体KS2CNR2起了很大的作用[22b,24]。在封端剂KS2CNR2的包裹下,新生成的纳米小颗粒会各向异性地进行生长,形成片状结构;同时,这些颗粒又受到奥斯特瓦尔德熟化过程(Ostwald ripening process)的驱使,也会各向同性地以枝晶的方式进行生长。平衡两者共同作用的结果,就导致了花状微米球结构的形成。
2.4光催化性能测试
由正交相AgInS2的晶体结构可知,Ag-S键长与In-S键长不相等,是一种变形的四面体,这种畸变构型会导致中心正负电荷分离而形成电场。在光子激发的过程中,电场能有效促进电子与空穴的分离,进而增强光催化性能[25];另一方面,AgInS2花状微米球的三维空间结构是由众多纳米级厚度的薄片堆聚而成,能把MB分子吸入薄片与薄片之间的间隙,从而增大光催化剂与MB分子之间的接触面积,即能比零维的纳米颗粒提供更多的光催化活性中心。为此,我们用可见光下降解MB的测试来评估AgInS2的光催化性能。如图5所示,随着光照时间的推进,溶液中MB的吸光度越来越小,表明其浓度也越来越低。最后,当光照时间经300 min后,由内插图可知,AgInS2花状微米球大约能降解81%的MB,表明其确实有一定的光催化降解有机污染物的能力。

图5 正交相AgInS2花状微米球光催化降解MB的吸收光谱Fig.5 Absorption spectra of MB photocatalytic degraded by orthorhombic AgInS2flowerlike microsphere
3 结论
采用二正辛基二硫代铵基甲酸钾、醋酸铜、硝酸银和硝酸铟作为反应试剂,我们利用热分解法成功制备了三维的亚稳相三元硫化物:正交相AgInS2和六方相CuInS2花状微米球。通过调控不同的反应温度,发现在250~280℃的范围内,能获得形貌较为均一且纯相的产物;而当温度低于180℃时,得到的大部分是二元的Ag2S和Cu2S,而温度超过320℃时,又会有新的三元杂相生成。另一方面,金属离子的投料比对亚稳相三元硫化物MInS2的生成也有一定的影响:适当过量的In有利于AgInS2的生成;但对Cu而言,只要保证Cu和In的物质的量之和不多于S的量,均能得到纯相的CuInS2,其原因在于Cu、In在晶体结构中是混合占据,而Ag、In是有序占据。此外,长碳链的有机配体在产物形貌演化过程中也起了重要作用,在其促进的各向异性生长与奥斯特瓦尔德熟化进程驱动的各项同性生长共同作用下,形成了MInS2三维花状微米球结构。而光催化实验则表明,AgInS2花状微米球在可见光下能较好地降解MB。
[1]Zeng Z,Wang A Q,Ping L L,et al.Mater.Lett.,2015,141: 225-227
[2]Peng S,Zhang S,Mhaisalkar S G,et al.Phys.Chem.Chem. Phys.,2012,14:8523-8529
[3]Liu B J,Li X Y,Zhao Q D,et al.Appl.Catal.B,2016,185: 1-10
[4]Chevallier T,Blevennec G L,Chandezon F.Nanoscale,2016, 8:7612-7620
[5]Wu L,Chen S Y,Fan F J,et al.J.Am.Chem.Soc.,2016, 138:5576-5584
[6]SUN Qian(孙倩),GUAN Rong-Feng(关荣锋),ZHANG Da-Feng(张大峰).J.Synth.Cryst.(人工晶体学报),2013,2(1): 65-71
[7]Lei S J,Wang C Y,Liu L,et al.Chem.Mater.,2013,25: 2991-2997
[8]Kruszynska M,Borchert H,Parisi J,et al.J.Am.Chem. Soc.,2010,132(45):15976-15986
[9](a)Mohadesi A,Ranjbar M,Karimi M A.J.Mater.Sci.-Mater. Electron.,2016,27:522-525
(b)Tang A W,Hu Z L,Yin Z,et al.Dalton Trans.,2015,44: 9251-9259
[10]Liu Z P,Tang K B,Wang D K,et al.Nanoscale,2013,5: 1570-1575
[11]Liu Z P,Wang L L,Hao Q Y,etal.CrystEngComm,2013,15: 7192-7198
[12]ZOU Xue-Jue(邹学军),DONG Yu-Ying(董玉瑛),RANG Chun-Qiu(冉春秋),et al.J.Wuhan Univ.:Nat.Sci.Ed.(武汉大学学报:理学版),2016,62(1):92-96
[13]Hu H M,Yang B J,Liu X Y,et al.Inorg.Chem.Commun., 2004,7:563-565
[14]Sheng X,Wang L,Luo Y P,et al.Nanoscale Res.Lett., 2011,6:562
[15]Abdelhady A L,Malik M A,O′Brien P.J.Mater.Chem., 2012,22(9):3781-3785
[16]Connor S T,Hsu C M,Weil B D,et al.J.Am.Chem.Soc., 2009,131(13):4962-4966
[17]Qi Y X,Liu Q C,Tang K B,et al.J.Phys.Chem.C,2009, 113:3939-3944
[18]Delgado G,Mora A J,Pineda C,et al.Mater.Res.Bull., 2001,36:2507-2517
[19]Tomic'S,Bernasconi L,Searle B G,et al.J.Phys.Chem.C, 2014,118:14478-14484
[20]Shan J N,Ju Y G.Appl.Phys.Lett.,2007,91(12):123103 [21]Jia C J,Sun L D,You L P,et al.J.Phys.Chem.B,2005, 109(8):3284-3290
[22](a)ZOU Zheng-Guang(邹正光),GAO Yao(高耀),LONG Fei (龙飞).J.Synth.Cryst.(人工晶体学报),2015,44(8):2164-2170
(b)Shi Y F,Wang Y,Wu L M.J.Phys.Chem.C,2013,117: 20054-20059
[23]Lu X,Zhuang Z,Peng Q,etal.CrystEngComm,2011,13(12): 4039-4045
[24]Fang F,Chen L,Chen Y B,et al.J.Phys.Chem.C,2010, 114:2393-2397
[25]Liu J J,Chen S F,Liu Q Z,et al.Comp.Mater.Sci.,2014, 91:159-164
Thermolysis Synthesis and Growth Mechanism of Metastable MInS2(M=Ag,Cu)Flowerlike Microsphere
WANG Yue*,1ZOU Xiao-Chuan1WANG Cun1SHIYong-Fang*,2
(1School of Biological and Chemical Engineering,Chongqing University of Education,Chongqing 400067,China)
(2Key Laboratory of Research on Chemistry and Physics of Optoelectronic Materials, Fujian Institute of Research on the Structure of Matter,Chinese Academy of Sciences,Fuzhou 350002,China)
3D metastable orthorhombic AgInS2and hexagonal CuInS2flowerlike microsphere were synthesized by the thermolysis method.The obtained products were characterized by X-ray diffraction(XRD),field-emission scanning electron microscope(FESEM),and the photocatalytic activity of AgInS2were investigated.Furthermore, the possible growth mechanism of metastable orthorhombic AgInS2and hexagonal CuInS2flowerlike microsphere was also proposed by means of thermogravimetric thermogravimetric and differential thermal analysis(TG-DTA). The results indicated that both the reaction temperature and feed ratio ofmetallic ion(nM/nIn)had an influence on the formation ofpure-phase MInS2,and the prepared AgInS2flowerlike microsphere could well degrade methylene blue(MB)under visible light irradiation.
metastable MInS2;flowerlike microsphere;thermolysis method;growth mechanism
O614.12
A
1001-4861(2016)12-2151-07
10.11862/CJIC.2016.233
2016-07-19。收修改稿日期:2016-09-17。
重庆市科委前沿与应用基础研究项目(No.cstc2013jcyjA50033,cstc2015jcyjA0317)、重庆市教委科学技术研究项目(No.KJ131512,KJ1501404)和重庆第二师范学院绿色合成与分析检测重点实验室基金(No.16xjpt08)资助。
*通信联系人。E-mail:b1083@163.com,shiyongfang@fjirsm.ac.cn
