一种新型可替宁抗原的合成
2016-12-14曾繁荣郑智彪郑曙剑廖祝元范卫永
曾繁荣,郑智彪,郑曙剑,廖祝元,范卫永
(1 江西青峰药业有限公司,江西 赣州 341000;2 杭州隆基生物技术有限公司,浙江 杭州 311121)
一种新型可替宁抗原的合成
曾繁荣,郑智彪,郑曙剑,廖祝元,范卫永
(1 江西青峰药业有限公司,江西 赣州 341000;2 杭州隆基生物技术有限公司,浙江 杭州 311121)
合成了(S)-可替宁半抗原及人工抗原,并鉴定其是否合成成功。以(S)-可替宁为起始原料,经硝化、还原和羧基化等一系列反应得到(S)-可替宁半抗原,再通过DCC法将半抗原与BSA偶联得到人工抗原;(S)-可替宁半抗原经HPLC-MS结构确认,人工抗原经紫外扫描和免疫学方法鉴定,结果表明目标半抗原及人工抗原合成成功。通过本文的合成方法可以得到活性强、免疫性强的人工抗原。
可替宁;半抗原;人工抗原;化学合成;免疫检测
(S)-可替宁,化学名为(S)-1-甲基-5-(3-吡啶基)-2-吡咯烷酮,结构式如图1所示,(S)-可替宁并非烟草中的固有成分,是烟草中的尼古丁在人体内进行初级代谢后的主要产物。进入人体内的尼古丁约80%在肝脏代谢为(S)-可替宁,另一部分以尼古丁原型存在,尼古丁原型及(S)-可替宁可随血液分布到人体各个部位。尼古丁在体内的半衰期不到30 min,而(S)-可替宁的半衰期较长为7~40 h[1],因此(S)-可替宁比尼古丁对ETS(环境烟草烟雾)更具特异性;是目前公认的评价ETS暴露的最佳生物标志[2]。

图1 (S)-可替宁结构
(S)-可替宁检测常用的方法有比色法、仪器法和免疫法。比色法是检测(S)-可替宁最简单和最廉价的方法。但由于其检出限高,不适合于ETS暴露较少人群的可替宁检测[3]。仪器法包括HPLC、GC、GC-MS等方法,虽有较高的灵敏度和精密度,但对检测样品的前处理要求高,步骤较多,另外,仪器和设备本身的昂贵,使其难以推广使用。免疫法中最常用的是酶联免疫吸附试验(ELISA)和免疫胶体层析技术,操作简便,需样量少,灵敏度高,特异性强,能够提供方便快捷的现场检测[4-5]。
为建立(S)-可替宁的免疫检测方法,必须将不具有免疫原性的(S)-可替宁小分子连接到生物大分子上形成具有免疫原性的人工抗原。本实验以(S)-可替宁为起始原料,经硝化[6]、还原和羧基化等一系列反应得到(S)-可替宁半抗原,再通过DCC法与BSA偶联得到人工抗原,合成路线如图2所示。
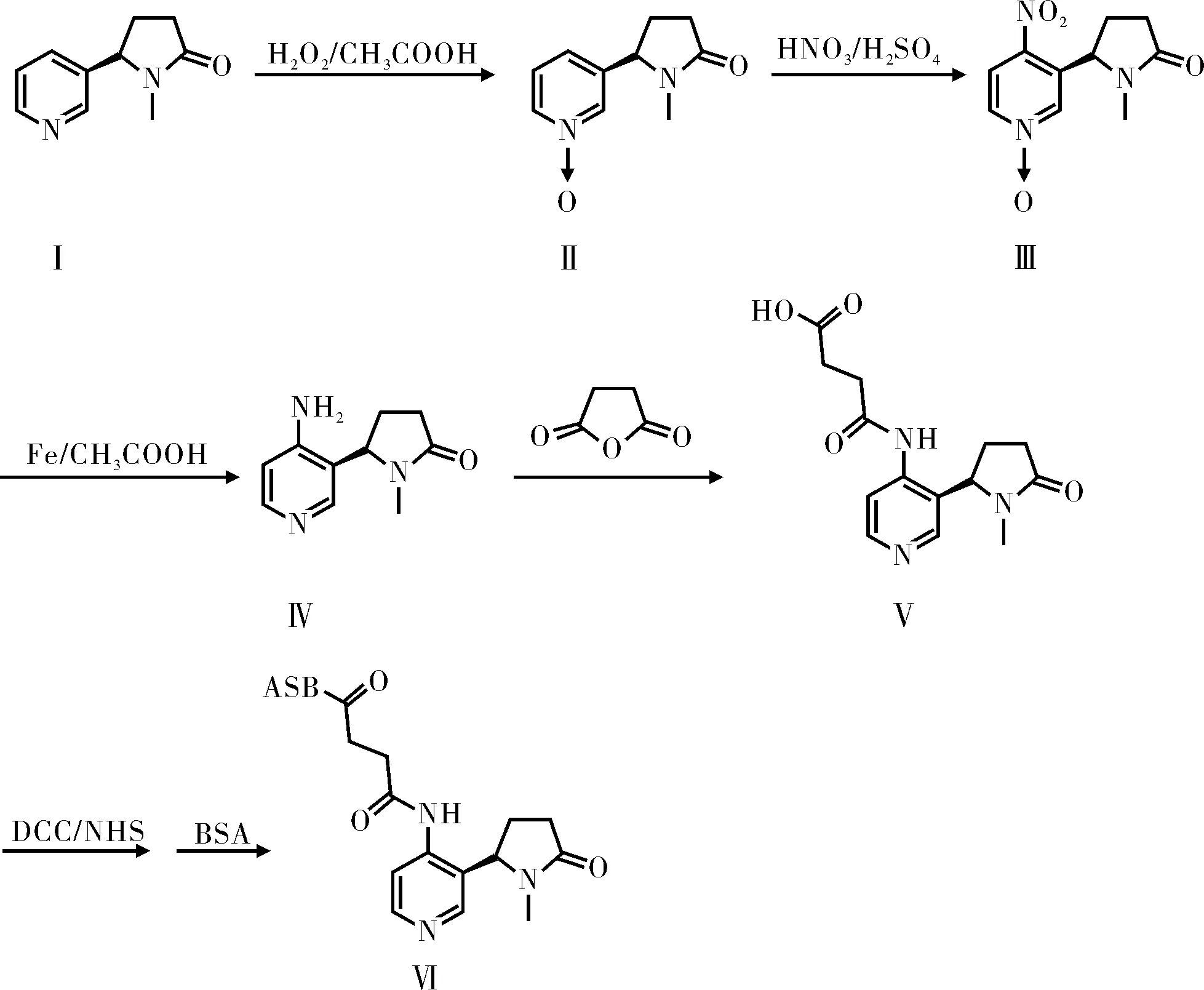
图2 可替宁人工抗原合成路线
1 实 验
1.1 仪器与试剂
Surveyor MSQ 型高效液相色谱-质谱联用仪,赛默飞世尔科技公司;U3010紫外可见分光光度计,天美(中国)科学仪器有限公司;Bio-RAD 680酶标仪,美国伯乐公司。(S)-可替宁(98%),百灵威科技;可替宁抗体(10 mg/mL),赛默飞世尔科技公司;可替宁对照抗原(10 mg/mL),赛默飞世尔科技公司;其它试剂均为市售分析纯。
1.2 抗原的合成
1.2.1 (S)-可替宁 N-氧化物Ⅱ合成
三口瓶中,1.76 g(S)-可替宁和5 mL冰乙酸加入,搅拌下,滴入1 mL 35%双氧水,70 ℃保温反应5 h,加入5 mL无水乙醇,搅拌10 min,50 ℃减压浓缩至无明显液体流出,加入20 mL水,用饱和碳酸钾溶液调成中性,分别用2×20 mL二氯甲烷萃取,有机层分别用20 mL饱和碳酸钾溶液洗涤,无水硫酸钠干燥,50 ℃减压浓缩至无明显液体流出,得1.65 g白色固体化合物Ⅱ。
1.2.2 (S)-4-硝基可替宁 N-氧化物Ⅲ合成
三口瓶中,18 mL浓硫酸和18 mL发烟硝酸加入,再慢加入1.6 g化合物Ⅱ,回流5 h后,将反应液慢倒入50 g冰水中,用饱和碳酸钾溶液慢调中性,分别用2×50 mL二氯甲烷萃取,无水硫酸钠干燥,50 ℃减压浓缩至无明显液体流出,将浓缩物用二氯甲烷重结晶得0.82 g黄色固体化合物Ⅲ。
1.2.3 (S)-4-氨基可替宁Ⅳ合成
三口瓶中,0.80 g黄色固体化合物Ⅲ和10 mL冰乙酸加入,搅拌下,2 g铁粉加入,回流5 h,热滤,滤液加入10 mL水,用10 mol/L氢氧化钠溶液调pH为12~14,过滤除去红色固体,滤液分别用2×30 mL二氯甲烷萃取,无水硫酸钠干燥,50 ℃减压浓缩至无明显液体流出,得0.48 g白色固体化合物Ⅳ。
1.2.4 (S)-可替宁半抗原Ⅴ合成
三口瓶中,0.45 g白色固体化合物Ⅳ、0.45 g丁二酸酐和5 mL吡啶加入,搅拌下,回流12 h,80 ℃减压浓缩至无明显液体流出,将浓缩物过柱得0.31 g白色固体化合物Ⅴ,即(S)-可替宁半抗原(展开剂:二氯甲烷:1,4-二氧六环:95%乙醇:25%氨水=8:1:8:1,Rf=0.5)。
1.2.5 可替宁人工抗原Ⅵ合成
单口瓶中,0.30 g白色固体化合物Ⅴ和5 mL DMF加入,搅拌溶解,再加入0.22 g DCC和0.12 g NHS,密封下室温下搅拌16 h,离心,取清液。搅拌下,将清液滴入到4 ℃的BSA溶液中(1.30 g溶于80 mL 0.01 mol/L的PBS中),4 ℃反应过夜,转入透析袋中,在0.01 mol/L PBS(pH 7.4)溶液中透析3天,早中晚各换一次透析液。透析后的反应液离心,取清液即为COT-BSA人工抗原Ⅵ。可替宁包被抗原合成方法同上(将载体蛋白由BSA替换为BGG和活化后的半抗原偶联)。
1.3 结构测试
1.3.1 (S)-可替宁半抗原的质谱鉴定
将(S)-可替宁半抗原溶于甲醇,配制1 mmol/L的甲醇溶液,用ESI-MS进行质谱鉴定。
1.3.2 可替宁人工抗原紫外光谱测试
将(S)-可替宁半抗原、BSA和COT-BSA分别配成0.01 mg/mL、0.2 mg/mL和0.2 mg/mL的溶液,在200~400 nm分别扫描其紫外吸收,根据扫描图谱进行偶联产物的鉴定。
1.3.3 (S)-可替宁人工抗原的活性测试
利用胶体金免疫层析法对可替宁人工抗原进行检测。用喷膜机以1.0 μg/cm的喷量,将人工抗原以3.0 mm的宽度喷在NC膜上,以可替宁抗体标记胶体金,结合玻璃纤维纸及吸水纸,组装成试纸条,对试纸条进行检测。
1.4 可替宁免疫原性检测
1.4.1 免疫方法
4只体重1 kg的新西兰大白兔,观察饲养一周后,各项生理指标正常。取4 mg可替宁免疫抗原(COT-BSA),加入用PBS稀释到4 mL,加入等体积的弗氏完全佐剂混合乳化至滴一滴到水中不扩散。初次免疫采取皮内多点注射与肌肉注射,分别于第15 d、第29 d、第43 d、第57 d、第64 d进行加强免疫,采用弗氏不完全佐剂,免疫抗原量保持不变。从第2次免疫开始,每次免疫7天后采少量血,分离血清用ELISA法测效价。
1.4.2 多抗血清效价检测
以COT-BGG为包被抗原,用包被稀释液稀释成1 μg/mL,在酶标上每孔包被100 μL,37 ℃孵育2 h;用酶标洗涤液洗板3次后,每孔加入封闭液200 μL,37 ℃封闭1 h;洗板4次,每孔分别加入1:200、1:400、1:800、1:1600、1:3200、1:6400、1:12800、1:25600、1:51200、1:102400、1:204800 稀释后的兔血清及空白对照PBS各100 μL,37 ℃孵育30 min;洗板4次后加入稀释后的酶标二抗100 μL,37 ℃孵育30 min;洗板4次,加入100 μL底物显色液,室温显色15 min后加入50 μL终止液终止显色;用酶标仪测定吸光度,吸收波长为450 nm。
2 结果与讨论
2.1 (S)-可替宁半抗原的质谱鉴定结果
(S)-可替宁半抗原的ESI-MS如图3所示,该化合物的[M+H]+峰为292,与(S)-可替宁半抗原的分子量291相吻合,表明是本实验所合成的半抗原。

图3 (S)-可替宁半抗原质谱图
2.2 可替宁人工抗原紫外光谱测试结果
(S)-COT半抗原、BSA和COT-BSA的紫外分光光度计的扫描结果如图4所示。
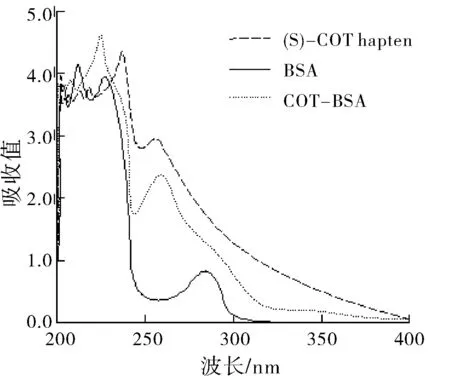
图4 (S)-COT hapten、BSA和COT-BSA的UV扫描图
从图4可以看出,(S)-COT半抗原在波长237 nm和255 nm处各有一个最大吸收峰,BSA在214 nm和285 nm处各有一个最大吸收峰;而COT-BSA与(S)-COT半抗原和BSA有明显不同,人工抗原的吸收峰在237 nm 处稍高于(S)-COT半抗原吸收值,在255 nm处明显高于BSA吸收值,根据紫外吸收的加合性可初步认为成功合成了人工抗原。
2.3 抗原活性分析
利用胶体金免疫层析法对本试验合成的抗原进行检测的结果如图5所示。
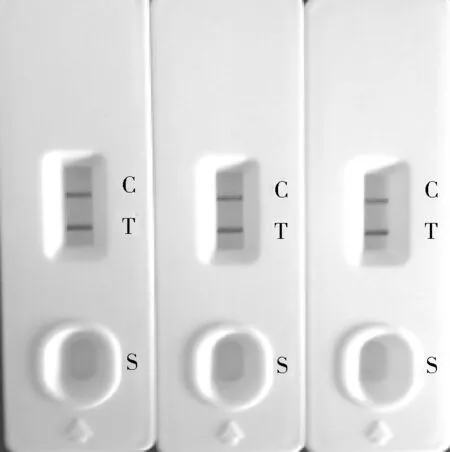
阴性检测:从左到右点膜样品依次为COT-BSA(0.5 mg/mL)、

阳性检测:从左到右待测样品浓度依次为
从图5可知,阴性检测结果表明在点膜浓度相近的情况下,新合成的人工抗原与对照抗原检测结果同相似,在检测区T线位置均有很深的紫红色且颜色深浅基本相同,证明合成的可替宁抗原活性与对照抗原活性相似,具有较高活性,能被抗体所识别并发生高效结合。阳性检测结果表明能被400 ng/mL的标准品完全抑制,从200 ng/mL和600 ng/mL的标准品对比证明可替宁标准品对合成的可替宁抗原有竞争性抑制,且有较好的梯度。
2.4 免疫过程血清效价变化结果
对用COT-BSA抗原免疫的四只兔子(分别标记为兔1,兔2,兔3,兔4)免疫的各阶段效价变化进行了测定,结果如图6所示。

图6 免疫期间血清效价变化
由图6可看出,免疫期内效价上升,四只兔在免疫期间效价变化整体趋势一致。血清效价在第30 d(第三次免疫)后迅速上升,并且兔1、兔2、兔3和兔4均在第57 d(第五次免疫)价效上升达到最大值,几天后效价基本不再上升,因此,取用COT-BSA抗原免疫兔血清,且应在第五次免疫后血清效价达到最高时采血(第五次免疫后一周),后期免疫效果基本不变。其中四只兔中兔2效价最高,免疫效果最好。
2.5 抗可替宁血清效价测定
以包被抗原常规的工作浓度1 μg/mL包被酶标板,二抗酶标记物稀释倍数1:2000,用间接ELISA法测定第五次免疫后的血清在450 nm测定的OD值,测定结果如表1所示。
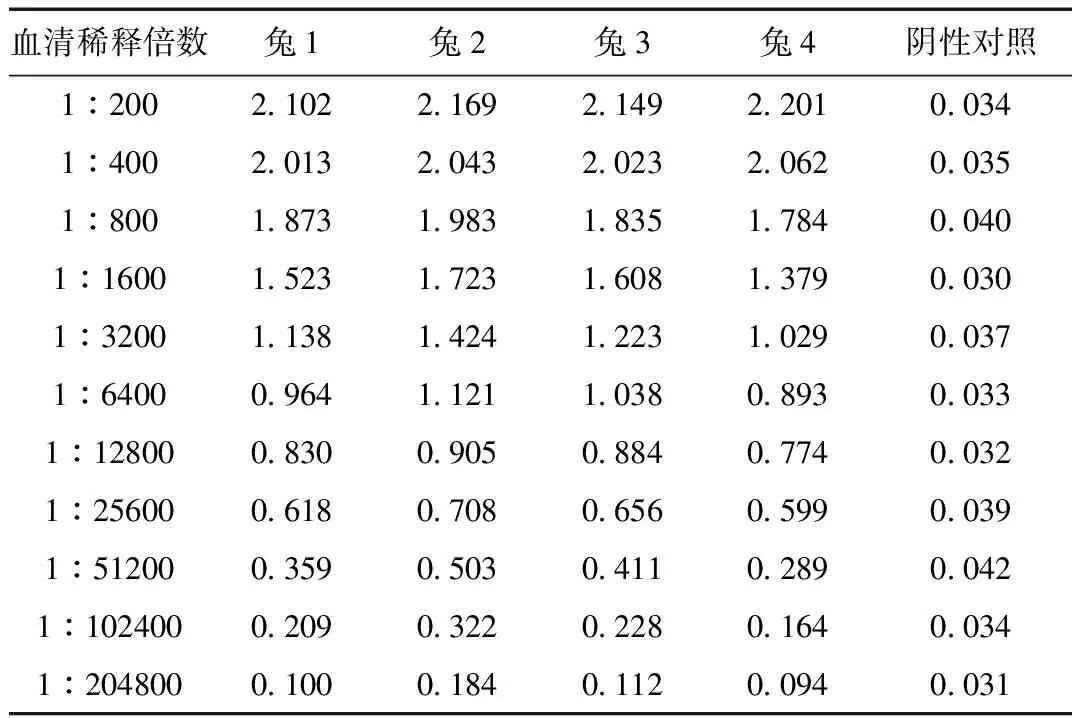
表1 第五次免疫后的血清的OD值
结果表明四只免疫兔子的兔血清效价均达到1:100000以上,表明均已产生很好的免疫效果,其中兔2效价最高能达到1:20万以上。说明该抗原具有很高的免疫原性。
3 结 论
本文可替宁半抗原的合成所选择的接入位点在吡啶环上,最大限度的保留了可替宁的结构,引入了一个氨基,并且用丁二酸酐延长了偶联臂,避免了可替宁半抗原与载体蛋白偶联时距离太近而被大分子蛋白包裹半抗原上的抗原决定簇;通过本文的合成方法能得到活性强、免疫性强的人工合成抗原,为下一步抗体的制备提供方便。
[1] John A Walling,Hsiang Yun Hu,Barbara EHasz.Haptens.tracers,immunogens and antibodies for immunoassays for cotinine derivatives[P].US5164504.
[2] 王俊,宋瑞金.人体内可替宁检测技术研究进展[J].环境与健康杂志, 2008(12):1111-1114.
[3] E Bruckert,N Jacob,L Lamaire,et al.Relationship between smoking status and serum lipids in a hyperlipidemic popuLation and analysis of possible confounding factors[J].Clinical Chemistry,1992,8(9):1698-705.[4] J W Gorrod,J Peyton.Analytical Determination of Nicotine and Related Compounds and their Metabolites[M].Amsterdam,Elsevier,1999:225-283.[5] Dhimant H Desai,Shantu Amin.Synthesis of a hapten to be used in development of immunoassays for trans-3′-hydroxycotinine,a major metabolite of cotinine[J].Chem. Res.Toxicol.,1991,4(5):524-527.[6] M Shibagaki,H Matsushita,H Kaneko,et al.The Syntheses of 4-Aminonicotine and 4-Aminocotinine[J].Heterocycles,1985,23(7):1681-1684.
Synthesis of A Novel Artificial Antigen of Cotinine
ZENGFan-rong1,ZHENGZhi-biao2,ZHENGShu-jian2,LIAOZhu-yuan1,FANWei-yong1
(1 Jiangxi Qingfeng Pharmaceutical Co., Ltd., Jiangxi Ganzhou 341000; 2 Hangzhou Clongene Biotech Co., Ltd., Zhejiang Hangzhou 311121, China)
To synthesize and identify the hapten and artificial antigen of cotinine, the hapten of (S)-cotinine was synthesized from (S)-cotinine through a series of reactions including nitration, reduction and carboxylation, etc. The (S)-cotinine hapten was coupled with BSA by means of DCC method. The structure of (S)-cotinine hapten was confirmed by HPLC-MS.The artificial antigen of cotinine was identified by UV spectroscopy and immunological analysis. The results indicated that the hapten and artificial antigens were prepared successfully. High activity and strong immunogenicity artificial antigen of cotinine can be obtained through the synthesis method.
cotinine; hapten; artificial antigen; chemical synthesis; immunoassay
曾繁荣,男,硕士研究生,主要从事药物合成和应用。
郑智彪,男,生物技术本科生,主要从事抗原合成与检测。
R285.5
A
1001-9677(2016)022-0053-04
