沙利度胺联合放化疗对小细胞肺癌患者生存质量及耐受性的影响
2016-10-18张静康红刚王宝中
张静 康红刚 王宝中
聊城市人民医院肿瘤科,山东聊城252000
沙利度胺联合放化疗对小细胞肺癌患者生存质量及耐受性的影响
张静#康红刚王宝中
聊城市人民医院肿瘤科,山东聊城252000
目的评价沙利度胺联合放化疗治疗对小细胞肺癌患者的生存质量及耐受性的影响。方法将67例局部晚期小细胞肺癌(SCLC)患者分为研究组和对照组。研究组35例采用放化疗联合口服沙利度胺,对照组32例仅接受常规放化疗,比较两组患者的疗效、不良反应及生存质量指标。结果研究组和对照组的客观有效率比较,差异无统计学意义(P=0.615)。两组患者治疗前后KPS评分、体质量的改善情况比较,差异有统计学意义(P<0.05),而PS评分比较,差异无统计学意义(P=0.222)。研究组患者放化疗期间恶心、呕吐发生率较对照组低,便秘、头晕发生率较对照组高,差异有统计学意义(P<0.05)。结论沙利度胺联合放化疗治疗小细胞肺癌可改善患者的生存质量,提高对放化疗的顺应性,值得进一步研究。
小细胞肺癌;沙利度胺;放化疗;生活质量;不良反应
Oncol Prog,2016,14(6)
小细胞肺癌(small cell lung carcinoma,SCLC)是肺癌中常见的一种类型,约占肺癌患者总数的20%,在我国的发病率处于较高水平。小细胞肺癌的恶性程度高,虽然初期治疗缓解率高,但很快出现复发转移,且转移范围广泛。目前我国治疗水平较低,局限期患者中位生存期约23个月,广泛期患者中位生存期为7~10个月。近年来抗血管生成药物在非小细胞肺癌(non-small cell lung carcinoma,NSCLC)中取得较好的效果[1]。如贝伐单抗延长了NSCLC患者的生存期[2],但很少有关抗血管生成药物治疗SCLC的报道。抗血管生成药物价格昂贵,对于普通患者长期应用,是沉重的经济负担。沙利度胺经证实有抗血管生成,提高患者免疫力的口服药物,价格便宜,易于被普通患者接受。本研究采用口服沙利度胺联合化放疗治疗SCLC患者,观察患者对其耐受性及生活质量的变化情况,现报道如下。
1 资料与方法
1.1一般资料
选取2012年3月至2014年3月在聊城市人民医院进行治疗的67例局限期SCLC患者。入组标准:①全部病例均经病理及影像学证实为局限期SCLC,至少有一个影像学可测量指标;②患者功能状态评分(Karnofsky,KPS)≥70分;③患者体力状况评分(performance status,PS)≤2分;④血常规、肝肾功、心电图、心脏彩超等检查未提示有明显异常;⑤年龄<70岁;⑥预计生存期≥6个月。排除标准:①为广泛期SCLC;②患者治疗依从性差,认知障碍;③合并血栓、恶病质及心脑血管等基础疾病;④既往对沙利度胺有过敏史。将采用同期放化疗联合沙利度胺口服的35例患者设为研究组,将仅接受常规同期放化疗的32例患者设为对照组,两组临床基本资料比较,差异无统计学意义(P>0.05)。(表1)
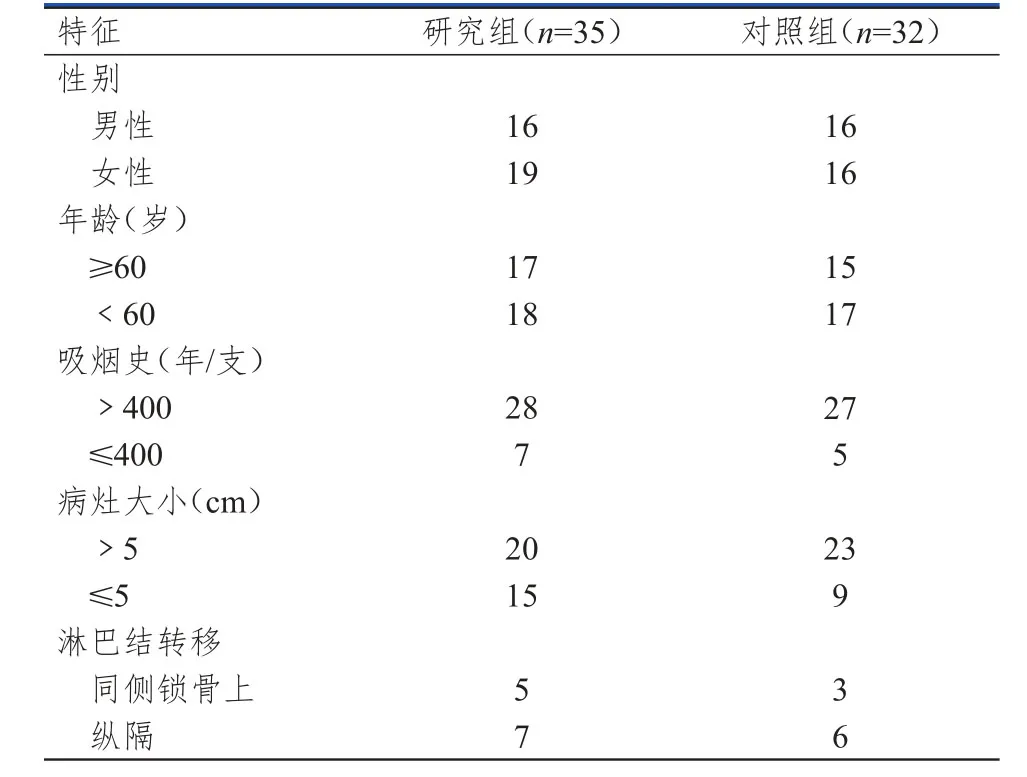
表1 两组患者临床基本资料
1.2治疗方案
研究组35例采用同期放化疗联合沙利度胺口服,对照组32例仅接受常规同期放化疗,两组放疗计划及化疗方案均相同。具体如下:①放射治疗,CT模拟定位机行模拟定位,扫描图像通过局域网络传输至三维治疗计划系统进行三维图像重建。用直线加速器6MV-X线照射,放疗5~6周,每周5次,每日1次,2 Gy/次,总放疗中位剂量为50~60 Gy。②化疗方案:第1~4天顺铂30 mg,第1~5天依托泊苷l00 mg,每3周为一个周期,共完成4~6个周期化疗。化疗过程中给予5-HT3受体拮抗剂、质子泵抑制剂、氯丙嗪、甲氧氯普胺等止吐;化疗前及化疗结束后第2天、第7天检测血常规、肝肾功、出凝血机制。③沙利度胺给药方法,研究组患者自放化疗第1天起每晚口服沙利度胺100 mg,第2周开始增加至每晚200 mg,维持至疗效评价。
1.3评价标准
1.3.1疗效评估患者放化疗结束后4周进行疗效评价,采用RECIST实体瘤评价标准,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)。
1.3.2生活质量①睡眠质量评估:根据国际通用的SPIEGEL睡眠量表[3]规定的6项内容(入睡时间、总睡眠时间、夜醒次数、睡眠深度、做梦情况、醒后感觉),分别对两组患者治疗前后进行睡眠量表评分。②KPS评分标准:治疗后的KPS评分增加或减少10分以上为改善或恶化,上下波动低于10分为稳定。③体质量变化评价标准:体质量增加或减少5%及以上为好转或恶化,波动小于5%为稳定。④PS评分标准:治疗后的PS评分增加或减少1分以上为恶化或改善,上下波动低于1分为稳定。
1.3.3放化疗不良反应评定标准按照“WHO化疗不良反应评价标准”及“美国放射治疗肿瘤协作组急性放射损伤分级标准”进行评价[4]。
1.4统计学方法
应用SPSS19.0统计软件进行统计学分析。-计数资料采用χ2检验,计量资料以均数±标准差(±s)表示,采用t检验。P<0.05为差异有统计学意义。
2 结果
2.1两组患者近期疗效比较
所有患者均化疗至少4个周期,研究组有3例因嗜睡沙利度胺减量。研究组总有效率为88.58%(31/35),与对照组的84.38%(27/32)比较,差异无统计学意义(χ2=0.253,P=0.615)。(表2)
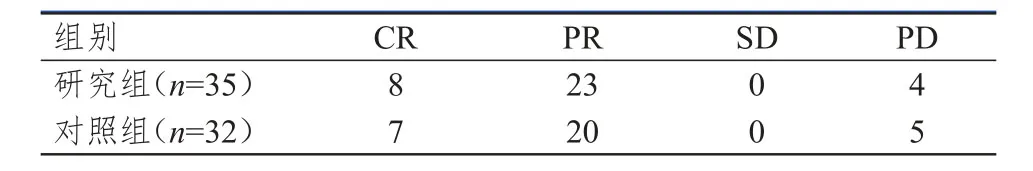
表2 两组患者近期疗效
2.2两组患者生活质量变化的比较
经过4~6周期化疗及放疗后,研究组患者的睡眠量表评分,与治疗前比较,差异无统计学意义(P=0.856);而对照组治疗后睡眠量表评分,低于治疗前,差异有统计学意义(P=0.015),详见表3。治疗后研究组KPS评分及体质量变化情况均优于对照组,差异有统计学意义(P<0.05)PS评分比较,差异无统计学意义(P=0.222),详见表4。
表3 两组患者治疗前后SPIEGEL睡眠量表评分比较(分,±s)
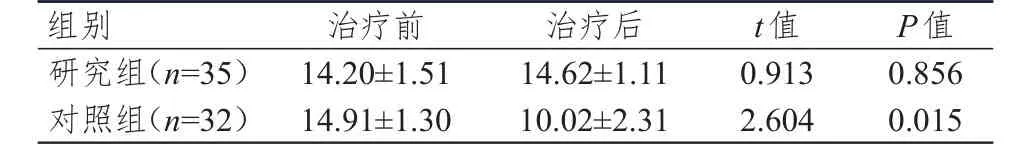
表3 两组患者治疗前后SPIEGEL睡眠量表评分比较(分,±s)
组别研究组(n=35)对照组(n=32)治疗前14.20±1.51 14.91±1.30治疗后14.62±1.11 10.02±2.31 t值0.913 2.604 P值0.856 0.015
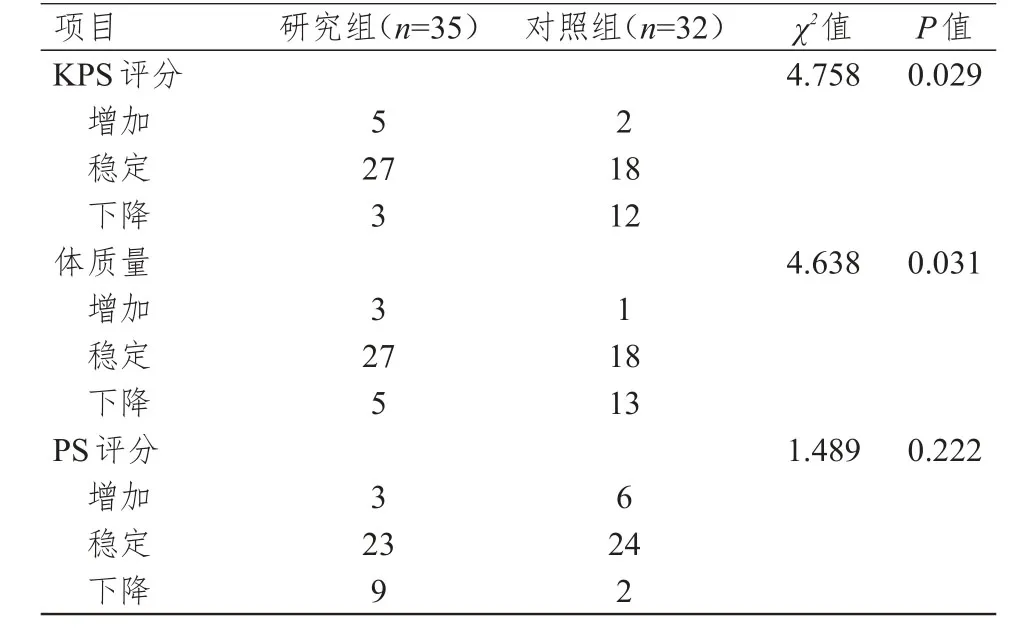
表4 两组患者KPS评分、PS评分及体质量变化情况比较
2.3两组患者不良反应发生情况比较
研究组患者放化疗期间恶心、呕吐发生率低于对照组,头昏、嗜睡、便秘发生率高于对照组,差异有统计学意义(P<0.05);血栓形成及栓塞情况在本研究中未发现。两组患者其他不良反应如放射性皮炎、放射性肺炎、骨髓抑制等比较,差异无统计学意义(P>0.05)。(表5)

表5 两组患者不良反应发生率比较[n(%)]
3 讨论
小细胞肺癌生长迅速,恶性程度高,生存期短,早期发现患者不足10%,虽然对放化疗敏感,但易出现继发性耐药而导致复发转移率高。同步放化疗虽然是目前国际对于局部晚期肿瘤的标准治疗方案,但我国患者耐受性较差。国外有研究显示早期加入放疗未改善总生存期,故本研究采用序贯/交替化放疗[5]。
20世纪70年代“肿瘤血管新生学说”的创始人Folkman[6]提出了“肿瘤组织生长、转移,必须依靠新生血管生成来提供足够的氧气和营养物质来维持”,以此为基础,抗血管生成治疗成为肿瘤治疗的主要研究方向。血管内皮生长因子(human vascular endothelial growth factor,VEGF)是最有效的促血管生长因子,以VEGF及其受体VEGFR为靶点的治疗是癌症药物治疗的热点。贝伐单抗是一种重组的人源化单克隆抗体,是美国第一个获得批准上市的抑制肿瘤血管生成的药物,体内、体外检测证实,它可选择性地与VEGF结合,并阻断其生物活性,从而抑制血管内皮细胞增殖和新生血管形成,达到抗肿瘤目的。国外贝伐单抗联合化疗在非小细胞肺癌的临床研究中延长了患者的生存期[2]。国内血管内皮抑素(恩度)联合化疗治疗NSCLC能明显提高初、复治者的临床受益率、疾病进展时间及生存时间[1]。虽然抗血管生成治疗取得了较好的效果,但由于价格昂贵,基于目前国内经济状况,尤其是地方医院很多患者难以接受。
沙利度胺已被证实具有抗肿瘤作用且价格便宜,易于接受。主要机制包括抑制血管生成,调节T淋巴细胞功能,诱导肿瘤细胞凋亡,抑制核转录因子,调节血管内皮细胞黏附分子表达等[7]。在肝癌[8-9]、非小细胞肺癌[10-11]、结肠癌[12]、食管癌[4]患者中进行的临床试验证实,联合沙利度胺可以改善患者生存质量,不良反应可以耐受,并在一定程度上改善了生存。基于国内外研究,沙利度胺可以改善生存质量且耐受性良好。本研究结果表明抗血管生成药物沙利度胺联合放化疗在局部晚期小细胞肺癌治疗过程中的安全性良好,患者生存质量得到改善,但未见疗效提高,可能与小细胞肺癌初期治疗疗效普遍较好及患者随访时间短有关。
本研究发现治疗过程中沙利度胺联合放化疗患者恶心呕吐的发生率较仅放化疗患者少,可能因其具有止吐作用,降低了化疗药物所致的恶心呕吐有关。而沙利度胺常见的不良反应如嗜睡、便秘发生率增加,但未出现血栓栓塞情况。在国外一些关于沙利度胺的临床试验中增加了血栓栓塞的风险[10],但未提高相关死亡率,为避免血栓栓塞事件发生,本研究增加预防血栓栓塞知识宣教及每周复查出凝血机制了解凝血状况。本研究发现研究组患者睡眠、KPS评分及体质量变化情况较对照组稳定,可能与沙利度胺增加患者食欲,改善睡眠的作用有关。虽然提高嗜睡、乏力的发生率,但患者的生活质量得到保证,治疗耐受性进一步提高。本研究为沙利度胺联合放化疗的初步研究,由于病例数较少且随访时间较短未进行生存时间相关研究,所以需要延长随访时间,且对于KPS评分高、PS≤1分的患者能否延长生存,延缓疾病进展是进一步研究的课题。
[1]王金万,孙燕,刘永煜,等.重组人血管内皮抑素联合NP方案治疗晚期NSCLC随机、双盲、对照、多中心Ⅲ期临床研究[J].中国肺癌杂志,2005,8(4):283-290.
[2]Tsai CM,Au JS,Chang GC,et al.Safty and efficacy of first line bevacizumad with chemotherapy in Asian patients with advanced nonsquamous NSCLC:results from the phase IV MO19390(sail)study[J].J Thorac Oncol,2011,6(6):1092-1097.
[3]潘集阳.睡眠障碍临床诊疗[M].广州:华南理工大学出版社,2001:282-287.
[4]佘明金,马祖胜,李桂芝,等.同步放化疗联合沙利度胺治疗中晚期食管癌的临床随机对照研究[J].中国肿瘤临床,2010,37(15):882-886.
[5]Sun JM,Ahn YC,Choi EK,et al.Phase III trial of concurrent thoracic radiotherapy with either first-or third-cycle chemotherapy for limited-disease small-cell lung cancer[J]. Ann Oncol,2013,24(8):2088-2092.
[6]Folkman J.Role of angiogenesis in tumor growth and metastasis[J].Semin Oncol,2002,29(6 Suppl 16):15-18.
[7]潘骥群,鲁光平,于志坚.沙利度胺抗肿瘤的研究进展[J].中华肿瘤防治杂志,2012,19(7):552-555.
[8]Chen YY,Yen HH,Chou KC,et al.Thalidomide-based multidisciplinary treatment for patients with advanced hepatocellular carcinoma:a retrospective analysis[J].World J Gastroenterol,2012,18(5):466-471.
[9]Shao YY,Lin ZZ,Hsu C,et al.Efficacy,safety,and potential biomarkers of thalidomide plus metronomic chemotherapy for advanced hepatocellular carcinoma[J].Oncology,2012,82(1):59-66.
[10]Hoang T,Dahlberg SE,Schiller JH,et al.Randomizedphase III study of thoracic radiation in combination with paclitaxel and carboplatin with or without thalidomide in patients with stage III non-small-cell lung cancer:the ECOG 3598 study[J].J Clin Oncol,2012,30(6):616-622.
[11]Young RJ,Tin AW,Brown NJ,et al.Analysis of circulating angiogenic biomarkers from patients in two phase III trials in lung cancer of chemotherapy alone or chemotherapy and thalidomide[J].Br J Cancer,2012,106(6):1153-1159.
[12]Lv J,Liu N,Liu KW,et al.A randomised controlled phase II trial of the combination of XELOX with thalidomide for the first-line treatment of metastatic colorectal cancer[J].Cancer Bio Med,2012,9(2):111-114.
The effect of thalidomide combined with chemoradiotherapy on the quality of life and tolerance of SCLC patients
ZHANG Jing#KANG Hong-gang WANG Bao-zhong
Department of Oncology,Liaocheng People’s Hospital,Liaocheng 252000,Shandong,China
ObjectiveTo investigate the impact of chemoradiotherapy plus thalidomide on the quality of life and tolerance in patients with small cell lung cancer(SCLC).MethodA total of 67 patients were enrolled in the study,with 35 cases received chemoradiotherapy+thalidomide(study group),and other 32 cases had chemoradiotherapy alone(control group).Endpoints including tumor response rate,toxicity,and quality of life were evaluated.ResultThe objective response rate was similar in both groups(P=0.615),while the KPS scores and body mass in the two groups before and after treatment were significantly different(P<0.05),and PS scores were comparable(P=0.222).Nausea and vomiting were less,while constipation and dizziness were more in study group compared with control group(P<0.05).ConclusionThalidomide in combination with chemoradiotherapy is effective in improving the quality of life in patients with SCLC,ameliorating the treatment compliance,which is clinically applicable.
small cell lung carcinoma;thalidomide;chemoradiotherapy;quality of life;adverse reactions
R734.2
A
10.11877/j.issn.1672-1535.2016.14.06.15
2015-11-05)
(corresponding author),邮箱:sdzhangji83@126.com
