地佐辛复合舒芬太尼用于剖宫产术后的镇痛效果观察
2016-10-17汪力新
汪力新
河南漯河市中心医院麻醉科 漯河 462000
地佐辛复合舒芬太尼用于剖宫产术后的镇痛效果观察
汪力新
河南漯河市中心医院麻醉科漯河462000
目的观察地佐辛复合舒芬太尼用于剖宫产术后的镇痛效果。方法将腰-硬膜外联合阻滞(ECSA)麻醉的72例足月单胎择期剖宫产的产妇随机分为2组,每组36例,术后均采用PCEA。S组镇痛泵药液为舒芬太尼2 μg/kg+托烷司琼4 mg+0.9%氯化钠注射液。DS组为地佐辛0.3 mg/kg+舒芬太尼1μg/kg+左旋布比卡因3 mg/kg。2组药液均用生理盐水稀释至100 mL。观察并记录2组患者术后2 h、12 h、24 g、48 h的疼痛评分及术后镇痛期间恶心呕吐、呼吸抑制、尿储留等不良反应情况。结果2组术后疼痛评分差异无统计学意义(P>0.05),但DS组不良反应发生率明显低于S组(P<0.05)。结论地佐辛复合舒芬太尼应用于剖宫产术后镇痛,效果良好,不良反应少。
地佐辛;舒芬太尼;镇痛效果;泌乳素
2014-01—2016-03间,我们对经腰-硬膜外联合阻滞(ECSA)麻醉的72例足月单胎择期剖宫产的产妇,分别采用舒芬太尼和地佐辛复合舒芬太尼实施术后自控镇痛泵镇痛,并比较不用用药方法的镇痛效果和不良反应发生情况,现报道如下。
1 资料与方法
1.1一般资料本组72例产妇,年龄23~34岁,孕周37~41周,体质量60~81 kg,均为足月单胎初产妇。ASA分级Ⅰ~Ⅱ级,无心、肺疾病和严重肝肾功能异常及凝血功能障碍等。无合并妊高征及胎儿窘迫等病理妊娠患者,无麻醉药过敏史及成瘾史。随机分为地佐辛组(D组)和地佐辛复合舒芬太尼组(DS组),每组36例。均经院医学伦理委员会通过且本人及家属自愿签署知情同意书。2组产妇的年龄、孕周、体质量等一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2方法产妇宫口开大2~3 cm后,采用腰硬联合麻醉,穿刺部位选择L2-3或L3-4间隙。药物选用布比卡因重比重10~12 mg。麻醉平面控制在T6以下。剖宫产结束后即接上自控镇痛泵。S组术后镇痛泵配方:舒芬太尼2 μg/kg+托烷司琼4 mg+0.9%氯化钠注射液至100 mL。DS组:地佐辛0.4 mg/kg+舒芬太尼1 μg/kg+托烷司琼4 mg+0.9%氯化钠注射液至100 mL。参数设定:持续输注量2 mL/h,单次按压剂量0.5 mL,锁定时间15~30 min。
1.3观察项目观察组产妇在术后第2 h、12 h、24 h及48 h时的镇痛效果及不良反应发生率。镇痛效果采用视觉模拟评分法(VAS)记录,按照疼痛程度设为0~10分。镇痛效果好:0~3分。镇痛效果可:3~5分。镇痛效果差:6~10分。

2 结果
2.12组术后不同观察时间点VAS评分情况2组产妇均顺利完成手术,2组术后不同观察时间点VAS评分差异无统计学意义(P>0.05),见表1。

表1 2组术后不同观察时间点VAS评分情况±s)
2.22组术后不良反应发生情况S组术后不良反应发生率(30.56%)高于DS组(13.89%),2组差异有统计学意义(P<0.05),见表2
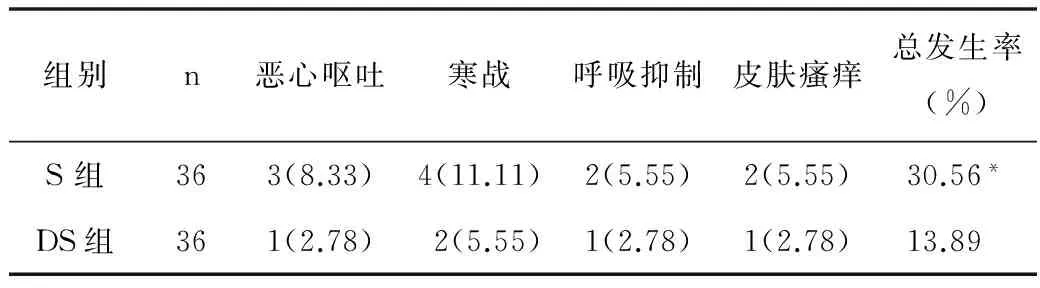
表2 2组术后发生不良反应情况比较[n(%)]
注:*P<0.05
3 讨论
CSEA兼有腰麻起效快,作用完善,肌松良好的特点,又有连续硬膜外阻滞的作用,时间灵活、用药可控性强、生理干扰轻的特点。良好的术后镇痛能显著提高产妇的舒适度和改善其泌乳状况。舒芬太尼是一种特异性u-阿片受体激动剂,对u-受体的亲和力比芬太尼强7~10倍,用于术后镇痛起效快,镇痛效果强,持续时间长,是目前PCIA较为理想的镇痛药。但大剂量舒芬太尼可引起呼吸抑制,且恶心、呕吐等发生率比较高[2]。如何在取得良好镇痛效果的同时降低不良反应的发生率,成为静脉自控镇痛的临床研究的重点。地佐辛是阿片受体混合激动-拮抗剂,对激动κ受体而产生强镇痛作用,并对μ受体有部分激动作用。同时还产生一定程度的拮抗作用,故在应用过程中呼吸抑制、恶心呕吐等不良反应会减少。我们对36例剖宫产产妇实施地佐辛复合舒芬太尼术后自控镇痛泵镇痛,与单一应用舒芬太尼自控镇痛泵镇痛比较,在减少阿片类药物用量的基础上,仍能保证良好的镇痛效果,而且不良反应更少,与闫诺等[3]报告结果基本一致。
[1]卢静, 兰志勋, 蔡兵,等. 地佐辛联合舒芬太尼用于剖宫产术后自控静脉镇痛效果观察[J]. 四川医学, 2013, 34(10):1 507-1 509.
[2]徐建国. 成人术后疼痛治疗进展[J].临床麻醉学杂志,2011,27(3):299-301.
[3]闫诺,杨程,陈宁.地佐辛联合舒芬太尼用于术后自控静脉镇痛效果观察[J].海南医学院报,2011,17(3):403.
(收稿2016-04-10)
R614.2
B
1077-8991(2016)06-0102-02
