菊花破壁饮片的HPLC指纹图谱研究△
2016-09-25刘星云王慧玲彭丽华成金乐
刘星云,王慧玲,彭丽华,成金乐*
(1.广州中医药大学 中药资源科学与工程研究中心,岭南中药资源教育部重点实验室,广东 广州 510006;2.国家中医药管理局 中药破壁饮片技术与应用重点研究室,广东 中山 528437;3.中山市中智药业集团有限公司,广东 中山 528437)
菊花破壁饮片的HPLC指纹图谱研究△
刘星云1,2,3,王慧玲2,3,彭丽华2,3,成金乐1,2,3*
(1.广州中医药大学 中药资源科学与工程研究中心,岭南中药资源教育部重点实验室,广东 广州 510006;2.国家中医药管理局 中药破壁饮片技术与应用重点研究室,广东 中山 528437;3.中山市中智药业集团有限公司,广东 中山 528437)
目的:建立菊花破壁饮片HPLC指纹图谱,并分析破壁饮片成品与其中间品、原料的化学成分相关性,为菊花破壁饮片整体质量评价提供依据。方法:采用高效液相色谱法,十八烷基硅烷键合硅胶为填充剂的色谱柱(250 mm×4.6 mm,5 μm),以乙腈-0.5%磷酸溶液为流动相进行梯度洗脱,检测波长:348 nm,柱温:35 ℃。结果:建立了菊花破壁饮片的HPLC指纹图谱,得到了15个共有特征峰,11批样品的相似度达0.98以上,方法学考察结果符合指纹图谱技术要求。结论:所建立的方法稳定、可靠、重复性好,可用于菊花破壁饮片质量控制和综合评价。
菊花;破壁饮片;指纹图谱;HPLC
菊花来源于菊科植物菊ChrysanthemummorifoliumRamat.的干燥头状花序,具有散风清热、平肝明目、清热解毒的功能。该药材按产地和加工方法不同,分为“滁菊”、“亳菊”、“贡菊”、“杭菊”等品种[1]。菊花破壁饮片是将符合《中华人民共和国药典》要求的杭白菊粉碎至D90<45 μm的粉体,不添加成型剂制成的30~100目的干燥颗粒状饮片,可直接冲泡服用。与传统饮片相比,菊花破壁饮片具有全成分保留,成分利用率高,质量均一,应用方式简单、快捷和灵活等特点[2]。由于外观性状及显微特征均被破坏,传统饮片的质量评价标准已不能满足菊花破壁饮片质量控制要求,而基于整体化学表征基础上的中药HPLC指纹图谱能反映中药组分全貌,能对破壁饮片的内在质量进行综合评价[3],所以课题组对菊花破壁饮片首次开展HPLC指纹图谱研究。为进一步考察破壁饮片制备过程对菊花传统饮片中化学成分的影响,本课题组还比较、分析了菊花破壁饮片(成品)-菊花破壁粉体(中间品)-菊花传统饮片(原料)三者的相关性。
1 仪器与试药
1.1 仪器
安捷伦1200RRLC快速液相色谱仪(配有G1315C型号DAD检测器、G4218A的ELSD检测器、G1312B二元泵、G1329B自动进样器、G1322A脱气机、G1316B柱温箱,Agilent ChemStation色谱工作站);明澈TM-D24UV纯水系统,KQ-400KOE型超声波清洗器(昆山市超声仪器有限公司);电热恒温水浴锅DK-S24(上海森信实验仪器有限公司);万分之一电子天平AB204-S(METTLER TOLEOD)、十万分之一电子天平AUW220D(岛津公司)。
1.2 试药和试剂
菊花破壁饮片共10批(批号分别为S1:021311501;S2:0212092701;S3:20131002;S4:20130903;S5:20130902;S6:20130901;S7:20130802;S8:20130801;S9:20120902;S10:20120901;S11:20120701);杭白菊3批(批号分别为Ⅰ:0212092701;Ⅱ:0213011501;Ⅲ:20131201),均由中山市中智药业集团有限公司提供,经中山市中智药业集团有限公司贾世清中药师鉴定为ChrysanthemummorifoliumRamat.的干燥头状花序,凭证标本保存于广州中医药大学。将3批杭白菊(批号:0212092701,0213011501,20131201)分别按照法定炮制工艺制成相对应批次的菊花传统饮片、菊花破壁粉体和菊花破壁饮片(均由中山市中智药业集团有限公司制备)。
绿原酸对照品(批号:110753-201314)、异绿原酸A对照品(批号:111782-201204),木犀草苷对照品(批号:111720-200905),均购于中国食品药品检定研究院;色谱甲醇(瑞典Oceanpak公司),色谱乙腈(安徽时联特种溶剂有限公司),其余试剂为分析纯。
2 方法与结果
2.1 色谱条件
以十八烷基硅烷键合硅胶为填充剂的色谱柱(250 mm×4.6mm,5 μm);流动相为乙腈(A)-0.5%磷酸溶液(B),梯度洗脱程序见表1;柱温:35 ℃;检测波长:348 nm;流速:0.6 mL·min-1。
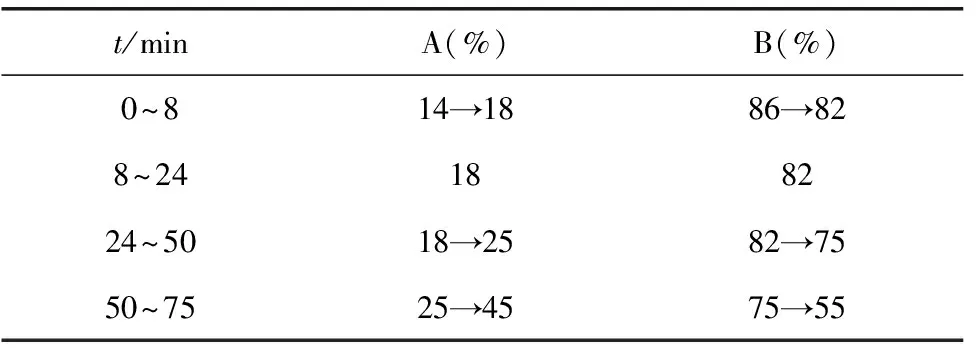
表1 流动相梯度洗脱程序
2.2 供试品溶液的制备
取菊花破壁饮片约0.25 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,称定重量,超声提取40 min(功率320 W,频率4200 Hz),放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.3对照品溶液的制备
精密称取绿原酸、木犀草苷、异绿原酸A对照品适量,加70%甲醇溶解配成质量浓度分别为0.173、0.152、0.249 mg·mL-1的混合对照品溶液。
2.4 方法学考察
2.4.1 专属性试验 精密吸取空白溶剂(甲醇)10 μL注入液相色谱仪,按照2.1项下色谱条件进行测定,在相应保留时间处无色谱峰,表明甲醇对测定结果无干扰。
2.4.2 精密度试验 取菊花破壁饮片(批号:20131002)样品,按2.2项下方法制备供试品溶液,连续进样6次,按2.1项下色谱条件进行测定,记录图谱。经计算,6次进样谱图的相似度达0.999以上,共有峰相对峰面积的RSD<3.4%,表明仪器精密度良好。
2.4.3 重复性试验 取同一批次菊花破壁饮片(批号:20131002)样品6份,精密称定,按2.2项下方法分别制备供试品溶液6份,按2.1项下色谱条件进行测定,记录图谱。6份样品所得指纹图谱的相似度均高于0.999;各主要色谱峰的峰面积RSD<2.0%,表明本方法的重复性符合指纹图谱控制技术的要求。
2.4.4 稳定性试验 取菊花破壁饮片(批号:20131002)样品,精密称定,按2.2项下方法制备供试品溶液。分别于0、3、6、9、12、16、24 h测定,计算24 h内各主要色谱峰峰面积RSD及所得图谱的相似度。结果7张谱图的相似度达0.999以上,主要色谱峰峰面积RSD<3.0%,说明该样品在24 h内性质稳定。
2.5 指纹图谱的建立
2.5.1 指纹图谱采集 取11批次菊花破壁饮片,分别按2.2项下方法制备供试品溶液,取供试品溶液20 μL及对照品溶液5 μL,按2.1项下色谱条件进行分析,以6号峰(异绿原酸A)为参照峰,计算各批菊花破壁饮片指纹图谱中的相对保留时间和相对峰面积。结果见表2和表3。

表2 11批菊花破壁饮片共有指纹图谱共有峰的相对保留时间(n=11)

表3 11批菊花破壁饮片共有指纹图谱共有峰的相对峰面积(n=11)
2.5.2 共有模式的建立及相似度的测定 将11批菊花破壁饮片样品的指纹图谱导入 《中智药业集团中药指纹图谱数据库软件》(中智药业集团与中南大学合作开发),结果见图1,以中位数法生成菊花破壁饮片指纹图谱共有模式,共标定15个共有峰,并将共有模式的保留时间与对照品进行比对,指认出1号峰为绿原酸,3号峰为木犀草苷,6号峰为异绿原酸A,结果见图2和图3。6号峰高度适中,分离度好,保留时间适中,可作为参照峰。以共有模式为对照图谱,测得样品与对照指纹图谱之间的相似度,结果见表4。由表可知相似度均在0.984以上,说明各批次间菊花破壁饮片质量均一、稳定。
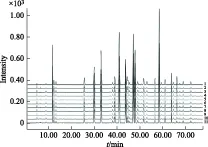
图1 11批菊花破壁饮片指纹图谱图

图2 菊花破壁饮片指纹图谱共有模式
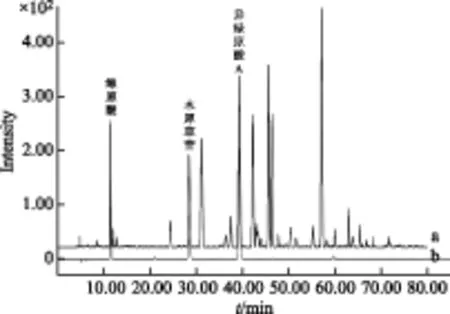
图3 菊花破壁饮片混合对照品溶液(a)和共有模式(b)的HPLC对比图

表4 11批菊花破壁饮片指纹图谱的相似度
3 菊花破壁饮片(成品)-破壁粉体(中间体)-传统饮片(原料)的相关性分析
本研究收集3批菊花传统饮片及其对应批次的破壁粉体和破壁饮片,按2.2项下方法制备供试品溶液,2.1项下色谱条件进行分析,记录图谱中样品的相对保留时间和相对峰面积,菊花传统饮片、破壁粉体和破壁饮片的指纹图谱见图4。分别分析各批次的原料-中间品-成品之间的相似度,结果见表5。分析可知,同批次样品的原料、破壁粉体及破壁饮片之间相似度在0.990以上,表明菊花传统饮片经超微粉碎再制成破壁饮片的工艺流程中有效成分基本没有改变,各主要成分相关性良好。

注:Ⅰ1、Ⅰ2、Ⅰ3依次表示批号为20131201的传统饮片、破壁粉体、破壁饮片;Ⅱ1、Ⅱ2、Ⅱ3依次表示批号为0213011501的传统饮片、破壁粉体、破壁饮片;Ⅲ1、Ⅲ2、Ⅲ3依次表示批号为0212092701的传统饮片、破壁粉体、破壁饮片。图4 菊花破壁饮片原料-中间品-成品的指纹图谱
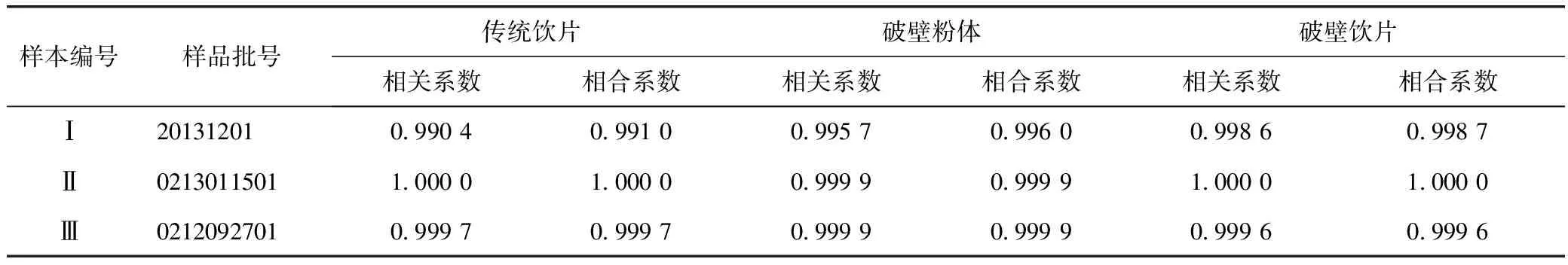
表5 各批次菊花破壁饮片的原料-中间品-成品间相关性分析(n=3)
4 讨论
在选择检测波长过程中,采用二极管阵列检测器对菊花样品进行全波长扫描,由三维谱图得出,在348 nm处样品出峰数量多,峰分布均匀且基线平稳,反应信息量较大,故选取348 nm作为指纹图谱最佳检测波长。同时在有关文献的基础上[4-8],考察不同流动相(乙腈-水,乙腈-0.5%磷酸溶液,乙腈-0.3%磷酸溶液,乙腈-0.1%磷酸溶液),选择乙腈-0.5%磷酸溶液作为流动相并对洗脱梯度进行优化,以达到较好的峰形及分离效果。同时比较了不同流速(0.6、0.8、1.0、1.2 mL·min-1)、不同柱温(25、30、35 ℃)、不同色谱柱[Agilent ZORBAX SB-C18(250 mm×4.6 mm,5 μm),Waters Symmetry C18(250 mm× 4.6 mm,5 μm),Phenomenex Synergi 4u Fusion-RP 80A(250 mm×4.6 mm,5 μm),Thermo ODS HPERSIL C18(250 mm×4.6 mm,5 μm)]的效果,最终确定了该方法的色谱条件。
本研究同时对同来源的菊花破壁饮片-中间体-传统饮片进行指纹图谱研究并分析三者之间的相关性,结果显示三者之间全谱相似度均大于0.99,各色谱峰的保留时间几乎一致,但存在一定的含量差异。结果表明菊花传统饮片经破壁粉碎并制成破壁饮片的过程中,化学成分组成无明显的变化,破壁技术未造成主成分流失以及新化学成分的转化或生成。图4中,保留时间20 min和80 min处,由批号为20131201杭白菊制备的样品Ⅰ1~Ⅰ3相对应的色谱峰远远小于其他两批制成的样品(Ⅱ1~Ⅱ3、Ⅲ1~Ⅲ3)。参考相关文献[9-10],推测:由于菊花采收时间及开放状态的不同,故3批菊花本身所含的化学成分和含量存在差异,故其制成的相应破壁粉体和破壁饮片的组成成分和含量也存在相应差异,因此可以体现该指纹图谱对菊花破壁饮片能起到源头的控制,确保菊花破壁饮片的质量稳定、均一,也提示了选材时应采用同产地、同采收时间、同开放状态的杭白菊。
本研究建立的指纹图谱方法精密度、重复性、稳定性良好,可为菊花破壁饮片质量控制标准的制定、品质评价、活性成分的药理药效学提供科学依据和指导作用。为更全面、科学地评价菊花破壁饮片的内在质量,后续仍需在本指纹图谱研究的基础上结合气相色谱和液相色谱等多手段对菊花中绿原酸、木犀草苷、异绿原酸A等重要指标成分进行含量差异分析,为菊花破壁饮片和传统饮片之间的剂量换算和服用方式提供参考。
[1] 国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2015:310-311.
[2] 成金乐,赖智填,彭丽华.中药破壁饮片研究[J].世界科学技术—中医药现代化,2014,16(2):254-262.
[3] 董鹏鹏,梅全喜.中药破壁饮片的质量控制与评价方法研究进展[J].中药材,2015,38(9):1996-1999.
[4] 胥爱丽,毕晓黎,罗文汇,等.菊花配方颗粒的HPLC指纹图谱研究[J].中国实验方剂学杂志,2011,17(4):80-82.
[5] 覃珊,温学森.HPLC同时测定菊花中6种活性成分含量[J].中国中药杂志,2011,36(11):1474-1477.
[6] 刘晓,蔡皓,马晓青,等.硫磺熏蒸前后菊花的HPLC指纹图谱比较研究[J].中药材,2012,35(5):705-708.
[7] 赵玉丛,刘国际,任保增,等.菊花的HPLC指纹图谱研究[J].中草药,2005,36(10):116-119.
[8] 程宏英,冯启余,曹玉华,等.菊花中活性成分的高效液相色谱测定与指纹图谱研究[J].分析科学学报,2007,23(3):257-262.
[9] 覃珊.产后加工、采收期和花序不同部位对菊花质量影响的研究[D].济南:山东大学,2011.
[10] 白晓艳.采收期对药用菊花产量与质量的影响[J].河北林业科技,2015(3):10-11.
StudyonHPLCFingerprintofCellWall-BrokenDecoctionPiecesofChrysanthemiFlos
LIU Xingyun1,2,3,WANGHuiling2,3,PENGLihua2,3,CHENGJinle1,2,3*
(1.ResearchCenterofChineseHerbalResourceScienceandEngineering,GuangzhouUniversityofTraditionalChineseMedicine,KeyLaboratoryofChineseMedicinalResourcefromLingnan,MinistryofEducation,Guangzhou510006,China;2.KeyLaboratoryofCell-brokenDecoctionPiecestechnologyandApplicationofstateAdministrationofTraditionalChineseMedicine,Zhongshan528437,China;3.ZEUSPharmaceuticalgroup,Zhongshan528437,China)
Objective:To establish the HPLC fingerprint of Cell Wall-Broken Decoction Pieces of Chrysanthemi Flos,and analyze the relativity between its decoction pieces,broken powder and broken particle,helping to evaluate its quality comprehensively.Methods:RP-HPLC method was performed on an Agilent C18(250 mm×4.6 mm,5 μm)column with a gradient elution composed of acetonitrile-aqueous solution containing 0.5% phosphoric acid.The column temperature was set at 35 ℃,while the detective wavelength was set at 348 nm.Results:The chromatographic fingerprint common pattern was established.Fifteen mutual peaks were obtained from the chromatograms of eleven batches of samples.Conclusion:The method with good reproducibility is reliable and stable,which is feasible for quality control of cell wall-broken decoction pieces of Chrysanthemi Flos.
Chrysanthemi Flos;fingerprint;cell wall-broken decoction pieces;HPLC
2015-09-25)
中山市科技计划项目(2013A3FC0253)
*
成金乐,教授,研究方向:破壁饮片及产业化,创新中药研究与开发;Tel:(0760)85312928,E-mail: gdcjl9@126.com
10.13313/j.issn.1673-4890.2016.3.025
