0.03%他克莫司软膏的体外透皮吸收研究Δ
2016-09-23张鹏威苏文琴邝少轶
张鹏威,苏文琴,邝少轶,刘 玮
(1.海南医学院药学院,海口 571199;2.海南通用三洋药业有限公司,海口 570312)
0.03%他克莫司软膏的体外透皮吸收研究Δ
张鹏威1*,苏文琴1,邝少轶1,刘玮2#
(1.海南医学院药学院,海口571199;2.海南通用三洋药业有限公司,海口570312)
目的:研究0.03%他克莫司软膏经离体裸鼠皮的透皮吸收情况,并比较国产受试制剂与进口参比制剂的差异。方法:采用改良Franz扩散池法进行体外透皮试验,以高效液相色谱-质谱法(HPLC-MS)测定国产受试制剂和进口参比制剂0.03%他克莫司软膏的体外透皮渗透量、渗透速率和滞后时间。结果:受试制剂与参比制剂的24 h体外透皮累积渗透量分别为(3 907±1 191)、(3 896±1 064)ng/cm2,渗透速率分别为186.7、182.9 ng(/cm2·h),滞后时间分别为1.95、2.00 h,二者差异无统计学意义(P>0.05)。结论:受试制剂有良好的透皮性能,其在裸鼠离体皮肤的透皮吸收性能与参比制剂相当。
他克莫司软膏;体外透皮吸收;裸鼠;高效液体色谱-质谱法
他克莫司是一种大环内酯类的免疫抑制剂,外用可作为抗菌药物,其主要通过阻断钙调神经磷酸酶活化而抑制皮损处T细胞的活化;另外,亦可通过调节其他免疫细胞相关因子的释放来改善皮损处的炎症反应[1]。这种抗炎活性与外用糖皮质激素相似,但是外用他克莫司不具有糖皮质激素那样的副作用。他克莫司在特异性皮炎、白癜风、银屑病等治疗中疗效良好,目前也无该药增加局部感染和肿瘤发生的证据[2]。临床上,外用他克莫司软膏及水凝胶等制剂有0.1%和0.03%两种规格,目前国内外已有0.1%他克莫司软膏体外透皮吸收研究报道[2-5],但0.03%规格制剂由于药物浓度低,采用常规检测仪器无法测定,因此少见报道。为此,本文建立了高效液相色谱-质谱法(HPLC-MS),以研究0.03%他克莫司软膏体外透皮吸收情况,并以进口他克莫司软膏为参比制剂进行了对比,为该药临床使用提供了试验依据。
1 材料
1.1仪器
RYJ-6B透皮试验仪(上海黄海药检仪器有限公司);Agilent 1200 HPLC-6100 MS仪(美国安捷伦公司);TDL-80-2B台式离心机(上海安亭科学仪器厂);WD-12水浴氮吹仪(杭州奥盛仪器有限公司);MS105DU电子天平(梅特勒-托利多有限公司)。
1.2药品与试剂
他克莫司软膏(受试制剂,批号:20121101,规格:3 mg∶10 g)、他克莫司对照品(批号:S121001,纯度:99.6%)均购自海南皇隆制药股份有限公司提供;他克莫司软膏[参比制剂,安斯泰来制药(中国)有限公司,批号:032330,规格:3 mg∶10 g];吉非替尼对照品(内标,海口南陆医药科技有限公司,批号:20130901,纯度:99.92%);0.9%氯化钠注射液(安徽双鹤药业有限责任公司,批号:140304);纯化水和重蒸馏水为自制,其他试剂均为国产分析纯。
1.3动物
裸鼠,♀,体质量为21~25 g,年龄约为6周龄,购于长沙东创实验动物科技股份有限公司,动物合格证号:43004700008035。
2 方法与结果
2.1离体鼠皮的处理
取裸鼠,断颈处死,从颈部环形剪开皮肤,剥离皮肤,剪下腹部皮肤,小心去除皮肤上的残留附属物,检查皮肤完整性,剔除有皮损皮肤,置于含生理盐水的封口袋中,随机编号,于0℃冷藏保存备用。从处死裸鼠至透皮试验时间不超过48 h。
2.2透皮渗透试验
取裸鼠6只,均分为2组进行体外透皮试验,间隔24 h后,进行交叉试验。取按“2.1”项下处理后的鼠皮,吸干水分,固定于Franz扩散池的供给池与接收池之间,皮肤角质层面向供给池,真皮层面向接收池。分别取1 g受试制剂或参比制剂涂抹于鼠皮(扩散面积2.54 cm2)上,在橡胶皮桌面上用力振动扩散池,使软膏与鼠皮间气泡溢出,然后以保鲜膜覆盖供给池口。以32℃无水乙醇-生理盐水(3∶7,V/V)为接收液,将接收池置于(32±0.5)℃的透皮试验仪中,以300 r/min进行搅拌并计时。分别于2、4、6、8、12、24 h抽取全部溶液,并精密测定其体积Vi,同时立即补充32℃空白接收液。所取样品立即置于-18℃冷冻,集中测定他克莫司含量。按公式计算累积渗透量Q(nng/cm2),其中Qn为第n个时间点累积渗透量,ci为第i时间点药物浓度,Vi为第i时间点接收液体积,S为有效渗透面积,稳态渗透速率Js[ng(/cm2·h)]为达到稳态渗透后Qn对t的回归方程斜率。数据分析采用SPSS 11.0软件处理,正态计量指标采用均数±标准差(±s)表示,两组间比较采用独立样本t检验,P<0.05表示差异有统计学意义。
2.3接收液中他克莫司含量的测定
2.3.1溶液的制备对照品贮备液:将他克莫司对照品用甲醇制备成104 μg/ml的标准贮备液,置于4℃中保存,使用时用甲醇稀释至所需浓度。内标溶液:将吉非替尼对照品用甲醇制备成203.8 μg/ml的内标贮备液,置于4℃中保存,使用时用甲醇稀释至679.3 ng/ml。空白溶液:取处理好的裸鼠皮肤2 g,剪碎,加适量空白接收液制成匀浆,加2 g空白软膏基质(不含他克莫司),再加入空白接收液至500 ml,超声30 min,过滤,即得。
2.3.2接收液的处理吸取4 ml接收液,置于10 ml离心管中,加入内标溶液15 μl,涡旋混匀;加乙酸乙酯2 ml,涡旋混合2 min,3 500 r/min(离心半径为80 mm)离心5 min;精密吸取上层有机相于40℃水浴氮气吹干,残渣用甲醇100 μl溶解,取3 μl进样测定。按内标法以峰面积计算他克莫司浓度。
2.3.3色谱条件色谱柱:Agilent Eclipse Extend-C18(150 mm×3.0 mm,3.5 μm);流动相:A为甲醇,B为10 mmol/L醋酸铵水溶液,梯度洗脱[0 min(18%B)→12 min(18%B)→13 min (5%B)→15 min(18%B)],流速:0.5 ml/min;柱温:25℃;进样量:3 μl。
2.3.4质谱条件电喷雾电离源(ESI),选择性正离子监测(SIM),[M+H]+质荷比(m/z):821.6(他克莫司)、446.5(吉非替尼);碰撞诱导解离,干燥气体流速:10 L/min,干燥气:氮气;温度:350℃;压力:40 psi;毛细管电压:3 000 V。吉非替尼和他克莫司的质谱图见图1。

图1 质谱图Fig 1 Mass chromatograms
2.3.5专属性试验取空白基质渗透接收液、空白溶液+他克莫司对照品+内标、渗透12 h的样品(受试制剂)接收液,按“2.3.2”项下方法处理后进样测定,记录色谱。结果显示,他克莫司和内标峰之间分离良好,溶液中无内源性物质干扰测定,色谱图见图2。
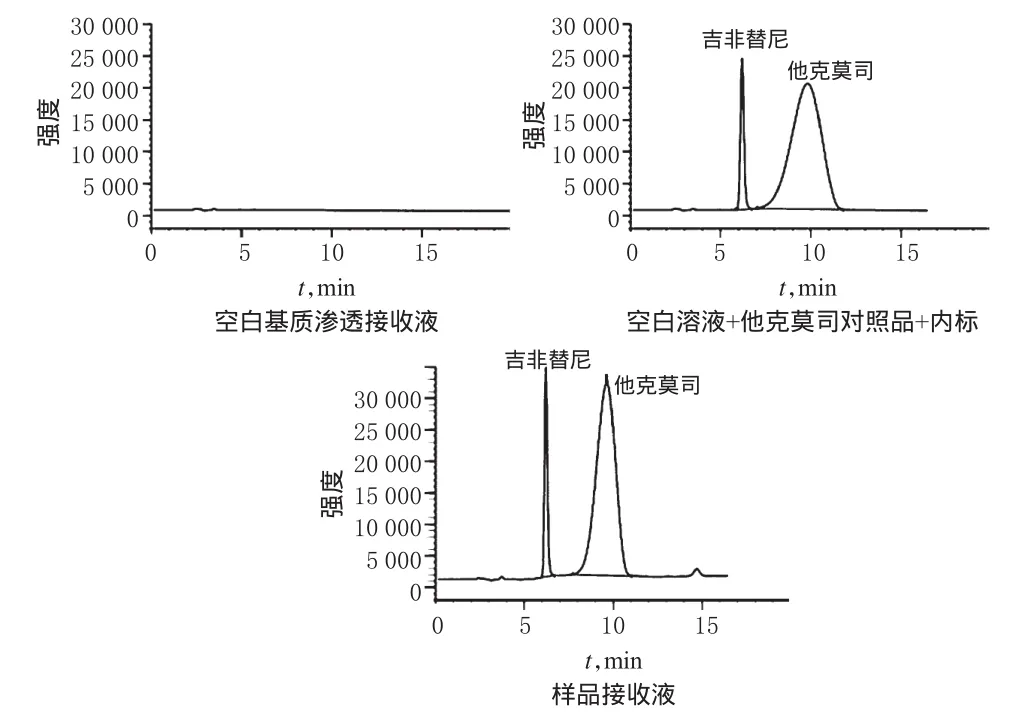
图2 总离子流色谱图Fig 2 Total ions chromatograms
2.3.6线性关系考察用空白溶液将他克莫司贮备液制备成他克莫司质量浓度分别为20.8、41.6、104、208、416、832 ng/ml的系列质控样品,按“2.3.2”项下方法处理后,进样测定。以他克莫司与内标峰面积的比值(f)为纵坐标,以他克莫司质量浓度(c)为横坐标进行线性回归分析,得回归方程为f=0.013 96c-0.005 4(r=0.999 9)。结果表明他克莫司检测质量浓度的线性范围为20.8~832 ng/ml,定量下限为20.8 ng/ml。
2.3.7精密度试验按“2.3.6”项下方法制备他克莫司质量浓度分别为41.6、208、624 ng/ml的质控样品,每个浓度5份,按“2.3.2”项下方法处理后,进样测定,考察批内精密度。结果低、中、高质量浓度质控样品的批内RSD分别为3.51%、4.35%、3.92%(n=5),均小于15%,符合生物样品检测的要求。
2.3.8仪器精密度试验取他克莫司质量浓度为208 ng/ml的质控样品,按“2.3.2”项下方法处理后,重复进样5次,记录峰面积。结果,他克莫司和内标峰面积的比值RSD为0.71%(n= 5),表明仪器精密度良好,符合测定要求。
2.3.9加样回收率试验按“2.3.6”项下方法制备他克莫司质量浓度分别为41.6、208、624 ng/ml的质控样品,每个浓度5份,分别按“2.3.2”项下方法处理后,进样测定,计算加样回收率。结果,低、中、高质量浓度质控样品的平均加样回收率分别为107.8%、107.2%、107.5%,RSD分别为3.99%、3.20%、3.88% (n=5)。
2.3.10稳定性试验按“2.3.6”项下方法制备他克莫司质量浓度分别为41.6、208、624 ng/ml的质控样品,分别于室温放置8 h和-20℃下放置5 d后,按“2.3.2”项下方法处理后,进样测定,每个浓度测定5份。结果,低、中、高质量浓度质控样品于室温放置8 h的RSD分别为15.29%、5.91%、8.17%(n=5),于-20℃放置5 d的RSD分别为7.47%、7.22%、6.79%(n= 5),均符合生物样品测定要求。
2.4透皮渗透试验结果
2种制剂的体外累积渗透量见表1(表中ND表示低于定量下限,视为未检出)。
表1 2种制剂的体外累积渗透量(±s,n=6,ng/cm2)Tab 1 Accumulative permeation amount in vitro of 2 preparations(±s,n=6,ng/cm2)

表1 2种制剂的体外累积渗透量(±s,n=6,ng/cm2)Tab 1 Accumulative permeation amount in vitro of 2 preparations(±s,n=6,ng/cm2)
样品受试制剂参比制剂取样时间2 h ND ND 4 h 102.5±98.4 110.0±66.4 6 h 419.9±147.6 440.0±201.4 8 h 1 168±506 1 151±498 12 h 2 256±961 2 196±861 24 h 3 907±1 191 3 896±1 064
由表1可知,他克莫司在2 h时累积渗透量较少,均低于定量下限,到4 h才有较明显的药物渗透,但需要到6 h才能达到稳态渗透。2种制剂间24 h的累积渗透量差异无统计学意义(P>0.05)。将达到渗透平衡时的第6、8、12、24 h累积渗透量Q对时间t进行线性回归,所得直线斜率即渗透速率Js,将线性回归方程外延至Q=0,以其对应时间t作为滞后时间Tlag,结果见表2。
表2 2种制剂的体外渗透速率和滞后时间(±s,n=6)Tab 2 Permeation rate in vitro and delay time of 2 preparations(±s,n=6)

表2 2种制剂的体外渗透速率和滞后时间(±s,n=6)Tab 2 Permeation rate in vitro and delay time of 2 preparations(±s,n=6)
样品受试制剂参比制剂Tlag,h 1.95 2.00回归曲线方程Q=183.7t-358.0 Q=182.9t-365.8 Js,ng/(cm2·h)186.7 182.9 r 0.978 20.982 2
由表2可知,受试制剂和参比制剂的Js和Tlag均无明显差异。
3 讨论
一般认为,猪皮结构与人皮肤相似,体外透皮试验采用猪皮能较好地预测药物经人体皮肤吸收情况,但猪成本相对较高。根据2012年欧盟发布的《透皮贴剂质量指南》,透皮制剂在体外渗透试验中,在无法采用人体皮肤时,可以采用人造皮肤、猪皮、豚鼠皮、裸鼠皮等[6]。由于本研究受试制剂与参比制剂采用相同试验条件,故可以采用裸鼠皮比较不同制剂间的体外渗透差异,为体内吸收提供依据。
由于透皮接收溶液里含有皮肤组织浸出物,因此本文含量测定方法学参照生物样品定量分析方法验证指导原则进行。由于接收池容积较小,不同时段接收液成分略有不同,而方法学考察需要大量空白接收液,因此将皮肤组织用空白接收液做成匀浆,加入空白基质充分溶解后过滤,因此其成分与空白基质的接收液近似,故以此用于方法学考察用溶剂。
由于他克莫司在水中几乎不溶,易溶于乙醇。进行体外透皮试验时,接收液需要形成漏槽条件(Sink condition),另外要求接收液尽量不破坏或影响正常皮肤的生理功能[6]。在他克莫司体外渗透试验中,相关文献分别选用生理盐水-无水乙醇(50∶50)、生理盐水-无水乙醇(70∶30)、生理盐水-无水乙醇(75∶25)、磷酸盐溶液-无水乙醇(70∶30)为透皮接收介质[2-4,7],笔者在考虑到他克莫司溶解性基础上,选用生理盐水-无水乙醇(70∶30)作为接收液。该接收液满足漏槽条件,其基本成分与体液接近。
根据2012年欧盟发布的《透皮贴剂质量指南》,透皮制剂在体外渗透试验中,取样点需要满足表征渗透行为要求,通常不少于5个取样点,并且最小取样时间要尽可能早,如15 min 或30 min[6]。通常认为,第1个取样点要尽可能早的原因是为了验证皮肤是否存在破损,因为一般药物经皮渗透都有一定的滞后时间Tlag,若皮肤破损则在很短时间内即可检测到较显著量的渗透药物。在预试验中笔者曾进行过0.5、1、2 h时间点取样,然而由于本制剂里药物浓度本身较低(0.03%),因此在120 min内的接收液中药物浓度均低于检测限,无法检测。因此将第1个取样时间点确定为2 h。
在进行渗透接收液药物浓度检测时,本课题组首先考察了样品处理方法比较简单的HPLC-紫外检测器法,然而由于药物浓度较低,而且本药的紫外吸收较弱,因此其色谱峰较小,无法满足定量测定要求。因此改用HPLC-MS法测定,本法灵敏度高,然而本法要求样品和流动相里无可挥发性成分,否则影响检测灵敏度[8]。因此,笔者根据药物性质,将接收液用乙酸乙酯萃取,将其中的氯化钠和皮肤组织浸出物分离。方法学验证表明,该法灵敏度高,精密度和准确度符合生物样品检测要求。
[1]Kino T,Hatanaka H,Miyata S,et al.FK-506,a novel immunosuppressant isolated from a Streptomyces.Ⅱ.immunosuppressive effect of FK-506 in vitro[J].J Antibiotics,1987,40(9):1 256.
[2]杨建强,宋颖.他克莫司软膏治疗局限性慢性单纯性苔藓临床观察[J].中国药房,2010,21(10):915.
[3]李龙年.FK506-SLN水凝胶的制备及其体外透皮和药效学研究[D].广州:南方医科大学,2012:17.
[4]Nam SH,Ji XY,Park JS.Investigation of tacrolimus loaded nanostructured lipid carriers for topical drug delivery [J].Bull Korean Chem Soc,2011,32(3):956.
[5]Pople PY,Singh KK.Development and evaluation of colloidal modified nanolipid carrier:application to topical delivery of tacrolimus[J].Eur J Pharm Biopharm,2011,79(1):82.
[6]Quality Working Party,European Medicines Agency.Guideline on quality of transdermal patches[EB/OL].(2012-08-23)[2016-04-23].http://www.damienbove.com/pdf/ wc500132404.pdf.
[7]汪宏,王维,张建华,等.他克莫司软膏的体外透皮吸收研究[J].华西药学杂志,2014,29(2):119.
[8]黄艳,吴月,郭晓烽,等.LC-MS法测定人血浆中赖诺普利样品前处理方法改进[J].药学与临床研究,2008,16 (2):104.
(编辑:邹丽娟)
Study on Percutaneous Absorption in vitro of 0.03% Tacrolimus Ointment
ZHANG Pengwei1,SU Wenqin1,KUANG Shaoyi1,LIU Wei2
(1.School of Pharmacy,Hainan Medical University,Haikou 571199,China;2.Hainan Tongyong-Sanyo Pharmaceutical Co.,Ltd.,Haikou 570312,China)
OBJECTIVE:To study the percutaneous absorption of 0.03%Tacrolimus ointment,and to compare the difference of domestic test preparation and imported reference preparation.METHODS:Modified Franz diffusion cells were adopted in transdermal test in vitro;HPLC-MS method was used to determine permeation amount and rate in vitro,delay time of domestic test preparation and imported reference preparation 0.03%Tacrolimus ointment.RESULTS:24 h in vitro permeation amount of test and reference preparations were(3 907±1 191)and(3 896±1 064)ng/cm2;permeation rates were 186.7 and 182.9 ng(/cm2·h);delay time were 1.95 and 2.00 h,respectively(P>0.05).CONCLUSIONS:Test preparation shows good percutaneous property,and is similar to reference preparation in penetration absorbency through nude mice skin.
Tacrolimus ointment;Percutaneous absorption in vitro;Nude mice;HPLC-MS
R965
A
1001-0408(2016)22-3051-03
10.6039/j.issn.1001-0408.2016.22.09
海南省应用技术研发与示范推广专项(No. ZDXM2015122)
*副教授,博士。研究方向:药物制剂开发和药物质量标准研究。电话:0898-31350722。E-mail:zpw0803@163.com
高级工程师。研究方向:药物制剂开发。电话:0898-68710202。E-mail:13519891999@139.com
2016-05-06
2016-06-08)
