吲哚美辛口服自微乳化给药系统的大鼠体内药动学研究
2016-09-14滕希峰李钟方壬德李国全黄诗莹何洋何琳广东药科大学国家中医药管理局岭南药材生产与开发重点研究室广东广州50006医药化工学院广东中山58458广州市医疗救助服务中心广东广州5060
滕希峰,李钟,方壬德,李国全,黄诗莹,何洋,何琳(广东药科大学.国家中医药管理局岭南药材生产与开发重点研究室,广东广州50006;.医药化工学院,广东中山58458;.广州市医疗救助服务中心,广东广州5060)
吲哚美辛口服自微乳化给药系统的大鼠体内药动学研究
滕希峰1,李钟1,方壬德1,李国全3,黄诗莹1,何洋2,何琳2
(广东药科大学1.国家中医药管理局岭南药材生产与开发重点研究室,广东广州510006;2.医药化工学院,广东中山528458;3.广州市医疗救助服务中心,广东广州510630)
目的研究吲哚美辛口服自微乳化给药系统(IDM-SMEDDS)在大鼠体内的药动学特征。方法大鼠灌胃给予IDM-SMEDDS(给药剂量按IDM计为8.0 mg/kg),采用HPLC法测定IDM在大鼠血浆中的药物浓度,以IDM原料药制备混悬液作为参比,绘制两者血药浓度-时间曲线,DAS Ver2.0药动学软件计算药动学参数。结果IDM-SMEDDS的药动学过程符合二室模型,权重因子为1/C2,IDM混悬液的药动学过程符合一室模型,权重因子为1/C2;大鼠口服IDM-SMEDDS的Cmax为42.56 μg/mL、Tmax为1 h、AUC0-48 h为814.25(μg·h)/mL,口服IDM混悬液的Cmax为9.72 μg/mL、Tmax为6 h、AUC0-48 h为134.57 (μg·h)/mL。结论自微乳化给药系统可以提高吲哚美辛的口服生物利用度。
吲哚美辛;自微乳化给药系统;药动学参数
口服制剂具有给药方便、患者依从性高的特点,是最方便的给药方式。由高通量筛选获得的候选药物中,40%的化合物属于难溶性药物[1]。难溶性药物在体内消化道的溶出是吸收的限速步骤,因溶解度小、吸收不好、生物利用度低,因此很难获得较好的治疗效果。研究发现,自微乳化给药系统是一种能够很好地改善口服药物生物利用度的新剂型[2]。自微乳化给药系统 (self-microemulsifying drug delivery systems,SMEDDS)是由药物、油相、一种(或多种)乳化剂和一种(或多种)助乳化剂组成均相混合物,可以在水溶液中自发形成透明或轻微浅蓝色乳光的O/W型乳滴,具有热力学及动力学稳定性的性质,粒径范围为10~300 nm。只需要轻微搅拌,或经口服后在胃肠道内蠕动,即可自发形成微乳。由于形成的微乳具有大的表面积、渗透性好及避免药物代谢酶及糖蛋白p-GP的破坏等优势,可为提高水难溶性药物的口服吸收提供一种新的剂型。吲哚美辛在水中溶解度为0.004 g/L[3],pH为7.4时的油水分配系数为1.49[4]。在生物药剂分类系统(biopharmaceutical classification system,BCS)中属第Ⅱ类,渗透性高但溶解度低[5-6]。本课题组前期已制备了IDM-SMEDDS[7],本文主要考察IDM-SMEDDS在大鼠体内的药动学行为,以自制IDM混悬液为参比,为SMEDDS的体内研究提供依据。
1 仪器与材料
1.1仪器
BP211D型十万分之一电子分析天平(德国赛多利斯);JB-2型恒温磁力搅拌器(上海智光仪器仪表有限公司);IKI磁力搅拌器(无锡市宇寿医疗器械有限公司);ZH-2型自动漩涡混合器(天津药典标准仪器厂);HH-2型数显恒温水浴锅(金坛市富华仪器有限公司);KQ-100DE型数控超声波清洗仪(昆山市超声仪器有限公司);800型电动离心机(广州富城仪器厂);TGL-16B型高速台式离心机(上海安亭科学仪器厂);激光粒度散射仪(英国马尔文);依利特230高效液相色谱仪(大连依利特分析仪器有限公司);UV230+紫外-可见检测器(大连依利特分析仪器有限公司);EC2000色谱工作站(大连依利特分析仪器有限公司)。
1.2试剂
吲哚美辛对照品(供含量测定用,批号:100258-200403,中国药品生物制品检定所);吲哚美辛原料药[阿拉丁试剂(上海)有限公司,质量分数>99%,批号:060619];自制 IDM-SMEDDS(规格:30 mg/ 0.45 g,批号:20140519);萘普生钠对照品(批号: 100330-200101,中国药品生物制品检定所);油酸乙酯(上海飞祥化工厂)、吐温-80(批号:10200319,上海申宇医药化工有限公司)、聚乙二醇400(进口分装,批号:20090419,广东光华化学厂有限公司)、无水乙醚(广州化学试剂厂)、冰醋酸均为市售分析纯;制剂所用水为纯化水(pH=6.0);甲醇(色谱纯,天津四友精细化学品有限公司);高效液相色谱分析所用水为双蒸水(阻值>16)。
1.3动物
SD大鼠12只,雌雄各半,体质量200~250 g,SPF级,购自南方医科大学实验动物中心,许可证号为 SCXK(粤)2011-0015。饲养条件:温度18~29℃,日温差≤3℃,相对湿度40%~70%。水为纯化水,饲料购于南方医科大学实验动物中心。
2 方法与结果
2.1对照品溶液的配制
2.1.1吲哚美辛对照品溶液的配制 精密称取吲哚美辛对照品10.08 mg,置于100 mL容量瓶中,甲醇适量振摇溶解并稀释至刻度,即得质量浓度为100.8 μg/mL的吲哚美辛甲醇储备液。另取该溶液1.0 mL至10 mL容量瓶中,用甲醇稀释至刻度,制得质量浓度为10.08 μg/mL的吲哚美辛对照品溶液。
2.1.2内标溶液配制 精密称取内标物萘普生钠对照品10.50 mg,置于100 mL容量瓶中,甲醇溶解,摇匀稀释至刻度,制得质量浓度为105.0 μg/mL的萘普生钠对照品溶液。另取该溶液1.0 mL至10 mL容量瓶中,用甲醇稀释至刻度,制得质量浓度为10.50 μg/mL的内标溶液。
2.2血浆样品处理
精密移取血浆150 μL于5 mL带塞EP管中,依次加内标物萘普生钠对照品溶液50 μL及10%乙酸溶液 100 μL,涡旋振荡 2 min,加入无水乙醚3 mL,涡旋振荡5 min,10 000 r/min离心10 min,吸取上层无水乙醚提取液,向管内下层液再加入无水乙醚3 mL重复萃取1次。合并2次的无水乙醚提取液,置40℃水浴蒸干,蒸干后,用无水乙醚1 mL润洗管壁,再次蒸干,将管内残留物用甲醇-水-冰醋酸(体积比58∶22∶0.05)150 μL溶解,10 000 r/min离心10 min,取上清液20 μL,HPLC测定。
2.3IDM-SMEDDS生物样品分析方法的建立
2.3.1色谱条件 色谱柱为岛津VP-ODS C18色谱柱(4.6 mm×150 mm,5 μm);柱温:25℃;流动相为甲醇-水-冰醋酸(体积比 58∶22∶0.05);流速: 1.0 mL/min;检测波长:254 nm;进样量:20 μL。
2.3.2专属性试验 分别取空白血浆、血浆+吲哚美辛对照品(质量浓度为10.08 μg/mL)+内标物(质量浓度为10.50 μg/mL)、IDM-SMEDDS给药1 h血浆样品,按“2.3.1”项下色谱条件进样检测,记录色谱图,见图1。结果表明,各峰分离度符合要求,理论塔板数按吲哚美辛计算不低于5 000,吲哚美辛的保留时间在13 min左右,内标物萘普生钠的保留时间在6 min左右,与杂质峰可实现基线分离,内源性物质对样品测定无干扰,方法专属性好。

图1 大鼠血浆中IDM-SMEDDS的HPLC图谱Figure 1 HPLC chromatograms of IDM-SMEDDS in rats plasma
2.3.3标准曲线与定量下限 精密称取吲哚美辛对照品40.16 mg,置100 mL容量瓶中,甲醇适量振摇溶解并稀释至刻度,即得质量浓度为 401.6 μg/mL的吲哚美辛甲醇储备液,分别移取 0.10、0.50、1.00、1.50、6.00、8.00、10.00 mL,用甲醇分别配制成质量浓度为4.016、20.08、40.16、60.24、241.0、321.3、401.6μg/mL的系列吲哚美辛溶液。精密移取空白大鼠血浆150 μL,分别加入上述系列质量浓度的吲哚美辛溶液50 μL,再加入“2.1.2”项下内标物萘普生钠对照品溶液 50 μL,涡旋混合2 min,得1.004、5.020、10.04、15.06、60.25、80.32、100.4 μg/mL的血浆吲哚美辛质量浓度样品。标准曲线方程以药物峰面积(Ai)与内标物峰面积(As)的比值(A)对质量浓度(ρ)进行线性回归,得线性回归方程A=0.129 ρ-0.280,r=0.999 4。结果表明血浆吲哚美辛质量浓度在1.004~100.4 μg/mL范围内与峰面积比值线性关系良好。血浆样品最低定量限为1.004 μg/mL。
2.3.4精密度试验 取大鼠空白血浆150 μL,加入质量浓度分别为4.016、241.0、401.6 μg/mL的吲哚美辛溶液各50 μL,再加入内标物萘普生钠对照品溶液50 μL,制备成低、中、高3个质量浓度的血样各6份,按“2.2”项下操作,于同1天重复测定,记录峰面积,根据随行标准曲线方程计算各样品中吲哚美辛的质量浓度,计算日内精密度,RSD结果分别为1.1%、1.8%、1.9%。同法操作,连续测定3天,计算日间精密度,RSD结果分别为3.3%、2.6%、1.3%,符合生物分析方法指导原则要求[8]。
2.3.5样品稳定性试验 配制低、中、高3种质量浓度(1.004、60.25、100.4 μg/mL)的吲哚美辛血浆标准溶液,每种浓度3份,经历3次冰冻-解冻循环后,按“2.2”项下操作处理血浆样品,考察其稳定性。结果低、中、高3个质量浓度RSD分别为3.8%、4.2%、2.9%,表明冻融条件对血浆样品的检测结果没有明显的影响。
2.3.6绝对回收率试验 配制质量浓度分别为1.004、60.25、100.4 μg/mL的吲哚美辛溶液,直接进样20 μL,其峰面积作为对照组的峰面积,另取大鼠空白血浆150 μL,分别加不同浓度的吲哚美辛溶液,使成质量浓度为1.004、60.25、100.4 μg/mL的样品溶液,按“2.2”项下操作处理血浆样品,分别记录对照组的峰面积及样品的峰面积,绝对回收率分别为(78.42±2.1)%、(71.41±1.6)%、(78.53±3.1)%。
2.4IDM-SMEDDS和IDM混悬液大鼠体内血药浓度的测定
2.4.1给药与血样采集 取健康SD大鼠12只,体质量200~250 g,随机分成2组,每组6只,给药前禁食12 h,自由饮水。分别灌胃给予IDM-SMEDDS与自制IDM混悬液,给药剂量按IDM计均为8.0 mg/kg。分别于给药前取空白血浆,给药后0.5、1、2、3、4、6、8、10、24、36、48 h大鼠眼眶静脉丛取血0.5 mL,置于肝素化离心管中,3 000 r/min离心15 min,分离并吸取上层血浆(约0.2 mL),备用。
2.4.2血药浓度的测定 将待测样品不同时间点的峰面积与内标物峰面积的比值代入标准曲线分别计算灌胃给药后IDM-SMEDDS与IDM混悬液在大鼠体内的血药浓度,绘制血药浓度-时间曲线(n= 6),结果见图2。从图中可见IDM-SMEDDS的血药浓度明显高于IDM混悬液。
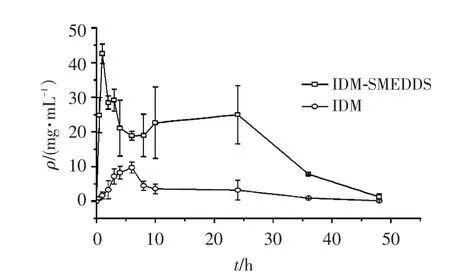
图2 血浆中IDM-SMEDDS和IDM混悬液的血药浓度-时间曲线Figure 2 The plasma concentration-time curves of IDMSMEDDS and IDM suspension in rats after oral administration(s,n=6)
2.5药动学参数计算
用DAS 2.0软件处理IDM-SMEDDS和IDM混悬液的血药浓度数据,对IDM-SMEDDS和IDM混悬液的平均血药浓度-时间曲线分别进行房室模型拟合,根据AIC(Akaike′s information criterion)值和R2(拟合值与实测值之间的相关系数)进行综合比较,AIC值越小,R2值越大,则拟合效果越好。根据AIC最小原则判断IDM-SMEDDS和IDM混悬液的隔室模型,结果表明,IDM-SMEDDS的药动学符合二室模型,IDM混悬液的药动学符合一室模型。权重因子均为1/C2。用统计矩法估算二者的药动学参数,并用t检验对药动学参数间进行统计学分析,结果见表1。
可见,灌胃给予IDM-SMEDDS后,大鼠血浆中的Cmax为42.56 μg/mL,自制IDM混悬液的Cmax为9.72 μg/mL,前者是后者的4.38倍;灌胃给予IDMSMEDDS后,大鼠血浆中的Tmax为1 h,自制IDM混悬液的Tmax为6 h,前者比后者达峰时间减少;灌胃给予IDM-SMEDDS后,大鼠血浆中的 AUC0-48 h为814.25(μg·h)/mL,而 IDM 混悬液 AUC0-48 h为134.57(μg·h)/mL,前者是后者的6.05倍。
表1 IDM-SMEDDS和IDM混悬液的大鼠血浆中部分药动学参数Table 1 The pharmacokinetic parameters of IDM-PMC and IDM suspension in rats plasma after oral administration,n=6)

表1 IDM-SMEDDS和IDM混悬液的大鼠血浆中部分药动学参数Table 1 The pharmacokinetic parameters of IDM-PMC and IDM suspension in rats plasma after oral administration,n=6)
与IDM混悬液比较:*P<0.05;**P<0.005。
药动学参数 IDM-SMEDDS IDM混悬液Tmax/h 1.0 6.0 Cmax/(μg·mL-1) 42.56±2.82** 9.72±1.58 AUC0-48 h/(μg·h·mL-1) 814.25±234.69* 134.57±62.24 AUC0-∞/(μg·h·mL-1) 936.50±122.04** 135.72±62.27 AUM0-48 h/(μg·h·mL-1) 14 177.26±3 918.04*1 976.28±1 061.73 MRT0-48 h/h 17.45±0.21* 14.26±1.44
3 讨论
本文采用HPLC法测定大鼠体内IDM的血药浓度,预试验时分别以甲醇、三氯甲烷、正己烷、无水乙醚、丙酮等为萃取试剂萃取血液中的吲哚美辛,结果显示甲醇沉淀蛋白质的能力佳,但是甲醇挥发后有大量蛋白析出,影响血药浓度的测定,比较上述试剂以无水乙醚萃取的效果最好,故本法选取无水乙醚为萃取溶剂。方法学考察结果显示,内源性杂质与吲哚美辛能得到较好分离,空白血浆吲哚美辛的回收率大于70%,且结果准确、重复性良好,符合生物样品分析的要求。
吲哚美辛在水中溶解度为0.004 g/L,几乎不溶,制成IDM-SMEDDS后溶解度增加。因吲哚美辛为非甾体抗炎药,市售口服片剂、胶囊规格为25 mg/片,本文未考察其最大载药量,直接制成30 mg 的IDM-SMEDDS。从大鼠灌胃给予IDM混悬液和IDM-SMEDDS来看,IDM的Cmax为9.72 μg/mL,制成IDM-SMEDDS后Cmax为42.56 μg/mL,而且达峰时间提前,提示将难溶性药物制成自微乳化给药系统可以提高生物利用度及起效快。药动学结果表明,IDM-SMEDDS符合二室模型,IDM混悬液符合一室模型,原因可能是IDM-SMEDDS吸收很快或者存在独特的吸收机理,抑或是选择采样的时间点的问题,在体内的药-时过程为二室模型,更准确深入研究需要增加吸收相的时间点。
[1]杨鹏飞,陈卫东.纳米乳提高难溶性药物生物利用度的研究进展[J].中国药学杂志,2013,48(15):1238-1244.
[2]FABIAN H,GLEN P,SABINE H,et al.In vivo evaluation of anoralself-microemulsifyingdrugdeliverysystem (SMEDDS)for leuprorelin[J].Int J Pharma,2014,472: 20-26.
[3]QIAO Mingxi,CHEN Dawei,MA Xichen,et al.Injectable biodegradabletemperature-responsivePLGA-PEG-PLGA copolymers:synthesis and effect of copolymer-composition on the drug release from the copolymer-based hydrogels[J]. Int J Pharma,2005,294(1/2):103-112.
[4]KIM J Y,KU Y S.Enhanced absorption of indomethacin after oral or rectal administration of a self-emulsifying system containing indomethacin to rats[J].Int J Pharma, 2000,194(1):81-89.
[5]叶雯,王永禄,李学明.生物药剂学分类系统在难溶性药物处方中的应用[J].中国医院药学杂志,2013,33(7): 568-570.
[6]刘洋,隗丽,董玲,等.多成分体系下中药生物药剂学分类系统的构建分析[J].中国中药杂志,2014,39(23): 4479-4483.
[7]何琳,廖巍,卢秀霞,等.吲哚美辛自微乳肠溶胶囊的处方设计及体外溶出度评价[J].广东药学院学报,2013,29 (4):351-356.
[8]张立康,汪小珍,李婉姝,等.姜黄素在大鼠体内药代动力学和生物利用度研究[J].中国药理学通报,2011,27 (10):1458-1462.
(责任编辑:陈翔)
Study on the pharmacokinetics of indomethacin oral self-microemulifying drug delivery system(SMEDDS)in rats
TENG Xifeng1,LI Zhong1,FANG Rende1,LI Guoquan3,HUANG Shiying1,HE Yang2,HE Lin2
(1.Key Laboratory of State Administration of Traditional Chinese Medicine for Production&Development of Cantonese Medicinal Materials,Guangdong Pharmaceutical University,Guangzhou 510006,China;2.School of Chemistry and Chemical Engineering,Guangdong Pharmaceutical University,Zhongshan 528458,China;3.Guangzhou Medical Assistance Service Center,Guangzhou 510630,China)
Objective To study the pharmacokinetics of indomethacin oral self-microemulsifying drug delivery system(IDM-SMEDDS)in rats.Methods IDM-SMEDDS was given to rats by oral administration (8.0 mg/kg).HPLC method was used to determine the plasma concentration of IDM.The plasma concentration-time profiles were obtained in contrast with indomethacin suspension.The pharmacokinetic parameters were calculated by using DAS ver2.0 as pharmacokinetic software.Results Pharmacokinetics of IDM-SMEDDS was accord with two-compartment model with the weight factor of 1/C2.IDM suspension was accord with one-compartment model with the weight factor of 1/C2.After given IDM-SMEDDS,the Cmaxwas 42.56 μg/mL,Tmaxwas 1 h,and AUC0-48 hwas 814.25(μg·h)/mL.After given self-made IDM suspension,the Cmaxwas 9.72 μg/mL,Tmaxwas 6 h,and AUC0-48 hwas 134.57(μg·h)/mL.Conclusion The self-microemulsifying drug delivery system can increase the oral bioavailability of indomethacin.
indomethacin;self-microemulsifying drug delivery system;pharmacokinetics
天然药物化学
R965.5
A
1006-8783(2016)04-0406-04
10.16809/j.cnki.1006-8783.2016062708
2016-06-27
广东药学院“创新强校工程”医药化工省级实验教学示范中心资助项目;广东省医学科学技术研究基金项目(A2015345);广东省科技计划项目(2016A020226018)
滕希峰(1977—),男,讲师,主要从事中药资源与新药研发,电话:020-39352176,Email:xfteng78@163.com;通信作者:何洋,女,高级实验师,主要从事新药研究与开发工作,电话:0760-88207977,Email:heyang626@163.com;何琳,女,高级实验师,主要从事药剂新剂型与新技术,电话:0760-88207977,Email:helin721@163.com。
网络出版时间:2016-07-011 10:09 网络出版地址:http://www.cnki.net/kcms/detail/44.1413.R.20160711.1009.001.html
